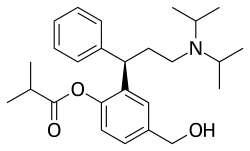
Fesoterodina
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Fesobig, Toviaz |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a609021 |
| Datos de licencia |
|
| Vías de administración | Por la boca |
| Código ATC |
|
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 52% (metabolito activo) |
| Unión de proteínas | 50% (metabolito activo) |
| Metabolismo | Hígado ( mediado por CYP2D6 y 3A4 ) |
| Vida media de eliminación | 7–8 horas (metabolito activo) |
| Excreción | Riñón (70%) y heces (7%) |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.184.854 |
| Datos químicos y físicos | |
| Fórmula | C26H37NO3 |
| Masa molar | 411,586 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La fesoterodina ( DCI , utilizada como fumarato bajo la marca Toviaz ) es un fármaco antimuscarínico desarrollado por Schwarz Pharma AG para tratar el síndrome de vejiga hiperactiva (VH). [2] Fue aprobado por la Agencia Europea de Medicamentos en abril de 2007, [3] la Administración de Alimentos y Medicamentos de los Estados Unidos el 31 de octubre de 2008 [4] y Health Canada el 9 de febrero de 2012. [5]
La fesoterodina es un profármaco . La desfesoterodina es degradada por las esterasas plasmáticas a su metabolito activo .
Eficacia
La fesoterodina tiene la ventaja de permitir una dosificación más flexible que otros antagonistas muscarínicos . [6] Su tolerabilidad y efectos secundarios son similares a los de otros antagonistas muscarínicos y, como fármaco nuevo, parece poco probable que produzca grandes cambios en las prácticas de tratamiento de la vejiga hiperactiva. [6]
Un estudio japonés de 2017 demostró que la urgencia y la incontinencia de urgencia mejoran después de 3 días de administración del fármaco, y que la eficacia total se puede evaluar después de 7 días de administración. Se descubrió que la vejiga hiperactiva se resolvió en el 88 % de los pacientes después de siete días de uso. [7]
Referencias
- ^ "Actualizaciones de seguridad de la marca de la monografía del producto". Health Canada . 6 de junio de 2024 . Consultado el 8 de junio de 2024 .
- ^ "La fesoterodina, nuevo fármaco candidato para el tratamiento de la vejiga hiperactiva: Pfizer adquirirá los derechos exclusivos a nivel mundial". Medical News Today . 17 de abril de 2006. Archivado desde el original el 16 de mayo de 2011 . Consultado el 2 de noviembre de 2007 .
- ^ "Toviaz: Informe público europeo de evaluación, revisión 3 - Publicado el 02/06/08". Agencia Europea de Medicamentos . 2 de junio de 2008. Archivado desde el original el 1 de abril de 2008.
- ^ "Toviaz (fumarato de fesoterodina) de Pfizer recibe la aprobación de la FDA para el tratamiento de la vejiga hiperactiva" (Comunicado de prensa). Pfizer Inc. 2008-10-31. Archivado desde el original el 2018-09-20 . Consultado el 2008-11-06 .
- ^ "Notificación de decisión para TOVIAZ". Archivado desde el original el 23 de abril de 2012. Consultado el 20 de abril de 2012 .
- ^ ab Vella M, Cardozo L (septiembre de 2011). "Revisión de fesoterodina". Opinión de expertos sobre seguridad de medicamentos . 10 (5): 805–8. doi :10.1517/14740338.2011.591377. PMID 21639817. S2CID 9653506.
- ^ " Sato N, Fuji K, Ogawa Y (2017). "Transacciones de la Sociedad de la Universidad Showa: La 335.ª reunión". Revista de Ciencias Médicas de la Universidad Showa . 29 (2): 201–217. doi : 10.15369/sujms.29.201 . ISSN 2185-0968.

