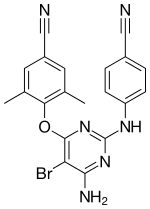
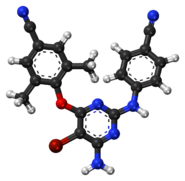
Etravirina
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Inteligencia |
| Otros nombres | TMC125 |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a608016 |
| Datos de licencia |
|
Categoría de embarazo |
|
| Vías de administración | Por la boca |
| Código ATC |
|
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Unión de proteínas | 99,9% |
| Metabolismo | Hígado ( mediado por CYP3A4 , CYP2C9 y CYP2C19 ) |
| Vida media de eliminación | 41±20 horas |
| Excreción | Heces (93,7%), orina (1,2%) |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| Química biológica | |
| Base de datos de sustancias químicas del NIAID |
|
| Ligando PDB |
|
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.207.546 |
| Datos químicos y físicos | |
| Fórmula | C20H15BrN6O |
| Masa molar | 435,285 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La etravirina ( ETR , [3] ), vendida bajo la marca Intelence, es un medicamento antirretroviral utilizado para el tratamiento del VIH . [1] La etravirina es un inhibidor no nucleósido de la transcriptasa inversa (NNRTI) del virus de inmunodeficiencia humana tipo 1 (VIH-1) . [1] A diferencia de los agentes de la clase, la resistencia a otros NNRTI no parece conferir resistencia a la etravirina. [4] La etravirina es comercializada por Janssen , una subsidiaria de Johnson & Johnson . En enero de 2008, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó su uso para personas con resistencia establecida a otros medicamentos, lo que lo convirtió en el 30.º medicamento contra el VIH aprobado en los Estados Unidos y el primero en ser aprobado en 2008. [5] También fue aprobado para su uso en Canadá en abril de 2008. [6]
La etravirina está autorizada en Estados Unidos, Canadá, Israel, Rusia, Australia, Nueva Zelanda y la Unión Europea [7] y está bajo revisión regulatoria en Suiza. [8]
Usos médicos
En los EE. UU., la etravirina está indicada para el tratamiento de la infección por VIH-1 en pacientes con experiencia en tratamiento de dos años de edad o más. [1]
En la UE, la etravirina, en combinación con un inhibidor de la proteasa potenciado y otros antirretrovirales, está indicada para el tratamiento de la infección por el virus de inmunodeficiencia humana tipo 1 (VIH-1) en personas de seis años de edad o más que hayan recibido tratamiento antirretroviral con anterioridad. [2]
Contraindicación
Las personas con problemas hereditarios raros de intolerancia a la galactosa , deficiencia de lactasa de Lapp o malabsorción de glucosa o galactosa no deben tomar este etravine. [9]
Efectos adversos
En 2009, la información de prescripción de la FDA para etravirina se modificó para incluir "informes posteriores a la comercialización de casos de síndrome de Stevens-Johnson , necrólisis epidérmica tóxica y eritema multiforme , así como reacciones de hipersensibilidad caracterizadas por erupción cutánea, hallazgos constitucionales y, a veces, disfunción orgánica, incluida insuficiencia hepática ". [10]
Mecanismo de acción
La etravirina es un inhibidor no nucleósido de la transcriptasa inversa (INNTI) de segunda generación , diseñado para ser activo contra el VIH con mutaciones que confieren resistencia a los dos INNTI de primera generación más comúnmente prescritos, la mutación K103N para efavirenz y la Y181C para nevirapina . [11] Esta potencia parece estar relacionada con la flexibilidad de la etravirina como molécula. La etravirina es una diarilpirimidina (DAPY), un tipo de molécula orgánica con cierta isomería conformacional que puede unirse a la enzima transcriptasa inversa en múltiples conformaciones , lo que permite una interacción más robusta entre la etravirina y la enzima, incluso en presencia de mutaciones. [12]
Química
La etravina se forma como cristales ortorrómbicos incoloros en el grupo espacial Pna2 1 . [13] Se han informado las estructuras de estos y de varias formas de solvato y sal. [13] [14]
Investigación
Se ha estudiado el uso de etravina en aplicaciones de reposicionamiento de fármacos . Se ha demostrado que la etravirina provoca un aumento en la producción de frataxina . [15]
Referencias
- ^ abcd "Intelence-comprimido de etravirina". DailyMed . 15 de agosto de 2023 . Consultado el 14 de agosto de 2024 .
- ^ ab "Intelence EPAR". Agencia Europea de Medicamentos (EMA) . 28 de agosto de 2008. Consultado el 14 de agosto de 2024 .El texto se ha copiado de esta fuente, cuyos derechos de autor pertenecen a la Agencia Europea de Medicamentos. Se autoriza la reproducción siempre que se cite la fuente.
- ^ "Apéndice A: Clave de acrónimos". Pautas para el uso de agentes antirretrovirales en adultos y adolescentes infectados por el VIH-1 . Departamento de Salud y Servicios Humanos . Archivado desde el original el 31 de agosto de 2012.
- ^ Stellbrink HJ (octubre de 2007). "Medicamentos antivirales en el tratamiento del SIDA: ¿qué hay en desarrollo?". Revista Europea de Investigación Médica . 12 (9): 483–495. PMID 17933730.
- ^ "La FDA aprueba el fármaco contra el VIH etravirina". Associated Press . 18 de enero de 2008.[ enlace muerto ]
- ^ "El primer nuevo INNTI en casi una década en beneficio de los canadienses con VIH/SIDA" (PDF) (Comunicado de prensa). Janssen-Ortho Inc. 1 de abril de 2008. Archivado desde el original (PDF) el 2 de noviembre de 2010. Consultado el 9 de julio de 2008 .
- ^ "Intelence recibe autorización de comercialización en la Unión Europea para la terapia combinada contra el VIH". Tibotec. Archivado desde el original el 28 de septiembre de 2011. Consultado el 29 de agosto de 2008 .
- ^ "Etravirina (TMC125, Intelence) obtuvo aprobación acelerada en EE.UU." aidsmap . Archivado desde el original el 2 de enero de 2010 . Consultado el 24 de enero de 2008 .
- ^ "Etravine: Resumen de las características del producto" (PDF) . EMEA . p. 5. Archivado desde el original (PDF) el 20 de agosto de 2016 . Consultado el 13 de julio de 2011 .
- ^ "Información de seguridad de Medwatch de la FDA". Administración de Alimentos y Medicamentos . Consultado el 27 de agosto de 2009 .[ enlace muerto ]
- ^ Evans D (15 de enero de 2008). "Etravirina: cuenta regresiva para el lanzamiento". AIDSmeds.com. Archivado desde el original el 19 de enero de 2008. Consultado el 2 de febrero de 2008 .
- ^ Das K, Clark AD, Lewi PJ, Heeres J, De Jonge MR, Koymans LM, et al. (mayo de 2004). "Funciones de la adaptabilidad conformacional y posicional en el diseño basado en la estructura de TMC125-R165335 (etravirina) e inhibidores no nucleósidos de la transcriptasa inversa relacionados que son altamente potentes y eficaces contra variantes del VIH-1 resistentes a fármacos y de tipo salvaje". Journal of Medicinal Chemistry . 47 (10): 2550–2560. doi :10.1021/jm030558s. PMID 15115397.
- ^ ab Rajput L, Sanphui P, Desiraju GR (7 de agosto de 2013). "Nuevas formas sólidas del fármaco anti-VIH etravirina: sales, cocristales y solubilidad". Crecimiento y diseño de cristales . 13 (8): 3681–3690. doi :10.1021/cg4007058. ISSN 1528-7483.
- ^ Muresan-Pop M, Macavei S, Turza A, Borodi G (noviembre de 2021). "Nuevos solvatos y una sal del compuesto anti-VIH etravirina". Acta Crystallographica Sección C: Química estructural . 77 (Pt 11): 698–706. doi :10.1107/S2053229621010482. PMID 34738540. S2CID 243761396.
- ^ Alfedi G, Luffarelli R, Condò I, Pedini G, Mannucci L, Massaro DS, et al. (Marzo de 2019). "El cribado de reposicionamiento de fármacos identifica a la etravirina como un potencial terapéutico para la ataxia de Friedreich". Trastornos del movimiento . 34 (3): 323–334. doi :10.1002/mds.27604. PMID 30624801. S2CID 58567610.

