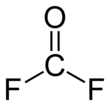
Fluoruro de carbonilo
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Difluoruro de carbonilo | |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.005.941 | ||
| Número CE |
| ||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
| Número de la ONU | 2417 | ||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| COF 2 | |||
| Masa molar | 66,007 g·mol −1 | ||
| Apariencia | Gas incoloro | ||
| Olor | Picante y muy irritante [1] | ||
| Densidad | 2,698 g/L (gas), 1,139 g/cm 3 (líquido en el punto de fusión) | ||
| Punto de fusión | -111,26 °C (-168,27 °F; 161,89 K) | ||
| Punto de ebullición | -84,57 °C (-120,23 °F; 188,58 K) | ||
| Reacciona [2] | |||
| Presión de vapor | 55,4 atm (20 °C) [2] | ||
| Estructura | |||
| C2v | |||
| 0,95 D | |||
| Peligros | |||
| Seguridad y salud en el trabajo (SST/OHS): | |||
Principales peligros | Muy tóxico, reacciona con el agua para liberar HF. | ||
| Etiquetado SGA : | |||
   | |||
| Peligro | |||
| H290 , H314 , H330 , H370 | |||
| P234 , P260 , P261 , P264 , P270 , P271 , P280 , P284 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P307+P311 , P310 , P311 , P320 , P321 , P363 , P390 , P403+P233 , P404 , P405 , P410+P403 , P501 | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | Ininflamable | ||
| NIOSH (límites de exposición a la salud en EE. UU.): | |||
PEL (Permisible) | ninguno [2] | ||
REL (recomendado) | TWA 2 ppm (5 mg/m3 ) ST 5 ppm (15 mg/m3 ) [ 2] | ||
IDLH (Peligro inmediato) | Dakota del Norte [2] | ||
| Compuestos relacionados | |||
Compuestos relacionados | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El fluoruro de carbonilo es un compuesto químico con la fórmula C O F 2 . Es un oxohaluro de carbono . Este gas, al igual que su análogo fosgeno , es incoloro y altamente tóxico. La molécula es plana con simetría C 2v , longitudes de enlace de 1,174 Å (C=O) y 1,312 Å (C–F), y un ángulo de enlace F–C–F de 108,0°. [3]
Preparación y propiedades
El fluoruro de carbonilo se produce generalmente como producto de descomposición de hidrocarburos fluorados en la descomposición térmica de los mismos, por ejemplo a partir de trifluorometanol o tetrafluorometano en presencia de agua:
- CF4 + H2O → COF2 + 2HF
El fluoruro de carbonilo también se puede preparar mediante la reacción del fosgeno con fluoruro de hidrógeno y la fluoración del monóxido de carbono , aunque esta última tiende a dar lugar a una sobrefluoración a tetrafluoruro de carbono . La fluoración del monóxido de carbono con difluoruro de plata es conveniente:
- CO2 + 2 AgF2 → COF2 + 2 AgF
El fluoruro de carbonilo es inestable en presencia de agua y se hidroliza a dióxido de carbono y fluoruro de hidrógeno : [4]
- COF2 + H2O → CO2 + 2HF
Seguridad
El fluoruro de carbonilo es muy tóxico, con un límite de exposición recomendado de 2 ppm como promedio ponderado en el tiempo de 8 horas y de 5 ppm como exposición a corto plazo (promedio de 15 minutos), donde 1 ppm = 2,70 mg de fluoruro de carbonilo por 1 m 3 de aire. [1]
Referencias
- ^ ab "Fluoruro de carbonilo". Guía de bolsillo de NIOSH sobre peligros químicos . CDC Centros para el Control y la Prevención de Enfermedades . Consultado el 10 de septiembre de 2013 .
- ^ abcde Guía de bolsillo del NIOSH sobre peligros químicos. "#0108". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ Greenwood, Norman N. ; Earnshaw, Alan (1997). Química de los elementos (2.ª ed.). Butterworth-Heinemann . págs. 304–305. ISBN 978-0-08-037941-8.
- ^ MW Farlow; EH Man; CW Tullock (1960). "Fluoruro de carbonilo". Síntesis inorgánicas . Síntesis inorgánicas. Vol. 6. págs. 155-158. doi :10.1002/9780470132371.ch48. ISBN 9780470132371.