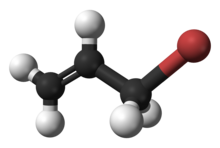
Bromuro de alilo
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC preferido 3-Bromoprop-1-eno | |
| Otros nombres Bromuro de alilo 3-bromopropeno 3-bromopropileno 3-bromo-1-propeno Bromoalileno Bromuro de 2-propenilo | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| Araña química | |
| Tarjeta informativa de la ECHA | 100.003.134 |
| Número CE |
|
Identificador de centro de PubChem |
|
| Número RTECS |
|
| UNIVERSIDAD | |
| Número de la ONU | 1099 |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C3H5Br | |
| Masa molar | 120,977 g·mol −1 |
| Apariencia | Líquido transparente a amarillo claro. |
| Olor | Desagradable, irritante, picante. |
| Densidad | 1,398 g/ cm3 |
| Punto de fusión | -119 °C (-182 °F; 154 K) |
| Punto de ebullición | 71 °C (160 °F; 344 K) |
| 0,38 g/100 g de H2O [ 1 ] | |
| registro P | 1.79 [1] |
| Presión de vapor | 18,6 kPa |
| −58,6·10 −6 cm3 · mol −1 [1] | |
Índice de refracción ( n D ) | 1,4697 (20 °C, 589,2 nm) |
| Viscosidad | 0,471 cP [1] |
| ≈1,9 D [1] | |
| Termoquímica | |
Entalpía estándar de formación (Δ f H ⦵ 298 ) | 12,2 kJ·mol −1 (líquido) 45,2 kJ·mol −1 (gas) [1] |
Entalpía de vaporización (Δ f H vap ) | 32,73 kJ·mol −1 [1] |
| Peligros | |
| Etiquetado SGA : | |
     | |
| Peligro | |
| H225 , H301 , H314 , H330 , H331 , H340 , H350 , H400 | |
| P201 , P202 , P210 , P233 , P240 , P241 , P242 , P243 , P260 , P261 , P264 , P270 , P271 , P273 , P280 , P281 , P284 , P301+P310 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P308+P313 , P310 , P311 , P320 , P321 , P330 , P363 , P370+P378 , P391 , P403+P233 , P403+P235 , P405 , P501 | |
| NFPA 704 (rombo cortafuegos) | |
| punto de inflamabilidad | -2 a -1 °C |
| 280 °C (536 °F; 553 K) | |
| Límites de explosividad | 4,3–7,3 % |
Valor límite umbral (TLV) | 0,1 ppm [1] (promedio ponderado en el tiempo), 0,2 ppm [1] (límite de exposición profesional) |
| Ficha de datos de seguridad (FDS) | Hojas de datos de seguridad de materiales en la Universidad de Oxford |
| Compuestos relacionados | |
Compuestos relacionados | Cloruro de alilo Yoduro de alilo |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
El bromuro de alilo ( 3-bromopropeno ) es un haluro orgánico . Es un agente alquilante utilizado en la síntesis de polímeros, productos farmacéuticos, perfumes [2] y otros compuestos orgánicos. El bromuro de alilo es un líquido incoloro, aunque las muestras comerciales aparecen de color amarillo o marrón. Es un agente alquilante irritante y potencialmente peligroso . El bromuro de alilo es más reactivo pero más caro que el cloruro de alilo , y estas consideraciones guían su uso. [3]
Preparación
Hidrohalogenación
El bromuro de alilo se produce comercialmente a partir de alcohol alílico y ácido bromhídrico : [3]
- CH2 = CHCH2OH + HBr → CH2 = CHCH2Br + H2O
También se puede preparar mediante la reacción de intercambio de halógeno entre cloruro de alilo y ácido bromhídrico o mediante la bromación alílica del propeno . [3]
Reacciones y usos
El bromuro de alilo es un agente alquilante electrofílico. [4] Reacciona con nucleófilos , como aminas , carbaniones , alcóxidos , etc., para introducir el grupo alilo :
- CH 2 =CHCH 2 Br + Nu − → CH 2 =CHCH 2 Nu + Br − (Nu − es un nucleófilo)
Se utiliza en la síntesis de compuestos que contienen la funcionalidad alílica, como los productos farmacéuticos metohexital , secobarbital y tiamilal . [3]
El bromuro de alilo reacciona con el metal magnesio en éter seco para formar bromuro de alilmagnesio , un reactivo de Grignard: [5]
- CH2 = CHCH2Br + Mg → CH2 = CHCH2MgBr
Referencias
- ^ abcdefghi Haynes, William M.; Lide, David R.; Bruno, Thomas J. (2016). Manual de química y física del CRC: un libro de referencia rápida de datos químicos y físicos (2016-2017, 97.ª ed.). Boca Raton, Florida. ISBN 978-1-4987-5428-6. OCLC 930681942.
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) - ^ PubChem. "Banco de datos de sustancias peligrosas (HSDB): 622". pubchem.ncbi.nlm.nih.gov . Consultado el 4 de marzo de 2022 .
- ^ abcd Yoffe, David; Frim, Ron; Ukeles, Shmuel D.; Dagani, Michael J.; Barda, Henry J.; Benya, Theodore J.; Sanders, David C. (2013). "Compuestos de bromo". Ullmann's Encyclopedia of Industrial Chemistry . págs. 1–31. doi :10.1002/14356007.a04_405.pub2. ISBN 978-3-527-30385-4.
- ^ Bolton, Roger (15 de abril de 2001), "Bromuro de alilo", en John Wiley & Sons, Ltd (ed.), Enciclopedia de reactivos para síntesis orgánica , Chichester, Reino Unido: John Wiley & Sons, Ltd, págs. ra045, doi :10.1002/047084289x.ra045, ISBN 978-0-471-93623-7, consultado el 4 de marzo de 2022
- ^ Mazerolles, Pierre; Boussaguet, Paul; Huc, Vicente (1999). "6-cloro-1-hexeno y 8-cloro-1-octeno". Síntesis orgánicas . 76 : 221. doi : 10.15227/orgsyn.076.0221.
Enlaces externos
- Entrada en chemicalland21.com



