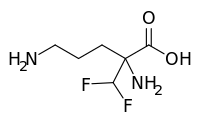
Eflornitina
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Vaniqa, Iwilfin, otros |
| Otros nombres | α-difluorometilornitina o DFMO |
| AHFS / Drogas.com | Monografía |
| Datos de licencia |
|
| Vías de administración | intravenoso , tópico |
| Código ATC | |
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | 100% (intravenoso) Insignificante (tópico) |
| Metabolismo | No metabolizado |
| Vida media de eliminación | 8 horas |
| Excreción | Riñón |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh | |
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Datos químicos y físicos | |
| Fórmula | C6H12F2N2O2 |
| Masa molar | 182,171 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La eflornitina , que se vende bajo la marca Vaniqa , entre otras, es un medicamento que se utiliza para tratar la tripanosomiasis africana (enfermedad del sueño) y el crecimiento excesivo de vello facial en las mujeres. [1] [3] [4] Específicamente, se utiliza para la segunda etapa de la enfermedad del sueño causada por T. b. gambiense y se puede utilizar con nifurtimox . [3] [5] Se toma por vía intravenosa (inyección en una vena) o tópica . [3] [4] Es un inhibidor de la ornitina descarboxilasa . [2]
Los efectos secundarios comunes cuando se aplica como crema incluyen sarpullido, enrojecimiento y ardor. [4] Los efectos secundarios de la forma inyectable incluyen supresión de la médula ósea , vómitos y convulsiones . [5] No está claro si es seguro usarlo durante el embarazo o la lactancia . [5] Se recomienda generalmente para niños mayores de 12 años. [5]
La eflornitina se desarrolló en la década de 1970 y comenzó a usarse con fines médicos en 1990. [6] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [7] En los Estados Unidos, la forma inyectable se puede obtener en los Centros para el Control y la Prevención de Enfermedades de EE. UU . [5] En las regiones del mundo donde la enfermedad es común, la eflornitina es proporcionada de forma gratuita por la Organización Mundial de la Salud . [8]
Usos médicos
Enfermedad del sueño
La enfermedad del sueño, o tripanosomiasis, se trata con pentamidina o suramina (dependiendo de la subespecie del parásito) administradas por inyección intramuscular en la primera fase de la enfermedad, y con melarsoprol y eflornitina por inyección intravenosa en la segunda fase de la enfermedad. La efornitina se administra comúnmente en combinación con nifurtimox , lo que reduce el tiempo de tratamiento a 7 días de infusiones de eflornitina más 10 días de comprimidos orales de nifurtimox. [9]
La eflornitina también es eficaz en combinación con otros fármacos, como el melarsoprol y el nifurtimox. Un estudio de 2005 comparó la seguridad de la eflornitina sola con el melarsoprol y descubrió que la eflornitina era más eficaz y segura en el tratamiento de la enfermedad del sueño de segunda etapa Trypanosoma brucei gambiense . [10] La eflornitina no es eficaz en el tratamiento de Trypanosoma brucei rhodesiense debido a la baja sensibilidad del parásito al fármaco. En cambio, se utiliza melarsoprol para tratar Trypanosoma brucei rhodesiense . [11] Otro ensayo controlado aleatorio en Uganda comparó la eficacia de varias combinaciones de estos fármacos y descubrió que la combinación de nifurtimox y eflornitina era el régimen teórico de primera línea más prometedor. [12]
Se realizó un ensayo controlado aleatorio en Congo, Costa de Marfil, la República Democrática del Congo y Uganda para determinar si un régimen intravenoso de 7 días era tan eficaz como el régimen estándar de 14 días para los casos nuevos y recidivantes. Los resultados mostraron que el régimen acortado era eficaz en los casos de recaída, pero era inferior al régimen estándar para los casos nuevos de la enfermedad. [13]
El tratamiento combinado con nifurtimox-eflornitina (NECT) es un régimen eficaz para el tratamiento de la tripanosomiasis africana gambiense de segunda etapa . [14] [15]
Resistencia a los tripanosomas
Después de su introducción en el mercado en la década de 1980, la eflornitina ha reemplazado al melarsoprol como el medicamento de primera línea contra la tripanosomiasis africana humana (HAT) debido a su toxicidad reducida para el huésped. [13] La resistencia a la eflornitina del Trypanosoma brucei se informó ya a mediados de la década de 1980. [13]
Se cree que el gen TbAAT6, conservado en el genoma de los tripanosomas, es responsable del transportador transmembrana que lleva la eflornitina a la célula. [16] La pérdida de este gen debido a mutaciones específicas provoca resistencia a la eflornitina en varios tripanosomas. [17] Si se prescribe eflornitina a un paciente con tripanosomiasis africana humana causada por un tripanosoma que contiene un gen TbAAT6 mutado o ineficaz, entonces el medicamento será ineficaz contra la enfermedad. La resistencia a la eflornitina ha aumentado el uso de melarsoprol a pesar de su toxicidad, que se ha relacionado con la muerte del 5% de los pacientes receptores de TAH. [13]
Exceso de vello facial en mujeres
La crema tópica está indicada para el tratamiento del hirsutismo facial en mujeres. [1] [18] Es el único tratamiento tópico con prescripción que retarda el crecimiento del vello facial. [19] En estudios clínicos con Vaniqa, el 81% de las mujeres mostraron una mejoría clínica después de doce meses de tratamiento. [20] Se observaron resultados positivos después de ocho semanas. [21] Sin embargo, la interrupción de la crema provocó que el vello volviera a crecer a los niveles iniciales en 8 semanas. [22]
El tratamiento con Vaniqa reduce significativamente la carga psicológica del hirsutismo facial. [23]
Neuroblastoma
En los EE. UU., la eflornitina está indicada para reducir el riesgo de recaída en personas con neuroblastoma de alto riesgo. [2]
Contraindicaciones
Actual
El uso tópico está contraindicado en personas hipersensibles a la eflornitina o a alguno de los excipientes. [24]
A lo largo de los ensayos clínicos, los datos de un número limitado de embarazos expuestos indican que no hay evidencia clínica de que el tratamiento con Vaniqa afecte negativamente a las mujeres embarazadas o a los fetos. [24]
Administración oral
Cuando se administra por vía oral, se debe evaluar el riesgo-beneficio en personas con deterioro de la función renal o anomalías hematológicas preexistentes, así como en aquellas con deterioro del octavo nervio craneal. [25] No se han realizado estudios adecuados y bien controlados con eflornitina en relación con el embarazo en humanos. La eflornitina solo se debe utilizar durante el embarazo si el beneficio potencial supera el riesgo potencial para el feto. Sin embargo, dado que la tripanosomiasis africana tiene una alta tasa de mortalidad si no se trata, el tratamiento con eflornitina puede justificar cualquier riesgo potencial para el feto. [25]
Efectos secundarios
La eflornitina no es genotóxica; no se han observado efectos inductores de tumores en estudios de carcinogenicidad , incluido un estudio de fotocarcinogenicidad. [26] No se han detectado efectos teratogénicos . [27]
Actual
La forma tópica de elflornitina se vende bajo la marca Vaniqa. El efecto secundario más frecuente es el acné (7-14%). Otros efectos secundarios más frecuentes (> 1%) son problemas cutáneos, como reacciones cutáneas por pelos encarnados, caída del cabello, sensación de ardor, escozor u hormigueo, piel seca, picazón, enrojecimiento o sarpullido. [28]
Intravenoso
La forma de dosificación intravenosa de eflornitina se vende bajo la marca Ornidyl. La mayoría de los efectos secundarios relacionados con el uso sistémico a través de inyecciones son transitorios y reversibles al suspender el fármaco o disminuir la dosis. Las anomalías hematológicas ocurren con frecuencia, en un rango de 10 a 55%. Estas anomalías están relacionadas con la dosis y generalmente son reversibles. Se cree que la trombocitopenia se debe a un defecto de producción más que a una destrucción periférica. Se observaron convulsiones en aproximadamente el 8% de los pacientes, pero pueden estar relacionadas con el estado de la enfermedad más que con el fármaco. Se ha producido pérdida auditiva reversible en el 30-70% de los pacientes que reciben terapia a largo plazo (más de 4-8 semanas de terapia o una dosis total de >300 gramos); la audición de alta frecuencia se pierde primero, seguida de la audición de frecuencia media y baja. Debido a que el tratamiento para la tripanosomiasis africana es a corto plazo, es poco probable que los pacientes experimenten pérdida auditiva. [28]
Interacciones
Actual
No se han realizado estudios de interacción con la forma tópica. [24]
Mecanismo de acción
Descripción
La eflornitina es un " inhibidor suicida " que se une irreversiblemente a la ornitina descarboxilasa (ODC) e impide que el sustrato natural ornitina acceda al sitio activo (Figura 1). Dentro del sitio activo de la ODC, la eflornitina sufre una descarboxilación con la ayuda del cofactor piridoxal 5'-fosfato (PLP). Debido a su grupo difluorometilo adicional en comparación con la ornitina, la eflornitina puede unirse a un residuo Cys-360 vecino, permaneciendo permanentemente fijada dentro del sitio activo. [27]
Durante la reacción, el mecanismo de descarboxilación de la eflornitina es análogo al de la ornitina en el sitio activo, donde se produce la transaminación con PLP seguida de la descarboxilación. Durante el evento de descarboxilación, los átomos de fluoruro unidos al grupo metilo adicional extraen la carga negativa resultante de la liberación de dióxido de carbono, lo que hace que se libere un ion fluoruro. En el sustrato natural de ODC, el anillo de PLP acepta los electrones que resultan de la liberación de CO 2 . [ cita requerida ]
El átomo de fluoruro restante que se encuentra unido al grupo metilo adicional crea un carbono electrófilo que es atacado por el grupo tiol cercano de Cys-360, lo que permite que la eflornitina permanezca unida permanentemente a la enzima después de la liberación del segundo átomo de fluoruro y la transiminación.
Evidencia
El mecanismo de reacción de la ODC de Trypanosoma brucei con ornitina se caracterizó por espectroscopia UV-VIS para identificar intermediarios únicos que ocurrieron durante la reacción. El método específico de espectroscopia de flujo detenido de longitud de onda múltiple utilizó luz monocromática y fluorescencia para identificar cinco intermediarios específicos debido a cambios en las mediciones de absorbancia. [29] El número de recambio de estado estable, k cat , de ODC se calculó en 0,5 s −1 a 4 °C. [29] A partir de esta caracterización, se determinó que el paso limitante de la velocidad era la liberación del producto putrescina de la reacción de ODC con ornitina. Al estudiar el mecanismo de reacción hipotético para la eflornitina, la información recopilada del mapeo de péptidos radiactivos y eflornitina, cromatografía líquida de alta presión y secuenciación de péptidos en fase gaseosa sugirió que Lys-69 y Cys-360 están unidas covalentemente a la eflornitina en el sitio activo de ODC de T. brucei . [30] Utilizando espectrometría de masas de bombardeo de átomos rápidos (FAB-MS), se determinó que la conformación estructural de la eflornitina después de su interacción con ODC era ( S )-((2-(1-pirrolina-metil) cisteína, un aducto de imina cíclica. La presencia de este producto en particular fue apoyada por la posibilidad de reducir aún más el producto final a ( S )-((2-pirrol) metil) cisteína en presencia de NaBH 4 y oxidar el producto final a ( S )-((2-pirrolidina) metil) cisteína (Figura 2). [30]
Sitio activo
La inhibición suicida de la ODC por parte de la eflornitina impide físicamente que el sustrato natural ornitina acceda al sitio activo de la enzima (Figura 3). [27] Existen dos sitios activos distintos formados por la homodimerización de la ornitina descarboxilasa. El tamaño de la abertura hacia el sitio activo es de aproximadamente 13,6 Å. Cuando estas aberturas hacia el sitio activo están bloqueadas, no hay otras formas a través de las cuales la ornitina pueda ingresar al sitio activo. Durante la etapa intermedia de la eflornitina con PLP, su posición cerca de Cys-360 permite que se produzca una interacción. Como el fosfato de PLP se estabiliza mediante Arg 277 y un bucle rico en Gly (235-237), el grupo difluorometilo de la eflornitina puede interactuar y permanecer fijado tanto a Cys-360 como a PLP antes de la transiminación. Como se muestra en la figura, el anillo de pirrolina interfiere con la entrada de la ornitina (Figura 4). La eflornitina permanecerá unida permanentemente en esta posición a Cys-360. Como la ODC tiene dos sitios activos, se requieren dos moléculas de eflornitina para inhibir completamente la ODC de la descarboxilación de la ornitina.
- Figura 1
(A) Estructura 3D de la L-ornitina (B) Estructura 3D de la eflornitina. Esta molécula es similar a la estructura de la L-ornitina, pero su grupo alfa-difluorometilo permite la interacción con Cys-360 en el sitio activo. - Mecanismo de reacción de la ODC de eflornitina
- Figura 2
Evidencia experimental del producto final eflornitina [30] - Figura 3
Sitio activo de ODC formado por homodimerización (estructuras superficiales verdes y blancas) (A) Ornitina en el sitio activo de ODC, Cys-360 resaltada en amarillo (B) Producto de la descarboxilación de eflornitina unido a Cys 360 (resaltado en amarillo). El anillo de pirrolina impide que la ornitina entre al sitio activo [31]
Historia
La eflornitina se desarrolló inicialmente para el tratamiento del cáncer en el Instituto de Investigación Merrell Dow a fines de la década de 1970, pero se descubrió que no era eficaz para tratar las neoplasias malignas. Sin embargo, se descubrió que era muy eficaz para reducir el crecimiento del cabello, [32] así como para el tratamiento de la tripanosomiasis africana (enfermedad del sueño), [33] especialmente la forma de África occidental (Trypanosoma brucei gambiense).
Hirsutismo
En la década de 1980, Gillette obtuvo una patente por el descubrimiento de que la aplicación tópica de la crema de clorhidrato de eflornitina inhibe el crecimiento del vello. En la década de 1990, Gillette realizó estudios de determinación de dosis con eflornitina en mujeres con vello facial que demostraron que el fármaco ralentiza el ritmo de crecimiento del vello facial. Gillette presentó entonces una patente para la formulación de la crema de eflornitina. En julio de 2000, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) concedió una solicitud de nuevo fármaco para Vaniqa. Al año siguiente, la Comisión Europea emitió su autorización de comercialización. [ cita requerida ]
Tratamiento de la enfermedad del sueño
El medicamento fue registrado para el tratamiento de la enfermedad del sueño gambiense el 28 de noviembre de 1990. [11] Sin embargo, en 1995 Aventis (ahora Sanofi-Aventis) dejó de producir el medicamento, cuyo principal mercado eran los países africanos, porque no obtenía beneficios. [34]
En 2001, Aventis y la OMS formaron una asociación de cinco años, durante la cual Aventis produjo más de 320.000 viales de pentamidina, más de 420.000 viales de melarsoprol y más de 200.000 botellas de eflornitina, para ser donadas a la OMS y distribuidas por la asociación Médicos sin Fronteras (también conocida como Médicos Sin Fronteras) [35] [36] en países donde la enfermedad del sueño es endémica.
Según Médicos Sin Fronteras, esto sólo ocurrió después de "años de presión internacional" y coincidiendo con el período en que se generó atención mediática debido al lanzamiento de otro producto a base de eflornitina (Vaniqa, para la prevención del vello facial en mujeres), [34] mientras que su formulación salvadora de vidas (para la enfermedad del sueño) no se estaba produciendo.
Desde 2001 (cuando se reanudó la producción) hasta 2006, se realizaron 14 millones de diagnósticos, lo que contribuyó en gran medida a frenar la propagación de la enfermedad del sueño y a salvar casi 110.000 vidas. [ cita requerida ]
Sociedad y cultura

Formularios disponibles
Vaniqa es una crema de color blanco a blanquecino que se comercializa en tubos de 30 g y 60 g en Europa. [28] Vaniqa contiene un 15 % p/p de clorhidrato de eflornitina monohidrato, lo que corresponde a un 11,5 % p/p de eflornitina anhidra (UE) y un 13,9 % p/p de clorhidrato de eflornitina anhidra (EE. UU.), respectivamente, en una crema para administración tópica. [ cita requerida ]
Ornidyl, destinado a ser inyectado, se suministraba en una concentración de 200 mg de clorhidrato de eflornitina por ml. [37]
Mercado
Vaniqa, que ha recibido la aprobación para su comercialización por parte de la FDA de los EE. UU. y de la Comisión Europea [38] , entre otros, es actualmente el único tratamiento tópico con receta que retarda el crecimiento del vello facial. [19] Además de ser un tratamiento no mecánico y no cosmético, es la única opción de prescripción no hormonal y no sistémica disponible para mujeres con hirsutismo facial. [18] Vaniqa es comercializada por Almirall en Europa, SkinMedica en los EE. UU., Triton en Canadá, Medison en Israel y Menarini en Australia. [38]
Ornidyl, la forma inyectable de clorhidrato de eflornitina, está autorizada por Sanofi-Aventis, pero actualmente se encuentra descontinuada en los EE. UU. [39]
Investigación
Terapia preventiva con quimioterapia
Se ha observado que la ornitina descarboxilasa (ODC) exhibe una alta actividad en las células tumorales, promoviendo el crecimiento y la división celular, mientras que la ausencia de actividad de la ODC conduce al agotamiento de la putrescina , causando un deterioro de la síntesis de ARN y ADN. Por lo general, los medicamentos que inhiben el crecimiento celular se consideran candidatos para la terapia del cáncer, por lo que naturalmente se creyó que la eflornitina tenía una utilidad potencial como agente anticancerígeno. Al inhibir la ODC, la eflornitina inhibe el crecimiento y la división celular de células cancerosas y no cancerosas. [ cita requerida ]
Sin embargo, varios ensayos clínicos demostraron resultados menores. [40] Se encontró que la inhibición de ODC por eflornitina no mata las células proliferantes, lo que hace que la eflornitina sea ineficaz como agente quimioterapéutico. La inhibición de la formación de poliaminas por la actividad de ODC se puede mejorar por medios dietéticos y bacterianos porque se encuentran altas concentraciones en el queso, la carne roja y algunas bacterias intestinales, lo que proporciona reservas si se inhibe la ODC. [41] Aunque el papel de las poliaminas en la carcinogénesis aún no está claro, se ha apoyado que la síntesis de poliaminas es más un agente causal en lugar de un efecto asociativo en el cáncer. [40]
Otros estudios han sugerido que la eflornitina puede ayudar en cierta quimioprevención al reducir los niveles de poliaminas en la mucosa colorrectal, y hay evidencia preclínica adicional sólida disponible para la aplicación de eflornitina en la carcinogénesis colorrectal y cutánea. [40] [41] Esto ha hecho que la eflornitina sea una terapia quimiopreventiva respaldada específicamente para el cáncer de colon en combinación con otros medicamentos. Varios estudios adicionales han encontrado que la eflornitina en combinación con otros compuestos disminuye las concentraciones cancerígenas de etilnitrosourea, dimetilhidrazina, azoximetano, metilnitrosourea e hidroxibutilnitrosamina en el cerebro, la médula espinal, el intestino, la glándula mamaria y la vejiga urinaria. [41]
Usos veterinarios
La eflornitina es eficaz en ratones . [42] [43] Bacchi et al. 1980 encontró que el fármaco curaba la infección por T. b. brucei en ratones y, en general, no presenta toxicidad. [42] Klug et al. 2016 [42] opinan que esto demuestra una buena promesa para el tratamiento oral. Sin embargo, aunque Jansson et al. 2008 también trató eficazmente a ratones con él, encontraron que la farmacocinética de la administración oral en ratas era muy negativa. [43] Brun et al. 2010 [43] opinan que los resultados de Jansson han acabado con las perspectivas del tratamiento oral.
Referencias
- ^ abc "Vaniqa- crema de clorhidrato de eflornitina". DailyMed . 18 de septiembre de 2012 . Consultado el 26 de febrero de 2024 .
- ^ abc "Iwilfin-comprimido de clorhidrato de eflornitina". DailyMed . 21 de diciembre de 2023 . Consultado el 26 de febrero de 2024 .
- ^ abc «19.ª Lista Modelo de Medicamentos Esenciales de la OMS (abril de 2015)» (PDF) . OMS. Abril de 2015. Archivado (PDF) del original el 13 de mayo de 2015 . Consultado el 10 de mayo de 2015 .
- ^ abc "Eflornitina". Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud. Archivado desde el original el 20 de diciembre de 2016. Consultado el 28 de noviembre de 2016 .
- ^ abcde «CDC - Tripanosomiasis africana - Recursos para profesionales de la salud». Centros para el Control y la Prevención de Enfermedades (CDC) de Estados Unidos . 10 de agosto de 2016. Archivado desde el original el 28 de noviembre de 2016. Consultado el 6 de diciembre de 2016 .
- ^ Steverding D (2016). "Enfermedad del sueño y enfermedad de Nagana causada por Trypanosoma brucei". En Marcondes CB (ed.). Enfermedades transmitidas por artrópodos . Springer. pág. 292. ISBN 9783319138848Archivado desde el original el 10 de septiembre de 2017.
- ^ Organización Mundial de la Salud (2023). Selección y uso de medicamentos esenciales 2023: anexo web A: Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 23.ª lista (2023) . Ginebra: Organización Mundial de la Salud. hdl : 10665/371090 . OMS/MHP/HPS/EML/2023.02.
- ^ "Trypanosomiasis africana humana (enfermedad del sueño)". Organización Mundial de la Salud . Febrero de 2016. Archivado desde el original el 4 de diciembre de 2016. Consultado el 7 de diciembre de 2016 .
- ^ Babokhov P, Sanyaolu AO, Oyibo WA, Fagbenro-Beyioku AF, Iriemenam NC (julio de 2013). "Un análisis actual de las estrategias de quimioterapia para el tratamiento de la tripanosomiasis africana humana". Patógenos y salud global . 107 (5): 242–252. doi :10.1179/2047773213Y.0000000105. PMC 4001453. PMID 23916333 .
- ^ Priotto G, Fogg C, Balasegaram M, Erphas O, Louga A, Checchi F, et al. (diciembre de 2006). "Tres combinaciones de fármacos para la enfermedad del sueño en etapa avanzada causada por Trypanosoma brucei gambiense: un ensayo clínico aleatorizado en Uganda". PLOS Clinical Trials . 1 (8): e39. doi : 10.1371/journal.pctr.0010039 . PMC 1687208 . PMID 17160135.
- ^ ab Lutje V, Seixas J, Kennedy A (junio de 2013). "Quimioterapia para la tripanosomiasis africana humana en etapa II". Base de datos Cochrane de revisiones sistemáticas . 2013 (6): CD006201. doi :10.1002/14651858.cd006201.pub3. PMC 6532745. PMID 23807762 .
- ^ Chappuis F, Udayraj N, Stietenroth K, Meussen A, Bovier PA (septiembre de 2005). "La eflornitina es más segura que el melarsoprol para el tratamiento de la tripanosomiasis africana humana Trypanosoma brucei gambiense en etapa II". Clinical Infectious Diseases . 41 (5): 748–751. doi : 10.1086/432576 . PMID 16080099.
- ^ abcd Vincent IM, Creek D, Watson DG, Kamleh MA, Woods DJ, Wong PE, et al. (noviembre de 2010). "Un mecanismo molecular para la resistencia a la eflornitina en los tripanosomas africanos". PLOS Pathogens . 6 (11): e1001204. doi : 10.1371/journal.ppat.1001204 . PMC 2991269 . PMID 21124824.
- ^ "Tratamiento combinado con nifurtimox y eflornitina para la enfermedad del sueño (tripanosomiasis africana humana): la OMS concluye la capacitación de personal sanitario clave". Organización Mundial de la Salud. 23 de marzo de 2010. Archivado desde el original el 21 de octubre de 2014.
- ^ Franco JR, Simarro PP, Diarra A, Ruiz-Postigo JA, Samo M, Jannin JG (2012). "Monitoreo del uso de la terapia combinada nifurtimox-eflornitina (NECT) en el tratamiento de la tripanosomiasis africana humana gambiense de segunda etapa". Investigación e informes en medicina tropical . 3 : 93–101. doi : 10.2147/RRTM.S34399 . PMC 6067772 . PMID 30100776.
- ^ Sayé M, Miranda MR, di Girolamo F, de los Milagros Cámara M, Pereira CA (2014). "Proline modulates the Trypanosoma cruzi resistance to reactive oxygen spice and drugs through a novel D,L-proline transporter". PLOS ONE . 9 (3): e92028. Bibcode :2014PLoSO...992028S. doi : 10.1371/journal.pone.0092028 . PMC 3956872 . PMID 24637744.
- ^ Barrett MP, Boykin DW, Brun R, Tidwell RR (diciembre de 2007). "Tripanosomiasis africana humana: reactivación farmacológica de una enfermedad olvidada". British Journal of Pharmacology . 152 (8): 1155–71. doi :10.1038/sj.bjp.0707354. PMC 2441931 . PMID 17618313.
- ^ ab "Perfil de nuevos medicamentos del NHS y UKMi" (PDF) . Archivado desde el original (PDF) el 15 de febrero de 2010.
- ^ ab Balfour JA, McClellan K (junio de 2001). "Eflornitina tópica". American Journal of Clinical Dermatology . 2 (3): 197–201, discusión 202. doi :10.2165/00128071-200102030-00009. PMID 11705097. S2CID 26181011.
- ^ Schrode K, Huber F, Staszak J, et al. (The Eflornithine Study Group) (marzo de 2000). Evaluación de la seguridad a largo plazo de la crema de eflornitina al 15 % en el tratamiento de mujeres con vello facial excesivo, póster 294. 58.ª Reunión Anual de la Academia Estadounidense de Dermatología. San Francisco; EE. UU.
- ^ Schrode K, Huber F, Staszak J, Altman DJ, Shander D, Morton J, et al. (The Eflornithine Study Group) (marzo de 2000). Evaluación de seguridad y eficacia aleatorizada, doble ciego y controlada por vehículo de la crema de eflornitina al 15 % en el tratamiento de mujeres con vello facial excesivo. Póster 291. 58.ª Reunión Anual de la Academia de Dermatología. San Francisco; EE. UU.
- ^ Wolf JE, Shander D, Huber F, Jackson J, Lin CS, Mathes BM, et al. (enero de 2007). "Evaluación clínica aleatorizada y doble ciego de la eficacia y seguridad de la crema tópica de eflornitina HCl al 13,9 % en el tratamiento de mujeres con vello facial". Revista Internacional de Dermatología . 46 (1): 94–98. doi :10.1111/j.1365-4632.2006.03079.x. PMID 17214730. S2CID 10795478.
- ^ Jackson J, Caro JJ, Caro G, Garfield F, Huber F, Zhou W, et al. (Grupo de estudio de flornitina HCl) (septiembre de 2007). "El efecto de la crema de eflornitina al 13,9 % sobre las molestias y el malestar debidos al hirsutismo". Revista internacional de dermatología . 46 (9): 976–81. doi :10.1111/j.1365-4632.2007.03270.x. PMID 17822506. S2CID 25986442.
- ^ abc «Resumen de las características del producto Vaniqa 2008». Archivado desde el original el 5 de diciembre de 2009.
- ^ ab "Información sobre el medicamento Ornidyl". Archivado desde el original el 7 de junio de 2011.
- ^ Malhotra B, Noveck R, Behr D, Palmisano M (septiembre de 2001). "Absorción percutánea y farmacocinética de la crema de clorhidrato de eflornitina al 13,9 % en mujeres con vello facial no deseado". Journal of Clinical Pharmacology . 41 (9): 972–978. doi :10.1177/009127000104100907. PMID 11549102. Archivado desde el original el 12 de noviembre de 2016.
- ^ Monografía del producto abc Vaniqa (PDF) . Cipher Pharmaceuticals Inc. 8 de julio de 2015, a través del Registro de medicamentos y productos sanitarios de Canadá.
- ^ abc "Folleto informativo para pacientes de Vaniqa en EE. UU." (PDF) . Archivado (PDF) del original el 15 de febrero de 2010.
- ^ ab Brooks HB, Phillips MA (diciembre de 1997). "Caracterización del mecanismo de reacción de la ornitina descarboxilasa de Trypanosoma brucei mediante espectroscopia de flujo detenido de múltiples longitudes de onda". Bioquímica . 36 (49): 15147–15155. doi :10.1021/bi971652b. PMID 9398243.
- ^ abc Poulin R, Lu L, Ackermann B, Bey P, Pegg AE (enero de 1992). "Mecanismo de la inactivación irreversible de la ornitina descarboxilasa de ratón por alfa-difluorometilornitina. Caracterización de secuencias en los sitios de unión del inhibidor y la coenzima". The Journal of Biological Chemistry . 267 (1): 150–158. doi : 10.1016/S0021-9258(18)48472-4 . PMID 1730582.
- ^ Grishin NV, Osterman AL, Brooks HB, Phillips MA, Goldsmith EJ (noviembre de 1999). "Estructura de rayos X de la ornitina descarboxilasa de Trypanosoma brucei: la estructura nativa y la estructura en complejo con alfa-difluorometilornitina". Bioquímica . 38 (46): 15174–15184. doi :10.1021/bi9915115. PMID 10563800.
- ^ Wolf JE, Shander D, Huber F, Jackson J, Lin CS, Mathes BM, et al. (enero de 2007). "Evaluación clínica aleatorizada y doble ciego de la eficacia y seguridad de la crema tópica de eflornitina HCl al 13,9 % en el tratamiento de mujeres con vello facial". Revista Internacional de Dermatología . 46 (1): 94–98. doi :10.1111/j.1365-4632.2006.03079.x. PMID 17214730. S2CID 10795478.
- ^ Pepin J, Milord F, Guern C, Schechter PJ (diciembre de 1987). "Difluorometilornitina para la enfermedad del sueño causada por Trypanosoma brucei gambiense resistente al arseno". Lancet . 2 (8573): 1431–1433. doi :10.1016/S0140-6736(87)91131-7. PMID 2891995. S2CID 41019313.
- ^ ab "Confirmado el suministro de medicamentos contra la enfermedad del sueño". Médicos Sin Fronteras . 3 de mayo de 2001. Archivado desde el original el 21 de septiembre de 2015.
- ^ "Folleto de acceso a medicamentos de Sanofi-Aventis" (PDF) . Archivado (PDF) del original el 14 de noviembre de 2008.
- ^ "Iniciativas sanitarias de la IFPMA: enfermedad del sueño". Archivado desde el original el 29 de agosto de 2006.
- ^ "Datos sobre Ornidyl". Archivado desde el original el 20 de julio de 2011.
- ^ ab Programa de Capacitación Vaniqa Módulo 5 (Informe).
- ^ "Drugs@FDA: Productos farmacéuticos aprobados por la FDA". www.accessdata.fda.gov . Archivado desde el original el 13 de agosto de 2014. Consultado el 17 de noviembre de 2016 .
- ^ abc Raul F (abril de 2007). "Reactivación de la 2-(difluorometil)ornitina (DFMO), un inhibidor de la biosíntesis de poliaminas, como agente quimiopreventivo del cáncer". Biochemical Society Transactions . 35 (Pt 2): 353–5. doi :10.1042/BST0350353. PMID 17371277.
- ^ abc Gerner EW, Meyskens FL (octubre de 2004). "Poliaminas y cáncer: moléculas antiguas, nuevos conocimientos". Nature Reviews. Cáncer . 4 (10): 781–792. doi :10.1038/nrc1454. PMID 15510159. S2CID 37647479.
- ^ abc Klug DM, Gelb MH, Pollastri MP (junio de 2016). "Estrategias de reutilización para el descubrimiento de fármacos contra enfermedades tropicales". Bioorganic & Medicinal Chemistry Letters . 26 (11). Elsevier : 2569–2576. doi :10.1016/j.bmcl.2016.03.103. PMC 4853260 . PMID 27080183. Documento sin fecha.
- ^ abc Büscher P, Cecchi G, Jamonneau V, Priotto G (noviembre de 2017). "Tripanosomiasis africana humana". Lanceta . 390 (10110). Elsevier : 2397–2409. doi :10.1016/s0140-6736(09)60829-1. PMID 28673422. S2CID 4853616.
Enlaces externos
 Medios relacionados con Eflornitina en Wikimedia Commons
Medios relacionados con Eflornitina en Wikimedia Commons- Número de ensayo clínico NCT02395666 para "Ensayo preventivo de difluorometilornitina (DFMO) en pacientes de alto riesgo con neuroblastoma en remisión" en ClinicalTrials.gov
- Número de ensayo clínico NCT02679144 para "Ensayo de terapia de mantenimiento del neuroblastoma (NMTT)" en ClinicalTrials.gov


![Figura 2 Evidencia experimental del producto final eflornitina[30]](http://upload.wikimedia.org/wikipedia/commons/thumb/f/f0/DFMO_inhibitor_product_evidence.svg/192px-DFMO_inhibitor_product_evidence.svg.png)
![Figura 3 Sitio activo de ODC formado por homodimerización (estructuras superficiales verdes y blancas) (A) Ornitina en el sitio activo de ODC, Cys-360 resaltada en amarillo (B) Producto de la descarboxilación de eflornitina unido a Cys 360 (resaltado en amarillo). El anillo de pirrolina impide que la ornitina entre al sitio activo[31]](http://upload.wikimedia.org/wikipedia/commons/thumb/3/33/Eflornithine_in_the_Active_Site.png/121px-Eflornithine_in_the_Active_Site.png)

