Ácido propiónico
| |||
| |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Ácido propanoico | |||
| Otros nombres Ácido carboximetánico Ácido etanocarboxílico Ácido etilfórmico Ácido metacetónico Ácido metilacético C3:0 ( Números lipídicos ) | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Banco de medicamentos | |||
| Tarjeta informativa de la ECHA | 100.001.070 | ||
| Número CE |
| ||
| Número E | E280 (conservantes) | ||
| |||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| Propiedades | |||
| C3H6O2 | |||
| Masa molar | 74,079 g·mol −1 | ||
| Apariencia | Líquido aceitoso e incoloro [1] | ||
| Olor | Picante, rancio, desagradable [1] | ||
| Densidad | 0,98797 g/cm3 [ 2] | ||
| Punto de fusión | -20,5 °C (-4,9 °F; 252,7 K) [8] | ||
| Punto de ebullición | 141,15 °C (286,07 °F; 414,30 K) [8] | ||
| Sublimes a −48 °C Δ subl H | |||
| 8,19 g/g (−28,3 °C) 34,97 g/g (−23,9 °C) Miscible (≥ −19,3 °C) [4] | |||
| Solubilidad | Miscible en EtOH , éter , CHCl 3[5] | ||
| registro P | 0,33 [6] | ||
| Presión de vapor | 0,32 kPa (20 °C) [7] 0,47 kPa (25 °C) [6] 9,62 kPa (100 °C) [3] | ||
Constante de la ley de Henry ( k H ) | 4,45·10 −4 L·atm/mol [6] | ||
| Acidez (p K a ) | 4.88 [6] | ||
| -43,50·10 −6 cm3 / mol | |||
Índice de refracción ( n D ) | 1.3843 [2] | ||
| Viscosidad | 1,175 cP ( 15 °C) [2] 1,02 cP (25 °C) 0,668 cP (60 °C) 0,495 cP (90 °C) [6] | ||
| Estructura | |||
| Monoclínico (−95 °C) [9] | |||
| P2 1 /c [9] | |||
a = 4,04 Å, b = 9,06 Å, c = 11 Å [9] α = 90°, β = 91,25°, γ = 90° | |||
| 0,63 D (22 °C) [2] | |||
| Termoquímica | |||
Capacidad calorífica ( C ) | 152,8 J/mol·K [5] [3] | ||
Entropía molar estándar ( S ⦵ 298 ) | 191 J/mol·K [3] | ||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −510,8 kJ/mol [3] | ||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | 1527,3 kJ/mol [2] [3] | ||
| Peligros | |||
| Seguridad y salud en el trabajo (SST/OHS): | |||
Principales peligros | Corrosivo | ||
| Etiquetado SGA : [7] | |||
   | |||
| Peligro | |||
| H314 [7] | |||
| P280 , P305+P351+P338 , P310 [7] | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | 54 °C (129 °F; 327 K) [7] | ||
| 512 °C (954 °F; 785 K) | |||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) | 1370 mg/kg (ratón, oral) [5] | ||
| NIOSH (límites de exposición a la salud en EE. UU.): | |||
PEL (Permisible) | ninguno [1] | ||
REL (recomendado) | TWA 10 ppm (30 mg/m3 ) TWA 15 ppm (45 mg/m3 ) [ 1] | ||
IDLH (Peligro inmediato) | Dakota del Norte [1] | ||
| Compuestos relacionados | |||
Ácidos carboxílicos relacionados | Ácido acético Ácido láctico Ácido 3-hidroxipropiónico Ácido tartrónico Ácido acrílico Ácido butírico | ||
Compuestos relacionados | 1-Propanol Propionaldehído Propionato de sodio Anhídrido propiónico | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El ácido propiónico ( / p r oʊ p i ˈ ɒ n ɪ k / , de las palabras griegas πρῶτος : prōtos , que significa "primero", y πίων : píōn , que significa "grasa"; también conocido como ácido propanoico ) es un ácido carboxílico natural con fórmula química CH
3es
2CO
2H. Es un líquido con un olor penetrante y desagradable que se parece un poco al olor corporal . El anión CH
3es
2CO−
2Así como las sales y ésteres del ácido propiónico se conocen como propionatos o propanoatos .
Aproximadamente la mitad de la producción mundial de ácido propiónico se consume como conservante tanto para piensos animales como para alimentos para consumo humano. También es útil como intermediario en la producción de otros productos químicos, especialmente polímeros.
Historia
El ácido propiónico fue descrito por primera vez en 1844 por Johann Gottlieb , quien lo encontró entre los productos de degradación del azúcar. [10] Durante los siguientes años, otros químicos produjeron ácido propiónico por diferentes medios, ninguno de ellos se dio cuenta de que estaban produciendo la misma sustancia. En 1847, el químico francés Jean-Baptiste Dumas estableció que todos los ácidos eran el mismo compuesto, al que llamó ácido propiónico, de las palabras griegas πρῶτος (prōtos), que significa primero , y πίων (piōn), que significa grasa , porque es el H(CH
2)
norteÁcido COOH que exhibe las propiedades de los otros ácidos grasos , como producir una capa aceitosa cuando se sala del agua y tener una sal de potasio jabonosa . [11]
Propiedades
El ácido propiónico tiene propiedades físicas intermedias entre las de los ácidos carboxílicos más pequeños, el fórmico y el acético , y los ácidos grasos más grandes . Es miscible con agua, pero se puede eliminar del agua añadiendo sal. Al igual que los ácidos acético y fórmico, está formado por pares de moléculas unidas por enlaces de hidrógeno tanto en el líquido como en el vapor.
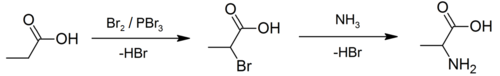
El ácido propiónico muestra las propiedades generales de los ácidos carboxílicos: puede formar derivados de amida , éster , anhídrido y cloruro . Experimenta la reacción de Hell-Volhard-Zelinsky que implica la α- halogenación de un ácido carboxílico con bromo , catalizada por tribromuro de fósforo , en este caso para formar ácido 2-bromopropanoico, CH
3CHBrCOOH . [12] Este producto se ha utilizado para preparar una mezcla racémica de alanina mediante amonólisis . [13] [14]
Fabricar
Químico
En la industria, el ácido propiónico se produce principalmente mediante la hidrocarboxilación de etileno utilizando carbonilo de níquel como catalizador: [15]
También se produce por oxidación aeróbica del propionaldehído . En presencia de sales de cobalto o manganeso (el más utilizado es el propionato de manganeso), esta reacción se produce rápidamente a temperaturas tan suaves como 40-50 °C:
En el pasado, se producían grandes cantidades de ácido propiónico como subproducto de la fabricación de ácido acético. En la actualidad, el mayor productor mundial de ácido propiónico es BASF , con una capacidad de producción de aproximadamente 150 kt/a.
Biotecnológico
La producción biotecnológica de ácido propiónico utiliza principalmente cepas de Propionibacterium . [16] Sin embargo, la producción a gran escala de ácido propiónico por Propionibacteria enfrenta desafíos como la inhibición severa de los productos finales durante el crecimiento celular y la formación de subproductos (ácido acético y ácido succínico ). [17] Un enfoque para mejorar la productividad y el rendimiento durante la fermentación es mediante el uso de técnicas de inmovilización celular, que también promueven la fácil recuperación, la reutilización de la biomasa celular y mejoran la tolerancia al estrés de los microorganismos. [18] En 2018, la tecnología de impresión 3D se utilizó por primera vez para crear una matriz para la inmovilización celular en la fermentación. La producción de ácido propiónico por Propionibacterium acidipropionici inmovilizado en perlas de nailon impresas en 3D se eligió como estudio modelo. Se demostró que esas perlas impresas en 3D podían promover la unión celular de alta densidad y la producción de ácido propiónico, que podría adaptarse a otros bioprocesos de fermentación. [19] Se han probado otras matrices de inmovilización celular, como el Poraver de vidrio reciclado y el biorreactor de lecho fibroso. [20] [21]
Se han probado métodos alternativos de producción mediante ingeniería genética de cepas de Escherichia coli para incorporar la vía necesaria, el ciclo Wood-Werkman. [22]
Usos industriales
El ácido propiónico inhibe el crecimiento de moho y algunas bacterias en niveles entre 0,1 y 1% en peso. Como resultado, parte del ácido propiónico producido se consume como conservante tanto para piensos animales como para alimentos para consumo humano. Para piensos animales, se utiliza directamente o como su sal de amonio . Esta aplicación representa aproximadamente la mitad de la producción mundial de ácido propiónico. El antibiótico monensina se añade al pienso para ganado para favorecer a las propionibacterias sobre los productores de ácido acético en el rumen ; esto produce menos dióxido de carbono y la conversión alimenticia es mejor. Otra aplicación importante es como conservante en productos horneados, que utilizan las sales de sodio y calcio . [15] Como aditivo alimentario , está aprobado para su uso en la UE, [23] EE. UU., [24] Australia y Nueva Zelanda. [25]
El ácido propiónico también es útil como intermediario en la producción de otros productos químicos, especialmente polímeros. El acetato de celulosa-propionato es un termoplástico útil . El propionato de vinilo también se utiliza. En aplicaciones más especializadas, también se utiliza para fabricar pesticidas y productos farmacéuticos . Los ésteres de ácido propiónico tienen olores a frutas y a veces se utilizan como disolventes o saborizantes artificiales. [15]
En las plantas de biogás , el ácido propiónico es un producto intermedio común, que se forma por fermentación con bacterias de ácido propiónico. Su degradación en ambientes anaeróbicos (por ejemplo, plantas de biogás) requiere la actividad de comunidades microbianas complejas. [26]
En la producción del queso Jarlsberg se utiliza una bacteria de ácido propiónico para darle sabor y agujeros. [27]
Biología
El ácido propiónico se produce biológicamente en forma de su éster de coenzima A, propionil-CoA , a partir de la descomposición metabólica de los ácidos grasos que contienen un número impar de átomos de carbono , y también de la descomposición de algunos aminoácidos . Las bacterias del género Propionibacterium producen ácido propiónico como producto final de su metabolismo anaeróbico . Esta clase de bacterias se encuentra comúnmente en los estómagos de los rumiantes y en las glándulas sudoríparas de los humanos , y su actividad es parcialmente responsable del olor del queso emmental , el "queso suizo" americano y el sudor .
El metabolismo del ácido propiónico comienza con su conversión a propionil coenzima A , el primer paso habitual en el metabolismo de los ácidos carboxílicos . Dado que el ácido propiónico tiene tres carbonos, el propionil-CoA no puede entrar directamente en la beta oxidación ni en los ciclos del ácido cítrico . En la mayoría de los vertebrados , el propionil-CoA se carboxila a D - metilmalonil-CoA , que se isomeriza a L -metilmalonil-CoA. Una enzima dependiente de la vitamina B12 cataliza la reorganización de L -metilmalonil-CoA a succinil-CoA , que es un intermediario del ciclo del ácido cítrico y puede incorporarse fácilmente allí. [28]
El ácido propiónico actúa como sustrato para la gluconeogénesis hepática a través de la conversión a succinil-CoA. [29] [30] Además, la administración de ácido propiónico exógeno da como resultado una mayor producción de glucosa endógena de la que se puede explicar mediante la conversión gluconeogénica sola. [31] El ácido propiónico exógeno puede regular positivamente la producción de glucosa endógena a través de aumentos en la norepinefrina y el glucagón , lo que sugiere que la ingestión crónica de ácido propiónico puede tener consecuencias metabólicas adversas. [32]
En la acidemia propiónica , un trastorno genético hereditario poco frecuente, el propionato actúa como una toxina metabólica en las células del hígado al acumularse en las mitocondrias como propionil-CoA y su derivado, metilcitrato, dos inhibidores del ciclo del ácido tricarboxílico. El propanoato se metaboliza oxidativamente por la glía , lo que sugiere una vulnerabilidad astrocítica en la acidemia propiónica cuando se puede acumular propionil-CoA intramitocondrial. La acidemia propiónica puede alterar la expresión génica neuronal y glial al afectar la acetilación de histonas. [33] [34] Cuando el ácido propiónico se infunde directamente en los cerebros de roedores, produce un comportamiento reversible (p. ej., hiperactividad , distonía , deterioro social, perseverancia ) y cambios cerebrales (p. ej., neuroinflamación innata, agotamiento de glutatión) que pueden usarse como un medio para modelar el autismo en ratas. [33]
Aparición humana
La piel humana alberga varias especies de Propionibacteria . La más notable es Cutibacterium acnes (antes conocida como Propionibacterium acnes ), que vive principalmente en las glándulas sebáceas de la piel y es una de las principales causas del acné . [35] Se observa que el propionato es uno de los ácidos grasos de cadena corta más comunes producidos en el intestino grueso de los humanos por la microbiota intestinal en respuesta a los carbohidratos no digeribles ( fibra dietética ) en la dieta. [36] [37] Se ha revisado el papel de la microbiota intestinal y sus metabolitos, incluido el propionato, en la mediación de la función cerebral. [38]
Un estudio en ratones sugiere que el propionato es producido por las bacterias del género Bacteroides en el intestino y que ofrece cierta protección contra la Salmonella allí. [39] Otro estudio descubre que el propionato de ácido graso puede calmar las células inmunes que aumentan la presión arterial, protegiendo así al cuerpo de los efectos dañinos de la presión arterial alta. [40]
Bacteriología
La especie bacteriana Coprothermobacter platensis produce propionato al fermentar gelatina. [41] Prevotella brevis y Prevotella ruminicola también generan propionato al fermentar glucosa. [42]
Sales y ésteres de propionato
El ion propionato / ˈp r oʊ p i ə n eɪ t / , o propanoato , es C
2yo
5C O O−
, la base conjugada del ácido propiónico. Es la forma que se encuentra en los sistemas biológicos a pH fisiológico . Un compuesto propiónico o propanoico es una sal carboxilato o un éster de ácido propiónico. En estos compuestos, el propionato se escribe a menudo en forma abreviada como CH
3es
2CO
2o simplemente EtCO
2.
Los propionatos no deben confundirse con los propenoatos (comúnmente conocidos como acrilatos ), los iones/sales/ésteres del ácido propenoico (también conocido como ácido 2-propenoico o ácido acrílico ).
Ejemplos
Sales
- Propionato de sodio NaC
2yo
5CO
2 - Propionato de potasio KC
2yo
5CO
2 - Propionato de calcio Ca(C
2yo
5CO
2)
2 - Propionato de circonio Zr(C
2yo
5CO
2)
4
Ésteres
- Propionato de metilo C
2yo
5(CO)OCH
3 - Propionato de etilo C
2yo
5(CO)OC
2yo
5 - Propionato de propilo C
2yo
5(CO)OC
3yo
7 - Propionato de pentilo C
2yo
5(CO)OC
5yo
11 - Propionato de fluticasona C
25yo
31F
3Oh
5S
Véase también
Referencias
- ^ abcde Guía de bolsillo del NIOSH sobre peligros químicos. "#0529". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ abcde Lagowski, JJ, ed. (2012). La química de los disolventes no acuosos. Vol. III. Elsevier. pág. 362. ISBN 978-0323151030.
- ^ abcdef Ácido propanoico en Linstrom, Peter J.; Mallard, William G. (eds.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69 , Instituto Nacional de Estándares y Tecnología, Gaithersburg (MD) (consultado el 13 de junio de 2014)
- ^ Seidell, Atherton; Linke, William F. (1919). Solubilidades de compuestos inorgánicos y orgánicos (2.ª ed.). D. Van Nostrand Company. pág. 569.
- ^ abc "chemister.ru (copia archivada)". Archivado desde el original el 9 de octubre de 2016 . Consultado el 13 de junio de 2014 .
- ^ abcde CID 1032 de PubChem
- ^ abcde Sigma-Aldrich Co. , Ácido propiónico. Recuperado el 13 de junio de 2014.
- ^ ab Lide, David R., ed. (2009). Manual de química y física del CRC (90.ª edición). Boca Raton, Florida : CRC Press . ISBN 978-1-4200-9084-0.
- ^ abc Strieter, FJ; Templeton, DH; Scheuerman, RF; Sass, RL (1962). "La estructura cristalina del ácido propiónico". Acta Crystallographica . 15 (12): 1233–1239. Código Bibliográfico :1962AcCry..15.1233S. doi :10.1107/S0365110X62003278.
- ^ Johann Gottlieb (1844) "Ueber die Einwirkung von schmelzendem Kalihydrat auf Rohrzucker, Gummi, Stärkmehl und Mannit" (Sobre el efecto del hidróxido de potasio fundido sobre el azúcar sin refinar, el caucho, el almidón en polvo y el manitol), Annalen der Chemie und Pharmacie , 52 : 121–130. Después de combinar azúcar sin refinar con un exceso de hidróxido de potasio y destilar el resultado, Gottlieb obtuvo un producto al que llamó "Metacetonsäure" (ácido metaacetónico) en la p. 122: "Das Destillat ist stark sauer und enthält Ameisensäure, Essigsäure und eine neue Säure, welche ich, aus unten anzuführenden Gründen, Metacetonsäure nene". (El destilado es fuertemente ácido y contiene ácido fórmico, ácido acético y un nuevo ácido, que por razones que se expondrán más adelante llamo "ácido meta-acetónico").
- ^ Dumas, Malaguti y F. Leblanc (1847) "Sur l'identité des acides métacétonique et butyro-acétique" [Sobre la identidad del ácido metacetónico y el ácido butiroacético], Comptes rendus , 25 : 781–784. El ácido propiónico se nombra en la p. 783: "Ces caractères nous ont conduits à désigner cet acide sous le nom d' acide propionique , nom qui rappelle sa place dans la serie des acides gras: il en est le premier". (Estas características nos llevaron a designar a este ácido con el nombre de ácido propiónico , nombre que recuerda su lugar en la serie de los ácidos grasos: es el primero de ellos.)
- ^ Marvel, CS; du Vigneaud, V. (1931). "Ácido α-bromoisovalérico". Organic Syntheses . 11 : 20. doi :10.15227/orgsyn.011.0020; Volúmenes recopilados , vol. 2, pág. 93.
- ^ Tobie, Walter C.; Ayres, Gilbert B. (1937). "Síntesis de d,l-alanina con rendimiento mejorado a partir de ácido α-bromopropiónico y amoníaco acuoso". Revista de la Sociedad Química Americana . 59 (5): 950. doi : 10.1021/ja01284a510 .
- ^ Tobie, Walter C.; Ayres, Gilbert B. (1941). "dl-Alanina". Síntesis orgánicas . doi : 10.15227/orgsyn.009.0004; Volúmenes recopilados , vol. 1, pág. 21.
- ^ abc Samel, Ulf-Rainer; Kohler, Walter; Jugador, Armin Otto; Keuser, Ullrich; Yang, Shang-Tian; Jin, Ying; Lin, Meng; Wang, Zhongqiang; Teles, Joaquim Henrique (2018). "Ácido propiónico y derivados". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a22_223.pub4. ISBN 978-3527306732.
- ^ Piwowarek, Kamil; Lipińska, Edyta; Hać-Szymańczuk, Elżbieta; Kieliszek, Marek; Ścibisz, Iwona (2018). "Propionibacterium SPP.—fuente de ácido propiónico, vitamina B12 y otros metabolitos importantes para la industria". Microbiología y Biotecnología Aplicadas . 102 (2): 515–538. doi :10.1007/s00253-017-8616-7. PMC 5756557 . PMID 29167919. S2CID 23599974.
- ^ Liu, Long; Zhu, Yunfeng; Li, Jianghua; Wang, Miao; Lee, Pengsoon; Du, Guocheng; Chen, Jian (2012). "Producción microbiana de ácido propiónico a partir de propionibacterias: estado actual, desafíos y perspectivas". Critical Reviews in Biotechnology . 32 (4): 374–381. doi :10.3109/07388551.2011.651428. PMID 22299651. S2CID 25823025.
- ^ Alonso, Saúl; Rendueles, Manuel; Díaz, Mario (2015). "Un nuevo enfoque para monitorizar las respuestas fisiológicas inducidas por estrés en microorganismos inmovilizados". Applied Microbiology and Biotechnology . 99 (8): 3573–3583. doi :10.1007/s00253-015-6517-1. PMID 25776062. S2CID 860853.
- ^ Belgrano, Fabricio dos Santos; Diegel, Olaf; Pereira, Nei; Hatti-Kaul, Rajni (2018). "Inmovilización celular en matrices impresas en 3D: un estudio modelo sobre la fermentación del ácido propiónico". Tecnología de recursos biológicos . 249 : 777–782. Código Bibliográfico :2018BiTec.249..777B. doi :10.1016/j.biortech.2017.10.087. PMID 29136932.
- ^ Dishisha, Tarek; Alvarez, Maria Teresa; Hatti-Kaul, Rajni (2012). "Producción continua y por lotes de ácido propiónico a partir de glicerol utilizando células libres e inmovilizadas de Propionibacterium acidipropionici" (PDF) . Bioresource Technology . 118 : 553–562. Bibcode :2012BiTec.118..553D. doi :10.1016/j.biortech.2012.05.079. PMID 22728152. S2CID 29658955.
- ^ Suwannakham, Supaporn; Yang, Shang-Tian (2005). "Fermentación de ácido propiónico mejorada por el mutante Propionibacterium acidipropionici obtenido por adaptación en un biorreactor de lecho fibroso". Biotecnología y bioingeniería . 91 (3): 325–337. doi :10.1002/bit.20473. PMID 15977254.
- ^ Gonzalez-Garcia, Ricardo A.; McCubbin, Timothy; Turner, Mark S.; Nielsen, Lars K.; Marcellin, Esteban (2020). "Ingeniería de Escherichia coli para la producción de ácido propiónico a través del ciclo Wood-Werkman". Biotecnología y bioingeniería . 117 (1): 167–183. doi : 10.1002/bit.27182 . PMID 31556457. S2CID 203438727.
- ^ "Aditivos aprobados actualmente por la UE y sus números E". Agencia de Normas Alimentarias del Reino Unido . Consultado el 27 de octubre de 2011 .
- ^ "Listado de aditivos alimentarios, parte II". Administración de Alimentos y Medicamentos de Estados Unidos . Consultado el 27 de octubre de 2011 .
- ^ "Norma 1.2.4 - Etiquetado de ingredientes". Código de Normas Alimentarias de Australia y Nueva Zelanda . Comlaw.au. 8 de septiembre de 2011. Consultado el 27 de octubre de 2011 .
- ^ Ahlert, Stephan; Zimmermann, Rita; Ebling, Johannes; König, Helmut (2016). "Análisis de consorcios de degradación de propionato de plantas de biogás agrícola". MicrobiologyOpen . 5 (6): 1027–1037. doi : 10.1002/mbo3.386 . PMC 5221444 . PMID 27364538.
- ^ Cita de www.jarlsberg.com: "En la producción de Jarlsberg®, se utilizan bacterias de ácido propiónico (¡la receta secreta!) para darle al queso su sabor y agujeros característicos".
- ^ Lehninger, Albert L. (2005). Principios de bioquímica de Lehninger. Nelson, David L. (David Lee), 1942-, Cox, Michael M. (Cuarta edición). Nueva York: WH Freeman. ISBN 0-7167-4339-6.OCLC 55476414 .
- ^ Aschenbach, JR; Kristensen, NB; Donkin, SS; Hammon, HM; Penner, GB (diciembre de 2010). "Gluconeogénesis en vacas lecheras: el secreto para hacer leche dulce a partir de masa agria". IUBMB Life . 62 (12): 869–77. doi : 10.1002/iub.400 . PMID 21171012. S2CID 21117076.
- ^ Perry, Rachel J.; Borders, Candace B.; Cline, Gary W.; Zhang, Xian-Man; Alves, Tiago C.; Petersen, Kitt Falk; Rothman, Douglas L.; Kibbey, Richard G.; Shulman, Gerald I. (21 de marzo de 2016). "El propionato aumenta el ciclo hepático del piruvato y la anaplerosis y altera el metabolismo mitocondrial". Revista de química biológica . 291 (23): 12161–12170. doi : 10.1074/jbc.m116.720631 . ISSN 0021-9258. PMC 4933266 . PMID 27002151.
- ^ Ringer, AI (2 de agosto de 1912). "La conversión cuantitativa del ácido propiónico en glucosa". Journal of Biological Chemistry . 12 : 511–515. doi : 10.1016/S0021-9258(18)88686-0 .
- ^ Tirosh, Amir; Calay, Ediz S.; Tuncman, Gurol; Claiborn, Kathryn C.; Inouye, Karen E.; Eguchi, Kosei; Alcala, Michael; Rathaus, Moran; Hollander, Kenneth S.; Ron, Idit; Livne, Rinat (24 de abril de 2019). "El propionato de ácido graso de cadena corta aumenta la producción de glucagón y FABP4, lo que afecta la acción de la insulina en ratones y humanos". Science Translational Medicine . 11 (489): eaav0120. doi : 10.1126/scitranslmed.aav0120 . ISSN 1946-6234. PMID 31019023.
- ^ ab DF MacFabe; DP Cain; K. Rodriguez-Capote; AE Franklin; JE Hoffman; F. Boon; AR Taylor; M. Kavaliers; K.-P. Ossenkopp (2007). "Efectos neurobiológicos del ácido propiónico intraventricular en ratas: posible papel de los ácidos grasos de cadena corta en la patogénesis y las características de los trastornos del espectro autista". Behavioural Brain Research . 176 (1): 149–169. doi :10.1016/j.bbr.2006.07.025. PMID 16950524. S2CID 3054752.
- ^ NHT Nguyen; C. Morland; S. Villa Gonzalez; F. Rise; J. Storm-Mathisen; V. Gundersen; B. Hassel (2007). "El propionato aumenta la acetilación de histonas neuronales, pero es metabolizado oxidativamente por la glía. Relevancia para la acidemia propiónica". Journal of Neurochemistry . 101 (3): 806–814. doi : 10.1111/j.1471-4159.2006.04397.x . PMID 17286595. S2CID 514557.
- ^ Bojar, Richard A.; Holland, Keith T. (2004). "Acné y propionibacterium acnes". Clinics in Dermatology . 22 (5): 375–379. doi :10.1016/j.clindermatol.2004.03.005. PMID 15556721.
- ^ Cani, Patrice D.; Knauf, Claude (27 de mayo de 2016). "Cómo los microbios intestinales se comunican con los órganos: el papel de las vías endocrinas y nerviosas". Metabolismo molecular . 5 (9): 743–752. doi :10.1016/j.molmet.2016.05.011. PMC 5004142 . PMID 27617197.
- ^ den Besten, G; van Eunen, K; Groen, AK; Venema, K; Reijngoud, DJ; Bakker, BM (septiembre de 2013). "El papel de los ácidos grasos de cadena corta en la interacción entre la dieta, la microbiota intestinal y el metabolismo energético del huésped". Journal of Lipid Research . 54 (9): 2325–40. doi : 10.1194/jlr.R036012 . PMC 3735932 . PMID 23821742.
- ^ Rogers, GB; Keating, DJ; Young, RL; Wong, ML; Licinio, J.; Wesselingh, S. (2016). "De la disbiosis intestinal a la función cerebral alterada y la enfermedad mental: mecanismos y vías". Psiquiatría molecular . 21 (6): 738–748. doi : 10.1038/mp.2016.50 . PMC 4879184 . PMID 27090305. S2CID 18589882.
- ^ Jacobson, Amanda; Lam, Lilian; Rajendram, Manohary; Tamburini, Fiona; Honeycutt, Jared; Pham, Trung; Van Treuren, Will; Pruss, Kali; Stabler, Stephen Russell; Lugo, Kyler; Bouley, Donna M.; Vilches-Moure, Jose G.; Smith, Mark; Sonnenburg, Justin L.; Bhatt, Ami S.; Huang, Kerwyn Casey; Monack, Denise (2018). "Un metabolito producido por comensales intestinales media la resistencia a la colonización de la infección por Salmonella". Cell Host & Microbe . 24 (2): 296–307.e7. doi :10.1016/j.chom.2018.07.002. PMC 6223613 . PMID 30057174.
- ^ Bartolomaeus, Hendrik; Balogh, András; Yakoub, Mina; Homann, Susana; Markó, Lajos; Höges, Sascha; Tsvetkov, Dmitri; Krannich, Alejandro; Wundersitz, Sebastián; Avery, Elena G.; Haase, Nadine; Kräker, Kristin; Hering, Lidia; Maase, Martina; Kusche-Vihrog, Kristina; Grandoch, María; Fielitz, Jens; Kempa, Stefan; Gollasch, Maik; Zhumadilov, Zhaxybay; Kozhakhmetov, Samat; Kushugulova, Almagul; Eckardt, Kai-Uwe; Dechend, Ralf; Grupa, Lars Christian; Forslund, Sofía K.; Müller, Dominik N.; Stegbauer, Johannes; Wilck, Nicola (2019). "El propionato de ácido graso de cadena corta protege del daño cardiovascular hipertensivo". Circulation . 139 (11): 1407–1421. doi :10.1161/CIRCULATIONAHA.118.036652. PMC 6416008 . PMID 30586752.
- ^ Etchebehere, C.; Pavan, ME; Zorzópulos, J.; Soubes, M.; Muxí, L. (octubre de 1998). "Coprothermobacter platensis sp. nov., una nueva bacteria anaerobia proteolítica termófila aislada de un lodo mesófilo anaerobio". Revista Internacional de Bacteriología Sistemática . 48 Pt 4 (4): 1297–1304. doi : 10.1099/00207713-48-4-1297 . ISSN 0020-7713. PMID 9828430.
- ^ Zhang, Bo; Lingga, Christopher; De Groot, Hannah; Hackmann, Timothy J (30 de septiembre de 2023). "La actividad oxidorreductasa de Rnf equilibra los cofactores redox durante la fermentación de glucosa a propionato en Prevotella". Research Gate . Consultado el 26 de septiembre de 2024 .
Enlaces externos
- Datos de referencia estándar del NIST para el ácido propánico
- Ficha internacional de seguridad química 0806
- Guía de bolsillo del NIOSH sobre peligros químicos
- Los ácidos propiónicos. Toxicidad gastrointestinal en diversas especies
- Ficha técnica del ácido propiónico