Estradiol
 | |
 | |
| Nombres | |
|---|---|
| Pronunciación | / ˌ ɛ s t r ə ˈ d aɪ oʊ l / ES -trə- DY -ohl [1][2] |
| Nombre IUPAC Estra-1,3,5(10)-trieno-3,17β-diol | |
| Nombre sistemático de la IUPAC ( 1S ,3aS , 3bR , 9bS , 11aS ) -11a-Metil-2,3,3a,3b,4,5,9b,10,11,11a-decahidro-1H - ciclopenta[ a ]fenantreno-1,7-diol | |
| Otros nombres Estradiol; E2; 17β-estradiol; 17β-estradiol | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| EBICh | |
| Química biológica | |
| Araña química | |
| Banco de medicamentos | |
| Tarjeta informativa de la ECHA | 100.000.022 |
| Número CE |
|
| BARRIL | |
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| Propiedades | |
| C18H24O2 | |
| Masa molar | 272,38 g/mol |
| -186,6·10 −6 cm3 / mol | |
| Farmacología | |
| G03CA03 ( OMS ) | |
| Datos de licencia |
|
| Oral , sublingual , intranasal , tópica / transdérmica , vaginal , intramuscular o subcutánea (como éster ), implante subdérmico | |
| Farmacocinética : | |
| Oral: <5% [3] | |
| ~98%: [3] [4] • Albúmina : 60% • SHBG : 38% • Libre: 2% | |
| Hígado (a través de hidroxilación , sulfatación , glucuronidación ) | |
| Oral: 13–20 horas [3] Sublingual: 8–18 horas [5] Tópico (gel): 36,5 horas [6] | |
| Orina : 54% [3] Heces : 6% [3] | |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
El estradiol ( E2 ), también llamado estrógeno , estradiol , es una hormona esteroide estrógena y la principal hormona sexual femenina . Está involucrado en la regulación de los ciclos reproductivos femeninos , como los ciclos estrales y menstruales . El estradiol es responsable del desarrollo de las características sexuales secundarias femeninas, como los senos , el ensanchamiento de las caderas y un patrón femenino de distribución de grasa . También es importante en el desarrollo y mantenimiento de los tejidos reproductivos femeninos, como las glándulas mamarias , el útero y la vagina durante la pubertad , la edad adulta y el embarazo . [7] También tiene efectos importantes en muchos otros tejidos, incluidos los huesos , la grasa , la piel , el hígado y el cerebro .
Aunque los niveles de estradiol en los machos son mucho más bajos que en las hembras, el estradiol también tiene papeles importantes en los machos. Además de en los humanos y otros mamíferos , el estradiol también se encuentra en la mayoría de los vertebrados y crustáceos , insectos , peces y otras especies animales . [8] [9]
El estradiol se produce especialmente dentro de los folículos de los ovarios , pero también en otros tejidos, incluidos los testículos , las glándulas suprarrenales , la grasa, el hígado , los senos y el cerebro. El estradiol se produce en el cuerpo a partir del colesterol a través de una serie de reacciones e intermediarios . [10] La vía principal implica la formación de androstenediona , que luego es convertida por la aromatasa en estrona y posteriormente se convierte en estradiol. Alternativamente, la androstenediona se puede convertir en testosterona , que luego se puede convertir en estradiol. Tras la menopausia en las mujeres, la producción de estrógenos por los ovarios se detiene y los niveles de estradiol disminuyen a niveles muy bajos.
Además de su función como hormona natural, el estradiol se utiliza como medicamento , por ejemplo, en la terapia hormonal para la menopausia y en la terapia hormonal feminizante para mujeres transgénero ; para obtener información sobre el estradiol como medicamento, consulte el artículo sobre estradiol (medicamento) .
Función biológica
Desarrollo sexual
El desarrollo de las características sexuales secundarias en las mujeres es impulsado por los estrógenos, para ser específicos, el estradiol. [11] [12] Estos cambios se inician en el momento de la pubertad , la mayoría se mejoran durante los años reproductivos y se vuelven menos pronunciados con la disminución del soporte de estradiol después de la menopausia . Por lo tanto, el estradiol produce el desarrollo de los senos y es responsable de los cambios en la forma del cuerpo , afectando los huesos, las articulaciones y la deposición de grasa . [11] [12] En las mujeres, el estradiol induce el desarrollo de los senos, el ensanchamiento de las caderas , una distribución de grasa femenina (con grasa depositada particularmente en los senos, las caderas, los muslos y las nalgas) y la maduración de la vagina y la vulva , mientras que media el brote de crecimiento puberal (indirectamente a través del aumento de la secreción de la hormona del crecimiento ) [13] y el cierre epifisario (limitando así la altura final ) en ambos sexos. [11] [12]
Reproducción
Sistema reproductor femenino
En la mujer, el estradiol actúa como hormona de crecimiento para el tejido de los órganos reproductivos, apoyando el revestimiento de la vagina , las glándulas cervicales, el endometrio y el revestimiento de las trompas de Falopio. Mejora el crecimiento del miometrio . El estradiol parece necesario para mantener los ovocitos en el ovario . Durante el ciclo menstrual , el estradiol producido por los folículos en crecimiento desencadena, a través de un sistema de retroalimentación positiva, los eventos hipotálamo-hipofisarios que conducen al aumento de la hormona luteinizante , induciendo la ovulación. En la fase lútea, el estradiol, junto con la progesterona , prepara el endometrio para la implantación . Durante el embarazo , el estradiol aumenta debido a la producción placentaria . El efecto del estradiol, junto con la estrona y el estriol , en el embarazo es menos claro. Pueden promover el flujo sanguíneo uterino, el crecimiento del miometrio, estimular el crecimiento de los senos y, a término, promover el ablandamiento cervical y la expresión de los receptores de oxitocina miometriales . [ cita requerida ] En los babuinos, el bloqueo de la producción de estrógenos conduce a la pérdida del embarazo, lo que sugiere que el estradiol tiene un papel en el mantenimiento del embarazo. Se está investigando el papel de los estrógenos en el proceso de iniciación del parto . Las acciones del estradiol son necesarias antes de la exposición a la progesterona en la fase lútea. [ cita requerida ]
Sistema reproductor masculino
El efecto del estradiol (y de los estrógenos en general) sobre la reproducción masculina es complejo. El estradiol se produce por acción de la aromatasa principalmente en las células de Leydig de los testículos de los mamíferos , pero también por algunas células germinales y las células de Sertoli de los mamíferos inmaduros. [14] Funciona ( in vitro ) para prevenir la apoptosis de los espermatozoides masculinos . [15] Mientras que algunos estudios a principios de la década de 1990 afirmaron una conexión entre la disminución global del recuento de espermatozoides y la exposición al estrógeno en el medio ambiente, [16] estudios posteriores no encontraron tal conexión, ni evidencia de una disminución general en el recuento de espermatozoides. [17] [18] La supresión de la producción de estradiol en una subpoblación de hombres subfértiles puede mejorar el análisis del semen . [19]
Los varones con ciertas afecciones genéticas de los cromosomas sexuales , como el síndrome de Klinefelter , tendrán un nivel más alto de estradiol. [20]
Sistema esquelético
El estradiol tiene un efecto profundo sobre los huesos. Las personas que no lo tienen (ni otros estrógenos) se volverán altas y eunucoides , ya que el cierre epifisario se retrasa o puede no producirse. [21] La densidad ósea también se ve afectada, lo que resulta en osteopenia temprana y osteoporosis . [22] Los niveles bajos de estradiol también pueden predecir fracturas, y las mujeres posmenopáusicas tienen la mayor incidencia de fracturas óseas . [23] Las mujeres que han pasado la menopausia experimentan una pérdida acelerada de masa ósea debido a una deficiencia relativa de estrógenos. [24]
Salud de la piel
El receptor de estrógeno , así como el receptor de progesterona , se han detectado en la piel , incluso en los queratinocitos y fibroblastos . [25] [26] En la menopausia y después, la disminución de los niveles de hormonas sexuales femeninas da como resultado atrofia , adelgazamiento y aumento de las arrugas de la piel y una reducción de la elasticidad , firmeza y fuerza de la piel. [25] [26] Estos cambios en la piel constituyen una aceleración del envejecimiento cutáneo y son el resultado de la disminución del contenido de colágeno , irregularidades en la morfología de las células epidérmicas de la piel , disminución de la sustancia fundamental entre las fibras de la piel y reducción de los capilares y el flujo sanguíneo . [25] [26] La piel también se vuelve más seca durante la menopausia, lo que se debe a la reducción de la hidratación de la piel y de los lípidos superficiales (producción de sebo). [25] Junto con el envejecimiento cronológico y el fotoenvejecimiento, la deficiencia de estrógenos en la menopausia es uno de los tres factores principales que influyen predominantemente en el envejecimiento de la piel. [25]
La terapia de reemplazo hormonal que consiste en un tratamiento sistémico con estrógeno solo o en combinación con un progestágeno, tiene efectos beneficiosos considerables y bien documentados sobre la piel de las mujeres posmenopáusicas. [25] [26] Estos beneficios incluyen un mayor contenido de colágeno de la piel, grosor y elasticidad de la piel e hidratación de la piel y lípidos superficiales. [25] [26] Se ha descubierto que el estrógeno tópico tiene efectos beneficiosos similares sobre la piel. [25] Además, un estudio ha descubierto que la crema tópica de progesterona al 2% aumenta significativamente la elasticidad y firmeza de la piel y disminuye observablemente las arrugas en mujeres peri y posmenopáusicas. [26] La hidratación de la piel y los lípidos superficiales, por otro lado, no cambiaron significativamente con la progesterona tópica. [26] Estos hallazgos sugieren que la progesterona, como el estrógeno, también tiene efectos beneficiosos sobre la piel y puede ser protectora independiente contra el envejecimiento de la piel. [26]
Sistema nervioso
Los estrógenos pueden producirse en el cerebro a partir de precursores de esteroides. Como antioxidantes , se ha descubierto que tienen una función neuroprotectora . [27]
Los circuitos de retroalimentación positiva y negativa del ciclo menstrual involucran al estradiol ovárico como vínculo con el sistema hipotálamo-hipofisario para regular las gonadotropinas . [28]
Se considera que el estrógeno desempeña un papel importante en la salud mental de las mujeres, y se ha sugerido que existen vínculos entre el nivel hormonal, el estado de ánimo y el bienestar. Las caídas o fluctuaciones repentinas de los niveles de estrógeno, o los períodos prolongados de niveles bajos sostenidos, pueden estar correlacionados con una disminución significativa del estado de ánimo. Se ha demostrado que la recuperación clínica de la depresión posparto, perimenopausia y posmenopausia es eficaz después de que los niveles de estrógeno se estabilizan o se restablecen. [29] [30]
Se descubrió que los volúmenes de las estructuras cerebrales sexualmente dimórficas en mujeres transgénero cambiaban y se aproximaban a las estructuras cerebrales femeninas típicas cuando se exponían al estrógeno concomitantemente con la privación de andrógenos durante un período de meses, [31] lo que sugiere que el estrógeno y/o los andrógenos tienen un papel importante que desempeñar en la diferenciación sexual del cerebro, tanto antes del nacimiento como más tarde en la vida.
También hay evidencia de que la programación del comportamiento sexual masculino adulto en muchos vertebrados depende en gran medida del estradiol producido durante la vida prenatal y la primera infancia. [32] Todavía no se sabe si este proceso juega un papel significativo en el comportamiento sexual humano, aunque la evidencia de otros mamíferos tiende a indicar una conexión. [33]
Se ha descubierto que el estrógeno aumenta la secreción de oxitocina y aumenta la expresión de su receptor , el receptor de oxitocina , en el cerebro . [34] En las mujeres, se ha descubierto que una dosis única de estradiol es suficiente para aumentar las concentraciones circulantes de oxitocina. [35]
Cánceres ginecológicos
El estradiol se ha relacionado con el desarrollo y la progresión de cánceres como el cáncer de mama, el cáncer de ovario y el cáncer de endometrio. El estradiol afecta a los tejidos diana principalmente al interactuar con dos receptores nucleares llamados receptor de estrógeno α (ERα) y receptor de estrógeno β (ERβ). [36] [37] Una de las funciones de estos receptores de estrógeno es la modulación de la expresión génica . Una vez que el estradiol se une a los ER, los complejos receptores se unen a secuencias de ADN específicas , posiblemente causando daño al ADN y un aumento en la división celular y la replicación del ADN . Las células eucariotas responden al ADN dañado estimulando o alterando las fases G1, S o G2 del ciclo celular para iniciar la reparación del ADN . Como resultado, se produce la transformación celular y la proliferación de células cancerosas. [38]
Sistema cardiovascular
El estrógeno afecta a ciertos vasos sanguíneos . Se ha demostrado una mejora en el flujo sanguíneo arterial en las arterias coronarias . [39] El 17-beta-estradiol (E2) se considera el estrógeno más potente que se encuentra en los seres humanos. El E2 influye en la función vascular, la apoptosis y el daño durante la isquemia y la reperfusión cardíacas. El E2 puede proteger el corazón y los miocitos cardíacos individuales de las lesiones relacionadas con la isquemia. Después de un ataque cardíaco o de largos períodos de hipertensión, el E2 inhibe los efectos adversos de la remodelación patológica del corazón. [40]
Durante el embarazo , los niveles elevados de estrógenos, concretamente estradiol, aumentan la coagulación y el riesgo de tromboembolia venosa .
| Incidencia absoluta de primera TEV por 10.000 personas-año durante el embarazo y el período posparto | ||||||||
|---|---|---|---|---|---|---|---|---|
| Datos suecos A | Datos suecos B | Datos en inglés | Datos daneses | |||||
| Periodo de tiempo | norte | Tasa (IC del 95%) | norte | Tasa (IC del 95%) | norte | Tasa (IC del 95%) | norte | Tasa (IC del 95%) |
| Embarazo fuera del horario laboral | 1105 | 4.2 (4.0–4.4) | 1015 | 3.8 (?) | 1480 | 3.2 (3.0–3.3) | 2895 | 3.6 (3.4–3.7) |
| Anteparto | 995 | 20,5 (19,2–21,8) | 690 | 14.2 (13.2–15.3) | 156 | 9,9 (8,5–11,6) | 491 | 10,7 (9,7–11,6) |
| Trimestre 1 | 207 | 13,6 (11,8–15,5) | 172 | 11.3 (9.7–13.1) | 23 | 4.6 (3.1–7.0) | 61 | 4.1 (3.2–5.2) |
| Trimestre 2 | 275 | 17,4 (15,4–19,6) | 178 | 11,2 (9,7–13,0) | 30 | 5.8 (4.1–8.3) | 75 | 5.7 (4.6–7.2) |
| Trimestre 3 | 513 | 29,2 (26,8–31,9) | 340 | 19,4 (17,4–21,6) | 103 | 18,2 (15,0–22,1) | 355 | 19,7 (17,7–21,9) |
| Alrededor de la entrega | 115 | 154,6 (128,8–185,6) | 79 | 106,1 (85,1–132,3) | 34 | 142,8 (102,0–199,8) | – | |
| Posparto | 649 | 42,3 (39,2–45,7) | 509 | 33,1 (30,4–36,1) | 135 | 27,4 (23,1–32,4) | 218 | 17,5 (15,3–20,0) |
| Posparto temprano | 584 | 75,4 (69,6–81,8) | 460 | 59,3 (54,1–65,0) | 177 | 46,8 (39,1–56,1) | 199 | 30,4 (26,4–35,0) |
| Posparto tardío | 65 | 8,5 (7,0–10,9) | 49 | 6,4 (4,9–8,5) | 18 | 7.3 (4.6–11.6) | 319 | 3.2 (1.9–5.0) |
| Razones de tasas de incidencia (IRR) de la primera TEV durante el embarazo y el período posparto | ||||||||
| Datos suecos A | Datos suecos B | Datos en inglés | Datos daneses | |||||
| Periodo de tiempo | TIR* (IC del 95%) | TIR* (IC del 95%) | TIR (IC del 95 %)† | TIR (IC del 95 %)† | ||||
| Embarazo fuera del horario laboral | Referencia (es decir, 1,00) | |||||||
| Anteparto | 5,08 (4,66–5,54) | 3,80 (3,44–4,19) | 3.10 (2.63–3.66) | 2,95 (2,68–3,25) | ||||
| Trimestre 1 | 3,42 (2,95–3,98) | 3,04 (2,58–3,56) | 1,46 (0,96–2,20) | 1,12 (0,86–1,45) | ||||
| Trimestre 2 | 4,31 (3,78–4,93) | 3.01 (2.56–3.53) | 1,82 (1,27–2,62) | 1,58 (1,24–1,99) | ||||
| Trimestre 3 | 7,14 (6,43–7,94) | 5.12 (4.53–5.80) | 5,69 (4,66–6,95) | 5,48 (4,89–6,12) | ||||
| Alrededor de la entrega | 37,5 (30,9–44,45) | 27,97 (22,24–35,17) | 44,5 (31,68–62,54) | – | ||||
| Posparto | 10.21 (9.27–11.25) | 8,72 (7,83–9,70) | 8.54 (7.16–10.19) | 4,85 (4,21–5,57) | ||||
| Posparto temprano | 19.27 (16.53–20.21) | 15,62 (14,00–17,45) | 14.61 (12.10–17.67) | 8,44 (7,27–9,75) | ||||
| Posparto tardío | 2,06 (1,60–2,64) | 1,69 (1,26–2,25) | 2,29 (1,44–3,65) | 0,89 (0,53–1,39) | ||||
| Notas: Datos suecos A = Uso de cualquier código para TEV independientemente de la confirmación. Datos suecos B = Uso solo de TEV confirmada por algoritmo. Posparto temprano = Primeras 6 semanas después del parto. Posparto tardío = Más de 6 semanas después del parto. * = Ajustado por edad y año calendario. † = Ratio no ajustado calculado en base a los datos proporcionados. Fuente: [41] | ||||||||
Otras funciones
El estradiol tiene efectos complejos en el hígado . Afecta la producción de múltiples proteínas , incluidas lipoproteínas , proteínas de unión y proteínas responsables de la coagulación sanguínea . [ cita requerida ] En cantidades altas, el estradiol puede provocar colestasis , por ejemplo, colestasis del embarazo .
Ciertas afecciones ginecológicas dependen del estrógeno, como la endometriosis , los leiomiomas uterinos y el sangrado uterino . [ cita requerida ]
Actividad biológica
El estradiol actúa principalmente como un agonista del receptor de estrógeno (ER), un receptor nuclear de hormonas esteroides . Hay dos subtipos del ER, ERα y ERβ , y el estradiol se une potentemente a ambos receptores y los activa. El resultado de la activación del ER es una modulación de la transcripción y expresión génica en las células que expresan ER , que es el mecanismo predominante por el cual el estradiol media sus efectos biológicos en el cuerpo. El estradiol también actúa como un agonista de los receptores de estrógeno de membrana (mER), como GPER (GPR30), un receptor no nuclear recientemente descubierto para el estradiol, a través del cual puede mediar una variedad de efectos rápidos no genómicos . [42] A diferencia del caso del ER, GPER parece ser selectivo para el estradiol y muestra afinidades muy bajas para otros estrógenos endógenos, como la estrona y el estriol . [43] Otros mER además de GPER incluyen ER-X , ERx y G q -mER . [44] [45]
Los ERα/ERβ se encuentran en estado inactivo atrapados en complejos chaperonas multimoleculares organizados alrededor de la proteína de choque térmico 90 (HSP90), que contiene la proteína p23 y la inmunofilina, y se encuentran mayoritariamente en el citoplasma y parcialmente en el núcleo. En la vía clásica E2 o vía clásica del estrógeno, el estradiol entra en el citoplasma , donde interactúa con los ER. Una vez unidos a E2, los ER se disocian de los complejos chaperonas moleculares y se vuelven competentes para dimerizarse, migrar al núcleo y unirse a secuencias de ADN específicas ( elemento de respuesta al estrógeno , ERE), lo que permite la transcripción génica que puede tener lugar durante horas y días.
Administrado mediante inyección subcutánea en ratones, el estradiol es aproximadamente 10 veces más potente que la estrona y aproximadamente 100 veces más potente que el estriol. [46] [47] [48] Como tal, el estradiol es el principal estrógeno en el cuerpo, aunque se dice que los roles de la estrona y el estriol como estrógenos no son insignificantes. [48]
| Estrógeno | ESReceptor de estrógeno Banco de Reserva de AustraliaInformación sobre herramientas sobre afinidad de enlace relativa(%) | Peso uterino (%) | Uterotrofia | LHInformación sobre herramientas Hormona luteinizanteniveles (%) | SHBGInformación sobre herramientas Globulina transportadora de hormonas sexuales Banco de Reserva de AustraliaInformación sobre herramientas sobre afinidad de enlace relativa(%) |
|---|---|---|---|---|---|
| Control | – | 100 | – | 100 | – |
| Estradiol (E2) | 100 | 506 ± 20 | +++ | 12–19 | 100 |
| Estrona (E1) | 11 ± 8 | 490 ± 22 | +++ | ? | 20 |
| Estriol (E3) | 10 ± 4 | 468 ± 30 | +++ | 8–18 | 3 |
| Estetrol (E4) | 0,5 ± 0,2 | ? | Inactivo | ? | 1 |
| 17α-estradiol | 4,2 ± 0,8 | ? | ? | ? | ? |
| 2-Hidroxiestradiol | 24 ± 7 | 285 ± 8 | + b | 31–61 | 28 |
| 2-Metoxiestradiol | 0,05 ± 0,04 | 101 | Inactivo | ? | 130 |
| 4-Hidroxiestradiol | 45 ± 12 | ? | ? | ? | ? |
| 4-Metoxiestradiol | 1,3 ± 0,2 | 260 | ++ | ? | 9 |
| 4-Fluoroestradiol a | 180 ± 43 | ? | +++ | ? | ? |
| 2-Hidroxiestrona | 1,9 ± 0,8 | 130 ± 9 | Inactivo | 110–142 | 8 |
| 2-Metoxiestrona | 0,01 ± 0,00 | 103 ± 7 | Inactivo | 95–100 | 120 |
| 4-Hidroxiestrona | 11 ± 4 | 351 | ++ | 21–50 | 35 |
| 4-Metoxiestrona | 0,13 ± 0,04 | 338 | ++ | 65–92 | 12 |
| 16α-Hidroxiestrona | 2,8 ± 1,0 | 552 ± 42 | +++ | 7–24 | <0,5 |
| 2-Hidroxiestriol | 0,9 ± 0,3 | 302 | + b | ? | ? |
| 2-Metoxiestriol | 0,01 ± 0,00 | ? | Inactivo | ? | 4 |
| Notas: Los valores son media ± DE o rango. ER RBA = Afinidad de unión relativa a los receptores de estrógeno del citosol uterino de la rata . Peso uterino = Cambio porcentual en el peso húmedo uterino de ratas ovariectomizadas después de 72 horas con la administración continua de 1 μg/hora a través de bombas osmóticas implantadas subcutáneamente . Niveles de LH = Niveles de hormona luteinizante en relación con el valor inicial de ratas ovariectomizadas después de 24 a 72 horas de administración continua a través de implante subcutáneo. Notas al pie: a = Sintético (es decir, no endógeno ). b = Efecto uterotrófico atípico que se estabiliza en 48 horas (la uterotrofia del estradiol continúa linealmente hasta 72 horas). Fuentes: Ver plantilla. | |||||
Bioquímica

Biosíntesis
El estradiol, al igual que otras hormonas esteroides , se deriva del colesterol . Después de la escisión de la cadena lateral y utilizando la vía Δ 5 o Δ 4 , la androstenediona es el intermediario clave. Una parte de la androstenediona se convierte en testosterona, que a su vez sufre una conversión en estradiol por la aromatasa. En una vía alternativa, la androstenediona se aromatiza a estrona , que posteriormente se convierte en estradiol a través de la 17β-hidroxiesteroide deshidrogenasa (17β-HSD). [50]
Durante los años reproductivos, la mayor parte del estradiol en las mujeres es producido por las células de la granulosa de los ovarios mediante la aromatización de la androstenediona (producida en las células de los folículos de la teca) a estrona, seguida de la conversión de estrona a estradiol por la 17β-HSD. La corteza suprarrenal y, en los hombres, los testículos también producen cantidades más pequeñas de estradiol . [ cita médica requerida ]
El estradiol no se produce únicamente en las gónadas ; en particular, las células grasas producen precursores activos del estradiol y continuarán haciéndolo incluso después de la menopausia. [51] El estradiol también se produce en el cerebro y en las paredes arteriales .
En los hombres, aproximadamente entre el 15 y el 25% del estradiol circulante se produce en los testículos . [52] [53] El resto se sintetiza mediante la aromatización periférica de la testosterona en estradiol y de la androstenediona en estrona (que luego se transforma en estradiol mediante la 17β-HSD periférica). [52] [53] Esta aromatización periférica ocurre predominantemente en el tejido adiposo , pero también ocurre en otros tejidos como el hueso , el hígado y el cerebro . [52] Aproximadamente entre 40 y 50 μg de estradiol se producen por día en los hombres. [52]
Distribución
En el plasma, el estradiol se une en gran medida a la SHBG y a la albúmina . Solo alrededor del 2,21 % (± 0,04 %) del estradiol se encuentra libre y es biológicamente activo. El porcentaje permanece constante durante todo el ciclo menstrual . [54]
Metabolismo
Vías metabólicas del estradiol en humanos Estradiol no identificado no identificado Descripción: Vías metabólicas implicadas en el metabolismo del estradiol y otros estrógenos naturales (p. ej., estrona , estriol ) en los seres humanos. Además de las transformaciones metabólicas que se muestran en el diagrama, se produce conjugación (p. ej., sulfatación y glucuronidación ) en el caso del estradiol y los metabolitos del estradiol que tienen uno o más grupos hidroxilo (–OH) disponibles . Fuentes: Ver página de plantilla. |
La inactivación del estradiol incluye la conversión a estrógenos menos activos, como la estrona y el estriol. El estriol es el principal metabolito urinario . [ cita requerida ] El estradiol se conjuga en el hígado para formar conjugados de estrógeno como el sulfato de estradiol , el glucurónido de estradiol y, como tal, se excreta a través de los riñones . Algunos de los conjugados solubles en agua se excretan a través del conducto biliar y se reabsorben parcialmente después de la hidrólisis del tracto intestinal . Esta circulación enterohepática contribuye a mantener los niveles de estradiol.
El estradiol también se metaboliza por hidroxilación en estrógenos catecol . En el hígado, se metaboliza de forma no específica por CYP1A2 , CYP3A4 y CYP2C9 por 2-hidroxilación en 2-hidroxiestradiol , y por CYP2C9 , CYP2C19 y CYP2C8 por 17β-hidroxi deshidrogenación en estrona , [55] con otras enzimas del citocromo P450 (CYP) y transformaciones metabólicas involucradas también. [56]
El estradiol también se conjuga con un éster en formas lipoidales de estradiol como palmitato de estradiol y estearato de estradiol hasta cierto punto; estos ésteres se almacenan en el tejido adiposo y pueden actuar como un reservorio de estradiol de muy larga duración. [57] [58]
Excreción
El estradiol se excreta en forma de conjugados de estrógenos glucurónidos y sulfatos en la orina . Después de una inyección intravenosa de estradiol marcado en mujeres, casi el 90% se excreta en la orina y las heces en un plazo de 4 a 5 días. [59] [60] La recirculación enterohepática provoca un retraso en la excreción de estradiol. [59]
Niveles

Los niveles de estradiol en mujeres premenopáusicas son muy variables a lo largo del ciclo menstrual y los rangos de referencia varían ampliamente de una fuente a otra. [62] Los niveles de estradiol son mínimos y según la mayoría de los laboratorios varían de 20 a 80 pg/mL durante la fase folicular temprana a media (o la primera semana del ciclo menstrual, también conocida como menstruación). [63] [64] Los niveles de estradiol aumentan gradualmente durante este tiempo y a través de la fase folicular media a tardía (o la segunda semana del ciclo menstrual) hasta la fase preovulatoria. [62] [63] En el momento de la preovulación (un período de aproximadamente 24 a 48 horas), los niveles de estradiol aumentan brevemente y alcanzan sus concentraciones más altas de cualquier otro momento durante el ciclo menstrual. [62] Los niveles circulantes suelen estar entre 130 y 200 pg/mL en este momento, pero en algunas mujeres pueden llegar a 300 a 400 pg/mL, y el límite superior del rango de referencia de algunos laboratorios es incluso mayor (por ejemplo, 750 pg/mL). [62] [63] [65] [66] [67] Después de la ovulación (o mitad del ciclo) y durante la segunda mitad del ciclo menstrual o la fase lútea, los niveles de estradiol se estabilizan y fluctúan entre alrededor de 100 y 150 pg/mL durante la fase lútea temprana y media, y en el momento de la fase lútea tardía, o unos días antes de la menstruación, alcanzan un mínimo de alrededor de 40 pg/mL. [62] [64] Los niveles medios integrados de estradiol durante un ciclo menstrual completo han sido informados por diferentes fuentes como 80, 120 y 150 pg/mL. [64] [68] [69] Aunque existen informes contradictorios, un estudio encontró niveles medios integrados de estradiol de 150 pg/mL en mujeres más jóvenes, mientras que los niveles medios integrados oscilaron entre 50 y 120 pg/mL en mujeres mayores. [69]
Durante los años reproductivos de las mujeres humanas, los niveles de estradiol son algo más altos que los de estrona, excepto durante la fase folicular temprana del ciclo menstrual; por lo tanto, el estradiol puede considerarse el estrógeno predominante durante los años reproductivos femeninos humanos en términos de niveles séricos absolutos y actividad estrogénica. [ cita requerida ] Durante el embarazo, el estriol se convierte en el estrógeno circulante predominante, y este es el único momento en el que el estetrol se encuentra en el cuerpo, mientras que durante la menopausia, predomina la estrona (ambos basados en los niveles séricos). [ cita requerida ] El estradiol producido por los humanos varones, a partir de la testosterona, está presente en niveles séricos aproximadamente comparables a los de las mujeres posmenopáusicas (14-55 versus <35 pg/mL, respectivamente). [ cita requerida ] También se ha informado que si se comparan las concentraciones de estradiol en un hombre de 70 años con las de una mujer de 70 años, los niveles son aproximadamente de 2 a 4 veces más altos en el hombre. [70]
| Grupo | E2 ( prod .) | E2 (niveles) | E1 (niveles) | Relación |
|---|---|---|---|---|
| Niñas púberes Estadio I de Tanner (infancia) Estadio II de Tanner (edades 8 a 12) Estadio III de Tanner (edades 10 a 13) Estadio IV de Tanner (edades 11 a 14) Estadio V de Tanner (edades 12 a 15) Folicular (días 1 a 14) Lútea (días 15 a 28) | ? ? ? ? ? ? | 9 (<9–20) pg/ml 15 (<9–30) pg/ml 27 (<9–60) pg/ml 55 (16–85) pg/ml 50 (30–100) pg/ml 130 ( 70–300) pg/ml | 13 (<9–23) pg/mL 18 (10–37) pg/mL 26 (17–58) pg/mL 36 (23–69) pg/mL 44 (30–89) pg/mL 75 (39– 160) pg/mL | ? ? ? ? ? ? |
| Niños prepúberes | ? | 2–8 pg/ml | ? | ? |
| Mujeres premenopáusicas Fase folicular temprana (días 1 a 4) Fase folicular media (días 5 a 9) Fase folicular tardía (días 10 a 14) Fase lútea (días 15 a 28) Anticonceptivo oral ( anovulatorio ) | 30–100 μg/día 100–160 μg/día 320–640 μg/día 300 μg/día ? | 40 a 60 pg/ml 60 a 100 pg/ml 200 a 400 pg /ml 190 pg/ml 12 a 50 pg/ml | ¿40–60 pg/ml ? 170–200 pg/ml 100–150 pg/ml ? | 0,5–1 ? 1–2 1,5 ? |
| Mujeres posmenopáusicas | 18 μg/día | 5–20 pg/ml | 30–70 pg/ml | 0,3–0,8 |
| Mujeres embarazadas Primer trimestre (semanas 1 a 12) Segundo trimestre (semanas 13 a 26) Tercer trimestre (semanas 27 a 40) | ? ? ? | 1000 a 5000 pg/ml 5000 a 15 000 pg/ml 10 000 a 40 000 pg/ml | ? ? ? | ? ? ? |
| Hombres a | 20–60 μg/día | 27 (20–55) pg/ml | 20–90 pg/ml | 0,4–0,6 |
| Notas al pie: a = El formato es "valor medio (rango)" o simplemente "rango". Fuentes: [71] [72] [73] [74] [75] [61] [76] | ||||
Medición
En las mujeres, el estradiol sérico se mide en un laboratorio clínico y refleja principalmente la actividad de los ovarios. El análisis de sangre de estradiol mide la cantidad de estradiol en la sangre. [77] Se utiliza para comprobar la función de los ovarios, la placenta y las glándulas suprarrenales. [77] Esto puede detectar el estrógeno basal en mujeres con amenorrea o disfunción menstrual, y para detectar el estado de hipoestrogenicidad y menopausia. Además, el control de estrógenos durante la terapia de fertilidad evalúa el crecimiento folicular y es útil para controlar el tratamiento. Los tumores productores de estrógenos mostrarán niveles altos persistentes de estradiol y otros estrógenos. En la pubertad precoz , los niveles de estradiol aumentan de forma inapropiada.
Rangos
Los resultados de laboratorio individuales siempre deben interpretarse utilizando los rangos proporcionados por el laboratorio que realizó la prueba.
| Tipo de paciente | Límite inferior | Límite superior | Unidad |
|---|---|---|---|
| Macho adulto | 50 [78] | 200 [78] | pmol/L |
| 14 | 55 | pg/ml | |
| Hembra adulta ( fase folicular , día 5) | 70 [78] 95% PI (estándar) | 500 [78] 95 % IP | pmol/L |
| 110 [79] 90% PI (usado en el diagrama ) | 220 [79] 90% IP | ||
| 19 (95% IP) | 140 (95 % IP) | pg/ml | |
| 30 (90% IP) | 60 (90% IP) | ||
| Hembra adulta ( pico preovulatorio ) | 400 [78] | 1500 [78] | pmol/L |
| 110 | 410 | pg/ml | |
| Hembra adulta ( fase lútea ) | 70 [78] | 600 [78] | pmol/L |
| 19 | 160 | pg/ml | |
| Hembra adulta – libre (no unida a proteínas) | 0.5 [80] [ ¿investigación original? ] | 9 [80] [ ¿Investigación original? ] | pg/ml |
| 1.7 [80] [ ¿Investigación original? ] | 33 [80] [ ¿Investigación original? ] | pmol/L | |
| Mujer posmenopáusica | No aplica [78] | < 130 [78] | pmol/L |
| N / A | <35 | pg/ml |
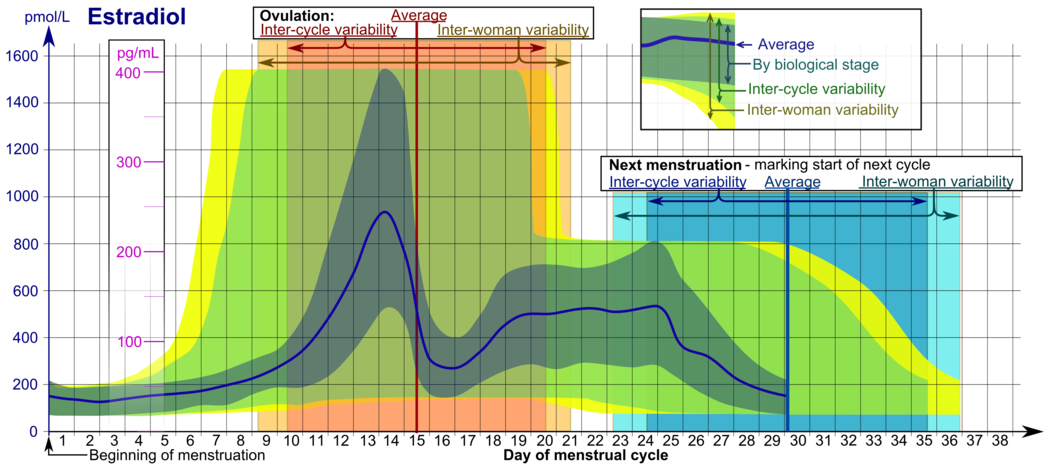
- Los rangos denotados Por etapa biológica pueden usarse en ciclos menstruales monitoreados de cerca con respecto a otros marcadores de su progresión biológica, comprimiéndose o estirándose la escala de tiempo a cuánto más rápido o más lento, respectivamente, progresa el ciclo en comparación con un ciclo promedio.
- Los rangos denotados Variabilidad interciclo son más apropiados para usar en ciclos no monitoreados con solo el comienzo de la menstruación conocido, pero donde la mujer conoce con precisión las duraciones promedio de su ciclo y el momento de la ovulación, y que son algo regulares en promedio, comprimiéndose o estirándose la escala de tiempo a cuánto es más corta o más larga la duración promedio del ciclo de una mujer, respectivamente, que el promedio de la población.
- Los rangos denotados Variabilidad intermujer son más apropiados para usar cuando se desconocen las duraciones promedio del ciclo y el momento de la ovulación, pero solo se da el comienzo de la menstruación. [81]
En el ciclo menstrual normal, los niveles de estradiol suelen ser <50 pg/mL durante la menstruación, aumentan con el desarrollo folicular (pico: 200 pg/mL), descienden brevemente durante la ovulación y vuelven a aumentar durante la fase lútea hasta alcanzar un segundo pico. Al final de la fase lútea, los niveles de estradiol descienden hasta sus niveles menstruales, a menos que haya un embarazo.
Durante el embarazo, los niveles de estrógeno, incluido el estradiol, aumentan de forma constante hacia el término. La fuente de estos estrógenos es la placenta , que aromatiza las prohormonas producidas en la glándula suprarrenal fetal.
| Sexo | Hormona sexual | Fase reproductiva | Tasa de producción de sangre | Tasa de secreción gonadal | Tasa de depuración metabólica | Rango de referencia (niveles séricos) | |
|---|---|---|---|---|---|---|---|
| Unidades del SI | Unidades no pertenecientes al SI | ||||||
| Hombres | Androstenediona | – | 2,8 mg/día | 1,6 mg/día | 2200 L/día | 2,8–7,3 nmol/L | 80–210 ng/dl |
| Testosterona | – | 6,5 mg/día | 6,2 mg/día | 950 L/día | 6,9–34,7 nmol/L | 200–1000 ng/dl | |
| Estrona | – | 150 μg/día | 110 μg/día | 2050 L/día | 37–250 pmol/L | 10–70 pg/ml | |
| Estradiol | – | 60 μg/día | 50 μg/día | 1600 L/día | <37–210 pmol/L | 10–57 pg/ml | |
| Sulfato de estrona | – | 80 μg/día | Insignificante | 167 L/día | 600–2500 pmol/L | 200–900 pg/ml | |
| Mujer | Androstenediona | – | 3,2 mg/día | 2,8 mg/día | 2000 L/día | 3,1–12,2 nmol/L | 89–350 ng/dl |
| Testosterona | – | 190 μg/día | 60 μg/día | 500 L/día | 0,7–2,8 nmol/L | 20–81 ng/dl | |
| Estrona | Fase folicular | 110 μg/día | 80 μg/día | 2200 L/día | 110–400 pmol/L | 30–110 pg/ml | |
| Fase lútea | 260 μg/día | 150 μg/día | 2200 L/día | 310–660 pmol/L | 80–180 pg/ml | ||
| Posmenopausia | 40 μg/día | Insignificante | 1610 L/día | 22–230 pmol/L | 6–60 pg/ml | ||
| Estradiol | Fase folicular | 90 μg/día | 80 μg/día | 1200 L/día | <37–360 pmol/L | 10–98 pg/ml | |
| Fase lútea | 250 μg/día | 240 μg/día | 1200 L/día | 699–1250 pmol/L | 190–341 pg/ml | ||
| Posmenopausia | 6 μg/día | Insignificante | 910 L/día | <37–140 pmol/L | 10–38 pg/ml | ||
| Sulfato de estrona | Fase folicular | 100 μg/día | Insignificante | 146 L/día | 700–3600 pmol/L | 250–1300 pg/ml | |
| Fase lútea | 180 μg/día | Insignificante | 146 L/día | 1100–7300 pmol/L | 400–2600 pg/ml | ||
| Progesterona | Fase folicular | 2 mg/día | 1,7 mg/día | 2100 L/día | 0,3–3 nmol/L | 0,1–0,9 ng/ml | |
| Fase lútea | 25 mg/día | 24 mg/día | 2100 L/día | 19–45 nmol/L | 6–14 ng/ml | ||
Notas y fuentes Notas: "La concentración de un esteroide en la circulación está determinada por la velocidad a la que se secreta de las glándulas, la velocidad del metabolismo del precursor o las prehormonas en el esteroide y la velocidad a la que es extraído por los tejidos y metabolizado. La tasa de secreción de un esteroide se refiere a la secreción total del compuesto de una glándula por unidad de tiempo. Las tasas de secreción se han evaluado tomando muestras del efluente venoso de una glándula a lo largo del tiempo y restando la concentración de hormona arterial y venosa periférica. La tasa de depuración metabólica de un esteroide se define como el volumen de sangre que se ha depurado completamente de la hormona por unidad de tiempo. La tasa de producción de una hormona esteroide se refiere a la entrada en la sangre del compuesto de todas las fuentes posibles, incluida la secreción de las glándulas y la conversión de prohormonas en el esteroide de interés. En estado estacionario, la cantidad de hormona que entra en la sangre de todas las fuentes será igual a la velocidad a la que se está depurando (tasa de depuración metabólica) multiplicada por la concentración en sangre (tasa de producción = tasa de depuración metabólica × concentración). Si hay poca contribución del metabolismo de las prohormonas al conjunto circulante de esteroides, entonces la tasa de producción se aproximará a la tasa de secreción". Fuentes: Ver plantilla. | |||||||
Uso médico
El estradiol se utiliza como medicamento , principalmente en la terapia hormonal para los síntomas de la menopausia , así como en la terapia hormonal feminizante para personas trans. [82]
Química
El estradiol es un esteroide estrano . [82] También se lo conoce como 17β-estradiol (para distinguirlo del 17α-estradiol ) o como estra-1,3,5(10)-trieno-3,17β-diol. Tiene dos grupos hidroxilo , uno en la posición C3 y el otro en la posición 17β, así como tres dobles enlaces en el anillo A. Debido a sus dos grupos hidroxilo, el estradiol a menudo se abrevia como E2. Los estrógenos estructuralmente relacionados, estrona (E1), estriol (E3) y estetrol (E4) tienen uno, tres y cuatro grupos hidroxilo, respectivamente.
Neuropsicofarmacología
En un estudio aleatorizado, doble ciego y controlado con placebo, se demostró que el estradiol tiene efectos específicos de género en la sensibilidad a la justicia. En general, cuando la división de una cantidad dada de dinero se enmarcaba como justa o injusta en una versión modificada del juego del ultimátum , el estradiol aumentó la tasa de aceptación de propuestas enmarcadas en términos justos entre los hombres y la disminuyó entre las mujeres. Sin embargo, entre el grupo placebo, "la mera creencia de recibir tratamiento con estradiol aumentó significativamente la aceptación de ofertas enmarcadas en términos injustos en ambos sexos", lo que indica que los llamados factores "ambientales" desempeñaron un papel en la organización de las respuestas hacia estas presentaciones del juego del ultimátum . [83]
Historia
El descubrimiento del estrógeno se atribuye generalmente a los científicos estadounidenses Edgar Allen y Edward A. Doisy . [84] [85] En 1923, observaron que la inyección de líquido de folículos ováricos porcinos producía cambios de tipo puberal y estral (incluidos cambios vaginales , uterinos y de las glándulas mamarias y receptividad sexual ) en ratones y ratas sexualmente inmaduros y ovariectomizados . [84] [85] [86] Estos hallazgos demostraron la existencia de una hormona producida por los ovarios y que está involucrada en la maduración sexual y la reproducción . [84] [85] [86] En el momento de su descubrimiento, Allen y Doisy no nombraron la hormona, y simplemente se refirieron a ella como una "hormona ovárica" u "hormona folicular"; [85] otros se refirieron a ella de diversas formas como feminina , foliculina , menformón , telicinina y emmenina . [87] [88] En 1926, Parkes y Bellerby acuñaron el término estrina para describir la hormona basándose en su capacidad para inducir el estro en animales. [89] [87] La estrona fue aislada y purificada independientemente por Allen y Doisy y el científico alemán Adolf Butenandt en 1929, y el estriol fue aislado y purificado por Marrian en 1930; fueron los primeros estrógenos en ser identificados. [85] [90] [91]
El estradiol, el más potente de los tres estrógenos principales, fue el último de los tres en ser identificado. [85] [89] Fue descubierto por Schwenk y Hildebrant en 1933, quienes lo sintetizaron mediante la reducción de la estrona. [85] El estradiol fue posteriormente aislado y purificado de los ovarios de cerdas por Doisy en 1935, con su estructura química determinada simultáneamente, [92] y fue referido de diversas formas como dihidroteelina , dihidrofoliculina , hormona dihidrofolicular y dihidroxiestrina . [85] [93] [94] En 1935, el nombre estradiol y el término estrógeno fueron establecidos formalmente por el Comité de Hormonas Sexuales de la Organización de la Salud de la Liga de las Naciones ; Esto siguió a los nombres estrona (que inicialmente se llamó theelin, progynon, folliculin y ketohydroxyestrin) y estriol (inicialmente llamado theelol y trihydroxyestrin) habiendo sido establecidos en 1932 en la primera reunión de la Conferencia Internacional sobre la Estandarización de Hormonas Sexuales en Londres . [89] [95] Después de su descubrimiento, Inhoffen y Hohlweg desarrollaron una síntesis parcial de estradiol a partir del colesterol en 1940, y Anner y Miescher desarrollaron una síntesis total en 1948. [85]
Sociedad y cultura
Etimología
El nombre estradiol deriva de estra- , griego οἶστρος ( oistros , que literalmente significa "brío o inspiración"), [96] que se refiere al sistema de anillo esteroide estrano , y -diol , un término químico y sufijo que indica que el compuesto es un tipo de alcohol que lleva dos grupos hidroxilo .
Referencias
- ^ Ford SR, Roach SS (7 de octubre de 2013). Farmacología clínica introductoria de Roach. Lippincott Williams & Wilkins. pp. 525–. ISBN 978-1-4698-3214-2.
- ^ Hochadel M (1 de abril de 2015). Referencia de medicamentos de Mosby para profesionales de la salud. Elsevier Health Sciences. págs. 602–. ISBN 978-0-323-31103-8.
- ^ abcde Stanczyk FZ, Archer DF, Bhavnani BR (junio de 2013). "Etinilestradiol y 17β-estradiol en anticonceptivos orales combinados: farmacocinética, farmacodinamia y evaluación de riesgos". Anticoncepción . 87 (6): 706–27. doi :10.1016/j.contraception.2012.12.011. PMID 23375353.
- ^ Falcone T, Hurd WW (2007). Medicina y cirugía reproductiva clínica. Elsevier Health Sciences. pp. 22–. ISBN 978-0-323-03309-1Archivado desde el original el 10 de enero de 2023 . Consultado el 22 de octubre de 2016 .
- ^ Price TM, Blauer KL, Hansen M, Stanczyk F, Lobo R, Bates GW (marzo de 1997). "Farmacocinética de dosis única de administración sublingual versus oral de 17 beta-estradiol micronizado". Obstetricia y ginecología . 89 (3): 340–5. doi :10.1016/S0029-7844(96)00513-3. PMID 9052581. S2CID 71641652.
- ^ Naunton M, Al Hadithy AF, Brouwers JR, Archer DF (2006). "Gel de estradiol: revisión de la farmacología, farmacocinética, eficacia y seguridad en mujeres menopáusicas". Menopausia . 13 (3): 517–27. doi :10.1097/01.gme.0000191881.52175.8c. PMID 16735950. S2CID 42748448.
- ^ Ryan KJ (agosto de 1982). "Bioquímica de la aromatasa: importancia para la fisiología reproductiva femenina". Cancer Research . 42 (8 Suppl): 3342s–3344s. PMID 7083198.
- ^ Mechoulam R, Brueggemeier RW, Denlinger DL (septiembre de 1984). "Estrógenos en insectos". Ciencias de la vida celular y molecular . 40 (9): 942–944. doi :10.1007/BF01946450. S2CID 31950471.
- ^ Ozon R (1972). "Estrógenos en peces, anfibios, reptiles y aves". En Idler DR (ed.). Esteroides en vertebrados no mamíferos . Oxford: Elsevier Science. págs. 390–414. ISBN 978-0323140980Archivado desde el original el 10 de enero de 2023 . Consultado el 17 de octubre de 2020 .
- ^ Saldanha, Colin J., Luke Remage-Healey y Barney A. Schlinger. "Señalización sináptica: síntesis y acción de esteroides en la sinapsis". Endocrine reviews 32.4 (2011): 532–549.
- ^ abc McMillan JA, Feigin RD, DeAngelis C, Jones MD (2006). Pediatría de Oski: principios y práctica. Lippincott Williams & Wilkins. págs. 550–. ISBN 978-0-7817-3894-1.
- ^ abc Craig CR, Stitzel RE (2004). Farmacología moderna con aplicaciones clínicas. Lippincott Williams & Wilkins. págs. 706–. ISBN 978-0-7817-3762-3.
- ^ Preedy VR (2 de diciembre de 2011). Manual de crecimiento y seguimiento del crecimiento en la salud y la enfermedad. Springer Science & Business Media. pp. 2661–. ISBN 978-1-4419-1794-2Archivado desde el original el 10 de enero de 2023 . Consultado el 9 de junio de 2017 .
- ^ Carreau S, Lambard S, Delalande C, Denis-Galeraud I, Bilinska B, Bourguiba S (abril de 2003). "Expresión de la aromatasa y función de los estrógenos en las gónadas masculinas: una revisión". Biología reproductiva y endocrinología . 1 : 35. doi : 10.1186/1477-7827-1-35 . PMC 155680. PMID 12747806 .
- ^ Pentikäinen V, Erkkilä K, Suomalainen L, Parvinen M, Dunkel L (mayo de 2000). "El estradiol actúa como factor de supervivencia de las células germinales en el testículo humano in vitro". La Revista de Endocrinología Clínica y Metabolismo . 85 (5): 2057–67. doi : 10.1210/jcem.85.5.6600 . PMID 10843196.
- ^ Sharpe RM, Skakkebaek NE (mayo de 1993). "¿Están los estrógenos involucrados en la disminución del recuento de espermatozoides y en los trastornos del tracto reproductivo masculino?". Lancet . 341 (8857): 1392–5. doi :10.1016/0140-6736(93)90953-E. PMID 8098802. S2CID 33135527.
- ^ Handelsman DJ (2001). "Estrógenos y disminución del recuento de espermatozoides". Reproducción, fertilidad y desarrollo . 13 (4): 317–24. doi :10.1071/rd00103. PMID 11800170.
- ^ Fisch H, Goldstedin R (2003). "Environmental estrogens and sperm counts" (PDF) . Química pura y aplicada . 75 (11–12): 2181–2193. doi :10.1351/pac200375112181. S2CID 11068097. Archivado desde el original (PDF) el 4 de marzo de 2016 . Consultado el 29 de diciembre de 2015 .
- ^ Raman JD, Schlegel PN (febrero de 2002). "Inhibidores de la aromatasa para la infertilidad masculina". The Journal of Urology . 167 (2 Pt 1): 624–9. doi :10.1016/S0022-5347(01)69099-2. PMID 11792932.
- ^ Visootsak J, Graham JM (octubre de 2006). "Síndrome de Klinefelter y otras aneuploidías cromosómicas sexuales". Orphanet Journal of Rare Diseases . 1 (42): 42. doi : 10.1186/1750-1172-1-42 . PMC 1634840 . PMID 17062147.
- ^ Vanderschueren D, Laurent MR, Claessens F, Gielen E, Lagerquist MK, Vandenput L, et al. (Diciembre de 2014). "Acciones de los esteroides sexuales en los huesos masculinos". Revisiones endocrinas . 35 (6): 906–60. doi :10.1210/er.2014-1024. PMC 4234776 . PMID 25202834.
- ^ Carani C, Qin K, Simoni M, Faustini-Fustini M, Serpente S, Boyd J, et al. (Julio de 1997). "Efecto de la testosterona y el estradiol en un hombre con deficiencia de aromatasa". La Revista de Medicina de Nueva Inglaterra . 337 (2): 91–5. doi : 10.1056/NEJM199707103370204 . PMID 9211678.
- ^ Bergh C, Wennergren D, Möller M, Brisby H (21 de diciembre de 2020). "Incidencia de fracturas en adultos en relación con la edad y el género: un estudio de 27.169 fracturas en el Registro Sueco de Fracturas en un área de captación bien definida". PLOS ONE . 15 (12): e0244291. Bibcode :2020PLoSO..1544291B. doi : 10.1371/journal.pone.0244291 . PMC 7751975 . PMID 33347485.
- ^ Albright F , Smith PH, Richardson AM (31 de mayo de 1941). "Osteoporosis posmenopáusica: sus características clínicas". JAMA . 116 (22): 2465–2474. doi :10.1001/jama.1941.02820220007002.
- ^ abcdefgh Raine-Fenning NJ, Brincat MP, Muscat-Baron Y (2003). "Envejecimiento de la piel y menopausia: implicaciones para el tratamiento". American Journal of Clinical Dermatology . 4 (6): 371–8. doi :10.2165/00128071-200304060-00001. PMID 12762829. S2CID 20392538.
- ^ abcdefgh Holzer G, Riegler E, Hönigsmann H, Farokhnia S, Schmidt JB, Schmidt B (septiembre de 2005). "Efectos y efectos secundarios de la crema de progesterona al 2% en la piel de mujeres peri y posmenopáusicas: resultados de un estudio doble ciego, controlado con vehículo y aleatorizado". The British Journal of Dermatology . 153 (3): 626–34. doi :10.1111/j.1365-2133.2005.06685.x. PMID 16120154. S2CID 6077829.
- ^ Behl C, Widmann M, Trapp T, Holsboer F (noviembre de 1995). "El 17-beta estradiol protege a las neuronas de la muerte celular inducida por estrés oxidativo in vitro". Biochemical and Biophysical Research Communications . 216 (2): 473–82. doi :10.1006/bbrc.1995.2647. PMID 7488136.
- ^ Meethal SV, Liu T, Chan HW, Ginsburg E, Wilson AC, Gray DN, Bowen RL, Vonderhaar BK, Atwood CS (agosto de 2009). "Identificación de un circuito regulador para la síntesis de neuroesteroides: un mecanismo regulador agudo esteroidogénico dependiente de proteínas que involucra receptores del eje hipotálamo-hipofisario-gonadal". Journal of Neurochemistry . 110 (3): 1014–27. doi :10.1111/j.1471-4159.2009.06192.x. PMC 2789665 . PMID 19493163.
- ^ Douma SL, Husband C, O'Donnell ME, Barwin BN, Woodend AK (2005). "Trastornos del estado de ánimo relacionados con los estrógenos: factores del ciclo de vida reproductivo". Avances en la ciencia de la enfermería . 28 (4): 364–75. doi :10.1097/00012272-200510000-00008. PMID 16292022. S2CID 9172877.
- ^ Lasiuk GC, Hegadoren KM (octubre de 2007). "Los efectos del estradiol en los sistemas serotoninérgicos centrales y su relación con el estado de ánimo en las mujeres". Investigación biológica para enfermería . 9 (2): 147–60. doi :10.1177/1099800407305600. PMID 17909167. S2CID 37965502.
- ^ Hulshoff HE, Cohen-Kettenis PT, Van Haren NE, Peper JS, Brans RG, Cahn W, Schnack HG, Gooren LJ, Kahn RS (julio de 2006). "Cambiar de sexo cambia el cerebro: influencias de la testosterona y el estrógeno en la estructura del cerebro humano adulto". Revista Europea de Endocrinología . 155 (suppl_1): 107–114. doi : 10.1530/eje.1.02248 .
- ^ Harding CF (junio de 2004). «Modulación hormonal del canto: modulación hormonal del cerebro de las aves cantoras y comportamiento de canto». Anales de la Academia de Ciencias de Nueva York . 1016 (1): 524–39. Código Bibliográfico : 2004NYASA1016..524H. doi : 10.1196/annals.1298.030. PMID 15313793. S2CID 12457330. Archivado desde el original el 27 de septiembre de 2007.
- ^ Simerly RB (27 de marzo de 2002). "Wired for playback: organization and development of sexually dimorphic circuits in the mammalian forebrain" (PDF) . Revisión anual de neurociencia . 25 : 507–36. doi :10.1146/annurev.neuro.25.112701.142745. PMID 12052919. Archivado desde el original (PDF) el 1 de octubre de 2008. Consultado el 7 de marzo de 2007 .
- ^ Goldstein I, Meston CM, Davis S, Traish A (17 de noviembre de 2005). Función y disfunción sexual de la mujer: estudio, diagnóstico y tratamiento. CRC Press. pp. 205–. ISBN 978-1-84214-263-9.
- ^ Acevedo-Rodríguez A, Mani SK, Handa RJ (2015). "Receptor β de oxitocina y estrógeno en el cerebro: una descripción general". Fronteras en Endocrinología . 6 : 160. doi : 10.3389/fendo.2015.00160 . PMC 4606117 . PMID 26528239.
- ^ Bulzomi P, Bolli A, Galluzzo P, Leone S, Acconcia F, Marino M (enero de 2010). "La coadministración de naringenina y 17beta-estradiol previene el crecimiento de células cancerosas humanas inducidas por hormonas". IUBMB Life . 62 (1): 51–60. doi : 10.1002/iub.279 . PMID 19960539. S2CID 7903757.
- ^ Sreeja S, Santhosh Kumar TR, Lakshmi BS, Sreeja S (julio de 2012). "El extracto de granada demuestra un perfil modulador selectivo del receptor de estrógeno en líneas celulares tumorales humanas y modelos in vivo de privación de estrógeno". The Journal of Nutritional Biochemistry . 23 (7): 725–32. doi :10.1016/j.jnutbio.2011.03.015. PMID 21839626.
- ^ Thomas CG, Strom A, Lindberg K, Gustafsson JA (junio de 2011). "El receptor de estrógeno beta disminuye la supervivencia de las células cancerosas defectuosas en p53 después de un daño en el ADN al afectar la señalización del punto de control G₂/M". Investigación y tratamiento del cáncer de mama . 127 (2): 417–27. doi :10.1007/s10549-010-1011-z. PMID 20623183. S2CID 6752694.
- ^ Collins P, Rosano GM, Sarrel PM, Ulrich L, Adamopoulos S, Beale CM, McNeill JG, Poole-Wilson PA (julio de 1995). "El 17 beta-estradiol atenúa la constricción arterial coronaria inducida por acetilcolina en mujeres pero no en hombres con enfermedad cardíaca coronaria". Circulation . 92 (1): 24–30. doi :10.1161/01.CIR.92.1.24. PMID 7788912.
- ^ Knowlton, AA; Lee, AR (julio de 2012). "Estrógeno y sistema cardiovascular". Farmacología y terapéutica . 135 (1): 54–70. doi :10.1016/j.pharmthera.2012.03.007. PMC 5688223 . PMID 22484805.
- ^ Abdul Sultan A, West J, Stephansson O, Grainge MJ, Tata LJ, Fleming KM, Humes D, Ludvigsson JF (noviembre de 2015). "Definición de tromboembolia venosa y medición de su incidencia mediante registros sanitarios suecos: un estudio de cohorte de embarazos a nivel nacional". BMJ Open . 5 (11): e008864. doi :10.1136/bmjopen-2015-008864. PMC 4654387 . PMID 26560059.
- ^ Prossnitz ER, Barton M (mayo de 2014). "Biología del estrógeno: nuevos conocimientos sobre la función de GPER y oportunidades clínicas". Endocrinología molecular y celular . 389 (1–2): 71–83. doi :10.1016/j.mce.2014.02.002. PMC 4040308 . PMID 24530924.
- ^ Prossnitz ER, Arterburn JB, Sklar LA (2007). "GPR30: receptor acoplado a proteína AG para estrógeno". Mol. Cell. Endocrinol . 265–266: 138–42. doi :10.1016/j.mce.2006.12.010. PMC 1847610. PMID 17222505 .
- ^ Soltysik K, Czekaj P (abril de 2013). "Receptores de estrógeno de membrana: ¿son una forma alternativa de acción del estrógeno?". Journal of Physiology and Pharmacology . 64 (2): 129–42. PMID 23756388.
- ^ Micevych PE, Kelly MJ (2012). "Regulación de la función hipotalámica por el receptor de estrógeno de membrana". Neuroendocrinología . 96 (2): 103–10. doi :10.1159/000338400. PMC 3496782 . PMID 22538318.
- ^ Labhart A (6 de diciembre de 2012). Endocrinología clínica: teoría y práctica. Springer Science & Business Media. pp. 548–. ISBN 978-3-642-96158-8Archivado desde el original el 10 de enero de 2023 . Consultado el 11 de noviembre de 2018 .
- ^ Tucker SB (2007). Fisiología materna, fetal y neonatal: una perspectiva clínica. Elsevier Health Sciences. pp. 43–. ISBN 978-1-4160-2944-1Archivado desde el original el 10 de enero de 2023 . Consultado el 7 de junio de 2017 .
- ^ ab Hall JE (31 de mayo de 2015). Guyton and Hall Textbook of Medical Physiology E-Book. Elsevier Health Sciences. págs. 1043–. ISBN 978-0-323-38930-3.
- ^ Häggström M, Richfield D (2014). "Diagrama de las vías de la esteroidogénesis humana". WikiJournal of Medicine . 1 (1). doi : 10.15347/wjm/2014.005 . ISSN 2002-4436.
- ^ Boron WF, Boulpaep EL (2003). Fisiología médica: un enfoque celular y molecular . Elsevier/Saunders. pág. 1300. ISBN 978-1-4160-2328-9.
- ^ Mutschler E, Schäfer-Korting M (2001). Arzneimittelwirkungen (en alemán) (8 ed.). Stuttgart: Wissenschaftliche Verlagsgesellschaft. págs.434, 444. ISBN 978-3-8047-1763-3.
- ^ abcd Melmed S (1 de enero de 2016). Williams Textbook of Endocrinology. Elsevier Health Sciences. págs. 710–. ISBN 978-0-323-29738-7Archivado desde el original el 10 de enero de 2023 . Consultado el 21 de marzo de 2018 .
- ^ ab Marcus R, Feldman D, Dempster DW, Luckey M, Cauley JA (13 de junio de 2013). Osteoporosis. Academic Press. págs. 331–. ISBN 978-0-12-398252-0.
- ^ Wu CH, Motohashi T, Abdel-Rahman HA, Flickinger GL, Mikhail G (agosto de 1976). "Estradiol-17 beta plasmático libre y unido a proteínas durante el ciclo menstrual". Revista de endocrinología clínica y metabolismo . 43 (2): 436–45. doi :10.1210/jcem-43-2-436. PMID 950372.
- ^ Cheng ZN, Shu Y, Liu ZQ, Wang LS, Ou-Yang DS, Zhou HH (febrero de 2001). "Papel del citocromo P450 en el metabolismo del estradiol in vitro". Acta Pharmacologica Sinica . 22 (2): 148–54. PMID 11741520.
- ^ Lee AJ, Cai MX, Thomas PE, Conney AH, Zhu BT (agosto de 2003). "Caracterización de los metabolitos oxidativos de 17beta-estradiol y estrona formados por 15 isoformas del citocromo p450 humano expresadas selectivamente". Endocrinología . 144 (8): 3382–98. doi : 10.1210/en.2003-0192 . PMID 12865317.
- ^ Oettel M, Schillinger E (6 de diciembre de 2012). Estrógenos y antiestrógenos I: fisiología y mecanismos de acción de los estrógenos y antiestrógenos. Springer Science & Business Media. págs. 235–237. ISBN 978-3-642-58616-3.
- ^ Oettel M, Schillinger E (6 de diciembre de 2012). Estrógenos y antiestrógenos II: farmacología y aplicación clínica de estrógenos y antiestrógenos. Springer Science & Business Media. pp. 268, 271. ISBN 978-3-642-60107-1.
- ^ ab Dorfman, Ralph I. (1961). "Metabolismo de las hormonas esteroides". Isótopos radiactivos en fisiología, diagnóstico y terapia / Künstliche Radioaktive Isotope in Physiologie Diagnostik und Therapie . págs. 1223-1241. doi :10.1007/978-3-642-49761-2_39. ISBN 978-3-642-49477-2.
- ^ Sandberg AA, Slaunwhite WR (agosto de 1957). "Estudios sobre esteroides fenólicos en sujetos humanos. II. El destino metabólico y la circulación hepatobiliar-entérica de C14-estrona y C14-estradiol en mujeres". J. Clin. Invest . 36 (8): 1266–78. doi :10.1172/JCI103524. PMC 1072719 . PMID 13463090.
- ^ ab "Estradiol" (PDF) . ilexmedical.com . Archivado (PDF) del original el 4 de febrero de 2024 . Consultado el 4 de julio de 2024 .
- ^ abcde Becker JB, Berkley KJ, Geary N, Hampson E, Herman JP , Young E (4 de diciembre de 2007). Diferencias sexuales en el cerebro: de los genes a la conducta. Oxford University Press. pp. 64–. ISBN 978-0-19-804255-6Los niveles de estradiol
son mínimos durante los primeros días de la fase folicular, pero se liberan concentraciones crecientes en la circulación general a medida que el folículo madura. Los niveles más altos se alcanzan aproximadamente de 24 a 48 horas antes del pico de LH. De hecho, el pico preovulatorio de estradiol representa su concentración más alta durante todo el ciclo menstrual. Las concentraciones séricas en este momento son típicamente de alrededor de 130-200 pg/mL, pero se pueden alcanzar concentraciones tan altas como 300-400 pg/mL en algunas mujeres. Después de una caída transitoria asociada con la ovulación, la secreción de estradiol se restablece por la producción del cuerpo lúteo durante la fase lútea. Los niveles de meseta de alrededor de 100-150 pg/mL (Abraham, 1978; Thorneycroft et al., 1971) se observan con mayor frecuencia durante el período de −10 a −5 días antes del inicio de la menstruación. Con la regresión del cuerpo lúteo, los niveles de estradiol disminuyen, gradualmente en algunas mujeres y precipitadamente en otras, durante los últimos días de la fase lútea. Esto marca el comienzo de la menstruación, el desprendimiento del endometrio. El estradiol sérico durante la menstruación es de aproximadamente 30 a 50 pg/ml. (Fuente.)
- ^ abc Strauss JR, Barbieri RL (2009). Endocrinología reproductiva de Yen y Jaffe: fisiología, fisiopatología y tratamiento clínico. Elsevier Health Sciences. págs. 807–. ISBN 978-1-4160-4907-4. Archivado del original el 10 de enero de 2023 . Consultado el 21 de diciembre de 2016 .
En la mayoría de los laboratorios, los niveles séricos de estradiol varían de 20 a 80 pg/mL durante la fase folicular temprana a media del ciclo menstrual y alcanzan un máximo de 200 a 500 pg/mL durante el pico preovulatorio. Durante la fase lútea media, los niveles séricos de estradiol varían de 60 a 200 pg/mL.
- ^ abc Christian C, von Schoultz B (15 de marzo de 1994). Terapia de reemplazo hormonal: ¿Dosis estandarizadas o adaptadas individualmente?. CRC Press. pp. 60–. ISBN 978-1-85070-545-1Los niveles plasmáticos de estradiol varían de 40 a 80 pg/mL durante la primera semana del ciclo ovárico (fase folicular temprana) y de 80 a 300 pg /
mL durante la segunda semana (fase folicular media y tardía, incluido el pico periovulatorio). Luego, durante la tercera y cuarta semanas, el estradiol fluctúa entre 100 y 150 pg/mL (fase lútea temprana y media) hasta 40 pg/mL unos días antes de la menstruación (fase lútea tardía). El nivel medio integrado de estradiol durante un ciclo normal completo de 28 días es de alrededor de 80 pg/mL.
- ^ Jameson JL, De Groot LJ (18 de mayo de 2010). Endocrinología: adultos y niños. Elsevier Health Sciences. pp. 2812–. ISBN 978-1-4557-1126-0A mitad del ciclo
: 150-750 pg/mL
- ^ Hay ID, Wass JA (26 de enero de 2009). Oncología endocrina clínica. John Wiley & Sons. págs. 623–. ISBN 978-1-4443-0023-9A mitad de
ciclo: 110-330 pg/mL
- ^ Dons RF (12 de julio de 1994). Manual de pruebas endocrinas y metabólicas. CRC Press. pp. 8–. ISBN 978-0-8493-7657-3Ovulatorio
: 200-400 pg/mL
- ^ Notelovitz M, van Keep PA (6 de diciembre de 2012). El climaterio en perspectiva: actas del Cuarto Congreso Internacional sobre la Menopausia, celebrado en Lake Buena Vista, Florida, del 28 de octubre al 2 de noviembre de 1984. Springer Science & Business Media. pp. 397–. ISBN 978-94-009-4145-8. Archivado del original el 10 de enero de 2023 . Consultado el 22 de octubre de 2016 .
[...] después de la menopausia, los niveles circulantes de estradiol disminuyen de una media premenopáusica de 120 pg/mL a solo 13 pg/mL.
- ^ ab Müller EE, MacLeod RM (6 de diciembre de 2012). Neuroendocrine Perspectives. Springer Science & Business Media. pp. 121–. ISBN 978-1-4612-3554-5. Archivado del original el 10 de enero de 2023 . Consultado el 22 de octubre de 2016 .
[...] concentración media de [estradiol] [premenopáusica] de 150 pg/mL [...]
- ^ Sayed Y, Taxel P (diciembre de 2003). "El uso de la terapia con estrógenos en hombres". Current Opinion in Pharmacology . 3 (6): 650–4. doi :10.1016/j.coph.2003.07.004. PMID 14644018.
- ^ Nichols KC, Schenkel L, Benson H (1984). "17 beta-estradiol para la terapia de reemplazo de estrógeno posmenopáusica". Obstet Gynecol Surv . 39 (4): 230–45. doi :10.1097/00006254-198404000-00022. PMID 6717863.
- ^ Cynthia C. Chernecky; Barbara J. Berger (31 de octubre de 2012). Pruebas de laboratorio y procedimientos de diagnóstico – Libro electrónico. Elsevier Health Sciences. pp. 488–. ISBN 978-1-4557-4502-9Archivado desde el original el 22 de agosto de 2023 . Consultado el 22 de agosto de 2023 .
- ^ Powers MS, Schenkel L, Darley PE, Good WR, Balestra JC, Place VA (agosto de 1985). "Farmacocinética y farmacodinamia de las formas de dosificación transdérmicas de 17 beta-estradiol: comparación con los estrógenos orales convencionales utilizados para el reemplazo hormonal". Am. J. Obstet. Gynecol . 152 (8): 1099–106. doi :10.1016/0002-9378(85)90569-1. PMID 2992279.
- ^ Kenneth L. Becker (2001). Principios y práctica de endocrinología y metabolismo. Lippincott Williams & Wilkins. págs. 889, 1059–1060, 2153. ISBN 978-0-7817-1750-2.
- ^ Lalit Bajaj; Stephen Berman (1 de enero de 2011). Berman's Pediatric Decision Making. Elsevier Health Sciences. págs. 160–. ISBN 978-0-323-05405-8Archivado desde el original el 11 de enero de 2023 . Consultado el 22 de agosto de 2023 .
- ^ Kuhl H (2003). "¿Estrógeno para el hombre?" [¿Estrógenos para el hombre?]. Blickpunkt der Mann . 1 (3): 6–12. ISSN 1727-0669. Archivado desde el original el 22 de agosto de 2023 . Consultado el 22 de agosto de 2023 .
- ^ ab "Análisis de sangre de estradiol: Enciclopedia Médica MedlinePlus". medlineplus.gov . Archivado desde el original el 18 de marzo de 2021 . Consultado el 6 de mayo de 2019 .
- ^ abcdefghij GPNotebook — rango de referencia (estradiol) Archivado el 9 de junio de 2012 en Wayback Machine. Recuperado el 27 de septiembre de 2009.
- ^ ab Valores tomados del día 1 después del pico de LH en: Stricker R, Eberhart R, Chevailler MC, Quinn FA, Bischof P, Stricker R (2006). "Establecimiento de valores de referencia detallados para la hormona luteinizante, la hormona folículo estimulante, el estradiol y la progesterona durante diferentes fases del ciclo menstrual en el analizador Abbott ARCHITECT". Química clínica y medicina de laboratorio . 44 (7): 883–7. doi :10.1515/CCLM.2006.160. PMID 16776638. S2CID 524952.como PDF
- ^ abcd Cantidad total multiplicada por 0,022 según 2,2% presentada en: Wu CH, Motohashi T, Abdel-Rahman HA, Flickinger GL, Mikhail G (agosto de 1976). "Estradiol-17 beta plasmático libre y unido a proteínas durante el ciclo menstrual". The Journal of Clinical Endocrinology and Metabolism . 43 (2): 436–45. doi :10.1210/jcem-43-2-436. PMID 950372.[ ¿Investigación original? ]
- ^ Häggström M (2014). «Rangos de referencia para estradiol, progesterona, hormona luteinizante y hormona folículo estimulante durante el ciclo menstrual». WikiJournal of Medicine . 1 (1). doi : 10.15347/wjm/2014.001 . ISSN 2002-4436.
- ^ ab Kuhl H (agosto de 2005). "Farmacología de los estrógenos y progestágenos: influencia de diferentes vías de administración". Climaterio . 8 (1 Suppl 1): 3–63. doi :10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ Coenjaerts M, Pape F, Santoso V, Grau F, Stoffel-Wagner B, Philipsen A, Schultz J, Hurlemann R, Scheele D (septiembre de 2021). "Diferencias de sexo en la toma de decisiones económicas: el estradiol exógeno tiene efectos opuestos en el marco de equidad en mujeres y hombres". Eur. Neuropsychopharmacol . 50 (2): 46–54. doi :10.1016/j.euroneuro.2021.04.006. hdl : 20.500.11811/11066 . ISSN 0924-977X. PMID 33957337. S2CID 233982738.
- ^ abc Loriaux DL, Loriaux L (14 de marzo de 2016). Una historia biográfica de la endocrinología. John Wiley e hijos. págs. 345–. ISBN 978-1-119-20246-2.
- ^ abcdefghi Lauritzen C, Studd JW (22 de junio de 2005). Tratamiento actual de la menopausia. CRC Press. pp. 44–. ISBN 978-0-203-48612-2.
- ^ ab Allen E, Doisy EA (1923). "Una hormona ovárica". Revista de la Asociación Médica Estadounidense . 81 (10): 819. doi :10.1001/jama.1923.02650100027012. ISSN 0002-9955.
- ^ ab Gruhn JG, Kazer RR (11 de noviembre de 2013). Regulación hormonal del ciclo menstrual: la evolución de los conceptos. Springer Science & Business Media. págs. 69–73. ISBN 978-1-4899-3496-3.
- ^ Newerla GJ (1944). "La historia del descubrimiento y aislamiento de las hormonas sexuales femeninas". New England Journal of Medicine . 230 (20): 595–604. doi :10.1056/NEJM194405182302001. ISSN 0028-4793.
- ^ abc Fritz MA, Speroff L (28 de marzo de 2012). Endocrinología ginecológica clínica e infertilidad. Lippincott Williams & Wilkins. pp. 750–. ISBN 978-1-4511-4847-3.
- ^ Parl FF (2000). Estrógenos, receptores de estrógenos y cáncer de mama. IOS Press. pp. 4–. ISBN 978-0-9673355-4-4Archivado desde el original el 10 de enero de 2023 . Consultado el 27 de noviembre de 2016 .
- ^ Sartorelli AC, Johns DG (27 de noviembre de 2013). Agentes antineoplásicos e inmunosupresores. Springer Science & Business Media. pp. 104–. ISBN 978-3-642-65806-8.
- ^ Shoupe D, Haseltine FP (6 de diciembre de 2012). Anticoncepción. Springer Science & Business Media. pp. 2–. ISBN 978-1-4612-2730-4.
- ^ MacCorquodale DW, Thayer SA, Doisy EA (1935). "La hormona folicular ovárica cristalina". Biología experimental y medicina . 32 (7): 1182. doi :10.3181/00379727-32-8020P. ISSN 1535-3702. S2CID 83557813.
- ^ Sustancias químicas identificadas en medios biológicos humanos: una base de datos. División de Diseño y Desarrollo, División de Encuestas y Análisis, Oficina de Integración e Información de Programas, Oficina de Pesticidas y Sustancias Tóxicas, Agencia de Protección Ambiental. 1981. págs. 114–115.
- ^ Fausto-Sterling A (2000). Sexing the Body: Gender Politics and the Construction of Sexuality [Sexificar el cuerpo: políticas de género y la construcción de la sexualidad] . Basic Books. pp. 189–. ISBN 978-0-465-07714-4.
- ^ "Herramienta de estudio de palabras griegas: oistros". Biblioteca Digital Perseus . Archivado desde el original el 17 de marzo de 2012. Consultado el 28 de diciembre de 2011 .





