Cubano
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Cubano [1] | |||
| Nombre sistemático de la IUPAC Pentaciclo[4.2.0.0 2,5 .0 3,8 .0 4,7 ]octano | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Araña química | |||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C8H8 | |||
| Masa molar | 104,15 g/mol | ||
| Apariencia | Sólido cristalino transparente [2] | ||
| Densidad | 1,29 g/ cm3 | ||
| Punto de fusión | 133,5 °C (272,3 °F; 406,6 K) [3] | ||
| Punto de ebullición | 161,6 °C (322,9 °F; 434,8 K) [3] | ||
| Compuestos relacionados | |||
Hidrocarburos relacionados | Cuneano Dodecaedro Tetraedro Prismane Prismane C8 | ||
Compuestos relacionados | Octafluorocubano Octanitrocubano Octaazacubano Octasilacubano | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El cubano es un compuesto hidrocarbonado sintético con la fórmula C 8 H 8 . Consiste en ocho átomos de carbono dispuestos en las esquinas de un cubo , con un átomo de hidrógeno unido a cada átomo de carbono. Una sustancia cristalina sólida , el cubano es uno de los hidrocarburos platónicos y un miembro de los prismanos . Fue sintetizado por primera vez en 1964 por Philip Eaton y Thomas Cole. [4] Antes de este trabajo, Eaton creía que el cubano sería imposible de sintetizar debido a los " ángulos de enlace de 90 grados requeridos ". [5] [6] La forma cúbica requiere que los átomos de carbono adopten un ángulo de enlace inusualmente agudo de 90°, que sería muy tenso en comparación con el ángulo de 109,45° de un carbono tetraédrico . Una vez formado, el cubano es bastante estable cinéticamente , debido a la falta de rutas de descomposición fácilmente disponibles. Es el hidrocarburo más simple con simetría octaédrica .
La elevada energía potencial y estabilidad cinética del cubano y sus compuestos derivados hacen que sean útiles para el almacenamiento controlado de energía. Por ejemplo, el octanitrocubano y el heptanitrocubano se han estudiado como explosivos de alto rendimiento. Estos compuestos también suelen tener una densidad muy alta para las moléculas de hidrocarburos. La alta densidad energética resultante significa que se puede almacenar una gran cantidad de energía en una cantidad de espacio comparativamente menor, una consideración importante para aplicaciones en el almacenamiento de combustible y el transporte de energía. Además, su geometría y estabilidad los convierten en isósteros adecuados para los anillos de benceno. [7]
Síntesis
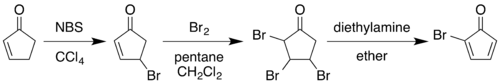
La síntesis clásica de 1964 comienza con la conversión de 2-ciclopentenona en 2-bromo ciclopentadienona : [4] [8]
La bromación alílica con N -bromosuccinimida en tetracloruro de carbono seguida de la adición de bromo molecular al alqueno da como resultado una 2,3,4-tribromociclopentanona. El tratamiento de este compuesto con dietilamina en éter dietílico provoca la eliminación de dos equivalentes de bromuro de hidrógeno para dar el producto dieno.
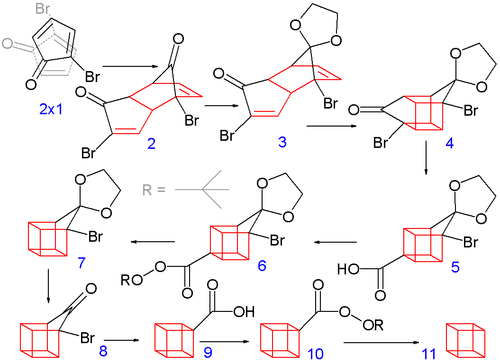
La construcción de la estructura de ocho carbonos del cubano comienza cuando la 2-bromociclopentadienona sufre una dimerización espontánea de Diels-Alder . Posteriormente, un cetal del isómero endo se desprotege selectivamente con ácido clorhídrico acuoso a 3 .
En el siguiente paso, el isómero endo 3 (con ambos grupos alqueno en estrecha proximidad) forma el isómero tipo jaula 4 en una cicloadición fotoquímica [2+2] . El grupo bromocetona se convierte en ácido carboxílico contraído en el anillo 5 en un reordenamiento de Favorskii con hidróxido de potasio . A continuación, tiene lugar la descarboxilación térmica a través del cloruro de ácido (con cloruro de tionilo ) y el peréster de terc -butilo 6 (con hidroperóxido de terc -butilo y piridina ) a 7 ; después, el acetal se elimina una vez más en 8. Un segundo reordenamiento de Favorskii da 9 , y finalmente otra descarboxilación da, a través de 10 , cubano ( 11 ).
Una síntesis de laboratorio más accesible de cubano disustituido implica la bromación del cetal de etileno de ciclopentanona para dar un derivado de tribromociclopentanona. Los pasos posteriores incluyen la deshidrobromación, la dimerización de Diels-Alder, etc. [9] [10]

El ácido cubano-1,4-dicarboxílico resultante se utiliza para sintetizar otros cubanos sustituidos. El cubano en sí puede obtenerse casi cuantitativamente mediante la descarboxilación fotoquímica del éster de tiohidroxamato (la descarboxilación de Barton ). [11]
Derivados
La síntesis del derivado octafenilo a partir del bromuro de níquel tetrafenilciclobutadieno por Freedman en 1962 es anterior a la del compuesto original. Es un compuesto incoloro escasamente soluble que se funde a 425–427 °C. [3] [12] [13] [14] En una publicación de 2014 se predijo la existencia de un hipercubano , con una estructura similar a la del hipercubo . [15] [16] Se han sintetizado dos isómeros del cubeno y se ha analizado computacionalmente un tercero . El alqueno en orto -cubeno es excepcionalmente reactivo debido a su geometría piramidalizada . En el momento de su síntesis, este era el alqueno más piramidalizado que se había fabricado. [17] El isómero meta -cubeno es incluso menos estable, y el isómero para -cubeno probablemente solo existe como un dirradical en lugar de un enlace diagonal real. [18]
En 2022, se sintetizaron tanto el heptafluorocubano como el octafluorocubano . [19] El octafluorocubano es de interés teórico debido a su estructura electrónica inusual , [20] que se indica por su susceptibilidad a sufrir una reducción a un anión detectable C
8F−
8, con un electrón libre atrapado dentro del cubo, convirtiéndolo en la caja más pequeña del mundo. [21]
Cubilcubanos y oligocubanos
El cubeno (1,2-deshidrocubano) y el 1,4-cubanodiil(1,4-deshidrocubano) son compuestos muy tensos que experimentan adición nucleofílica muy rápidamente, lo que ha permitido a los químicos sintetizar el cubilcubano. La solución de la estructura por difracción de rayos X ha demostrado que el enlace central del cubilcubano es extremadamente corto (1,458 Å), mucho más corto que el enlace simple CC típico (1,578 Å). Esto se atribuye al hecho de que los orbitales exocíclicos del cubilcubano son ricos en s y están cerca del núcleo. [22] Los químicos de la Universidad de Chicago ampliaron y modificaron la secuencia de una manera que permite la preparación de una serie de oligómeros de [n]cubilcubano. [23] Los [n]cubilcubanos son varillas moleculares rígidas con la promesa particular a la hora de hacer cristales líquidos con una transparencia UV excepcional. A medida que aumenta el número de unidades de cubano enlazadas, la solubilidad del [n]cubilcubano se desploma; como resultado, solo se han sintetizado cadenas de longitud limitada (hasta 40 unidades) en soluciones. El esqueleto de los [n]cubilcubanos todavía está compuesto por cubos de carbono enormemente tensos, lo que limita su estabilidad. Por el contrario, los investigadores de la Universidad Estatal de Pensilvania demostraron que el policubano sintetizado por reacción en estado sólido está compuesto en un 100% por carbono sp3 enlazado con un ángulo tetraédrico (109,5°) y exhibe propiedades ópticas excepcionales (alto índice de refracción ). [24]
Reacciones
El cuneano se puede producir a partir del cubano mediante una reorganización del enlace σ catalizada por iones metálicos . [25] [26]
Con un catalizador de rodio, primero se forma sin -triciclooctadieno, que puede descomponerse térmicamente en ciclooctatetraeno a 50–60 °C. [27]
Véase también
Referencias
- ^ Nomenclatura de la química orgánica: recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: The Royal Society of Chemistry . 2014. pág. 169. doi :10.1039/9781849733069-FP001. ISBN. 978-0-85404-182-4Los nombres conservados
adamantano y cubano se utilizan en la nomenclatura general y como nombres IUPAC preferidos.
- ^ "Inicio".
- ^ abc Biegasiewicz, Kyle; Griffiths, Justin; Savage, G. Paul; Tsanakstidis, John; Priefer, Ronny (2015). "Cubane: 50 años después". Chemical Reviews . 115 (14): 6719–6745. doi :10.1021/cr500523x. PMID 26102302.
- ^ ab Eaton, Philip E.; Cole, Thomas W. (1964). "Cubano". J. Am. Química. Soc. 86 (15): 3157–3158. doi :10.1021/ja01069a041.
- ^ Profesores, Escuela de verano de química de la Universidad de Nueva Gales del Sur (1963). Enfoque de la química: conferencias e informes de talleres de la ... Escuela de verano para profesores de química. La Universidad. pág. 98."Este compuesto fue descrito hace sólo unos meses y, curiosamente, es bastante fácil de fabricar, aunque hace sólo un año habría predicho que sería difícil, o incluso imposible, de sintetizar".
- ^ Moore, John W.; Stanitski, Conrad L.; Jurs, Peter C. (2002). Química: la ciencia molecular. Harcourt College Publishers. pág. 372. ISBN 978-0-03-032011-8."Este ángulo de enlace agudo crea una tensión de enlace grave en el cubano, un compuesto que antes se creía imposible de sintetizar debido a los ángulos de enlace de 90° requeridos".
- ^ Wiesenfeldt, Mario P.; Rossi-Ashton, James A.; Perry, Ian B.; Diesel, Johannes; Garry, Olivia L.; Bartels, Florian; Coote, Susannah C.; Ma, Xiaoshen; Yeung, Charles S.; Bennett, David J.; MacMillan, David WC (junio de 2023). "Acceso general a los cubanos como bioisósteros de benceno". Nature . 618 (7965): 513–518. doi :10.1038/s41586-023-06021-8. ISSN 1476-4687. PMC 10680098 .
- ^ Eaton, Philip E.; Cole, Thomas W. (1964). "El sistema Cubane". J. Am. Chem. Soc. 86 (5): 962–964. doi :10.1021/ja01059a072.
- ^ Bliese, Marianne; Tsanaktsidis, John (1997). "Cubano-1,4-dicarboxilato de dimetilo: una síntesis práctica a escala de laboratorio". Revista australiana de química . 50 (3): 189. doi :10.1071/C97021.
- ^ Fluorochem, Inc (julio de 1989). "Derivados de cubano para aplicaciones de propulsión" (PDF) . Archivado (PDF) desde el original el 9 de julio de 2021.
- ^ Eaton, Philip E. (1992). "Cubano: Ausgangsverbindungen für die Chemie der neunziger Jahre und des nächsten Jahrhunderts". Angewandte Chemie (en alemán). 104 (11): 1447-1462. Código bibliográfico : 1992AngCh.104.1447E. doi : 10.1002/ange.19921041105.
- ^ Freedman, HH (1961). "Derivados del tetrafenilciclobutadieno. II.1 Evidencia química del estado triplete". J. Am. Chem. Soc. 83 (9): 2195–2196. doi :10.1021/ja01470a037.
- ^ Freedman, HH; Petersen, DR (1962). "Derivados del tetrafenilciclobutadieno. IV.1 "Octafenilcubano"; un dímero del tetrafenilciclobutadieno". J. Am. Chem. Soc. 84 (14): 2837–2838. doi :10.1021/ja00873a046.
- ^ Pawley, GS; Lipscomb, WN; Freedman, HH (1964). "Estructura del dímero de tetrafenilciclobutadieno". J. Am. Chem. Soc. 86 (21): 4725–4726. doi :10.1021/ja01075a042.
- ^ Pichierri, F. (2014). "Hipercubano: predicción basada en DFT de un hidrocarburo de doble capa O h -simétrico". Chem. Phys. Lett . 612 : 198–202. Bibcode :2014CPL...612..198P. doi :10.1016/j.cplett.2014.08.032.
- ^ "Hipercubano: predicción basada en DFT de un hidrocarburo de doble capa Oh-simétrico".
- ^ Eaton, Philip E.; Maggini, Michele (1988). "Cubeno (1,2-deshidrocubano)". J. Am. Química. Soc . 110 (21): 7230–7232. doi :10.1021/ja00229a057.
- ^ Minyaev, Ruslan M.; Minkin, Vladimir I.; Gribanova, Tatyana N. (2009). "2.3 Un enfoque teórico para el estudio y diseño de sistemas prismáticos". En Dodziuk, Helena (ed.). Hidrocarburos deformados . Wiley. pág. 55. ISBN 9783527627141.
- ^ Sugiyama M, Akiyama M, Yonezawa Y, Komaguchi K, Higashi M, Nozaki K, Okazoe T (agosto de 2022). "Electrón en un cubo: síntesis y caracterización del perfluorocubano como aceptor de electrones". Science . 377 (6607): 756–759. Bibcode :2022Sci...377..756S. doi :10.1126/science.abq0516. PMID 35951682. S2CID 251515925.
- ^ Pichierri, F. Efectos de los sustituyentes en cubano e hipercubano: un estudio de DFT y QTAIM. Theor Chem Acc 2017; 136: 114. doi :10.1007/s00214-017-2144-5
- ^ Krafft MP, Riess JG (agosto de 2022). "Perfluorocubane: un pequeño devorador de electrones". Science . 377 (6607): 709. Bibcode :2022Sci...377..709K. doi :10.1126/science.adc9195. PMID 35951708. S2CID 251517529.
- ^ Gilardi, Richard.; Maggini, Michele.; Eaton, Philip E. (1 de octubre de 1988). "Estructuras de rayos X de cubilcubano y 2-tert-butilcubilcubano: enlaces jaula-jaula cortos". Revista de la Sociedad Química Americana . 110 (21): 7232–7234. doi :10.1021/ja00229a058. ISSN 0002-7863.
- ^ Eaton, Philip E. (1992). "Cubanes: materiales de partida para la química de los años 1990 y el nuevo siglo". Angewandte Chemie International Edition en inglés . 31 (11): 1421–1436. doi :10.1002/anie.199214211. ISSN 1521-3773.
- ^ Huang, Haw-Tyng; Zhu, Li; Ward, Matthew D.; Wang, Tao; Chen, Bo; Chaloux, Brian L.; Wang, Qianqian; Biswas, Arani; Gray, Jennifer L.; Kuei, Brooke; Cody, George D.; Epshteyn, Albert; Crespi, Vincent H.; Badding, John V.; Strobel, Timothy A. (21 de enero de 2020). "Nanoarquitectura a través de moléculas tensadas: andamiajes derivados de cubano y los nanohilos de carbono más pequeños". Revista de la Sociedad Química Estadounidense . 142 (42): 17944–17955. doi :10.1021/jacs.9b12352. ISSN 0002-7863. PMID 31961671. S2CID 210870993.
- ^ Smith, Michael B.; March, Jerry (2001). Química orgánica avanzada de March (quinta edición). John Wiley & Sons. pág. 1459. ISBN 0-471-58589-0.
- ^ Kindler, K.; Lührs, K. (1966). "Studien über den Mechanismus chemischer Reaktionen, XXIII. Hydrierungen von Nitrilen unter Verwendung von Terpenen als Wasserstoffdonatoren". Química. Ber. 99 : 227–232. doi :10.1002/cber.19660990135.
- ^ Cassar, Luigi; Eaton, Philip E.; Halpern, Jack (1970). "Catálisis de reacciones de simetría restringida por compuestos de metales de transición. Isomerización de valencia de cubano". Revista de la Sociedad Química Americana . 92 (11): 3515–3518. doi :10.1021/ja00714a075. ISSN 0002-7863.
Enlaces externos
- Síntesis cubana de Eaton en SynArchive.com
- Síntesis cubana de Tsanaktsidis en SynArchive.com
- Química cubana en el Imperial College de Londres