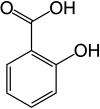
Ácido salicílico
| |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Ácido 2-hidroxibenzoico [1] | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Banco de medicamentos |
| ||
| Tarjeta informativa de la ECHA | 100.000.648 | ||
| Número CE |
| ||
| |||
| BARRIL | |||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C7H6O3 | |||
| Masa molar | 138,122 g/mol | ||
| Apariencia | Polvo cristalino incoloro a blanco. | ||
| Olor | Inodoro | ||
| Densidad | 1,443 g/cm3 ( 20 °C) [2] | ||
| Punto de fusión | 158,6 °C (317,5 °F; 431,8 K) | ||
| Punto de ebullición | 211 °C (412 °F; 484 K) a 20 mmHg [2] [3] | ||
| Sublimes a 76 °C [3] | |||
| |||
| Solubilidad | Soluble en éter , CCl4 , benceno , propanol , acetona , etanol , aceite de trementina , tolueno . | ||
| Solubilidad en benceno |
| ||
| Solubilidad en cloroformo |
| ||
| Solubilidad en metanol |
| ||
| Solubilidad en aceite de oliva | 2,43 g/100 g (23 °C) [3] | ||
| Solubilidad en acetona | 39,6 g/100 g (23 °C) [3] | ||
| registro P | 2.26 | ||
| Presión de vapor | 10,93 mPa [3] | ||
| Acidez (p K a ) |
| ||
| UV-vis (λmáx . ) | 210 nm, 234 nm, 303 nm (4 mg/dL en etanol) [3] | ||
| −72,23·10 −6 cm3 / mol | |||
Índice de refracción ( n D ) | 1.565 (20 °C) [2] | ||
| 2,65 D | |||
| Termoquímica | |||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −589,9 kJ/mol | ||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | -3,025 MJ/mol [6] | ||
| Farmacología | |||
| A01AD05 ( OMS ) B01AC06 ( OMS ) D01AE12 ( OMS ) N02BA01 ( OMS ) S01BC08 ( OMS ) | |||
| Peligros | |||
| Seguridad y salud en el trabajo (SST/OHS): | |||
Peligros para los ojos | Irritación severa | ||
Peligros para la piel | Irritación leve | ||
| Etiquetado SGA : [7] | |||
  | |||
| Peligro | |||
| H302 , H318 | |||
| P280 , P305+P351+P338 | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | 157 °C (315 °F; 430 K) taza cerrada [3] | ||
| 540 °C (1004 °F; 813 K) [3] | |||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) | 480 mg/kg (ratones, oral) | ||
| Ficha de datos de seguridad (FDS) | MSDS [ enlace roto ] | ||
| Compuestos relacionados | |||
Compuestos relacionados | Salicilato de metilo , Ácido benzoico , Fenol , Aspirina , Ácido 4-hidroxibenzoico , Salicilato de magnesio , Salicilato de colina , Subsalicilato de bismuto , Ácido sulfosalicílico , Salicilato sintasa | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El ácido salicílico es un compuesto orgánico con la fórmula HOC 6 H 4 COOH. [3] Un sólido incoloro (o blanco), de sabor amargo, es un precursor y un metabolito del ácido acetilsalicílico (aspirina). [3] Es una hormona vegetal , [8] y ha sido incluida en el Inventario de Sustancias Químicas de la Ley de Control de Sustancias Tóxicas (TSCA) de la EPA como un teratógeno experimental . [9] El nombre proviene del latín salix para sauce , del cual se identificó y derivó inicialmente. Es un ingrediente en algunos productos contra el acné . Las sales y ésteres del ácido salicílico se conocen como salicilatos . [3]
Usos
Medicamento

El ácido salicílico como medicamento se utiliza comúnmente para eliminar la capa más externa de la piel . Como tal, se utiliza para tratar verrugas , psoriasis , acné vulgar , tiña , caspa e ictiosis . [3] [10] [11]
Al igual que otros hidroxiácidos, el ácido salicílico es un ingrediente presente en muchos productos para el cuidado de la piel para el tratamiento de la dermatitis seborreica , el acné , la psoriasis , los callos , las durezas , la queratosis pilaris , la acantosis nigricans , la ictiosis y las verrugas. [12]
Usos en la fabricación
El ácido salicílico se utiliza como conservante de alimentos , bactericida y antiséptico . [13] [14]
El ácido salicílico se utiliza en la producción de otros productos farmacéuticos, incluidos el ácido 4-aminosalicílico , la sandulpirida y la landetimida (a través de la saletamida). [15] También se utiliza en la producción de ácido pícrico . [16]
El ácido salicílico ha sido durante mucho tiempo un material de partida clave para la fabricación de ácido acetilsalicílico (AAS o aspirina). [8] El AAS se prepara mediante la acetilación del ácido salicílico con el grupo acetilo del anhídrido acético o cloruro de acetilo . [17] El AAS es el estándar con el que se comparan todos los demás fármacos antiinflamatorios no esteroideos ( AINE ). En medicina veterinaria, este grupo de fármacos se utiliza principalmente para el tratamiento de trastornos musculoesqueléticos inflamatorios. [18]
El subsalicilato de bismuto , una sal de bismuto y ácido salicílico, "muestra una acción antiinflamatoria (debido al ácido salicílico) y también actúa como un antiácido y antibiótico suave". [3] Es un ingrediente activo en medicamentos para aliviar el estómago como Pepto-Bismol y algunas formulaciones de Kaopectate .
Otros derivados incluyen el salicilato de metilo , utilizado como linimento para aliviar el dolor articular y muscular, y el salicilato de colina , que se utiliza tópicamente para aliviar el dolor de las úlceras bucales . [3] [19] [20] El ácido aminosalicílico se utiliza para inducir la remisión en la colitis ulcerosa , y se ha utilizado como agente antituberculoso a menudo administrado en asociación con isoniazida . [21]
El salicilato de sodio es un fósforo útil en el rango espectral ultravioleta del vacío , con una eficiencia cuántica casi plana para longitudes de onda entre 10 y 100 nm. [22] Fluoresce en azul a 420 nm. Se prepara fácilmente sobre una superficie limpia rociando una solución saturada de la sal en metanol seguida de evaporación. [ cita requerida ]
Mecanismo de acción
El ácido salicílico modula la actividad enzimática de la COX-1 para disminuir la formación de prostaglandinas proinflamatorias. El salicilato puede inhibir competitivamente la formación de prostaglandinas. Las acciones antirreumáticas (antiinflamatorias no esteroides) del salicilato son resultado de sus mecanismos analgésicos y antiinflamatorios. [ cita requerida ]
El ácido salicílico, cuando se aplica a la superficie de la piel, actúa haciendo que las células de la epidermis se desprendan más fácilmente, evitando que los poros se obstruyan y permitiendo el crecimiento de nuevas células. El ácido salicílico inhibe la oxidación de la uridina-5-difosfoglucosa (UDPG) de forma competitiva con el NADH y de forma no competitiva con la UDPG. También inhibe de forma competitiva la transferencia del grupo glucuronilo del ácido uridina-5-fosfoglucurónico al aceptor fenólico. [23]
La acción retardante de la cicatrización de heridas de los salicilatos se debe probablemente principalmente a su acción inhibidora sobre la síntesis de mucopolisacáridos. [5]
Seguridad
Si se utilizan altas concentraciones de ungüento salicílico por vía tópica , pueden ingresar altos niveles de ácido salicílico a la sangre, requiriendo hemodiálisis para evitar complicaciones mayores. [24]
Las aplicaciones cosméticas del fármaco no plantean ningún riesgo significativo. [25] Incluso en el peor de los casos, en el que se utilizaran múltiples productos tópicos que contuvieran ácido salicílico, la concentración plasmática agregada de ácido salicílico estaba muy por debajo de lo permitido para el ácido acetilsalicílico (aspirina). [25] Dado que la aspirina oral (que produce concentraciones plasmáticas de ácido salicílico mucho más altas que las aplicaciones dérmicas de ácido salicílico) no plantea resultados adversos significativos para el embarazo en términos de frecuencia de muerte fetal, defectos de nacimiento o retraso del desarrollo, el uso de cosméticos que contengan ácido salicílico es seguro para las mujeres embarazadas. [25] El ácido salicílico está presente en la mayoría de las frutas y verduras, como por ejemplo en mayores cantidades en las bayas y en bebidas como el té.
Producción y reacciones químicas
Biosíntesis
El ácido salicílico se biosintetiza a partir del aminoácido fenilalanina . En Arabidopsis thaliana , se puede sintetizar a través de una vía independiente de la fenilalanina.
Síntesis química
Los vendedores comerciales preparan el salicilato de sodio tratando el fenolato de sodio (la sal sódica del fenol ) con dióxido de carbono a alta presión (100 atm) y alta temperatura (115 °C), un método conocido como reacción de Kolbe-Schmitt . La acidificación del producto con ácido sulfúrico da como resultado ácido salicílico:
A escala de laboratorio, también se puede preparar mediante la hidrólisis de aspirina (ácido acetilsalicílico) [26] o salicilato de metilo (aceite de gaulteria ) con un ácido o base fuerte; estas reacciones revierten las síntesis comerciales de esos productos químicos.
Reacciones
Al calentarse, el ácido salicílico se convierte en salicilato de fenilo : [27] [8]
- 2 HOC 6 H 4 CO 2 H → C 6 H 5 O 2 C 6 H 4 OH + CO 2 + H 2 O
Un calentamiento adicional produce xantona . [8]
El ácido salicílico como base conjugada es un agente quelante, con afinidad por el hierro (III). [28]
El ácido salicílico se degrada lentamente a fenol y dióxido de carbono a 200–230 °C: [29]
- C6H4OH ( CO2H ) → C6H5OH + CO2
Se conocen todos los isómeros del ácido clorosalicílico y del ácido diclorosalicílico . El ácido 5-clorosalicílico se produce por cloración directa del ácido salicílico. [8]
Historia

El sauce se ha utilizado desde hace mucho tiempo con fines medicinales. Dioscórides , cuyos escritos fueron muy influyentes durante más de 1.500 años, [30] utilizó 'Itea' (que posiblemente era una especie de sauce) como tratamiento para 'obstrucciones intestinales dolorosas', control de la natalidad, para 'aquellos que escupen sangre', para eliminar callos y durezas y, externamente, como una 'compresa caliente para la gota'. William Turner , en 1597, repitió esto, diciendo que la corteza de sauce, 'al quemarse hasta las cenizas y remojarse en vinagre, elimina los callos y otras protuberancias similares en los pies y los dedos de los pies'. [31] Algunas de estas curas pueden describir la acción del ácido salicílico, que puede derivarse de la salicina presente en el sauce. Sin embargo, es un mito moderno que Hipócrates usó el sauce como analgésico. [32]
Hipócrates , Galeno , Plinio el Viejo y otros sabían que las decocciones que contenían salicilato podían aliviar el dolor y reducir la fiebre. [33] [34]
Se utilizó en Europa y China para tratar estas afecciones. [35] Este remedio se menciona en textos del Antiguo Egipto , Sumeria y Asiria . [36]
Los cheroquis y otros indígenas americanos utilizan una infusión de la corteza para la fiebre y otros fines medicinales. [37] En 2014, los arqueólogos identificaron rastros de ácido salicílico en fragmentos de cerámica del siglo VII encontrados en el centro-este de Colorado. [38]
El reverendo Edward Stone , vicario de Chipping Norton, Oxfordshire , Inglaterra, informó en 1763 que la corteza del sauce era eficaz para reducir la fiebre. [39]

Un extracto de corteza de sauce, llamado salicina , por el nombre latino del sauce blanco ( Salix alba ), fue aislado y nombrado por el químico alemán Johann Andreas Buchner en 1828. [41] Una mayor cantidad de la sustancia fue aislada en 1829 por Henri Leroux, un farmacéutico francés. [42] Raffaele Piria , un químico italiano , fue capaz de convertir la sustancia en un azúcar y un segundo componente, que en la oxidación se convierte en ácido salicílico. [43] [44] El ácido salicílico también fue aislado de la hierba reina de los prados ( Filipendula ulmaria , anteriormente clasificada como Spiraea ulmaria ) por investigadores alemanes en 1839. [45] Su extracto causó problemas digestivos como irritación gástrica , sangrado , diarrea e incluso la muerte cuando se consumió en dosis altas.
En 1874, el médico escocés Thomas MacLagan experimentó con salicina como tratamiento para el reumatismo agudo , con un éxito considerable, como informó en The Lancet en 1876. [46] Mientras tanto, los científicos alemanes probaron el salicilato de sodio con menos éxito y efectos secundarios más graves. [47] [48]
En 1979, se descubrió que los salicilatos estaban involucrados en las defensas inducidas del tabaco contra el virus del mosaico del tabaco . [49] En 1987, se identificó al ácido salicílico como la señal largamente buscada que hace que las plantas termogénicas , como el lirio vudú, Sauromatum guttatum , produzcan calor. [50]
Fuentes dietéticas
El ácido salicílico se encuentra en las plantas en forma de ácido salicílico libre y sus ésteres carboxilados y glucósidos fenólicos. Varios estudios sugieren que los seres humanos metabolizan el ácido salicílico en cantidades mensurables a partir de estas plantas. [51] Las bebidas y alimentos con alto contenido de salicilatos incluyen cerveza , café , té , numerosas frutas y verduras, batata , nueces y aceite de oliva . [19] La carne, las aves, el pescado, los huevos, los productos lácteos, el azúcar, el pan y los cereales tienen un bajo contenido de salicilato. [19] [52]
Algunas personas con sensibilidad a los salicilatos dietéticos pueden tener síntomas de reacción alérgica , como asma bronquial , rinitis , trastornos gastrointestinales o diarrea , por lo que es posible que deban adoptar una dieta baja en salicilatos. [19]
Hormona vegetal
El ácido salicílico es una fitohormona fenólica , y se encuentra en plantas con funciones en el crecimiento y desarrollo de la planta, fotosíntesis , transpiración y absorción y transporte de iones . [53] El ácido salicílico está involucrado en la señalización endógena , mediando la defensa de la planta contra patógenos . [54] Desempeña un papel en la resistencia a patógenos (es decir, resistencia sistémica adquirida ) al inducir la producción de proteínas relacionadas con la patogénesis y otros metabolitos defensivos. [55] El papel de señalización de defensa de SA se demuestra más claramente por experimentos que lo eliminan: Delaney et al. 1994, Gaffney et al. 1993, Lawton et al. 1995 y Vernooij et al. 1994 utilizan cada uno Nicotiana tabacum o Arabidopsis expresando nahG , para la salicilato hidroxilasa . La inoculación de patógenos no produjo los niveles altos de SA que se suelen producir, no se produjo SAR y no se expresaron genes PR en las hojas sistémicas. De hecho, los sujetos eran más susceptibles a patógenos virulentos (e incluso normalmente avirulentos). [53]
De forma exógena , el ácido salicílico puede ayudar al desarrollo de las plantas mejorando la germinación de las semillas, la floración de los brotes y la maduración de los frutos, aunque una concentración demasiado alta de ácido salicílico puede regular negativamente estos procesos de desarrollo. [56]
El éster metílico volátil del ácido salicílico, el salicilato de metilo , también puede difundirse a través del aire, facilitando la comunicación entre plantas . [57] El salicilato de metilo es absorbido por los estomas de la planta cercana, donde puede inducir una respuesta inmune después de convertirse nuevamente en ácido salicílico. [58]
Transducción de señales
Se han identificado varias proteínas que interactúan con SA en plantas, especialmente las proteínas de unión al ácido salicílico (SABP) y los genes NPR (no expresadores de genes relacionados con la patogénesis), que son posibles receptores. [59]
Véase también
Referencias
- ^ "Front Matter". Nomenclatura de la química orgánica: recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: The Royal Society of Chemistry . 2014. p. 64. doi :10.1039/9781849733069-FP001 (inactivo el 11 de abril de 2024). ISBN 978-0-85404-182-4.
{{cite book}}: CS1 maint: DOI inactivo a partir de abril de 2024 ( enlace ) - ^ abc Haynes WM, ed. (2011). Manual de química y física del CRC (92.ª edición). Boca Raton, FL: CRC Press . pág. 3.306. ISBN 1-4398-5511-0.
- ^ abcdefghijklmnopqrs «Ácido salicílico». PubChem, Biblioteca Nacional de Medicina de EE. UU. 19 de noviembre de 2023. Consultado el 19 de noviembre de 2023 .
- ^ abc Atherton Seidell, William F. Linke (1952). Solubilidades de compuestos inorgánicos y orgánicos: una recopilación de datos de solubilidad de la literatura periódica. Suplemento a la tercera edición que contiene datos publicados durante los años 1939-1949. Van Nostrand .
- ^ ab Wishart DS , Djombou Feunang Y, Guo AC, Lo EJ, Marcu A, Grant JR, Sajed T, Johnson D, Li C, Sayeeda Z, Assempour N, Iynkkaran I, Liu Y, Maciejewski A, Gale N, Wilson A , Chin L, Cummings R, Le D, Pon A, Knox C, Wilson M. "Ácido salicílico | DrugBank Online". Banco de medicamentos . 5.0.
- ^ "Ácido salicílico". Archivado desde el original el 15 de febrero de 2017. Consultado el 17 de agosto de 2014 .
- ^ Sigma-Aldrich Co. , Ácido salicílico.
- ^ abcde Boullard O, Leblanc H, Besson B (2000). "Ácido salicílico". Enciclopedia de química industrial de Ullmann . doi :10.1002/14356007.a23_477. ISBN 3-527-30673-0.
- ^ Lewis Sr RJ (2008). Referencia de escritorio sobre productos químicos peligrosos. John Wiley & Sons. pág. 1217. ISBN 978-0-470-33445-4.
- ^ "Ácido salicílico". Drugs.com. Archivado desde el original el 18 de enero de 2017. Consultado el 15 de enero de 2017 .
- ^ Organización Mundial de la Salud (2009). Stuart MC, Kouimtzi M, Hill SR (eds.). Formulario Modelo de la OMS 2008. Organización Mundial de la Salud. p. 310. hdl : 10665/44053 . ISBN. 978-92-4-154765-9.
- ^ Madan RK, Levitt J (abril de 2014). "Una revisión de la toxicidad de las preparaciones tópicas de ácido salicílico". Revista de la Academia Estadounidense de Dermatología . 70 (4): 788–792. doi :10.1016/j.jaad.2013.12.005. PMID 24472429.
- ^ "Definición de ácido salicílico". MedicineNet.com . Archivado desde el original el 2011-12-09 . Consultado el 2010-10-12 .
- ^ Greene SA (2013). Manual de pesticidas y productos químicos agrícolas de Sittig. William Andrew. ISBN 978-0-8155-1903-4.
- ^ "Medicamentos que contienen el principio activo ácido salicílico - (emc)". www.medicines.org.uk . Consultado el 23 de octubre de 2022 .
- ^ "λ» LambdaSyn - Síntesis de Pikrinsäure ". www.lambdasyn.org . Consultado el 1 de agosto de 2024 .
- ^ Watson DG (2011). Química farmacéutica. Edimburgo: Churchill Livingstone. pág. 273. ISBN 978-0-7020-4850-0. Recuperado el 21 de mayo de 2022 .
- ^ "INFORME RESUMEN SOBRE ÁCIDO ACETILSALICÍLICO, ACETILSALICILATO DE SODIO, ÁCIDO ACETILSALICÍLICO DL-LISINA Y CARBASALATO DE CALCIO" (PDF) . No. EMEA/MRL/695/99–FINAL. COMITÉ DE MEDICAMENTOS VETERINARIOS. Agencia Europea para la Evaluación de Medicamentos Veterinarios e Inspecciones. Noviembre de 1999.
- ^ abcd «Dieta baja en salicilatos». Drugs.com. 19 de febrero de 2019. Archivado desde el original el 16 de diciembre de 2019. Consultado el 16 de diciembre de 2019 .
- ^ Wróblewska KB, Plewa S, Dereziński P, Muszalska-Kolos I (22 de diciembre de 2019). "Análisis de salicilato de colina: estabilidad química e identificación del producto de degradación". Moléculas . 25 (1): 51. doi : 10.3390/molecules25010051 . PMC 6983192 . PMID 31877863.
- ^ "Ácido aminosalicílico". Drugbank Online .
- ^ Samson, James (1976). Técnicas de espectroscopia ultravioleta al vacío . Wiley, .
- ^ Sanchez-Dominguez CN, Gallardo-Blanco HL, Salinas-Santander MA, Ortiz-Lopez R (julio de 2018). "Uridina 5′-difosfo-glucronosiltrasferasa: su papel en la farmacogenómica y la enfermedad humana". Medicina experimental y terapéutica . 16 (1): 3–11. doi :10.3892/etm.2018.6184. ISSN 1792-0981. PMC 5995049 . PMID 29896223.
- ^ Péc J, Strmenová M, Palencárová E, Pullmann R, Funiaková S, Visnovský P, Buchanec J, Lazarová Z (octubre de 1992). "Intoxicación por salicilatos después del uso de ungüento tópico de ácido salicílico por parte de un paciente con psoriasis". Cutis . 50 (4): 307–309. PMID 1424799.
- ^ abc Labib R, Bury D, Boisleve F, Eichenbaum G, Girard S, Naciff J, Leal M, Wong J (abril de 2018). "Una evaluación de seguridad basada en la cinética de la exposición de los consumidores al ácido salicílico de los productos cosméticos no demuestra evidencia de un riesgo para la salud por toxicidad del desarrollo". Toxicología y farmacología regulatorias . 94 : 245–251. doi : 10.1016/j.yrtph.2018.01.026 . PMID 29410076. S2CID 46877699.
- ^ "Hidrolisis de ASA a SA". Archivado desde el original el 8 de agosto de 2007 . Consultado el 31 de julio de 2007 .
- ^ Kuriakose G, Nagaraju N (2004). "Síntesis selectiva de salicilato de fenilo (Salol) mediante reacción de esterificación sobre catalizadores ácidos sólidos". Journal of Molecular Catalysis A: Chemical . 223 (1–2): 155–159. doi :10.1016/j.molcata.2004.03.057.
- ^ Jordan RB (1983). "Complejos de salicilato de metal (III): especies protonadas y pasos de formación que controlan la velocidad". Química inorgánica . 22 (26): 4160–4161. doi :10.1021/ic00168a070.
- ^ Kaeding WW (1 de septiembre de 1964). "Oxidación de ácidos aromáticos. IV. Descarboxilación de ácidos salicílicos". The Journal of Organic Chemistry . 29 (9): 2556–2559. doi :10.1021/jo01032a016.
- ^ Dioscórides P. "De Materia Médica" (PDF) .
- ^ Turner W. "The Herball, or Generall Historie of Plantes" (La herbolaria o historia general de las plantas) . Consultado el 8 de enero de 2022 .
- ^ Martyr P (18 de octubre de 2020). «¿Hipócrates y la corteza de sauce? Lo que sabes sobre la historia de la aspirina probablemente sea erróneo» . Consultado el 9 de enero de 2022 .
- ^ Norn S, Permin H, Kruse PR, Kruse E (2009). "De la corteza de sauce al ácido acetilsalicílico". Dansk Medicinhistorisk Årbog (en danés). 37 : 79–98. PMID 20509453. S2CID 10053542.
- ^ Vane JR (2000). "La lucha contra el reumatismo: desde la corteza de sauce hasta los fármacos ahorradores de COX-1". J Physiol Pharmacol . 51(4 Pt 1) (4 Pt 1): 573–86. PMID 11192932.
- ^ "Corteza de sauce". Centro Médico de la Universidad de Maryland . Universidad de Maryland . Archivado desde el original el 24 de diciembre de 2011. Consultado el 19 de diciembre de 2011 .
- ^ Goldberg DR (verano de 2009). «Aspirina: fármaco milagroso de finales de siglo». Revista Chemical Heritage . 27 (2): 26–30. Archivado desde el original el 20 de marzo de 2018. Consultado el 24 de marzo de 2018 .
- ^ Hemel PB, Chiltoskey MU (1975). Plantas Cherokee y sus usos: una historia de 400 años . Sylva, NC: Herald Publishing Co.; citado en Moerman D. "Una base de datos de alimentos, fármacos, colorantes y fibras de los pueblos nativos americanos, derivados de plantas". Archivado desde el original el 6 de diciembre de 2007.Una búsqueda en esta base de datos de "salix AND medicine" arroja 63 entradas.
- ^ "Encontraron cerámica de 1.300 años en Colorado que contiene 'aspirina natural' antigua". 12 de agosto de 2014. Archivado desde el original el 13 de agosto de 2014. Consultado el 13 de agosto de 2014 .
- ^ Stone, Edmund (1763). "Un relato del éxito de la corteza del sauce en la cura de las fiebres intermitentes". Philosophical Transactions of the Royal Society of London . 53 : 195–200. doi : 10.1098/rstl.1763.0033 .
- ^ "2013.0503 | Colecciones en línea". collections.thackraymuseum.co.uk . Consultado el 30 de mayo de 2024 .
- ^ Buchner A (1828). "Ueber das Rigatellische Fiebermittel und über eine in der Weidenrinde entdeckte alcaloidische Substanz" [Sobre el antipirético [es decir, un fármaco contra la fiebre] de Rigatelli y una sustancia alcaloide descubierta en la corteza de sauce]. Repertorio para la farmacia . Bei JL Schrag. págs. 405–.
Noch ist es mir aber nicht geglückt, den avetoro Bestandtheil der Weide, den ich
Salicin
nenen will, ganz frei von allem Färbestoff darzustellen.
[Todavía no he conseguido preparar el componente amargo del sauce, al que llamaré salicina , completamente libre de materia coloreada] - ^ Ver:
- Leroux H (1830). "Mémoire relatif à l'analyse de l'écorce de saule et à la découverte d'un principe immédiat propre à remplacer le sulfate de quinine" [Memoria sobre el análisis de la corteza de sauce y el descubrimiento de una sustancia que puede sustituir inmediatamente al sulfato de quinina ]. Journal de Chimie Médicale, de Pharmacie et de Toxicologie . 6 : 340–342.
- También apareció un informe sobre la presentación de Leroux ante la Academia Francesa de Ciencias en: Mémoires de l'Académie des sciences de l'Institut de France. Instituto de Francia. 1838. págs. 20–.
- ↑ Piría (1838). "Sur de neuveaux produits extraits de la salicine" [Sobre los nuevos productos extraídos de la salicina]. Cuentas rendus . 6 : 620–624. Archivado desde el original el 27 de julio de 2017. pag. 622:
Piria menciona "Hydrure de salicyle" (salicilato de hidrógeno, es decir, ácido salicílico).
- ^ Jeffreys D (2005). Aspirina: la extraordinaria historia de un fármaco maravilloso. Nueva York: Bloomsbury. pp. 38-40. ISBN 978-1-58234-600-7.
- ^ Löwig C, Weidmann S (1839). "III. Untersuchungen mit dem destillierten Wasser der Blüthen von Spiraea Ulmaria" [III. Investigaciones del agua destilada de las flores de Spiraea ulmaria ]. Annalen der Physik und Chemie; Beiträge zur Organischen Chemie (Contribuciones a la química orgánica) (46): 57–83.Löwig y Weidman llamaron al ácido salicílico Spiräasaure (ácido espiraea)
- ^ MacLagan TJ (28 de octubre de 1876). "El tratamiento del reumatismo agudo con salicina". The Lancet . 108 (2774): 383. doi :10.1016/S0140-6736(02)49509-8.
- ^ MacLagan T (1900). "El tratamiento del reumatismo agudo". The Lancet . 155 (3998): 1904. doi :10.1016/S0140-6736(01)70583-1. S2CID 58103130.
- ^ Buchanan WW, Kean WF (junio de 2002). "El tratamiento del reumatismo agudo con salicina, por TJ Maclagan — The Lancet, 1876". Revista de reumatología . 29 (6): 1321–1323. PMID 12064852.
- ^ Raskin I (julio de 1992). "Salicilato, una nueva hormona vegetal". Fisiología vegetal . 99 (3): 799–803. doi :10.1104/pp.99.3.799. PMC 1080546 . PMID 16669002.
- ^ Raskin I, Ehmann A, Melander WR, Meeuse BJ (septiembre de 1987). "Ácido salicílico: un inductor natural de la producción de calor en los lirios de Arum ". Science . 237 (4822): 1601–2. Bibcode :1987Sci...237.1601R. doi :10.1126/science.237.4822.1601. PMID 17834449. S2CID 3108513.
- ^ Malakar S, Gibson PR, Barrett JS, Muir JG (1 de abril de 2017). "Salicilatos dietéticos naturales: una mirada más cercana a los alimentos australianos comunes". Journal of Food Composition and Analysis . 57 : 31–39. doi :10.1016/j.jfca.2016.12.008.
- ^ Swain AR, Dutton SP, Truswell AS (agosto de 1985). "Salicilatos en los alimentos" (PDF) . Journal of the American Dietetic Association . 85 (8): 950–960. doi :10.1016/S0002-8223(21)03743-3. PMID 4019987. S2CID 42796737. Archivado (PDF) desde el original el 2019-04-05 . Consultado el 2019-12-16 .
- ^ ab Vlot AC, Dempsey DA, Klessig DF (2009). "Ácido salicílico, una hormona multifacética para combatir enfermedades". Revisión anual de fitopatología . 47 : 177–206. doi :10.1146/annurev.phyto.050908.135202. PMID 19400653.
- ^ Hayat, S., Ahmad, A. (2007). Ácido salicílico: una hormona vegetal . Springer . ISBN. 978-1-4020-5183-8.
- ^ Hooft Van Huijsduijnen RA, Alblas SW, De Rijk RH, Bol JF (1986). "Inducción por ácido salicílico de proteínas relacionadas con la patogénesis o resistencia a la infección por el virus del mosaico de la alfalfa en varias especies de plantas". Journal of General Virology . 67 (10): 2135–2143. doi : 10.1099/0022-1317-67-10-2135 .
- ^ Koo YM, Heo AY, Choi HW (febrero de 2020). "Ácido salicílico como protector seguro de las plantas y regulador del crecimiento". The Plant Pathology Journal . 36 (1): 1–10. doi :10.5423/PPJ.RW.12.2019.0295. PMC 7012573 . PMID 32089657.
- ^ Taiz L, Zeiger E (2002). Fisiología vegetal. Sunderland, Mass: Sinauer Associates. pag. 306.ISBN 0-87893-823-0. OCLC 50002466. Archivado desde el original el 5 de marzo de 2014.
- ^ Chamovitz D (2012). Lo que sabe una planta: una guía de campo sobre los sentidos de su jardín y más allá . Oxford, Inglaterra: Oneworld. ISBN 978-1-85168-910-1.OCLC 775030365 .
- ^ Kumar, D. 2014. Señalización del ácido salicílico en la resistencia a enfermedades. Plant Science 228:127–134.
Lectura adicional
- Schrör K (2016). Ácido acetilsalicílico (2.ª edición). John Wiley & Sons. págs. 9-10. ISBN 978-3-527-68502-8.
Enlaces externos
- Espectro MS del ácido salicílico
- Datos de seguridad de la hoja de datos de seguridad archivados el 3 de febrero de 2009 en Wayback Machine
- Fichas internacionales de seguridad química | CDC/NIOSH Archivado el 25 de octubre de 2017 en Wayback Machine
- "Sobre la síntesis de ácido salicílico" Archivado el 6 de agosto de 2020 en Wayback Machine : traducción al inglés del artículo fundamental de Hermann Kolbe en alemán de 1860 "Ueber Synthese der Salicylsäure" en Annalen der Chemie und Pharmacie en MJLPHD Archivado el 18 de octubre de 2020 en Máquina Wayback