Acifluorfeno
 | |
 | |
| Nombres | |
|---|---|
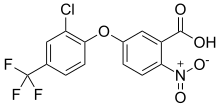
| Nombre IUPAC preferido Ácido 5-[2-cloro-4-(trifluorometil)fenoxi]-2-nitrobenzoico | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) |
|
| EBICh | |
| Química biológica | |
| Araña química | |
| Banco de medicamentos | |
| Tarjeta informativa de la ECHA | 100.051.468 |
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades [1] | |
| C14H7ClF3NO5 | |
| Masa molar | 361,66 g·mol −1 |
| Densidad | 1,573 g/ml |
| Punto de fusión | 155 °C |
| 250 g/L (20 °C) | |
| registro P | 1,18 (20 °C) |
| Acidez (p K a ) | 3.86 |
| Farmacología | |
| Estatus legal |
|
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
Acifluorfen es el nombre común de la ISO [2] para un compuesto orgánico utilizado como herbicida . Actúa inhibiendo la enzima protoporfirinógeno oxidasa, que es necesaria para la síntesis de clorofila . La soja tiene naturalmente una alta tolerancia al acifluorfen y sus sales , a través de la eliminación metabólica por la glutatión S -transferasa . [3] [4] Es eficaz contra las malezas de hoja ancha y los pastos y se utiliza agrícolamente en campos de cultivo de soja, maní, guisantes y arroz. [5]
Historia
Los éteres de nitrofenilo son una clase bien conocida de herbicidas, cuyo miembro más antiguo fue el nitrofeno , inventado por Rohm & Haas y registrado por primera vez para la venta en 1964. [6] Esta área de la química se volvió muy competitiva, con la presentación en 1969 y la concesión en 1974 de una patente de Mobil Oil Corporation al análogo estructural con un grupo COOCH 3 adyacente al grupo nitro del nitrofeno. [7] Este producto, bifenox , se lanzó con la marca Mowdown en 1981. Mientras tanto, Rohm & Haas introdujo el acifluorfeno (como su sal sódica con la marca Blazer) en 1980, habiéndolo desarrollado bajo el número de código RH-6201. [8] Tenía propiedades mucho mejores, incluido un espectro más amplio de efecto herbicida y buena seguridad para los cultivos de soja. La primera patente del material se publicó en diciembre de 1975, [9] aunque una patente belga anterior publicada en septiembre de 1973 había descrito la química relacionada. [10]
Síntesis
La preparación del acifluorfeno, descrita por primera vez en la patente de Rohm & Haas, incluye como pasos finales una condensación de Ullmann entre 2-cloro-4-trifluorometilfenol y 2-nitro-5-fluorobenzonitrilo. A continuación, el intermedio se hidroliza utilizando ácido bromhídrico en ácido acético como disolvente. [9]
Mecanismo de acción
El mecanismo de acción detallado del nitrofeno , el acifluorfeno y los herbicidas relacionados con el éter difenílico, como el fomesafeno, se desconocía en el momento de su invención. Los efectos visibles en las plantas enteras son la clorosis y la desecación : se propusieron varias hipótesis con respecto a las interacciones a nivel molecular que podrían explicar estos síntomas. [11] La explicación ahora aceptada para el daño es que estos compuestos inhiben la enzima protoporfirinógeno oxidasa , lo que conduce a una acumulación de protoporfirina IX en las células de la planta. Este es un potente fotosensibilizador que activa el oxígeno, lo que conduce a la peroxidación lipídica . Tanto la luz como el oxígeno son necesarios para que este proceso mate a la planta. [12] [13]
Uso
En los Estados Unidos , la Agencia de Protección Ambiental (EPA) es responsable de regular los pesticidas bajo la Ley Federal de Insecticidas, Fungicidas y Rodenticidas (FIFRA), la Ley de Protección de la Calidad de los Alimentos (FQPA) y la Ley de Mejora del Registro de Pesticidas (PRIA). [14] Un pesticida solo puede usarse legalmente de acuerdo con las instrucciones de la etiqueta que se incluye en el momento de la venta del pesticida. El propósito de la etiqueta es "proporcionar instrucciones claras para un rendimiento eficaz del producto al tiempo que se minimizan los riesgos para la salud humana y el medio ambiente". Una etiqueta es un documento legalmente vinculante que establece cómo se puede y debe usar el pesticida y el incumplimiento de la etiqueta tal como está escrita al usar el pesticida es un delito federal. [4] [15]
El acifluorfeno sódico normalmente se aplica postemergencia (cuando las malezas son visibles en el cultivo). Controla o suprime malezas de hoja ancha, pastos y juncos y es eficaz en una amplia gama de especies, incluidas Abutilon theophrasti , Acalypha ostryifolia , Acanthospermum hispidum , Amaranthus palmeri , Ambrosia artemisiifolia , Anoda cristata , Barbarea vulgaris , Brassica kaber , Calystegia sepium , Cannabis sativa , Cardiospermum halicacabum , Cassia obtusifolia , Chenopodium album , Citrullus lanatus , Convolvulus arvensis , Croton glandulosus , Cyperus esculentus , Datura stramonium , Digitaria , Echinochloa crus-galli , Eleusine indica , Euphorbia heterophylla , Helianthus annuus , Hibiscus trionum , Ipomoea quamoclit , Melochia corchorifolia , Mollugo verticillata , Polygonum convolvulus , Portulaca oleracea , Richardia scabra , Sesbania exaltata , Setaria faberi , Solanum rostratum , Sorghum halepense , Striga asiatica y Xanthium strumarium . El producto normalmente se utiliza en dosis de aplicación de 0,375 lb de ia por acre. [15]
El Servicio Geológico de Estados Unidos ha mapeado el uso anual estimado de acifluorfeno en la agricultura estadounidense y muestra que en 2018 [actualizar]se aplicaron aproximadamente 550 000 libras (250 000 kg), principalmente en soja. [16] El compuesto no está registrado para su uso en la Unión Europea , aunque un éter de nitrofenilo estrechamente relacionado, el bifenox , está disponible allí. [17]
Seguridad
En California, el acifluorfeno figura como "conocido por el estado como causante de cáncer o toxicidad reproductiva" según la Proposición 65. [ 18]
Véase también
Referencias
- ^ Base de datos de propiedades de pesticidas. "Acifluorfen". Universidad de Hertfordshire . Consultado el 3 de marzo de 2021 .
- ^ "Compendio de nombres comunes de pesticidas: acifluorfeno". BCPC .
- ^ Andrews, Christopher J.; Skipsey, Mark; Townson, Jane K.; Morris, Carol; Jepson, Ian; Edwards, Robert (1997). "Actividades de glutatión transferasa hacia herbicidas utilizados selectivamente en soja". Pesticide Science . 51 (2). Wiley : 213–222. doi :10.1002/(sici)1096-9063(199710)51:2<213::aid-ps622>3.0.co;2-l. ISSN 0031-613X.
- ^ ab "Mitigación de la etiqueta de revisión de registro para el acifluorfeno sódico" (PDF) . Agencia de Protección Ambiental de los Estados Unidos . 2 de junio de 2020 . Consultado el 5 de marzo de 2021 .
- ^ Acifluorfen, Red de Extensión Toxicológica
- ^ Base de datos de propiedades de pesticidas. "Nitrofen". Universidad de Hertfordshire . Consultado el 3 de marzo de 2021 .
- ^ Patente estadounidense 3784635, Theissen RJ, "Éteres de 4-trifluorometil-4'-nitrodifenilo herbicidas", expedida el 8 de enero de 1974, asignada a Mobil Oil Corporation
- ^ Base de datos de propiedades de pesticidas. "Acifluorfen-sodium". Universidad de Hertfordshire . Consultado el 3 de marzo de 2021 .
- ^ Patente estadounidense 3928416, Bayer HO; Swithenbank C. & Yih RY, "Éteres de 4-trifluorometil-4'-nitrodifenilo herbicidas", expedida el 23 de diciembre de 1975, asignada a Rohm & Haas
- ^ BE patente 796677, Bayer HO; Swithenbank C. & Yih RY, "Nouveaux ethers 4-trifluoromethyl-4'-nitro-difeniliques herbicides et leur application a la lutte contre les mauvaises herbes", publicado el 13 de septiembre de 1973, asignado a Rohm & Haas
- ^ Ridley, Stuart M. (1983). "Interacción de los cloroplastos con inhibidores". Fisiología vegetal . 72 (2): 461–468. doi :10.1104/pp.72.2.461. PMC 1066256 . PMID 16663025.
- ^ Dayan, Franck E.; Reddy, Krishna N.; Duke, Stephen O. (1999). "Relaciones estructura-actividad de los éteres de difenilo y otros inhibidores de la protoporfirinógeno oxidasa con puentes de oxígeno". Herbicidas peroxidantes . págs. 141–161. doi :10.1007/978-3-642-58633-0_5. ISBN 978-3-642-63674-5.
- ^ Nagano, Eiki (1999). "Eficacia herbicida de los inhibidores de la protoporfirinógeno oxidasa". Herbicidas peroxidantes . págs. 293–302. doi :10.1007/978-3-642-58633-0_11. ISBN . 978-3-642-63674-5.
- ^ "Acerca del registro de pesticidas". EPA de EE. UU . 27 de febrero de 2013. Consultado el 27 de febrero de 2021 .
- ^ de United Phosphorus, Inc (2012). "Ultra Blazer herbicide" (PDF) . Consultado el 6 de marzo de 2021 .
- ^ Servicio Geológico de Estados Unidos (12 de octubre de 2021). «Uso agrícola estimado de acifluorfeno, 2018» . Consultado el 13 de diciembre de 2023 .
- ^ Base de datos de propiedades de pesticidas. "Bifenox". Universidad de Hertfordshire . Consultado el 3 de marzo de 2021 .
- ^ La lista de la Proposición 65


