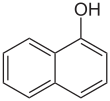
1-naftol
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Naftalen-1-ol | |||
| Otros nombres 1-Hidroxinaftaleno; 1-Naftalenol; α-Naftol | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| 1817321 | |||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.001.791 | ||
| Número CE |
| ||
| 69192 | |||
| BARRIL | |||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C10H8O | |||
| Masa molar | 144,17 g/mol | ||
| Apariencia | Sólido incoloro o blanco | ||
| Densidad | 1,10 g/ cm3 | ||
| Punto de fusión | 95 a 96 °C (203 a 205 °F; 368 a 369 K) | ||
| Punto de ebullición | 278 a 280 °C (532 a 536 °F; 551 a 553 K) | ||
| -98,2·10 −6 cm3 / mol | |||
| Peligros | |||
| Etiquetado SGA : [1] | |||
    | |||
| Peligro | |||
| H302 , H311 , H312 , H315 , H317 , H318 , H335 , H410 , H412 | |||
| P261 , P262 , P264 , P264+P265 , P270 , P271 , P272 , P273 , P280 , P301+P317 , P302+P352 , P304+P340 , P305+P354+P338 , P316 , P317 , P319 , P321 , P330 , P332+P317 , P333+P317 , P361+P364 , P362+P364 , P391 , P403+P233 , P405 , P501 | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El 1-naftol , o α-naftol , es un compuesto orgánico con la fórmula C 10 H 7 OH . Es un sólido blanco fluorescente . El 1-naftol se diferencia de su isómero 2-naftol por la ubicación del grupo hidroxilo en el anillo de naftaleno . Los naftoles son homólogos naftalénicos del fenol . Ambos isómeros son solubles en disolventes orgánicos simples . Son precursores de una variedad de compuestos útiles. [2]
Producción
El 1-naftol se prepara mediante dos rutas principales. [2] En un método, el naftaleno se nitra para dar 1-nitronaftaleno, que se hidrogena a la amina seguida de hidrólisis:
- C 10 H 8 + HNO 3 → C 10 H 7 NO 2 + H 2 O
- C10H7NO2 + 3H2 → C10H7NH2 + 2H2O
- C10H7NH2 + H2O → C10H7OH + NH3
Alternativamente, el naftaleno se hidrogena a tetralina , que se oxida a 1-tetralona , que sufre deshidrogenación .
Reacciones
Algunas reacciones del 1-naftol se pueden explicar con referencia a su tautomería, que produce una pequeña cantidad del tautómero ceto. [ cita requerida ]
Una consecuencia de esta tautomería es la reacción de Bucherer , la amonólisis del 1-naftol para dar 1-aminonaftaleno .
El 1-naftol se biodegrada mediante la formación de 1-naftol-3,4-óxido , que se convierte en 1,4-naftoquinona . [3]
La posición 4 del 1-naftol es susceptible al ataque electrofílico. Esta reacción regioselectiva se aprovecha en la preparación de colorantes diazoicos, que se forman utilizando sales de diazonio . La reducción de los derivados diazoicos da lugar al 4-amino-1-naftol. [4] [5]
La reducción parcial del 1-naftol da lugar al derivado tetrahidro, dejando intacto el anillo fenólico. [6] La hidrogenación completa está catalizada por el rodio. [7]
Aplicaciones y ocurrencia
El 1-naftol es un precursor de una variedad de insecticidas, incluido el carbaril , y productos farmacéuticos como el nadolol [8] [9] , así como del antidepresivo sertralina [10] y del agente terapéutico antiprotozoario atovacuona [11] . Sufre acoplamiento azoico para dar varios colorantes azoicos , pero estos son generalmente menos útiles que los derivados del 2-naftol [2] [12] .
El 1-naftol es un metabolito del insecticida carbaril y naftaleno . Junto con el TCPy , se ha demostrado que disminuye los niveles de testosterona en hombres adultos. [13]
Otros usos
El 1-naftol se utiliza en cada una de las siguientes pruebas químicas, que son anteriores al uso de métodos espectroscópicos y cromatográficos:
- La prueba de Molisch produce un compuesto de color rojo o morado para indicar la presencia de carbohidratos .
- La prueba rápida de furfural se vuelve violeta rápidamente (<30 s) si hay fructosa presente, lo que la distingue de la glucosa.
- La prueba de Sakaguchi se vuelve roja para indicar la presencia de arginina en las proteínas.
- La prueba de Voges-Proskauer cambia de color de amarillo a rojo para indicar que la glucosa se está descomponiendo en acetoína , que las bacterias utilizan para el almacenamiento de energía externa.
Seguridad
El 1-naftol ha sido descrito como "moderadamente tóxico". [2]
Referencias
- ^ "1-Naftol". pubchem.ncbi.nlm.nih.gov .
- ^ abcd Booth, Gerald (2005). "Derivados de naftaleno". Ullmann's Encyclopedia of Industrial Chemistry . Weinheim: Wiley-VCH. doi :10.1002/14356007.a17_009. ISBN 978-3527306732.. texto completo en PDF
- ^ Yoshito Kumagai; Yasuhiro Shinkai; Takashi Miura; Arthur K. Cho (2011). "La biología química de las naftoquinonas y sus implicaciones ambientales". Revisión anual de farmacología y toxicología . 52 : 221–47. doi :10.1146/annurev-pharmtox-010611-134517. PMID 21942631.
- ^ JB Conant; RE Lutz; BB Corson (1923). "Clorhidrato de 1,4-aminonaftol". Síntesis orgánicas . 3 : 7. doi :10.15227/orgsyn.003.0007.
- ^ Louis F. Fieser (1937). "Clorhidrato de 1,2-aminonaftol". Organic Syntheses . 17 : 9. doi :10.15227/orgsyn.017.0009.
- ^ C. David Gutsche; Hugo H. Pedro (1957). "Ar-Tetrahidro-a-Naftol". Síntesis orgánicas . 37 : 80. doi : 10.15227/orgsyn.037.0080.
- ^ AI Meyers; WN Beverung; R. Gault (1971). "Hidrogenación de núcleos aromáticos: 1-decalol". Organic Syntheses . 51 : 103. doi :10.15227/orgsyn.051.0103.
- ^ ME Condon; et al. (1978). "Agentes bloqueadores β-adrenérgicos no depresivos. 1. 3-amino-1-(5,6,7,8-tetrahidro-1-naftoxi)-2-propanoles sustituidos". Journal of Medicinal Chemistry (en alemán). 21 (9): 913–922. doi :10.1021/jm00207a014. PMID 31485.
- ^ DE 2258995, FR Hauck, CM Cimarusti, VL Narayan, "2,3-cis-1,2,3,4-Tetrahidro-5[2-hidroxi-3-(tert.-butilamino)-propoxi]-2,3-naftalindiol", publicado el 7 de junio de 1973, asignado a ER Squibb & Sons, Inc.
- ^ K. Vukics; T. Fodor; J. Fischer; I. Fellevári; S. Lévai (2002), "Mejora de la síntesis industrial del antidepresivo sertralina", Org. Process Res. Dev. (en alemán), vol. 6, n.º 1, págs. 82-85, doi :10.1021/op0100549
- ^ BN Roy; GP Singh; PS Lathi; MK Agarwal (2013). "Un nuevo proceso para la síntesis de atovacuona" (PDF) . Indian J. Chem. (en alemán). 52B : 1299–1312. Archivado desde el original (PDF) el 30 de mayo de 2022.
- ^ C. Kaiser; T. Jen; E. Garvey; WD Bowen; DF Colella; JR Wardell Jr. (1977). "Agentes adrenérgicos. 4. Derivados de fenoxipropanolamina sustituidos como posibles agonistas β-adrenérgicos". Journal of Medicinal Chemistry (en alemán). 20 (5): 687–689. doi :10.1021/jm00215a014. PMID 16136.
- ^ Meeker, John D.; Ryan, Louise; Barr, Dana B.; Hauser, Russ (enero de 2006). "Exposición a insecticidas no persistentes y hormonas reproductivas masculinas". Epidemiología . 17 (1): 61–68. doi : 10.1097/01.ede.0000190602.14691.70 . PMID 16357596. S2CID 24829926.
Enlaces externos
- Libro web de química del NIST 1-Naftalenol
- . Enciclopedia Británica . vol. 19 (11ª ed.). 1911. págs. 168-169.