Yodoformo
 | |||
| |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Triyodometano | |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| 1697010 | |||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.000.795 | ||
| Número CE |
| ||
| BARRIL | |||
| Malla | yodoformo | ||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| Propiedades | |||
| C I 3 | |||
| Masa molar | 393,732 g·mol −1 | ||
| Apariencia | Cristales de color amarillo claro pálido y opacos. | ||
| Olor | Parecido al azafrán [3] | ||
| Densidad | 4,008 g/cm3 [ 3] | ||
| Punto de fusión | 119 °C (246 °F; 392 K) [3] | ||
| Punto de ebullición | 218 °C (424 °F; 491 K) [3] | ||
| 100 mg/L [3] | |||
| Solubilidad en éter dietílico | 136 g/l | ||
| Solubilidad en acetona | 120 g/l | ||
| Solubilidad en etanol | 78 g/l | ||
| registro P | 3.118 | ||
Constante de la ley de Henry ( k H ) | 3,4 μmol·Pa −1 ·kg −1 | ||
| −117,1·10 −6 cm3 / mol | |||
| Estructura | |||
| Hexagonal | |||
| Tetraédrico en C | |||
| Termoquímica | |||
Capacidad calorífica ( C ) | 157,5 J/(K·mol) | ||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | 180,1 – 182,1 kJ/mol | ||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | −716,9 – −718,1 kJ/mol | ||
| Farmacología | |||
| D09AA13 ( OMS ) | |||
| Peligros | |||
| Etiquetado SGA : | |||
 | |||
| Advertencia | |||
| H315 , H319 , H335 | |||
| P261 , P280 , P305+P351+P338 | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | 204 °C (399 °F; 477 K) | ||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) |
| ||
| NIOSH (límites de exposición a la salud en EE. UU.): | |||
PEL (Permisible) | ninguno [4] | ||
REL (recomendado) | 0,6 ppm (10 mg/m3 ) [ 4] | ||
IDLH (Peligro inmediato) | En Dakota del Norte [4] | ||
| Compuestos relacionados | |||
Compuestos relacionados | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||

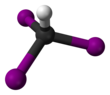
El yodoformo (también conocido como triyodometano ) es un compuesto organoyodado con la fórmula química C H I 3 . Es una sustancia cristalina, volátil y de color amarillo pálido, con un olor penetrante y característico (en los textos de química más antiguos, a veces se hace referencia al olor como el de los hospitales, donde el compuesto todavía se usa comúnmente) y, de manera análoga al cloroformo , un sabor dulzón. Ocasionalmente se usa como desinfectante .
Nombramiento
El nombre yodoformo tiene su origen en el "radical formilo", un término arcaico para la fracción HC, y se conserva por coherencia histórica. Un nombre completo y moderno es triyodometano. El "hidruro" en este último a veces se omite, [2] pero la IUPAC recomienda no hacerlo, ya que "triyoduro de carbono" también podría significar C 2 I 6 (hexayodoetano, un compuesto altamente inestable).
Estructura
La molécula adopta una geometría tetraédrica con simetría C 3v .
Síntesis y reacciones
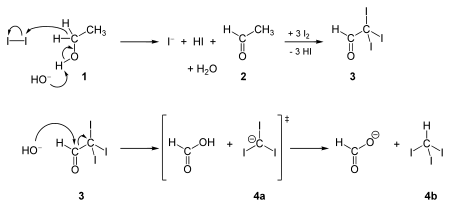
La síntesis de yodoformo fue descrita por primera vez por Georges-Simon Serullas en 1822, mediante reacciones de vapor de yodo con vapor sobre brasas al rojo vivo, y también mediante reacción de potasio con yodo etanólico en presencia de agua; [6] y casi al mismo tiempo de forma independiente por John Thomas Cooper . [7] Se sintetiza en la reacción del haloformo mediante la reacción de yodo e hidróxido de sodio con cualquiera de estos cuatro tipos de compuestos orgánicos: una metilcetona ( CH 3 COR ) , acetaldehído ( CH 3 CHO ), etanol ( CH 3 CH 2 OH ) y ciertos alcoholes secundarios ( CH 3 CHROH , donde R es un grupo alquilo o arilo).
La reacción del yodo y la base con las metilcetonas es tan fiable que se utiliza la prueba del yodoformo (aparición de un precipitado amarillo) para comprobar la presencia de una metilcetona. Esto también se aplica a la prueba de alcoholes secundarios específicos que contienen al menos un grupo metilo en la posición alfa .
Algunos reactivos (por ejemplo, yoduro de hidrógeno ) convierten el yodoformo en diyodometano . También es posible la conversión a dióxido de carbono : [8] El yodoformo reacciona con nitrato de plata acuoso para producir monóxido de carbono . Cuando se trata con plata elemental en polvo, el yodoformo se reduce, produciendo acetileno . Al calentarse, el yodoformo se descompone para producir yodo diatómico, gas de yoduro de hidrógeno y carbono.
Ocurrencia natural
El hongo bonete de ángel contiene yodoformo y muestra su olor característico.
Aplicaciones
El compuesto se utiliza a pequeña escala como desinfectante. [5] [9] A principios del siglo XX, se utilizaba en medicina como apósito cicatrizante y antiséptico para heridas y llagas y, aunque este uso ahora ha sido reemplazado en gran medida por antisépticos superiores , todavía se utiliza en otorrinolaringología en forma de pasta de parafina de yodoformo y subnitrato de bismuto (BIPP) como un relleno antiséptico para caries. [10] Es el ingrediente activo en muchos polvos para los oídos de perros y gatos , junto con el óxido de zinc y el ácido propiónico , que se utilizan para prevenir infecciones y facilitar la eliminación del vello de las orejas. [ cita requerida ]
Véase también
Referencias
- ^ "Front Matter". Nomenclatura de la química orgánica: recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: The Royal Society of Chemistry . 2014. pág. 661. doi :10.1039/9781849733069-FP001. ISBN . 978-0-85404-182-4
Los nombres conservados 'bromoformo' para HCBr
3
, 'cloroformo' para HCCl
3
y 'yodoformo' para HCI
3
son aceptablesen la nomenclatura general. Los nombres IUPAC preferidos son nombres sustitutivos.
- ^ ab "Yodoformo".
- ^ Registro abcdefg en la base de datos de sustancias GESTIS del Instituto de Seguridad y Salud Ocupacional
- ^ abc Guía de bolsillo del NIOSH sobre peligros químicos. "#0343". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ ab Índice Merck , 12.ª edición, 5054
- ^ Surellas, Georges-Simon (1822), Notes sur l'Hydriodate de potasse et l'Acide hydriodique. -- Hidrohidrato de carbono; moyen d'obtenir, à l'instant, ce composé triple [ Notas sobre el yodhidrato de potasio y sobre el ácido yodhídrico -- yoduro de carbono; medios para obtener instantáneamente este compuesto de tres elementos ] (en francés), Metz, Francia: Antoine, págs. 17–20, 28–29
- ^ James, Frank AJL (2004). "Cooper, John Thomas" . Oxford Dictionary of National Biography (edición en línea). Oxford University Press. doi :10.1093/ref:odnb/39361 . Consultado el 26 de enero de 2012 . (Se requiere suscripción o membresía a una biblioteca pública del Reino Unido).
- ^ Shreeve, WW; Leaver, F.; Siegel, I. (1952). "Un método para la conversión específica de yodoformo en dióxido de carbono". J. Am. Chem. Soc . 74 (9): 2404. doi :10.1021/ja01129a067.
- ^ Lyday, Phyllis A. (2005), "Yodo y compuestos de yodo", Ullmann's Encyclopedia of Industrial Chemistry , Wiley-VCH, Weinheim, págs. 1-13, doi :10.1002/14356007.a14_381.pub2, ISBN 9783527306732
- ^ Randhawa, GK; Graham, R.; Matharu, KS (2019). "Pasta de parafina con yodoformo de bismuto: historia y usos". British Journal of Oral and Maxillofacial Surgery . 57 (10): E53–E54. doi :10.1016/j.bjoms.2019.10.153.
Enlaces externos
- Guía de bolsillo del NIOSH sobre peligros químicos. "#0343". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- Preparación
- . Encyclopædia Britannica . Vol. 14 (11.ª ed.). 1911. pág. 726.