Vapor



El vapor es vapor de agua ( agua en fase gaseosa ), a menudo mezclado con aire y/o un aerosol de gotitas de agua líquida. Esto puede ocurrir debido a la evaporación o debido a la ebullición , donde se aplica calor hasta que el agua alcanza la entalpía de vaporización . El vapor saturado o sobrecalentado ( vapor de agua ) es invisible; sin embargo, el vapor húmedo, una niebla visible o un aerosol de gotitas de agua, a menudo se denomina "vapor". [1] : 6
Cuando el agua líquida se convierte en vapor, aumenta su volumen 1.700 veces a temperatura y presión estándar ; este cambio de volumen se puede convertir en trabajo mecánico mediante máquinas de vapor, como las máquinas de pistón alternativo y las turbinas de vapor , que son un subgrupo de las máquinas de vapor. Las máquinas de vapor de pistón desempeñaron un papel central en la Revolución Industrial y las turbinas de vapor modernas se utilizan para generar más del 80% de la electricidad mundial . Si el agua líquida entra en contacto con una superficie muy caliente o se despresuriza rápidamente por debajo de su presión de vapor , puede crear una explosión de vapor .
Tipos de vapor y conversiones
El vapor se crea tradicionalmente calentando una caldera mediante la quema de carbón y otros combustibles, pero también es posible crear vapor con energía solar. [2] [3] [4] El vapor de agua que incluye gotas de agua se describe como vapor húmedo . A medida que el vapor húmedo se calienta aún más, las gotas se evaporan y, a una temperatura lo suficientemente alta (que depende de la presión), toda el agua se evapora y el sistema está en equilibrio vapor-líquido . [5] Cuando el vapor ha alcanzado este punto de equilibrio, se lo conoce como vapor saturado .
El vapor sobrecalentado o vapor vivo es vapor a una temperatura superior a su punto de ebullición para la presión, que sólo se produce cuando toda el agua líquida se ha evaporado o se ha eliminado del sistema. [6]
Las tablas de vapor [7] contienen datos termodinámicos para agua/vapor saturado y suelen ser utilizadas por ingenieros y científicos en el diseño y operación de equipos donde se utilizan ciclos termodinámicos que involucran vapor. Además, los diagramas de fase termodinámicos para agua/vapor, como un diagrama de temperatura-entropía o un diagrama de Mollier que se muestra en este artículo, pueden ser útiles. Los diagramas de vapor también se utilizan para analizar ciclos termodinámicos.
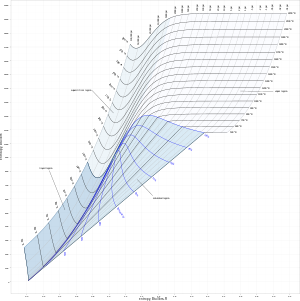 |  |  |
| Diagrama de entalpía-entropía (hs) para vapor | Diagrama de presión-entalpía (ph) para vapor | Diagrama de temperatura-entropía (Ts) para vapor |
Usos
Agrícola
En la agricultura , el vapor se utiliza para esterilizar el suelo para evitar el uso de agentes químicos nocivos y aumentar la salud del suelo . [8]
Doméstico

La capacidad del vapor para transferir calor también se utiliza en el hogar: para cocinar verduras, limpiar con vapor tejidos, alfombras y suelos y para calentar edificios. En cada caso, el agua se calienta en una caldera y el vapor transporta la energía a un objeto de destino. El vapor también se utiliza para planchar la ropa para añadir suficiente humedad con el calor para eliminar las arrugas y crear pliegues intencionados en la ropa.
Generación de electricidad (y cogeneración)
En el año 2000, aproximadamente el 90% de toda la electricidad se generaba utilizando vapor como fluido de trabajo , casi toda mediante turbinas de vapor . [9]
En la generación eléctrica, el vapor se condensa normalmente al final de su ciclo de expansión y se devuelve a la caldera para su reutilización. Sin embargo, en la cogeneración , el vapor se canaliza a los edificios a través de un sistema de calefacción urbana para proporcionar energía térmica después de su uso en el ciclo de generación eléctrica. El sistema de generación de vapor más grande del mundo es el sistema de vapor de la ciudad de Nueva York , que bombea vapor a 100.000 edificios de Manhattan desde siete plantas de cogeneración. [10]
Almacenamiento de energía

A pesar del parecido con una caldera, observe la falta de chimenea y también cómo los cilindros están en el extremo de la cabina, no en el extremo de la chimenea.
En otras aplicaciones industriales, el vapor se utiliza para almacenar energía , que se introduce y se extrae mediante transferencia de calor, generalmente a través de tuberías. El vapor es un depósito de gran capacidad para la energía térmica debido al alto calor de vaporización del agua .
Las locomotoras de vapor sin fuego eran locomotoras de vapor que funcionaban con un suministro de vapor almacenado a bordo en un gran tanque parecido a la caldera de una locomotora convencional. Este tanque se llenaba con vapor de proceso, como el que se encuentra disponible en muchos tipos de grandes fábricas, como las papeleras . La propulsión de la locomotora utilizaba pistones y bielas, como en una locomotora de vapor típica. Estas locomotoras se utilizaban principalmente en lugares donde existía riesgo de incendio en la caja de fuego de una caldera, pero también se utilizaban en fábricas que simplemente tenían un suministro abundante de vapor de sobra.
Esfuerzo mecánico
Las máquinas de vapor y las turbinas de vapor utilizan la expansión del vapor para impulsar un pistón o una turbina para realizar trabajo mecánico . La capacidad de devolver el vapor condensado como agua líquida a la caldera a alta presión con un gasto relativamente pequeño de potencia de bombeo es importante. La condensación de vapor en agua a menudo ocurre en el extremo de baja presión de una turbina de vapor, ya que esto maximiza la eficiencia energética , pero tales condiciones de vapor húmedo deben limitarse para evitar una erosión excesiva de las aspas de la turbina. Los ingenieros utilizan un ciclo termodinámico idealizado , el ciclo Rankine , para modelar el comportamiento de las máquinas de vapor. Las turbinas de vapor se utilizan a menudo en la producción de electricidad.
Esterilización
Un autoclave , que utiliza vapor a presión, se utiliza en laboratorios de microbiología y entornos similares para la esterilización .
El vapor, especialmente el vapor seco (muy sobrecalentado), puede utilizarse para la limpieza antimicrobiana, incluso a niveles de esterilización. El vapor es un agente antimicrobiano no tóxico. [11] [12]
Vapor en tuberías
El vapor se utiliza en las tuberías de servicios públicos. También se utiliza en el revestimiento y el trazado de tuberías para mantener la temperatura uniforme en tuberías y recipientes.
Procesos industriales
El vapor se utiliza en múltiples industrias por su capacidad de transferir calor para impulsar reacciones químicas, esterilizar o desinfectar objetos y mantener temperaturas constantes. En la industria maderera, el vapor se utiliza en el proceso de doblado de madera , matar insectos y aumentar la plasticidad. El vapor se utiliza para acentuar el secado del hormigón, especialmente en prefabricados. Se debe tener cuidado ya que el hormigón produce calor durante la hidratación y el calor adicional del vapor podría ser perjudicial para los procesos de reacción de endurecimiento del hormigón. En las industrias química y petroquímica , el vapor se utiliza en varios procesos químicos como reactivo. El craqueo con vapor de hidrocarburos de cadena larga produce hidrocarburos de menor peso molecular para combustible u otras aplicaciones químicas. El reformado con vapor produce gas de síntesis o hidrógeno .
Limpieza
Se utiliza para limpiar fibras y otros materiales, a veces como preparación para pintar. El vapor también es útil para derretir residuos de grasa y aceite endurecidos, por lo que resulta útil para limpiar suelos y equipos de cocina y motores y piezas de combustión interna. Entre las ventajas de utilizar vapor frente a un chorro de agua caliente se encuentran el hecho de que el vapor puede funcionar a temperaturas más altas y utiliza sustancialmente menos agua por minuto. [13]
Véase también
- Electrificación
- Vaporera o cocedor de alimentos
- Géiser : vapor generado geotérmicamente
- IAPWS : una asociación que mantiene correlaciones estándar internacionales para las propiedades termodinámicas del vapor, incluidas IAPWS-IF97 (para uso en simulación y modelado industrial) e IAPWS-95 (una correlación científica y de propósito general).
- Revolución industrial
- Vapor en vivo
- Producción en masa
- Energía nuclear y las centrales eléctricas utilizan vapor para generar electricidad.
- Oxidrógeno
- Psicrometría : mezclas de aire húmedo y vapor, humedad y aire acondicionado
- Central eléctrica de vapor
- Locomotora de vapor
- Esterilización (microbiología)
Referencias
- ^ "vapor" . Diccionario Oxford de inglés (edición en línea). Oxford University Press . (Se requiere suscripción o membresía a una institución participante).
- ^ Taylor, Robert A.; Phelan, Patrick E.; Adrian, Ronald J.; Gunawan, Andrey; Otanicar, Todd P. (2012). "Caracterización de la generación de vapor volumétrico inducido por luz en nanofluidos". Revista internacional de ciencias térmicas . 56 : 1–11. doi :10.1016/j.ijthermalsci.2012.01.012.
- ^ Taylor, Robert A.; Phelan, Patrick E.; Otanicar, Todd P.; Walker, Chad A.; Nguyen, Monica; Trimble, Steven; Prasher, Ravi (2011). "Aplicabilidad de nanofluidos en colectores solares de alto flujo". Revista de energías renovables y sostenibles . 3 (2): 023104. doi :10.1063/1.3571565. Archivado desde el original el 2022-12-02 . Consultado el 2022-06-14 .
- ^ Taylor, Robert A.; Phelan, Patrick E.; Otanicar, Todd; Adrian, Ronald J.; Prasher, Ravi S. (2009). "Generación de vapor en una suspensión líquida de nanopartículas utilizando un láser continuo enfocado". Applied Physics Letters . 95 (16): 161907. Bibcode :2009ApPhL..95p1907T. doi :10.1063/1.3250174.[ enlace muerto permanente ]
- ^ Singh, R Paul (2001). Introducción a la ingeniería alimentaria . Academic Press. ISBN 978-0-12-646384-2.[ página necesaria ]
- ^ "Vapor sobrecalentado". Spirax-Sarco Engineering . Archivado desde el original el 4 de marzo de 2007. Consultado el 23 de marzo de 2009 .
- ^ Malhotra, Ashok (2012). Tablas de propiedades del vapor: propiedades termodinámicas y de transporte . Plataforma de publicación independiente CreateSpace. ISBN 978-1-479-23026-6.[ página necesaria ]
- ^ van Loenen, Mariska CA; Turbett, Yzanne; Mullins, Chris E.; Feilden, Nigel EH; Wilson, Michael J.; Leifert, Carlo; Seel, Wendy E. (1 de noviembre de 2003). "El vapor del suelo a baja temperatura y de corta duración mata patógenos transmitidos por el suelo, plagas de nematodos y malezas". Revista Europea de Patología Vegetal . 109 (9): 993–1002. doi :10.1023/B:EJPP.0000003830.49949.34. ISSN 1573-8469. S2CID 34897804. Archivado desde el original el 12 de abril de 2022 . Consultado el 14 de junio de 2022 .
- ^ Wiser, Wendell H. (2000). "Contribuciones de las fuentes de energía a la generación de energía eléctrica". Recursos energéticos: aparición, producción, conversión, uso . Birkhäuser. pág. 190. ISBN 978-0-387-98744-6Archivado desde el original el 23 de enero de 2023. Consultado el 22 de febrero de 2016 .
- ^ Bevelhymer, Carl (10 de noviembre de 2003). «Steam». Gotham Gazette . Archivado desde el original el 23 de enero de 2023. Consultado el 14 de junio de 2022 .
- ^ Publicación de patente de la EP 2.091.572
- ^ Song, Liyan; Wu, Jianfeng; Xi, Chuanwu (2012). "Biopelículas en superficies ambientales: evaluación de la eficacia de desinfección de un nuevo sistema de vapor". American Journal of Infection Control . 40 (10): 926–30. doi :10.1016/j.ajic.2011.11.013. PMID 22418602.
- ^ "¿Por qué Steam?". Sitio web de Sioux Corporation . Sioux Corporation. Archivado desde el original el 31 de diciembre de 2017. Consultado el 24 de septiembre de 2015 .
Enlaces externos
- Propiedades termofísicas de sistemas de fluidos, tablas y gráficos de vapor del Instituto Nacional de Estándares y Tecnología, NIST
 Wikiversidad tiene tablas de Steam con figuras y código Matlab
Wikiversidad tiene tablas de Steam con figuras y código Matlab

