Reubicación específica del intestino
El alojamiento específico del intestino es el mecanismo por el cual las células T activadas y las células secretoras de anticuerpos (ASC) se dirigen tanto a las regiones inflamadas como a las no inflamadas del intestino para proporcionar una respuesta inmunitaria eficaz . Este proceso se basa en la interacción clave entre la integrina α4β7 y la adresina MadCAM-1 en las superficies de las células apropiadas. Además, esta interacción se ve reforzada por la presencia de CCR9 , un receptor de quimiocinas , que interactúa con TECK . El ácido retinoico derivado de la vitamina A regula la expresión de estas proteínas de la superficie celular.
Resumen de células T

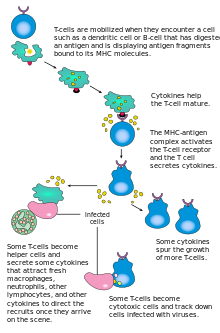
Las células T se producen en el timo y, al salir, migran hacia los órganos linfoides del cuerpo y alrededor de ellos, incluidos los ganglios linfáticos . En la paracorteza de los ganglios linfoides, quedan expuestas a células presentadoras de antígenos (CPA) profesionales, como las células dendríticas (CD). Las interacciones específicas entre las células T vírgenes y sus antígenos afines dan como resultado la activación de las células T. Las células T activadas, inmunoblastos , experimentan una expansión clonal antes de adquirir funciones efectoras. Las células T activadas luego emigran desde los ganglios linfáticos, a través del vaso linfático eferente , y migran alrededor del cuerpo en la sangre . [1]
En determinadas circunstancias, algunas células T activadas muestran una preferencia por patrullar ciertos tejidos . Esto se ha denominado "homing" de los linfocitos . El "homing" específico del intestino es el movimiento preferencial de las células T activadas hacia el intestino y el intestino . De esta manera, las células T se reclutan de manera efectiva para formar parte de la primera línea de defensa contra los patógenos . Esto se debe a que las células T se dirigen a los sitios de infección primarios y recirculan alrededor de ellos. En general, esto da como resultado una concentración extremadamente alta de linfocitos en esta región; el 70% de las células productoras de inmunoglobulina se encuentran en las superficies mucosas del cuerpo. [2]
Historia
Griselli fue el primero en sugerir que existían diferentes vías de migración de células T. [3]
Las teorías iniciales de que las células T no se dirigían al tejido sino a los antígenos fueron refutadas, ya que el trabajo de Cahill demostró que las células T purificadas se reubicarían en la región de activación. Por ejemplo, las células T activadas en los ganglios linfáticos de las placas de Peyer , que se encuentran en el intestino, regresarían al intestino. [1] Trabajos posteriores buscaron explicar la causa de esta orientación de las células T.

Originalmente se teorizó que el microambiente de los tejidos linfoides proporcionaba las señales para la migración preferencial de los linfocitos. [4] Si bien esto puede ser así hasta cierto punto, ahora se acepta ampliamente que el principal impulsor de la migración de los linfocitos son las interacciones entre las moléculas de adhesión de las células T ( receptores de migración de los linfocitos ) y los ligandos (adresinas) en las vénulas endoteliales altas (HEV) del tejido. Esta teoría surgió de la observación de que las integrinas de la superficie celular variaban entre diferentes poblaciones de células T. El trabajo comenzó a identificar las diferencias y lo que significaban para la migración de las células T.
Se hizo evidente que había niveles significativamente más altos de la integrina α4β7 en las células T activadas en comparación con las células T vírgenes. Además, esta integrina era mucho más común en las células T CD8+ activadas en las placas de Peyer (células T PP) en comparación con otros subconjuntos de células T, como las células T activadas en los ganglios linfáticos periféricos y mesentéricos .
Mecanismo
El mecanismo de localización específica del intestino se basa en gran medida en interacciones entre receptores.
Interacción rodante
Los linfocitos migran desde el torrente sanguíneo a través de una "interacción de rodadura" característica mediada por interacciones entre proteínas de la superficie celular. Esta "interacción de rodadura" ocurre en tres etapas:
- Unión inicial de una selectina linfocítica y su ligando . Esto crea una interacción inestable en la que el linfocito se mantiene ligeramente adherido a la pared del endotelio . La fuerza de la linfa hace que la célula ruede característicamente a lo largo del vaso. Un ejemplo de esto es la interacción entre la L-selectina y el ligando PNAD (direccionalidad del ganglio linfático periférico).
- Detención de la célula "rodante" mediante un paso de activación . Otras interacciones entre proteínas o la activación a través de quimiocinas hacen que se formen fuerzas más estables entre la célula y el vaso. La célula ahora está firmemente adherida a la pared del vaso. Siguiendo con el ejemplo, la célula se detendría mediante la interacción entre ICAM y LFA-1, que se refuerzan mediante quimiocinas.
- Cambio conformacional . La activación celular provoca un cambio conformacional que hace que la célula se aplane contra la pared del vaso. Una vez aplanada, la célula puede realizar una migración transendotelial . [1]
Interacciones específicas de proteínas intestinales
Los "receptores de localización" son cruciales en la formación de las interacciones que permiten el movimiento de los linfocitos.
Receptores implicados
Cámara MadCAM-1

La expresión de MadCAM-1 es continua en las vénulas endoteliales altas de las placas de Peyer y en los microvasos del tracto intestinal. [5] Los inhibidores de MadCAM-1 previenen la migración de células T al intestino.
El análisis estructural de la proteína MadCAM-1 muestra que se trata de una proteína transmembrana de 41,5 kDa con una pequeña cola citoplasmática y una gran región extracelular. Esta región extracelular incluye tres dominios similares a inmunoglobulinas (Ig). El último de los cuales tiene un 33% de identidad estructural con el dominio Ca 2 de IgA-1. Se prevé que los dos primeros dominios sean los más importantes en la interacción α4β7.
La proteína MadCAM-1 tiene homología estructural con los receptores de superficie vascular VCAM1 e ICAM en un 28% y 32% respectivamente. [6]
integrina α4β7
La integrina α4β7 se expresa en las células T activadas que tienen la impronta para la localización específica en el intestino. Es el contrarreceptor de la proteína MadCAM-1 y sus interacciones causan el paso de interacción inicial en el modelo de células "rodantes" de migración de linfocitos.
CCR9
Los receptores CCR9 se encuentran en las células T y participan en la formación de una interacción más estable entre el linfocito y la pared vascular. El ligando de las proteínas CCR9 es la proteína quimiocina CCL25 (también conocida como TECK). La CCL25 es una quimiocina que, al unirse a su receptor CCR9 en el linfocito, activa un cambio conformacional en las integrinas de superficie de ese linfocito, [7] lo que permite una unión de alta afinidad a la pared vascular y la posterior transmigración .
La quimiocina CCL25 es prevalente en el tejido epitelial del intestino delgado (7). Se ha demostrado que las células T CD8+ activadas en el tejido linfático de las placas de Peyer muestran un tropismo hacia la quimiocina CCL25. Las células T migran en gradiente ascendente hacia CCL25. [4]
Otras células
Todas las células dendríticas GALT ( tejido linfoide asociado al intestino ), con una cadena α CD103 , son capaces de producir células T que se dirigen al intestino. A partir de esto, se ha sugerido que las células dendríticas se imprimen de alguna manera antes de llegar a los órganos linfoides para inducir la capacidad de dirigirse al intestino. [8]
Regulación de la vitamina A
La vitamina A desempeña un papel fundamental en la respuesta de búsqueda de hogar específica del intestino. La evidencia muestra que la vitamina A se convierte en ácido retinoico (AR) por oxidación en las células dendríticas de las placas de Peyer. La presencia de AR da lugar a la expresión de los receptores de búsqueda de hogar clave, α4β7 y CCR9, en la superficie celular de las células T, posiblemente a través de la regulación transcripcional.
Producción de ácido retinoico
Las enzimas alcohol deshidrogenasas (ADH) y deshidrogenasa retiniana (RALDH) catalizan la oxidación de la vitamina A de la dieta a ácido retinoico. Es la presencia de este ácido retinoico lo que induce la expresión de CCR9 y α4β7. [9] Las concentraciones más bajas de ácido retinoico, dentro de la célula, dan como resultado una expresión reducida del receptor de quimiocina CCR9, lo que a su vez limita la capacidad de la célula para entrar en la mucosa intestinal. Si bien la expresión de α4β7 también se reduce con concentraciones más bajas de ácido retinoico, se predice que los niveles de ácido retinoico deben agotarse en mayor medida para afectar la expresión de α4β7 en comparación con CCR9. [10]
El análisis Western blot mostró que las células dendríticas de las placas de Peyer producen proteínas RALDH1 y ADH. Además, se ha descubierto que estas se expresan en las células epiteliales del intestino delgado. Por lo tanto, se dedujo que estas células son capaces de convertir la vitamina A en la principal forma fisiológica de AR: AR todo-trans. Los estudios que muestran la capacidad de las células dendríticas para catalizar el cambio de retinol a ácido retinoico confirman esta suposición. [10]

Efecto sobre la expresión de los receptores
Las investigaciones realizadas en ratones demostraron que el nivel de ácido retinoico en las células tenía un efecto significativo en la expresión de receptores en la superficie celular. Los modelos de ratones demostraron que incluso un aumento de 0,1 nM en la concentración de ácido retinoico en las células aumentaba la expresión de α4. Además, la expresión de β7 se incrementó al aumentar la concentración de ácido retinoico celular. Para asegurar que el aumento en la concentración de RA se debiera a las enzimas catalíticas ADH y RALDH, se utilizaron inhibidores de estas enzimas. Citral , un inhibidor de la enzima RALDH, suprimió la expresión de adhesinas α4β7 en la superficie celular, lo que sugiere que la catálisis de vitamina A → ácido retinoico era importante.
Capacidad de retorno al hogar
En teoría, esto debería aumentar la capacidad de las células T activadas para dirigirse al intestino. Pruebas de ello proceden de estudios realizados con ratones tratados con AR y con deficiencia de vitamina A. En los ratones con niveles elevados de AR se encontró una mayor cantidad de células T en el tejido intestinal. Las investigaciones realizadas con ratones con deficiencia de vitamina A confirmaron que lo contrario era cierto, ya que se encontró una cantidad significativamente menor de células T en la lámina propia intestinal en comparación con los ratones de control. Por el contrario, no se observó una disminución similar en la cantidad de células T en los pulmones y el hígado de los ratones con deficiencia, lo que implica que la vía de impronta de AR es exclusiva de las células T que se dirigen al intestino de forma específica. [11]
Regulación transcripcional por el ácido retinoico
Se ha teorizado que los niveles de AR afectan la expresión de los receptores MadCAM-1 y α4β7 mediante regulación transcripcional.
Los receptores RAR y RXR, que son los receptores nucleicos de la AR, pueden formar heterodímeros en determinadas condiciones celulares. En la conformación dimérica, los receptores pueden unirse a secuencias RARE o RXRE que se encuentran en el ADN. Estas regiones genéticas se encuentran a menudo en el extremo 5' de los genes, lo que sugiere que desempeñan un papel regulador. De hecho, suelen encontrarse cerca del comienzo o en los intrones de los genes regulados en respuesta a los niveles de retinoides.
Se han encontrado secciones de estas secuencias RARE, y además de las cajas RA, en los primeros exones de los genes que codifican los receptores b7 y CCR9. El uso de proteínas antagonistas contra la subunidad RAR mostró una reducción en la expresión de alfa. [12]
Por lo tanto, es posible que la expresión de los receptores alfa esté regulada transcripcionalmente por la concentración de RA en la célula.
Otros efectos de la vitamina A sobre la localización de los linfocitos
También se ha demostrado que el aumento de las concentraciones de vitamina A reduce la expresión de los receptores P-Lig, E-Lig y Fuct-VII in vitro. Esto sugiere que la vitamina A no solo aumenta la capacidad de las células T de llegar al intestino, sino que también reduce simultáneamente la probabilidad de que la célula se una a otro tejido.
Razones para la migración de los linfocitos
El argumento más convincente es que al dirigir los linfocitos a la región en la que fueron activados, es más probable que entren en contacto con su antígeno cognado. Se dirigen a la región en la que es más probable que se encuentre el antígeno del patógeno dentro de la periferia. Además, es posible que el tipo de tejido pueda tener un efecto sobre los rasgos fenotípicos de las células T tanto en la activación como en la migración a través del tejido. Por lo tanto, parecería sensato que las células T muestren signos de tejido preferencial, ya que es probable que desempeñen su función protectora en un entorno al que están más adaptadas.
Preocupaciones de salud
En las personas mayores es común que se produzca una disminución de la respuesta inmunitaria intestinal relacionada con la edad. Se ha planteado la hipótesis de que esta inmunosenescencia se debe a una alteración de la localización de los linfocitos en las placas de Peyer que se encuentran en el intestino. [13]
Este proceso no es exclusivo de los humanos y está documentado en otros animales, incluidos los macacos rhesus [14] y las ratas. Las investigaciones han demostrado que las ratas mayores tenían una expresión reducida de los receptores de localización específicos del intestino α4β7 y MadCAM-1. Estas ratas mayores tenían un 30 % menos de α4β7 y un 17 % menos de MadCAM-1 que sus equivalentes de rata juvenil. [15]
Si bien hasta la fecha no se ha demostrado una relación causal, se especula que la expresión reducida de los receptores es responsable de la pérdida general de la respuesta inmunitaria. Además, las modificaciones posteriores a la traducción pueden debilitar la afinidad de los receptores entre sí. [15]
Trabajo futuro
Se necesita mucho más trabajo para comprender completamente las condiciones necesarias para provocar la migración a tejidos específicos. Sin embargo, una mayor comprensión de este campo ofrece un gran potencial en la terapéutica médica. Puede ser posible dirigir vacunas orales atenuadas a la mucosa intestinal. De este modo, se espera que la vacuna sea más confiable y efectiva. Además, puede mejorar el tratamiento de la enfermedad intestinal crónica.
Otros linfocitos que se dirigen a tejidos específicos
La localización específica del intestino es la forma más conocida de localización de los linfocitos. Sin embargo, existen muchos otros ejemplos, entre los que se incluyen:
- Homing específico linfoide : Homing de células T vírgenes en el tejido linfático que rodea el cuerpo. La adhesina expresada por las células T vírgenes es la L-selectina (1). Una vez que las células T se activan, reprimen la expresión de la L-selectina para permitirles migrar libremente por el cuerpo a través de la sangre.
- Homing específico de la piel : actúa como un método para reclutar una gran cantidad de células T de memoria a la piel, lo que plantea un alto riesgo de infección. Nuevamente, esto implica la expresión de diferentes integrinas. En este caso, en los humanos, α4β1 y el antígeno linfocítico cutáneo ( CLA ) se expresan en la superficie de las células T. Estas integrinas interactúan con las moléculas de E-selectina que se encuentran en la piel inflamada.
- Direccionamiento específico de la mama : interviene en la redirección de las células T a las glándulas mamarias. Esto ocurre para que los linfocitos protectores se incluyan en la leche materna.
- Homing de células B : hasta el momento, existe un conocimiento limitado sobre este tema.
Referencias
- ^ abc Mackay (1993). "Reubicación de linfocitos ingenuos, de memoria y efectores". Current Opinion in Immunology . 5 (3): 423–427. doi :10.1016/0952-7915(93)90063-X. PMID 8347302.
- ^ von Andrian, Mempel (2003). "Homing y tráfico celular en los ganglios linfáticos". Nature Reviews Immunology . 3 (11): 867–878. doi :10.1038/nri1222. PMID 14668803. S2CID 5199142.
- ^ Iwata, Hirakiyama; et al. (2004). "El ácido retinoico imprime especificidad de localización intestinal en las células T". The Journal of Clinical Investigation . 21 (8): 527–538. doi :10.1172/JCI44262. PMC 3223921 . PMID 21737878.
- ^ ab Rodrigo Mora, Nono, Manjunath; et al. (2003). "Impresión selectiva de células T que se dirigen al intestino por células dendríticas de las placas de Peyer". Nature . 424 (6944): 88–93. Bibcode :2003Natur.424...88M. doi :10.1038/nature01726. hdl : 10533/174304 . PMID 12840763. S2CID 4402762.
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ) - ^ Schippers, A; Leuker, C; Pabst, O; Kochut, A; Prochnow, B; Gruber, AD; Leung, E; Krissansen, GW; Wagner, N; Müller, W (septiembre de 2009). "La molécula de adhesión celular adresina mucosa-1 controla la migración y la función de las células plasmáticas en el intestino delgado de ratones". Gastroenterología . 137 (3): 924–33. doi : 10.1053/j.gastro.2009.05.039 . PMID 19450594.
- ^ Briskin; et al. (1996). "Requerimientos estructurales para la unión de la adresina vascular mucosa a su receptor linfocítico alfa 4 beta 7. Temas comunes entre las interacciones de la familia integrina-Ig". Revista de Inmunología . 156 (2): 719–726. doi : 10.4049/jimmunol.156.2.719 . PMID 8543825. S2CID 25351049.
- ^ Parmo-Cabañas, M; García-Bernal D; García-Verdugo R; Kremer L; Márquez G; Teixidó J. (agosto de 2007). "Señalización intracelular necesaria para la adhesión de células T estimulada por CCL25 mediada por la integrina alfa4beta1". J. Leukoc. Biol . 82 (2): 380–91. doi :10.1189/jlb.1206726. hdl : 10261/72227 . PMID 17510295. S2CID 10625415.
- ^ Johansso-Lindbom; et al. (2005). "Especialización funcional de las células dendríticas CD103+ intestinales en la regulación de la localización selectiva de células T en tejidos". Revista de Medicina Experimental . 234 (1): 268–281. doi :10.1111/j.0105-2896.2009.00874.x. PMID 20193025. S2CID 22683173.
- ^ Duester (2000). "Familias de retinoides deshidrogenasas que regulan la función de la vitamina A: producción de pigmento visual y ácido retinoico". Revista Europea de Bioquímica . 8 (14): 4315–24. doi :10.1046/j.1432-1327.2000.01497.x. PMID 10880953. S2CID 23327657.
- ^ ab Berlin (1993). "La integrina alfa4beta7 media la unión de los linfocitos a la adresina vascular mucosal MAdCAM-1". Cell . 74 (1): 185–195. doi :10.1016/0092-8674(93)90305-a. PMID 7687523. S2CID 23742982.
- ^ Versnel (2004). "Ácido retinoico: un "elixir vitamínico" educativo para las células T que buscan el intestino". Inmunidad . 21 (4): 458–460. doi : 10.1016/j.immuni.2004.10.002 . PMID 15485623.
- ^ Iwata; et al. (2004). "El ácido retinoico imprime una huella específica de localización intestinal en las células T". Inmunidad . 21 (4): 527–538. doi : 10.1016/j.immuni.2004.08.011 . PMID 15485630.
- ^ Schmucker, DL; Owen, RL; Outenreath, R; Thoreux, K (2003). "Base para el deterioro relacionado con la edad en la inmunidad de la mucosa intestinal". Inmunología clínica y del desarrollo . 10 (2–4): 167–72. doi :10.1080/10446670310001642168. PMC 2485420 . PMID 14768948.
- ^ Taylor, LD; Daniels, CK; Schmucker, DL (abril de 1992). "El envejecimiento compromete la respuesta inmunitaria de la mucosa gastrointestinal en el mono rhesus". Inmunología . 75 (4): 614–8. PMC 1384839 . PMID 1592437.
- ^ ab Schmucker, Douglas L; Owen, Trevor M; Issekutz, Thomas B; Gonzales, Loida; Wang, Rose K (agosto de 2002). "Expresión de los receptores de localización de linfocitos α4β7 y MAdCAM-l en ratas jóvenes y viejas". Gerontología experimental . 37 (8–9): 1089–1095. doi :10.1016/S0531-5565(02)00065-7. PMID 12213559. S2CID 54328984.