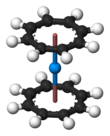
Uranoceno
| |||
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC Bis(η 8 -ciclooctatetraenil)uranio(IV) | |||
| Otros nombres Ciclooctatetraenuro de uranio U(COT) 2 | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| Araña química | |||
Identificador de centro de PubChem |
| ||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C 16 H 16 U | |||
| Masa molar | 446,33 g/mol | ||
| Apariencia | cristales verdes [1] | ||
| Peligros | |||
| Seguridad y salud en el trabajo (SST/OHS): | |||
Principales peligros | pirofórico, radiactivo y tóxico | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El uranoceno , U(C 8 H 8 ) 2 , es un compuesto organouranídico formado por un átomo de uranio intercalado entre dos anillos de ciclooctatetraenuro . Fue uno de los primeros compuestos organoactínidos que se sintetizaron. Es un sólido verde sensible al aire que se disuelve en disolventes orgánicos. El uranoceno, miembro de los " actinocenos ", un grupo de metalocenos que incorpora elementos de la serie de los actínidos . Es el sistema bis [8]anuleno -metal más estudiado, aunque no tiene aplicaciones prácticas conocidas. [2]
Síntesis, estructura y enlace
El uranoceno fue descrito por primera vez en 1968 por el grupo de Andrew Streitwieser , cuando se preparó mediante la reacción de ciclooctatetraenuro de dipotasio y tetracloruro de uranio en THF a 0 °C: [1]
El uranoceno es altamente reactivo al oxígeno, siendo pirofórico en el aire pero estable a la hidrólisis . La estructura cristalina de rayos X del uranoceno fue dilucidada por primera vez por el grupo de Ken Raymond . [3] Considerando que la molécula es U 4+ (C 8 H 8 2− ) 2 , los grupos η 8 - ciclooctatetraenuro son planares, como se espera para un anillo que contiene 10 electrones π , y son mutuamente paralelos, formando un sándwich que contiene el átomo de uranio . En el estado sólido, los anillos están eclipsados, confiriendo simetría D 8h a la molécula. En solución, los anillos giran con una energía de activación baja .
La espectroscopia fotoelectrónica demostró que el enlace uranio-ciclooctatetraenilo se debe principalmente a la mezcla de orbitales 6d del uranio en orbitales pi del ligando y, por lo tanto, a la donación de carga electrónica al uranio, con una interacción más pequeña de este tipo que involucra a los orbitales uranio ( 5f ) 2. [4] Los cálculos de la teoría electrónica concuerdan con este resultado [5] [6] y señalan que la interacción más débil de los orbitales 5f de capa abierta con los orbitales del ligando determina | M J |, la magnitud del número cuántico del momento angular a lo largo del eje de simetría óctuple del estado fundamental. [6]
Propiedades espectroscópicas
El uranoceno es paramagnético . Su susceptibilidad magnética es consistente con valores de 3 o 4 para | M J |, con el momento magnético acompañante siendo afectado por el acoplamiento espín-órbita . [7] Su espectro de RMN es consistente con un valor de | M J | de 3. [8] Los cálculos de teoría electrónica desde los más simples [9] hasta los más precisos [10] también dan valores de | M J | de 3 para el estado fundamental y 2 para el primer estado excitado, correspondientes a designaciones de simetría de doble grupo [11] de E 3g y E 2g para estos estados.
El color verde del uranoceno se debe a tres fuertes transiciones en su espectro visible . [1] [12] Además de encontrar frecuencias vibracionales, los espectros Raman indican la presencia de un estado electrónico excitado de baja altitud ( E 2g ). [12] [13] Sobre la base de los cálculos, [6] las transiciones visibles se asignan a transiciones principalmente de naturaleza 5f -a- 6d , dando lugar a estados E 2u y E 3u .
Compuestos análogos
Existen compuestos análogos de la forma M(C 8 H 8 ) 2 para M = ( Nd , Tb , Yb , Th , Pa , Np y Pu ). Las extensiones incluyen el derivado estable al aire U(C 8 H 4 Ph 4 ) 2 y la especie cicloheptatrienilo [U(C 7 H 7 ) 2 ] − . [2] Por el contrario, el bis(ciclooctatetraeno)hierro tiene una estructura muy diferente, con uno de cada uno de los ligandos η 6 - y η 4 -C 8 H 8 .
Referencias
- ^ abc Streitwieser, A.; Mueller-Westerhoff, U. (1968). "Bis(ciclooctatetraenil)uranio (uranoceno). Una nueva clase de complejos sándwich que utilizan orbitales atómicos f". J. Am. Chem. Soc. 90 (26): 7364. doi :10.1021/ja01028a044.
- ^ ab Seyferth, D. (2004). "Uranoceno. El primer miembro de una nueva clase de derivados organometálicos de los elementos f". Organometallics . 23 (15): 3562–3583. doi : 10.1021/om0400705 .
- ^ Zalkin, Allan; Raymond, Kenneth N. (1969). "Estructura del di-.pi.-ciclooctatetraeneuranio (uranoceno)". Revista de la Sociedad Química Estadounidense . 91 (20): 5667–5668. doi :10.1021/ja01048a055. ISSN 0002-7863.
- ^ Clark, JP; Green, JC (1977). "Una investigación de la estructura electrónica de los actinoides bis( eta -ciclo-octatetraeno) mediante espectroscopia de fotoelectrones de helio-(I) y -(II)". J. Chem. Soc., Dalton Trans. (5): 505–508. doi :10.1039/DT9770000505.
- ^ Roesch, N.; Streitwieser, A. (1983). "Estudio cuasirelativista de ondas dispersas SCF-X alfa del uranoceno, el toroceno y el ceroceno". J. Am. Chem. Soc. 105 (25): 7237–7240. doi :10.1021/ja00363a004.
- ^ abc Chang, AHH; Pitzer, RM (1989). "Estructura electrónica y espectros del uranoceno". J. Am. Chem. Soc. 111 (7): 2500–2507. doi :10.1021/ja00189a022.
- ^ Karraker, DG; Stone, JA; Jones, ER; Edelstein, N. (1970). "Bis(ciclooctatetraenil)neptunio(IV) y bis(ciclooctatetraenil)plutonio(IV)". J. Chem. Phys. 92 (16): 4841–4845. doi :10.1021/ja00719a014.
- ^ Fischer, RD (1979). "Espectroscopia de RMN de compuestos organometálicos de los elementos f: aplicaciones prácticas". En Marks, TJ; Fischer, RD (eds.). Volumen 44 – Organometálicos de los elementos f . Serie de Institutos de Estudios Avanzados de la OTAN: Serie C – Ciencias matemáticas y físicas. Dordrecht, Holanda: Reidel. págs. 337–377. ISBN 90-277-0990-4.
- ^ Hayes, RG; Edelstein, N. (1972). "Un cálculo orbital molecular elemental sobre U(C 8 H 8 ) 2 y su aplicación a la estructura electrónica de U(C 8 H 8 ) 2 , Np(C 8 H 8 ) 2 . y Pu(C 8 H 8 ) 2 ". J. Am. Chem. Soc . 94 (25): 8688–8691. doi :10.1021/ja00780a008.
- ^ Liu, W.; Dolg, M.; Fulde, P. (1997). "Estados electrónicos de baja altitud de lantanocenos y actinocenos M(C 8 H 8 ) 2 (M = Nd, Tb, Yb, U)". J. Chem. Phys. 107 (9): 3584–3591. Código Bibliográfico :1997JChPh.107.3584L. doi :10.1063/1.474698.
- ^ Herzberg, G. (1966). Espectros moleculares y estructura molecular III. Espectros electrónicos y estructura electrónica de moléculas poliatómicas . Princeton, Nueva Jersey: D. Van Nostrand. pág. 566.
- ^ ab Dallinger, RF; Stein, P.; Spiro, TG (1978). "Espectroscopia de resonancia Raman del uranoceno: observación de una banda electrónica polarizada de forma anómala y asignación de niveles de energía". J. Am. Chem. Soc. 100 (25): 7865–7870. doi :10.1021/ja00493a013.
- ^ Hager, JS; Zahardis, J.; Pagni, RM; et al. (2004). "Raman bajo nitrógeno. La espectroscopia Raman de alta resolución del uranoceno, toroceno y ferroceno cristalino". J. Chem. Phys. 120 (6): 2708–2718. Bibcode :2004JChPh.120.2708H. doi :10.1063/1.1637586. PMID 15268415.
Lectura adicional
- Los elementos f , Nikolas Kaltsoyannis y Peter Scott. ISBN 0-19-850467-5
- Química de los elementos , NN Greenwood y A. Earnshaw. ISBN 0-08-022057-6
- Lantánidos y actínidos: organoactínidos