Análogo de ácido nucleico
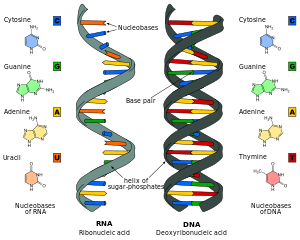
Los análogos de ácidos nucleicos son compuestos análogos ( estructuralmente similares) al ARN y ADN naturales , utilizados en medicina y en la investigación de biología molecular. Los ácidos nucleicos son cadenas de nucleótidos, que se componen de tres partes: una cadena principal de fosfato , un azúcar pentosa, ya sea ribosa o desoxirribosa , y una de cuatro nucleobases . Un análogo puede tener cualquiera de estos alterados. [1] Normalmente, las nucleobases análogas confieren, entre otras cosas, diferentes propiedades de apareamiento y apilamiento de bases. Los ejemplos incluyen bases universales, que pueden emparejarse con las cuatro bases canónicas, y análogos de la cadena principal de fosfato-azúcar como PNA , que afectan las propiedades de la cadena (PNA puede incluso formar una triple hélice ). [2] Los análogos de ácidos nucleicos también se denominan xenoácidos nucleicos y representan uno de los pilares principales de la xenobiología , el diseño de formas de vida nuevas en la naturaleza basadas en bioquímicas alternativas.
Los ácidos nucleicos artificiales incluyen los ácidos nucleicos peptídicos (PNA), los ácidos nucleicos morfolino y bloqueados (LNA), así como los ácidos nucleicos glicolados (GNA), los ácidos nucleicos treosa (TNA) y los ácidos nucleicos hexitol (HNA). Cada uno de ellos se distingue del ADN o ARN naturales por los cambios en la estructura principal de la molécula. Sin embargo, la teoría polielectrolítica del gen propone que una molécula genética requiere una estructura principal cargada para funcionar.
En mayo de 2014, los investigadores anunciaron que habían introducido con éxito dos nuevos nucleótidos artificiales en el ADN bacteriano y que, al incluir nucleótidos artificiales individuales en el medio de cultivo, habían logrado que la bacteria pasara 24 veces; no crearon ARNm ni proteínas capaces de utilizar los nucleótidos artificiales. Los nucleótidos artificiales presentaban dos anillos aromáticos fusionados.
Medicamento
Varios análogos de nucleósidos se utilizan como agentes antivirales o anticancerígenos. La polimerasa viral incorpora estos compuestos con bases no canónicas. Estos compuestos se activan en las células al convertirse en nucleótidos y se administran como nucleósidos, ya que los nucleótidos cargados no pueden atravesar fácilmente las membranas celulares. [ cita requerida ]
Biología molecular

Los análogos de ácidos nucleicos se utilizan en biología molecular para varios propósitos:
- Investigación de posibles escenarios del origen de la vida: Al probar diferentes análogos, los investigadores intentan responder a la pregunta de si el uso de ADN y ARN para la vida fue seleccionado a lo largo del tiempo debido a sus ventajas, o si fueron elegidos por casualidad arbitraria; [3]
- Como herramienta para detectar secuencias particulares: XNA se puede utilizar para etiquetar e identificar una amplia gama de componentes de ADN y ARN con alta especificidad y precisión; [4]
- Como enzima que actúa sobre sustratos de ADN, ARN y XNA, se ha demostrado que XNA tiene la capacidad de escindir y ligar ADN, ARN y otras moléculas de XNA de manera similar a las acciones de las ribozimas de ARN ; [3]
- Como herramienta con resistencia a la hidrólisis del ARN ;
- Investigación de los mecanismos utilizados por la enzima; y
- Investigación de las características estructurales de los ácidos nucleicos.
Análogos de la columna vertebral
Análogos de ARN resistentes a la hidrólisis
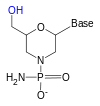
El grupo hidroxi 2' de la ribosa reacciona con el grupo hidroxi 3' unido al fosfato, lo que hace que el ARN sea demasiado inestable para ser utilizado o sintetizado de manera confiable. Para superar esto, se puede utilizar un análogo de la ribosa. Los análogos de ARN más comunes son el ARN 2'-O-metil-sustituido, el ácido nucleico bloqueado (LNA) o el ácido nucleico puenteado (BNA), el morfolino [5] [ 6] y el ácido nucleico peptídico ( PNA ). Aunque estos oligonucleótidos tienen un azúcar de cadena principal diferente (o, en el caso del PNA, un residuo de aminoácido en lugar del fosfato de ribosa), aún se unen al ARN o al ADN según el emparejamiento de Watson y Crick mientras son inmunes a la actividad de las nucleasas. No se pueden sintetizar enzimáticamente y solo se pueden obtener sintéticamente utilizando la estrategia de la fosforamidita o, para el PNA, otros métodos de síntesis de péptidos . [ cita requerida ]
Otros análogos notables utilizados como herramientas
Los didesoxinucleótidos se utilizan en la secuenciación . Estos trifosfatos de nucleósidos poseen un azúcar no canónico, la didesoxirribosa, que carece del grupo hidroxilo 3' normalmente presente en el ADN y, por lo tanto, no puede unirse con la siguiente base. La falta del grupo hidroxilo 3' termina la reacción en cadena, ya que las polimerasas del ADN lo confunden con un desoxirribonucleótido normal. Otro análogo de terminación de cadena que carece de un hidroxilo 3' e imita a la adenosina se llama cordicepina . La cordicepina es un fármaco contra el cáncer que tiene como objetivo la replicación del ARN . Otro análogo en la secuenciación es un análogo de nucleobase, 7-deaza-GTP, y se utiliza para secuenciar regiones ricas en CG; en cambio, la 7-deaza-ATP se llama tubercidina, un antibiótico. [ cita requerida ]
Precursores del mundo del ARN
Se ha sugerido que el mundo del ARN puede haber sido precedido por un "mundo similar al ARN" donde existían otros ácidos nucleicos con una estructura diferente, como GNA , PNA y TNA , sin embargo, la evidencia de esta hipótesis se ha calificado de "tenue". [7]
Análogos de base
Estructura y nomenclatura de las nucleobases
Las bases naturales se pueden dividir en dos clases según su estructura:
- Las pirimidinas son heterocíclicos de seis miembros con átomos de nitrógeno en la posición 1 y 3.
- Las purinas son bicíclicas y consisten en una pirimidina fusionada a un anillo de imidazol.
Se han insertado nucleótidos artificiales ( pares de bases no naturales (UBP) denominados d5SICS UBP y dNaM UBP ) en el ADN bacteriano, pero estos genes no sirvieron de modelo para el ARNm ni indujeron la síntesis de proteínas. Los nucleótidos artificiales presentaban dos anillos aromáticos fusionados que formaban un complejo (d5SICS–dNaM) que imitaba el par de bases natural (dG–dC). [8] [9] [10]
Mutágenos
Uno de los análogos de base más comunes es el 5-bromouracilo (5BU), la base anormal que se encuentra en el análogo de nucleótido mutagénico BrdU. Cuando un nucleótido que contiene 5-bromouracilo se incorpora al ADN, es más probable que se aparee con la adenina; sin embargo, puede cambiar espontáneamente a otro isómero que se aparea con una nucleobase diferente , la guanina . Si esto sucede durante la replicación del ADN, se insertará una guanina como el análogo de base opuesto y, en la siguiente replicación del ADN, esa guanina se apareará con una citosina. Esto da como resultado un cambio en un par de bases del ADN, específicamente una mutación de transición . [ cita requerida ]
Además, el ácido nitroso (HNO2) es un potente mutágeno que actúa sobre el ADN replicante y no replicante. Puede causar la desaminación de los grupos amino de la adenina, la guanina y la citosina. La adenina se desamina a hipoxantina , que se empareja con la citosina en lugar de la timina. La citosina se desamina a uracilo, que se empareja con la adenina en lugar de la guanina. La desaminación de la guanina no es mutagénica. Las mutaciones inducidas por el ácido nitroso también se inducen a mutar de nuevo al tipo salvaje. [ cita requerida ]
Fluoróforos

Comúnmente, los fluoróforos (como la rodamina o la fluoresceína ) se unen al anillo unido al azúcar (en para) a través de un brazo flexible, que presumiblemente sale del surco mayor de la hélice. Debido a la baja procesividad de los nucleótidos unidos a aductos voluminosos como los floróforos por las [Taq polimerasas], la secuencia se copia típicamente utilizando un nucleótido con un brazo y luego se acopla con un fluoróforo reactivo (marcaje indirecto):
- Reactivos con aminas: los nucleótidos aminoalílicos contienen un grupo amino primario en un enlace que reacciona con el colorante aminorreactivo, como la cianina o los colorantes Alexa Fluor , que contienen un grupo saliente reactivo como el éster succinimidílico (NHS). Los grupos amino de apareamiento de bases no se ven afectados.
- Reactivo de tiol: los nucleótidos que contienen tiol reaccionan con el fluoróforo unido a un grupo saliente reactivo como la maleimida.
- Los nucleótidos ligados a biotina se basan en el mismo principio de etiquetado indirecto (y estreptavidina fluorescente) y se utilizan en los DNAchips de Affymetrix .
Los fluoróforos encuentran una variedad de usos en la medicina y la bioquímica.
Análogos de bases fluorescentes
El análogo de base fluorescente más comúnmente utilizado y disponible comercialmente, la 2-aminopurina (2-AP), tiene un alto rendimiento cuántico de fluorescencia libre en solución (0,68) que se reduce considerablemente (aproximadamente 100 veces, pero altamente dependiente de la secuencia de bases) cuando se incorpora a ácidos nucleicos. [11] La sensibilidad de emisión de 2-AP al entorno inmediato es compartida por otros análogos de base fluorescentes prometedores y útiles como 3-MI, 6-MI, 6-MAP, [12] pirrolo-dC (también disponible comercialmente), [13] derivados modificados y mejorados de pirrolo-dC, [14] bases modificadas con furano [15] y muchas otras (ver revisiones recientes). [16] [17] [ 18] [19] [20] Esta sensibilidad al microambiente se ha utilizado en estudios de, por ejemplo, estructura y dinámica dentro del ADN y el ARN, dinámica y cinética de la interacción ADN-proteína y transferencia de electrones dentro del ADN. [ cita requerida ]
Un grupo recientemente desarrollado y muy interesante de análogos de bases fluorescentes que tiene un rendimiento cuántico de fluorescencia que es casi insensible a su entorno inmediato es la familia de citosinas tricíclicas. 1,3-Diaza-2-oxofenotiazina, tC, tiene un rendimiento cuántico de fluorescencia de aproximadamente 0,2 tanto en cadenas simples como en cadenas dobles, independientemente de las bases circundantes. [21] [22] También el oxo-homólogo de tC llamado tC O (ambos disponibles comercialmente), 1,3-diaza-2-oxofenoxazina, tiene un rendimiento cuántico de 0,2 en sistemas de doble cadena. [23] Sin embargo, es algo sensible a las bases circundantes en cadenas simples (rendimientos cuánticos de 0,14-0,41). Los altos y estables rendimientos cuánticos de estos análogos de base los hacen muy brillantes y, en combinación con sus buenas propiedades de análogo de base (dejan la estructura y estabilidad del ADN casi inalteradas), son especialmente útiles en anisotropía de fluorescencia y mediciones de FRET, áreas donde otros análogos de base fluorescentes son menos precisos. Además, en la misma familia de análogos de citosina, se ha desarrollado un análogo de base aceptor de FRET, tC nitro . [24] Junto con tC O como donante de FRET, esto constituye el primer par FRET de análogo de base de ácido nucleico jamás desarrollado. La familia tC se ha utilizado, por ejemplo, en estudios relacionados con la unión del ADN de la polimerasa y los mecanismos de polimerización del ADN.
Bases naturales no canónicas
En una célula, hay varias bases no canónicas presentes: islas CpG en el ADN (a menudo metiladas), todos los ARNm eucariotas (protegidos con una metil-7-guanosina) y varias bases de ARNr (metiladas). A menudo, los ARNt se modifican en gran medida postranscripcionalmente para mejorar su conformación o apareamiento de bases, en particular en o cerca del anticodón: la inosina puede aparearse con C, U e incluso con A, mientras que la tiouridina (con A) es más específica que el uracilo (con una purina). [25] Otras modificaciones de bases de ARNt comunes son la pseudouridina (que da su nombre al bucle TΨC ), la dihidrouridina (que no se apila porque no es aromática), la queuosina, la wyosina, etc. Sin embargo, todas estas son modificaciones de bases normales y no las coloca una polimerasa. [25]
Apareamiento de bases
Las bases canónicas pueden tener un grupo carbonilo o un grupo amina en los carbonos que rodean al átomo de nitrógeno más alejado del enlace glucosídico, lo que les permite aparearse ( emparejamiento de bases Watson-Crick) a través de enlaces de hidrógeno (amina con cetona, purina con pirimidina). La adenina y la 2-aminoadenina tienen uno o dos grupos amina, mientras que la timina tiene dos grupos carbonilo, y la citosina y la guanina son aminas y carbonilos mixtos (invertidos entre sí). [ cita requerida ]
| Pares de bases naturales | |
|---|---|
 |  |
| Un par de bases GC: carbonilo/amina de purina forma tres enlaces de hidrógeno intermoleculares con amina/carbonilo de pirimidina. | Un par de bases AT: amina de purina/- forma dos enlaces de hidrógeno intermoleculares con carbonilo/carbonilo de pirimidina. |
La razón precisa por la que solo hay cuatro nucleótidos es objeto de debate, pero hay varias posibilidades que no se utilizan. Además, la adenina no es la opción más estable para el emparejamiento de bases: en Cyanophage S-2L, se utiliza diaminopurina (DAP) en lugar de adenina. [26] La diaminopurina se empareja perfectamente con la timina, ya que es idéntica a la adenina, pero tiene un grupo amino en la posición 2 que forma 3 enlaces de hidrógeno intramoleculares, lo que elimina la principal diferencia entre los dos tipos de pares de bases (AT débil frente a CG fuerte). Esta estabilidad mejorada afecta a las interacciones de unión a proteínas que dependen de esas diferencias. Otras combinaciones incluyen:
- Isoguanina e isocitosina, que tienen sus aminas y cetonas invertidas en comparación con la guanina y la citosina estándar. Probablemente no se utilicen porque los tautómeros son problemáticos para el apareamiento de bases, pero isoC e isoG se pueden amplificar correctamente con PCR incluso en presencia de las 4 bases canónicas. [27]
- Diaminopirimidina y xantina, que se unen como la 2-aminoadenina y la timina pero con estructuras invertidas. Este par no se utiliza porque la xantina es un producto de desaminación.
| Disposiciones de pares de bases no utilizadas | ||
|---|---|---|
 | 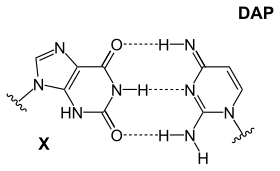 |  |
| Una base DAP-T: la amina purínica/amina forma tres enlaces de hidrógeno intermoleculares con la cetona pirimidínica/cetona. | Una base X-DAP: la cetona/cetona de purina forma tres enlaces de hidrógeno intermoleculares con la amina/amina de pirimidina. | Una base iG-iC: la amina/cetona de purina forma tres enlaces de hidrógeno intermoleculares con la amina/cetona de pirimidina. |
Sin embargo, la estructura correcta del ADN puede formarse incluso cuando las bases no están emparejadas a través de enlaces de hidrógeno; es decir, las bases se emparejan gracias a la hidrofobicidad, como han demostrado los estudios con isósteros de ADN (análogos con el mismo número de átomos) como el análogo de timina 2,4-difluorotolueno (F) o el análogo de adenina 4-metilbencimidazol (Z). [28] Un par hidrofóbico alternativo podría ser la isoquinolina y la pirrolo[2,3-b]piridina [29]
Otros pares de bases dignos de mención:
- También se han creado varias bases fluorescentes, como el par de bases 2-amino-6-(2-tienil)purina y pirrol-2-carbaldehído. [30]
- Bases coordinadas con metales, como el apareamiento entre un piridina-2,6-dicarboxilato (ligando tridentado) y una piridina (ligando monodentado) a través de una coordinación plana cuadrada con un ion de cobre central. [31]
- Las bases universales pueden aparearse indiscriminadamente con cualquier otra base, pero, en general, reducen considerablemente la temperatura de fusión de la secuencia; por ejemplo, los derivados de la 2'-desoxiinosina (desoxinucleótido de hipoxantina), los análogos de nitroazol y las bases aromáticas hidrófobas que no forman enlaces de hidrógeno (fuertes efectos de apilamiento). Se utilizan como prueba de concepto y, en general, no se utilizan en cebadores degenerados (que son una mezcla de cebadores).
- El número de pares de bases posibles se duplica cuando se considera el xDNA . El xDNA contiene bases expandidas, en las que se ha añadido un anillo de benceno, que puede aparearse con bases canónicas, lo que da como resultado cuatro pares de bases posibles adicionales (xA-T, xT-A, xC-G, xG-C) con ocho bases (o 16 bases si se utilizan los arreglos no utilizados). Otra forma de bases añadidas con benceno es el yDNA, en el que la base se ensancha por el benceno. [32]
| Nuevos pares de bases con propiedades especiales | ||
|---|---|---|
 |  |  |
| Una base FZ: el metilbencimidazol no forma enlaces de hidrógeno intermoleculares con tolueno F/F | Una base S-Pa: la purina tienil/amina forma tres enlaces de hidrógeno intermoleculares con pirrol -/carbaldehído | Una base xA-T: mismo enlace que AT |
Pares de bases de metal
En el apareamiento de bases metálicas, los enlaces de hidrógeno de Watson-Crick se reemplazan por la interacción entre un ion metálico con nucleósidos que actúan como ligandos. Las posibles geometrías del metal que permitirían la formación de dúplex con dos nucleósidos bidentados alrededor de un átomo metálico central son tetraédrica , dodecaédrica y plana cuadrada . La formación de complejos de metales con ADN puede ocurrir por la formación de pares de bases no canónicos a partir de nucleobases naturales con participación de iones metálicos y también por el intercambio de los átomos de hidrógeno que forman parte del apareamiento de bases de Watson-Crick por iones metálicos. [33] Se ha demostrado que la introducción de iones metálicos en un dúplex de ADN tiene propiedades magnéticas [34] o conductoras potenciales, [35] así como una mayor estabilidad. [36]
Se ha demostrado que la formación de complejos metálicos ocurre entre nucleobases naturales . Un ejemplo bien documentado es la formación de T-Hg-T, que involucra dos nucleobases de timina desprotonadas que se unen mediante Hg 2+ y forman un par de base metálica conectado. [37] Este motivo no da cabida a Hg 2+ apilado en un dúplex debido a un proceso de formación de horquilla intracatenaria que se favorece sobre la formación de dúplex. [38] Dos timinas una frente a la otra no forman un par de bases Watson-Crick en un dúplex; este es un ejemplo en el que un desajuste de pares de bases Watson-Crick se estabiliza mediante la formación del par de base metálica. Otro ejemplo de formación de complejos metálicos con nucleobases naturales es la formación de A-Zn-T y G-Zn-C a pH alto; Co 2+ y Ni 2+ también forman estos complejos. Estos son pares de bases Watson-Crick en los que el catión divalente está coordinado con las nucleobases. La unión exacta es motivo de debate. [39]
Se ha desarrollado una gran variedad de nucleobases artificiales para su uso como pares de bases metálicas. Estas nucleobases modificadas exhiben propiedades electrónicas ajustables, tamaños y afinidades de enlace que se pueden optimizar para un metal específico. Por ejemplo, se ha demostrado que un nucleósido modificado con un piridina-2,6-dicarboxilato se une firmemente a Cu 2+ , mientras que otros iones divalentes solo se unen de manera débil. El carácter tridentado contribuye a esta selectividad. El cuarto sitio de coordinación en el cobre está saturado por una nucleobase de piridina dispuesta de manera opuesta. [40] El sistema de apareamiento de bases metálicas asimétrico es ortogonal a los pares de bases de Watson-Crick. Otro ejemplo de una nucleobase artificial es aquella con nucleobases de hidroxipiridona, que pueden unirse a Cu 2+ dentro del dúplex de ADN. Se incorporaron cinco pares de bases de cobre-hidroxipiridona consecutivos en una doble cadena, que estaban flanqueados por una sola nucleobase natural en ambos extremos. Los datos de EPR mostraron que la distancia entre los centros de cobre se estimó en 3,7 ± 0,1 Å, mientras que un dúplex de ADN de tipo B natural es solo ligeramente más grande (3,4 Å). [41] El atractivo de apilar iones metálicos dentro de un dúplex de ADN es la esperanza de obtener cables metálicos autoensamblables nanoscópicos, aunque esto aún no se ha hecho realidad.
Par de bases no naturales (UBP)
Un par de bases no naturales (UBP) es una subunidad diseñada (o nucleobase ) de ADN que se crea en un laboratorio y no ocurre en la naturaleza. En 2012, un grupo de científicos estadounidenses dirigido por Floyd Romesberg, un biólogo químico del Instituto de Investigación Scripps en San Diego, California, publicó que su equipo había diseñado dos pares de bases no naturales llamados d5SICS y dNaM . [42] Más técnicamente, estos nucleótidos artificiales que llevan nucleobases hidrófobas presentan dos anillos aromáticos fusionados que forman un complejo o par de bases d5SICS–dNaM en el ADN. [10] [43] En 2014, el mismo equipo informó que habían sintetizado un plásmido que contenía pares de bases TA y CG naturales junto con el UBP de mejor rendimiento que el laboratorio de Romesberg había diseñado y lo había insertado en células de la bacteria común E. coli , que replicó con éxito los pares de bases no naturales a través de múltiples generaciones. [44] Este es el primer ejemplo conocido de un organismo vivo que transmite un código genético ampliado a generaciones posteriores. [10] [45] Esto se logró en parte mediante la adición de un gen de alga de apoyo que expresa un transportador de trifosfato de nucleótidos que importa de manera eficiente los trifosfatos de d5SICSTP y dNaMTP a las bacterias E. coli . [10] Luego, las vías de replicación bacterianas naturales los utilizan para replicar con precisión el plásmido que contiene d5SICS–dNaM. [ cita requerida ]
La incorporación exitosa de un tercer par de bases es un avance significativo hacia el objetivo de expandir en gran medida el número de aminoácidos que pueden ser codificados por el ADN, de los 20 aminoácidos existentes a 172 teóricamente posibles, expandiendo así el potencial de los organismos vivos para producir nuevas proteínas . [44] Anteriormente, las cadenas artificiales de ADN no codificaban nada, pero los científicos especularon que podrían diseñarse para fabricar nuevas proteínas que podrían tener usos industriales o farmacéuticos. [46] La transcripción de ADN que contiene pares de bases no naturales y la traducción del ARNm correspondiente se lograron recientemente. En noviembre de 2017, el mismo equipo del Instituto de Investigación Scripps que introdujo por primera vez dos nucleobases adicionales en el ADN bacteriano informó haber construido una bacteria E. coli semisintética capaz de producir proteínas utilizando dicho ADN. Su ADN contenía seis nucleobases diferentes : cuatro canónicas y dos añadidas artificialmente, dNaM y dTPT3 (estas dos forman un par). Las bacterias tenían dos bases de ARN correspondientes incluidas en dos nuevos codones, ARNt adicionales que reconocían estos nuevos codones (estos ARNt también contenían dos nuevas bases de ARN dentro de sus anticodones) y aminoácidos adicionales, lo que permitía a las bacterias sintetizar proteínas "no naturales". [47] [48]
Otra demostración de UBP fue lograda por el grupo de Ichiro Hirao en el instituto RIKEN en Japón. En 2002, desarrollaron un par de bases no natural entre 2-amino-8-(2-tienil)purina (s) y piridina-2-ona (y) que funciona in vitro en la transcripción y traducción, para la incorporación específica del sitio de aminoácidos no estándar en proteínas. [49] En 2006, crearon 7-(2-tienil)imidazo[4,5-b]piridina (Ds) y pirrol-2-carbaldehído (Pa) como un tercer par de bases para la replicación y la transcripción. [50] Posteriormente, se descubrió que Ds y 4-[3-(6-aminohexanamido)-1-propinil]-2-nitropirrol (Px) eran un par de alta fidelidad en la amplificación por PCR. [51] [52] En 2013, aplicaron el par Ds-Px a la generación de aptámeros de ADN mediante selección in vitro (SELEX) y demostraron que la expansión del alfabeto genético aumenta significativamente las afinidades de los aptámeros de ADN con las proteínas objetivo. [53]
Sistema ortogonal
Se ha propuesto y estudiado, tanto teórica como experimentalmente, la posibilidad de implementar un sistema ortogonal en el interior de las células independientemente del material genético celular para conseguir un sistema totalmente seguro [54] , con el posible aumento de los potenciales de codificación [55] . Varios grupos se han centrado en diferentes aspectos:
- Nuevas cadenas principales y pares de bases como los discutidos anteriormente;
- Las polimerasas de replicación y transcripción artificiales XNA comienzan generalmente a partir de la ARN polimerasa T7 ; [56]
- ( secuencias ribosómicas 16S con secuencias anti-Shine-Dalgarno alteradas que permiten la traducción únicamente de ARNm ortogonal con una secuencia Shine-Dalgarno alterada coincidente; [57] y
- Nuevo ARNt que codifica aminoácidos no naturales para un código genético expandido .
Véase también
- Biotina
- Apagador de oscuridad
- Desoxirribozima
- Código genético ampliado
- Fluoróforo
- Genética
- Biología molecular
- Ácido nucleico
- Nucleobase
- Nucleósido
- Nucleótido
- Síntesis de oligonucleótidos
- Ribozima
- Biología sintética
- Xenobiología
- xADN
- ADN de Hachimoji
- Sistema de Información Genética Expandido Artificialmente (AEGIS)
- Ácido xenonucleico
Referencias
- ^ Singer E (19 de julio de 2015). "Los químicos inventan nuevas letras para el alfabeto genético de la naturaleza". Wired . Consultado el 20 de julio de 2015 .
- ^ Petersson B, Nielsen BB, Rasmussen H, Larsen IK, Gajhede M, Nielsen PE, Kastrup JS (febrero de 2005). "Estructura cristalina de un oligómero de ácido nucleico peptídico (PNA) parcialmente autocomplementario que muestra una red dúplex-tríplex". Journal of the American Chemical Society . 127 (5): 1424–30. doi :10.1021/ja0458726. PMID 15686374.
- ^ ab Taylor AI, Pinheiro VB, Smola MJ, Morgunov AS, Peak-Chew S, Cozens C, Weeks KM, Herdewijn P, Holliger P (febrero de 2015). "Catalizadores a partir de polímeros genéticos sintéticos". Nature . 518 (7539): 427–30. Bibcode :2015Natur.518..427T. doi :10.1038/nature13982. PMC 4336857 . PMID 25470036.
- ^ Wang Q, Chen L, Long Y, Tian H, Wu J (2013). "Balizas moleculares de ácido xenonucleico para detectar ácido nucleico". Theranostics . 3 (6): 395–408. doi :10.7150/thno.5935. PMC 3677410 . PMID 23781286.
- ^ Summerton J, Weller D (junio de 1997). "Oligómeros antisentido de morfolino: diseño, preparación y propiedades". Desarrollo de fármacos antisentido y de ácidos nucleicos . 7 (3): 187–95. doi :10.1089/oli.1.1997.7.187. PMID 9212909. S2CID 19372403.
- ^ Summerton J (diciembre de 1999). "Oligómeros antisentido de morfolino: el caso de un tipo estructural independiente de la ARNasa H". Biochimica et Biophysica Acta (BBA) - Estructura y expresión génica . 1489 (1): 141–58. doi :10.1016/s0167-4781(99)00150-5. PMID 10807004.
- ^ Robertson, MP; Joyce, GF (1 de mayo de 2012). "Los orígenes del mundo del ARN". Cold Spring Harbor Perspectives in Biology . 4 (5): a003608. doi :10.1101/cshperspect.a003608. ISSN 1943-0264. PMC 3331698 . PMID 20739415.
- ^ Pollack A (7 de mayo de 2014). "Investigadores informan de un gran avance en la creación de un código genético artificial". New York Times . Consultado el 7 de mayo de 2014 .
- ^ Callaway E (7 de mayo de 2014). "Primera vida con ADN 'alienígena'". Nature . doi :10.1038/nature.2014.15179. S2CID 86967999.
- ^ abcd Malyshev DA, Dhami K, Lavergne T, Chen T, Dai N, Foster JM, Corrêa IR, Romesberg FE (mayo de 2014). "Un organismo semisintético con un alfabeto genético expandido". Nature . 509 (7500): 385–88. Bibcode :2014Natur.509..385M. doi :10.1038/nature13314. PMC 4058825 . PMID 24805238.
- ^ Ward DC, Reich E, Stryer L (marzo de 1969). "Estudios de fluorescencia de nucleótidos y polinucleótidos. I. Formicina, ribósido de 2-aminopurina, ribósido de 2,6-diaminopurina y sus derivados". The Journal of Biological Chemistry . 244 (5): 1228–37. doi : 10.1016/S0021-9258(18)91833-8 . PMID 5767305.
- ^ Hawkins ME (2001). "Análogos de nucleósidos de pteridina fluorescentes: una ventana a las interacciones del ADN". Bioquímica y biofísica celular . 34 (2): 257–81. doi :10.1385/cbb:34:2:257. PMID 11898867. S2CID 12134698.
- ^ Berry DA, Jung KY, Wise DS, Sercel AD, Pearson WH, Mackie H, Randolph JB, Somers RL (2004). "Pyrrolo-dC y pyrrolo-C: análogos fluorescentes de citidina y 2'-desoxicitidina para el estudio de oligonucleótidos". Tetrahedron Lett . 45 (11): 2457–61. doi :10.1016/j.tetlet.2004.01.108.
- ^ Wojciechowski F, Hudson RH (septiembre de 2008). "Propiedades de fluorescencia e hibridación de ácidos nucleicos peptídicos que contienen una fenilpirrolocitosina sustituida diseñada para acoplar guanina con un enlace de hidrógeno adicional". Journal of the American Chemical Society . 130 (38): 12574–75. doi :10.1021/ja804233g. PMID 18761442.
- ^ Greco NJ, Tor Y (agosto de 2005). "Los análogos de pirimidina fluorescentes simples detectan la presencia de sitios abásicos en el ADN". Journal of the American Chemical Society . 127 (31): 10784–85. doi :10.1021/ja052000a. PMID 16076156.
- ^ Rist MJ, Marino JP (2002). "Análogos de bases de nucleótidos fluorescentes como sondas de la estructura, dinámica e interacciones de los ácidos nucleicos". Curr. Org. Chem . 6 (9): 775–93. doi :10.2174/1385272023373914.
- ^ Wilson JN, Kool ET (diciembre de 2006). "Reemplazos de bases de ADN fluorescentes: reporteros y sensores para sistemas biológicos". Química orgánica y biomolecular . 4 (23): 4265–74. doi :10.1039/b612284c. PMID 17102869.
- ^ Wilhelmsson y Tor (2016). Análogos fluorescentes de bloques de construcción biomoleculares: diseño y aplicaciones . Nueva Jersey: Wiley. ISBN 978-1-118-17586-6.
- ^ Wilhelmsson LM (mayo de 2010). "Análogos de bases de ácidos nucleicos fluorescentes". Quarterly Reviews of Biophysics . 43 (2): 159–83. doi :10.1017/s0033583510000090. PMID 20478079. S2CID 10783202.
- ^ Sinkeldam RW, Greco NJ, Tor Y (mayo de 2010). "Análogos fluorescentes de bloques de construcción biomoleculares: diseño, propiedades y aplicaciones". Chemical Reviews . 110 (5): 2579–619. doi :10.1021/cr900301e. PMC 2868948 . PMID 20205430.
- ^ Wilhelmsson LM, Holmén A, Lincoln P, Nielsen PE, Nordén B (2001). "Un análogo de base de ADN altamente fluorescente que forma pares de bases Watson-Crick con guanina". J. Am. Chem. Soc . 123 (10): 2434–35. doi :10.1021/ja0025797. PMID 11456897.
- ^ Sandin P, Wilhelmsson LM, Lincoln P, Powers VE, Brown T, Albinsson B (2005). "Propiedades fluorescentes del análogo de base de ADN tC tras su incorporación al ADN: influencia insignificante de las bases vecinas en el rendimiento cuántico de fluorescencia". Investigación de ácidos nucleicos . 33 (16): 5019–25. doi :10.1093/nar/gki790. PMC 1201328 . PMID 16147985.
- ^ Sandin P, Börjesson K, Li H, Mårtensson J, Brown T, Wilhelmsson LM, Albinsson B (enero de 2008). "Caracterización y uso de un análogo de base de ADN fluorescente sin precedentes, brillante y estructuralmente no perturbador". Nucleic Acids Research . 36 (1): 157–67. doi :10.1093/nar/gkm1006. PMC 2248743 . PMID 18003656.
- ^ Börjesson K, Preus S, El-Sagheer AH, Brown T, Albinsson B, Wilhelmsson LM (abril de 2009). "Par de análogos de bases de ácidos nucleicos FRET que facilitan mediciones estructurales detalladas en sistemas que contienen ácidos nucleicos". Journal of the American Chemical Society . 131 (12): 4288–93. doi :10.1021/ja806944w. PMID 19317504.
- ^ ab Rodriguez-Hernandez A, Spears JL, Gaston KW, Limbach PA, Gamper H, Hou YM, Kaiser R, Agris PF, Perona JJ (octubre de 2013). "Base estructural y mecanicista para una eficiencia traduccional mejorada por 2-tiouridina en la posición de oscilación del anticodón del ARNt". Journal of Molecular Biology . 425 (20): 3888–906. doi :10.1016/j.jmb.2013.05.018. PMC 4521407 . PMID 23727144.
- ^ Kirnos MD, Khudyakov IY, Alexandrushkina NI, Vanyushin BF (noviembre de 1977). "La 2-aminoadenina es una adenina que sustituye a una base en el ADN del cianófago S-2L". Nature . 270 (5635): 369–70. Bibcode :1977Natur.270..369K. doi :10.1038/270369a0. PMID 413053. S2CID 4177449.
- ^ Johnson SC, Sherrill CB, Marshall DJ, Moser MJ, Prudent JR (2004). "Un tercer par de bases para la reacción en cadena de la polimerasa: inserción de isoC e isoG". Nucleic Acids Research . 32 (6): 1937–41. doi :10.1093/nar/gkh522. PMC 390373 . PMID 15051811.
- ^ Taniguchi Y, Kool ET (julio de 2007). "Isósteros no polares de bases de ADN dañadas: imitación eficaz de las propiedades mutagénicas de las 8-oxopurinas". Journal of the American Chemical Society . 129 (28): 8836–44. doi :10.1021/ja071970q. PMID 17592846.
- ^ Hwang GT, Romesberg FE (noviembre de 2008). "Repertorio de sustratos no naturales de las ADN polimerasas de las familias A, B y X". Revista de la Sociedad Química Americana . 130 (44): 14872–82. doi :10.1021/ja803833h. PMC 2675700. PMID 18847263 .
- ^ Kimoto M, Mitsui T, Harada Y, Sato A, Yokoyama S, Hirao I (2007). "Sondaje fluorescente de moléculas de ARN mediante un sistema de pares de bases no natural". Nucleic Acids Research . 35 (16): 5360–69. doi :10.1093/nar/gkm508. PMC 2018647 . PMID 17693436.
- ^ Atwell, Shane; Meggers, Eric; Spraggon, Glen; Schultz, Peter G. (diciembre de 2001). "Estructura de un par de bases mediado por cobre en el ADN". Revista de la Sociedad Química Estadounidense . 123 (49): 12364–12367. doi :10.1021/ja011822e. ISSN 0002-7863. PMID 11734038.
- ^ Liu H, Gao J, Lynch SR, Saito YD, Maynard L, Kool ET (octubre de 2003). "Una hélice genética de cuatro bases pareadas con tamaño expandido". Science . 302 (5646): 868–71. Bibcode :2003Sci...302..868L. doi :10.1126/science.1088334. PMID 14593180. S2CID 37244007.
- ^ Wettig SD, Lee JS (2003). "Investigación termodinámica del ADN-M: un nuevo complejo de ion metálico-ADN". Journal of Inorganic Biochemistry . 94 (1–2): 94–99. doi :10.1016/S0162-0134(02)00624-4. PMID 12620678.
- ^ Zhang HY, Calzolari A, Di Felice R (agosto de 2005). "Sobre la alineación magnética de iones metálicos en una doble hélice que imita el ADN". The Journal of Physical Chemistry B . 109 (32): 15345–48. doi :10.1021/jp052202t. PMID 16852946.
- ^ Aich P, Skinner RJ, Wettig SD, Steer RP, Lee JS (agosto de 2002). "Comportamiento de cables moleculares de largo alcance en un complejo metálico de ADN". Journal of Biomolecular Structure & Dynamics . 20 (1): 93–98. doi :10.1080/07391102.2002.10506826. PMID 12144356. S2CID 41568646.
- ^ Inteligente GH, Polborn K, Carell T (2005). "Un alto grado de estabilidad de ADN-dúplex Metall-Salen-Basenpaar". Angélica. Química. Int. Ed . 117 (44): 7370–74. Código bibliográfico : 2005AngCh.117.7370C. doi : 10.1002/ange.200501589.
- ^ Buncel E, Boone C, Joly H, Kumar R, Norris AR (1985). "Interacciones entre iones metálicos y biomoléculas. XII. Evidencias de RMN de 1H y 13C de la reacción preferida de la timidina sobre la guanosina en reacciones de intercambio y competencia con mercurio (II) y metilmercurio (II)". Inorg. Biochem . 25 : 61–73. doi :10.1016/0162-0134(85)83009-9.
- ^ Ono A, Togashi H (agosto de 2004). "Sensor basado en oligonucleótidos altamente selectivo para mercurio(II) en soluciones acuosas". Angewandte Chemie . 43 (33): 4300–02. doi :10.1002/anie.200454172. PMID 15368377.
- ^ Meggers E, Holland PL, Tolman WB, Romesberg FE, Schultz PG (2000). "Un nuevo par de bases de ADN mediado por cobre". J. Am. Chem. Soc . 122 (43): 10714–15. doi :10.1021/ja0025806.
- ^ Lee JS, Latimer LJ, Reid RS (1993). "Un cambio conformacional cooperativo en el ADN dúplex inducido por Zn2+ y otros iones metálicos divalentes". Bioquímica y biología celular . 71 (3–4): 162–68. doi :10.1139/o93-026. PMID 8398074.
- ^ Tanaka K, Tengeiji A, Kato T, Toyama N, Shionoya M (febrero de 2003). "Una matriz metálica autoensamblada discreta en ADN artificial". Science . 299 (5610): 1212–13. Bibcode :2003Sci...299.1212T. doi :10.1126/science.1080587. PMID 12595687. S2CID 22413126.
- ^ Malyshev DA, Dhami K, Quach HT, Lavergne T, Ordoukhanian P, Torkamani A, Romesberg FE (julio de 2012). "La replicación eficiente e independiente de la secuencia de ADN que contiene un tercer par de bases establece un alfabeto genético funcional de seis letras". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 109 (30): 12005–10. Bibcode :2012PNAS..10912005M. doi : 10.1073/pnas.1205176109 . PMC 3409741 . PMID 22773812.
- ^ Callaway E (7 de mayo de 2014). "Los científicos crean el primer organismo vivo con ADN 'artificial'". Nature News . Huffington Post . Consultado el 8 de mayo de 2014 .
- ^ ab Fikes BJ (8 de mayo de 2014). "Vida diseñada con código genético expandido". San Diego Union Tribune . Consultado el 8 de mayo de 2014 .
- ^ Sample I (7 de mayo de 2014). «Primeras formas de vida que transmiten ADN artificial diseñado por científicos estadounidenses». The Guardian . Consultado el 8 de mayo de 2014 .
- ^ Pollack A (7 de mayo de 2014). "Los científicos añaden letras al alfabeto del ADN, lo que aumenta la esperanza y el miedo". New York Times . Consultado el 8 de mayo de 2014 .
- ^ Zhang Y, Ptacin JL, Fischer EC, Aerni HR, Caffaro CE, San José K, Feldman AW, Turner CR, Romesberg FE (2017). "Un organismo semisintético que almacena y recupera mayor información genética". Naturaleza . 551 (7682): 644–47. Código Bib :2017Natur.551..644Z. doi : 10.1038/naturaleza24659. PMC 5796663 . PMID 29189780.
- ^ Un microbio "no natural" puede producir proteínas. BBC News . 29 de noviembre de 2017.
- ^ Hirao I, Ohtsuki T, Fujiwara T, Mitsui T, Yokogawa T, Okuni T, Nakayama H, Takio K, Yabuki T, Kigawa T, Kodama K, Yokogawa T, Nishikawa K, Yokoyama S (febrero de 2002). "Un par de bases antinatural para incorporar análogos de aminoácidos en proteínas". Biotecnología de la Naturaleza . 20 (2): 177–82. doi :10.1038/nbt0202-177. PMID 11821864. S2CID 22055476.
- ^ Hirao I, Kimoto M, Mitsui T, Fujiwara T, Kawai R, Sato A, Harada Y, Yokoyama S (septiembre de 2006). "Un sistema de pares de bases hidrofóbico no natural: incorporación específica de sitios de análogos de nucleótidos en ADN y ARN". Nature Methods . 3 (9): 729–35. doi :10.1038/nmeth915. PMID 16929319. S2CID 6494156.
- ^ Kimoto M, Kawai R, Mitsui T, Yokoyama S, Hirao I (febrero de 2009). "Un sistema de pares de bases no naturales para la amplificación por PCR eficiente y la funcionalización de moléculas de ADN". Nucleic Acids Research . 37 (2): e14. doi :10.1093/nar/gkn956. PMC 2632903 . PMID 19073696.
- ^ Yamashige R, Kimoto M, Takezawa Y, Sato A, Mitsui T, Yokoyama S, Hirao I (marzo de 2012). "Sistemas de pares de bases no naturales altamente específicos como tercer par de bases para la amplificación por PCR". Nucleic Acids Research . 40 (6): 2793–806. doi :10.1093/nar/gkr1068. PMC 3315302 . PMID 22121213.
- ^ Kimoto M, Yamashige R, Matsunaga K, Yokoyama S, Hirao I (mayo de 2013). "Generación de aptámeros de ADN de alta afinidad utilizando un alfabeto genético expandido". Nature Biotechnology . 31 (5): 453–57. doi :10.1038/nbt.2556. PMID 23563318. S2CID 23329867.
- ^ Schmidt M. "Xenobiología: una nueva forma de vida como herramienta definitiva de bioseguridad" Bioessays Vol 32(4):322–31
- ^ Herdewijn P, Marlière P (junio de 2009). "Hacia organismos genéticamente modificados seguros a través de la diversificación química de los ácidos nucleicos". Química y biodiversidad . 6 (6): 791–808. doi :10.1002/cbdv.200900083. PMID 19554563. S2CID 8572188.
- ^ Shinkai A, Patel PH, Loeb LA (junio de 2001). "El motivo A del sitio activo conservado de la ADN polimerasa I de Escherichia coli es altamente mutable". The Journal of Biological Chemistry . 276 (22): 18836–42. doi : 10.1074/jbc.M011472200 . PMID 11278911.
- ^ Rackham O, Chin JW (agosto de 2005). "Una red de pares ortogonales de ribosoma y ARNm". Nature Chemical Biology . 1 (3): 159–66. doi :10.1038/nchembio719. PMID 16408021. S2CID 37181098.