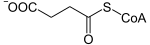
Succinil-CoA
 | |
| Nombres | |
|---|---|
| Nombre IUPAC Ácido 4-[(2-{3-[(2 R )-4-{[1,3-Dihidroxi-1,3-dioxo-3-(3′- O -fosfonoadenosin-5′- O -il)-1λ 5 ,3λ 5 -difosfoxan-1-il]oxi}-3,3-dimetilbutanamido]propanamido}etil)sulfanil]-4-oxobutanoico | |
| Nombre sistemático de la IUPAC Ácido (9R ) -1-[( 2R , 3S , 4R ,5R ) -5-(6-amino-9H - purin-9-il)-4-hidroxi-3-(fosfonooxi)oxolan-2-il]-3,5,9-trihidroxi-8,8-dimetil-3,5,10,14,19-pentaoxo-2,4,6-trioxa-18-tia-11,15-diaza-3λ5,5λ5- difosfadocosan - 22 -oico | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| EBICh | |
| Araña química | |
| Tarjeta informativa de la ECHA | 100.009.163 |
| Malla | Succinil-coenzima+A |
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C25H40N7O19P3S | |
| Masa molar | 867.608 |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La succinil-coenzima A , abreviada como succinil-CoA ( / ˌ s ʌ k s ɪ n əl ˌ k oʊ ˈ eɪ / ) o SucCoA , es un tioéster de ácido succínico y coenzima A.
Fuentes
Es un intermediario importante en el ciclo del ácido cítrico , donde se sintetiza a partir del α-cetoglutarato por la α-cetoglutarato deshidrogenasa mediante descarboxilación . Durante el proceso, se añade la coenzima A.
Con B12 como cofactor enzimático, también se sintetiza a partir de propionil CoA , el ácido graso de número impar, que no puede sufrir beta-oxidación. [1] El propionil-CoA se carboxila a D-metilmalonil-CoA, se isomeriza a L-metilmalonil-CoA y se reorganiza para producir succinil-CoA a través de una enzima dependiente de la vitamina B12 . Si bien el succinil-CoA es un intermediario del ciclo del ácido cítrico , no se puede incorporar fácilmente allí porque no hay consumo neto de succinil-CoA. El succinil-CoA primero se convierte en malato y luego en piruvato, donde luego se transporta a la matriz para ingresar al ciclo del ácido cítrico.
Destino
Se convierte en succinato a través de la liberación hidrolítica de la coenzima A por la succinil-CoA sintetasa (succinato tioquinasa).
Otro destino del succinil-CoA es la síntesis de porfirina , donde el succinil-CoA y la glicina se combinan por acción de la ALA sintasa para formar ácido δ-aminolevulínico (dALA). Este proceso es el paso fundamental en la biosíntesis del porfobilinógeno y, por lo tanto, de la hemoglobina.
Formación
El succinil CoA puede formarse a partir del metilmalonil CoA mediante la utilización de desoxiadenosil-B 12 (desoxiadenosilcobalamina) por la enzima metilmalonil-CoA mutasa . Esta reacción, que requiere vitamina B 12 como cofactor, es importante en el catabolismo de algunos aminoácidos de cadena ramificada, así como de los ácidos grasos de cadena impar.
Mapa interactivo de rutas
Haga clic en los genes, proteínas y metabolitos que aparecen a continuación para acceder a los artículos correspondientes. [§ 1]
- ^ El mapa interactivo de la ruta se puede editar en WikiPathways: "TCACycle_WP78".


