Síndrome del cuerno occipital
| Síndrome del cuerno occipital | |
|---|---|
| Otros nombres | Síndrome de Ehlers-Danlos tipo IX; Cutis Laxa ligado al cromosoma X |
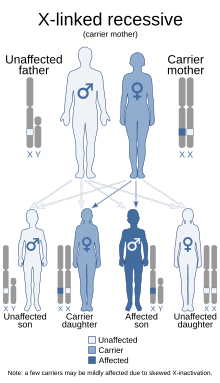 | |
| Esta condición se hereda de forma recesiva ligada al cromosoma X. | |
| Especialidad | Endocrinología |
| Complicaciones | Aneurismas aórticos |
| Medicamento | Inyecciones de droxidopa y cobre-histidina |
El síndrome del cuerno occipital ( OHS ), considerado anteriormente una variante del síndrome de Ehlers-Danlos , [1] es un trastorno mitocondrial y del tejido conectivo recesivo ligado al cromosoma X. Es causado por una deficiencia en el transporte del mineral esencial cobre , asociado con mutaciones en el gen ATP7A . [2] [3]
Se cree que sólo alrededor de 2/3 de los niños con SHO han heredado genéticamente el trastorno; el otro 1/3 no tiene la enfermedad en su historia familiar. Dado que el trastorno es recesivo ligado al cromosoma X, la enfermedad afecta más a los varones. Esto se debe a que no tienen un segundo cromosoma X, a diferencia de las mujeres, por lo que esencialmente carecen de la copia "de respaldo" con la función adecuada. Las mujeres tienen muchas más probabilidades de ser portadoras únicamente. Para que una mujer esté afectada, debe tener dos cromosomas X defectuosos, no sólo uno. [4]
El trastorno se considera una variante más leve de la enfermedad de Menkes . [5]
Signos y síntomas
Se caracteriza por una deficiencia en la excreción biliar de cobre que causa deformaciones en el esqueleto . Estas incluyen proyecciones en la parte posterior del cráneo ( exostosis óseas parasagitales que surgen del hueso occipital , los llamados "cuernos occipitales"), así como deformidades del codo , dislocación de la cabeza radial , extremos laterales en forma de martillo de las clavículas y anomalías de las caderas y la pelvis . [1] El SHO se presenta en la niñez temprana o media. [4] Los niños pueden presentar características como:
- Inteligencia normal/ligeramente retrasada
- Cuello largo, paladar alto y arqueado, cara alargada, frente alta.
- Flacidez de la piel y “doble articulación”
- Hernias inguinales
- Torsión de los vasos sanguíneos
- Divertículos de vejiga
- Disautonomía: incapacidad para regular partes del sistema nervioso.
- Diarrea crónica
- Cabello grueso
- Niveles bajos de ceruloplasmina (9–29 mg/dl) [6]
- Daños al sistema nervioso central [7]
- Pérdida de masa muscular [7]
Causas
El síndrome de OHS es una variante alélica más leve de la enfermedad de Menkes, que se presenta a una edad más tardía y se asocia con una neurodegeneración central mucho menos grave. La naturaleza más leve del síndrome de OHS suele atribuirse a mutaciones de unión de empalme "permeables" que permiten que se procesen correctamente entre el 20 y el 30 % de las transcripciones del ARN mensajero (ARNm) ATP7A. Al igual que en los casos de enfermedad de Menkes, las personas con síndrome de OHS manifiestan anomalías en el tejido conectivo resultantes de una actividad deficiente de la lisil oxidasa, una enzima que requiere cobre y que normalmente desamina la lisina y la hidroxilisina en el primer paso de la formación de enlaces cruzados de colágeno. Estas personas también suelen padecer signos y síntomas disautonómicos incómodos relacionados con una deficiencia parcial de la actividad de la dopamina-β-hidroxilasa (DBH). La DBH, otra enzima dependiente del cobre, normalmente convierte la dopamina en noradrenalina, un neurotransmisor crucial en las neuronas noradrenalinas. Un modelo natural de ratón de OHS, el llamado modelo moteado y manchado, recapitula las anomalías del tejido conectivo, la deficiencia de DBH y el daño leve del SNC observados en humanos. [8]
Diagnóstico
El diagnóstico inicial de la enfermedad de Menkes (EM) y sus variantes más leves, como el síndrome del cuerno occipital, se basa en los síntomas clínicos. Los niveles bajos de cobre y ceruloplasmina en suero respaldan la sospecha clínica de OHS, pero se necesita confirmación bioquímica en cultivo de tejidos. La prueba diagnóstica definitiva es la demostración de un defecto molecular en ATP7A. La demostración de las protuberancias óseas en el occipucio confirmará el diagnóstico, y estas pueden palparse en algunos pacientes. [9]
Tratamiento
Los tratamientos para niños con SHO dependen de la gravedad de su caso. Los niños con SHO a menudo reciben fisioterapia y terapia ocupacional. [4] Es posible que necesiten una sonda de alimentación para complementar la nutrición si no están creciendo lo suficiente. En un intento por mejorar la condición neurológica (convulsiones), se pueden administrar inyecciones de histidina de cobre o cloruro de cobre en las primeras etapas de la vida del niño. Sin embargo, se ha demostrado que las inyecciones de histidina de cobre son ineficaces para tratar las manifestaciones del tejido conectivo del SHO. [10]
Pronóstico
No se conoce la historia natural a largo plazo del síndrome de OHS. [8] Algunos pacientes han muerto repentinamente a los 17 años de edad, [11] mientras que un paciente ha sobrevivido hasta los 57 años. [12] Las causas de muerte incluyen insuficiencia respiratoria, [11] aneurisma aórtico, [13] y hemorragia intracraneal. [14]
Investigación
El NIH y Cyprium Therapeutics están coordinando el desarrollo conjunto de una terapia génica con virus adenoasociados denominada AAV-ATP7A para la enfermedad de Menkes y sus variantes más leves, como el síndrome del cuerno occipital. [15] En marzo de 2017, Cyprium Therapeutics adquirió los derechos comerciales y de desarrollo a nivel mundial del programa Menkes en el NIH/NICHD a través de CRADA y acuerdos de licencia con el NICHD. [16] El AAV-ATP7A todavía se encuentra en la etapa preclínica, aunque ha recibido la designación de medicamento huérfano de la FDA. [ cita requerida ]
Véase también
Referencias
- ^ ab Herencia mendeliana en línea en el hombre (OMIM): 304150
- ^ Scheiber, Ivo; Dringen, Ralf; Mercer, Julian FB (2013). "Capítulo 11. Cobre: efectos de la deficiencia y la sobrecarga". En Astrid Sigel, Helmut Sigel y Roland KO Sigel (ed.). Interrelaciones entre iones metálicos esenciales y enfermedades humanas . Iones metálicos en las ciencias de la vida. Vol. 13. Springer. págs. 359–387. doi :10.1007/978-94-007-7500-8_11. ISBN 978-94-007-7499-5. Número de identificación personal 24470097.
- ^ Tang J, Robertson S, Lem KE, Godwin SC, Kaler SG (noviembre de 2006). "El transporte funcional de cobre explica la preservación neurológica en el síndrome del cuerno occipital". Genética en Medicina . 8 (11): 711–8. doi : 10.1097/01.gim.0000245578.94312.1e . PMID 17108763.
- ^ abc Síndrome de Horn Archivado el 11 de octubre de 2016 en Wayback Machine , 9 de agosto de 2004.
- ^ Kennerson ML, Nicholson GA, Kaler SG, Kowalski B, Mercer JF, Tang J, et al. (marzo de 2010). "Las mutaciones sin sentido en el gen transportador de cobre ATP7A causan neuropatía motora hereditaria distal ligada al cromosoma X". American Journal of Human Genetics . 86 (3): 343–52. doi :10.1016/j.ajhg.2010.01.027. PMC 2833394 . PMID 20170900.
- ^ Kodama H, Murata Y, Kobayashi M (agosto de 1999). "Manifestaciones clínicas y tratamiento de la enfermedad de Menkes y sus variantes". Pediatrics International . 41 (4): 423–9. doi :10.1046/j.1442-200x.1999.01095.x. PMID 10453199. S2CID 21267747.
- ^ ab Wakai S, Ishikawa Y, Nagaoka M, Okabe M, Minami R, Hayakawa T (mayo de 1993). "Afectación del sistema nervioso central y atrofia muscular generalizada en el síndrome del cuerno occipital: síndrome de Ehlers-Danlos tipo IX. El primer caso japonés". Revista de ciencias neurológicas . 116 (1): 1–5. doi :10.1016/0022-510x(93)90081-9. PMID 8099605. S2CID 40538663.
- ^ ab Kaler SG (enero de 2011). "Enfermedades relacionadas con el transporte de cobre relacionadas con ATP7A: conceptos emergentes y tendencias futuras". Nature Reviews. Neurology . 7 (1): 15–29. doi :10.1038/nrneurol.2010.180. PMC 4214867 . PMID 21221114.
- ^ Horn N, Tümer Z (2003). "Capítulo 14: Enfermedad de Menkes y síndrome del cuerno occipital". En Royce PM, Steinmann B (eds.). Tejido conectivo y sus trastornos hereditarios: aspectos moleculares, genéticos y médicos (segunda edición). Wiley-Blackwell. págs. 651–685. doi :10.1002/0471221929.ch14. ISBN 978-0-471-25185-9.
- ^ Kodama H, Fujisawa C, Bhadhprasit W (marzo de 2011). "Patología, características clínicas y tratamientos de los trastornos metabólicos congénitos del cobre: enfoque en los aspectos neurológicos". Cerebro y desarrollo . 33 (3): 243–51. doi :10.1016/j.braindev.2010.10.021. PMID 21112168. S2CID 38032382.
- ^ ab Yasmeen S, Lund K, De Paepe A, De Bie S, Heiberg A, Silva J, Martins M, Skjørringe T, Møller LB (abril de 2014). "Síndrome del cuerno occipital y síndrome de Menkes clásico causado por mutaciones intrónicas profundas, que conducen a la activación del pseudoexón ATP7A". Revista Europea de Genética Humana . 22 (4): 517–21. doi :10.1038/ejhg.2013.191. PMC 3953917 . PMID 24002164.
- ^ Bonati MT, Verde F, Hladnik U, Cattelan P, Campana L, Castronovo C, Ticozzi N, Maderna L, Colombrita C, Papa S, Banfi P, Silani V (diciembre de 2017). "Variante patogénica ATP7A en una familia que presenta un fenotipo de síndrome del cuerno occipital variable". Informes de genética molecular y metabolismo . 13 : 14-17. doi :10.1016/j.ymgmr.2017.07.007. PMC 5522958 . PMID 28761814.
- ^ Quiroga E, Heneghan R (junio de 2015). "Aneurisma aórtico abdominal en un paciente con síndrome del cuerno occipital 2". Journal of Vascular Surgery Cases . 1 (2): 138–140. doi :10.1016/j.jvsc.2015.03.012. PMC 6849971 . PMID 31725130.
- ^ Proud VK, Mussell HG, Kaler SG, Young DW, Percy AK (octubre de 1996). "Variante distintiva de la enfermedad de Menkes con cuernos occipitales: delineación de la historia natural y el fenotipo clínico". American Journal of Medical Genetics . 65 (1): 44–51. doi :10.1002/(SICI)1096-8628(19961002)65:1<44::AID-AJMG7>3.0.CO;2-Y. PMID 8914740.
- ^ Donsante A, Yi L, Zerfas PM, Brinster LR, Sullivan P, Goldstein DS, Prohaska J, Centeno JA, Rushing E, Kaler SG (diciembre de 2011). "La adición del gen ATP7A al plexo coroideo da como resultado un rescate a largo plazo del defecto letal del transporte de cobre en un modelo de ratón con enfermedad de Menkes". Terapia molecular . 19 (12): 2114–23. doi :10.1038/mt.2011.143. PMC 3242653 . PMID 21878905.
- ^ "Presentación corporativa" (PDF) . Cyprium Therapeutics, Inc. Octubre de 2017.
Enlaces externos
- Entrada en GeneReviews/NCBI/NIH/UW sobre trastornos del transporte de cobre relacionados con ATP7A
- Síndrome del cuerno occipital en la Oficina de Enfermedades Raras del NIH