RB-101
 | |
 | |
| Datos clínicos | |
|---|---|
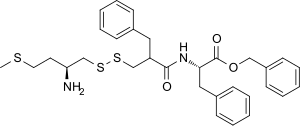
| Otros nombres | RB-101; (2 S )-2-[(2-([(2 S )-2-amino-4-metilsulfanilbutil]disulfanilmetil)-3-fenilpropanoil)amino]-3-fenilpropanoato de fenilmetilo |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Araña química |
|
| UNIVERSIDAD |
|
| Panel de control CompTox ( EPA ) |
|
| Datos químicos y físicos | |
| Fórmula | C31H38N2O3S3 |
| Masa molar | 582,84 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| |
| (verificar) | |
RB-101 es un fármaco que actúa como inhibidor de la encefalinasa , que se utiliza en investigaciones científicas.
El RB-101 es un profármaco que actúa dividiéndose en el enlace disulfuro una vez dentro del cerebro, para formar dos inhibidores enzimáticos selectivos y bloquear ambos tipos de enzimas zinc-metalopeptidasa encefalinasa. Esto inhibe la degradación de los péptidos opioides endógenos conocidos como encefalinas . [1] Estas dos enzimas, la aminopeptidasa N (APN) y la endopeptidasa neutra 24.11 (NEP), son responsables de la degradación de ambos tipos de encefalina que se encuentran naturalmente en el cuerpo, por lo que el RB-101 provoca una acumulación tanto de Met-encefalina como de Leu-encefalina . [2] [3]
Estos péptidos actúan principalmente en el receptor opioide delta , aunque también estimulan el receptor opioide mu hasta cierto punto a través de una interacción mediada por el receptor opioide delta con otro péptido, la colecistoquinina , y los efectos inhibidores de enzimas del RB-101 producen así una estimulación indirecta de ambos subtipos de receptores opioides. [4] Esto hace que el RB-101 sea fuertemente sinérgico con los antagonistas de la colecistoquinina , como la proglumida . [5] [6]
A diferencia del inhibidor de la encefalinasa más comúnmente utilizado , el racecadotril , que solo actúa periféricamente y tiene efectos antidiarreicos , el RB-101 puede ingresar al cerebro y, por lo tanto, produce una variedad de efectos, actuando como analgésico , ansiolítico y antidepresivo . [7] Se cree que las acciones antidepresivas y ansiolíticas están mediadas por el receptor opioide delta, mientras que los efectos analgésicos probablemente resulten de una mezcla de actividad mu y delta. [8] Los estudios en animales sugieren que es probable que el RB-101 también sea útil para aliviar los síntomas de la abstinencia aguda de opioides [9] y en el manejo de la dependencia de opioides. [10] [11] [12]
Una ventaja significativa de inhibir la degradación de los péptidos opioides endógenos en lugar de estimular los receptores opioides con fármacos exógenos es que los niveles de péptidos opioides solo aumentan ligeramente con respecto a los niveles naturales, lo que evita la sobreestimulación y la regulación negativa de los receptores opioides. Esto significa que incluso cuando se usa RB-101 en dosis altas durante períodos prolongados de tiempo, no se desarrolla dependencia del fármaco ni tolerancia a sus efectos analgésicos. [13] [14] En consecuencia, aunque RB-101 puede producir potentes efectos analgésicos a través del sistema opioide, es poco probable que sea adictivo. [15] [16]
A diferencia de los agonistas opioides convencionales, el RB-101 tampoco produjo depresión respiratoria , lo que sugiere que podría ser un fármaco mucho más seguro que los analgésicos opioides tradicionales. [17] El RB-101 también potenció poderosamente los efectos de analgésicos tradicionales como el ibuprofeno y la morfina , lo que sugiere que podría usarse para aumentar la acción de una dosis baja de opioides normales que de otro modo serían ineficaces. [18]
El RB-101 en sí no es activo por vía oral y, por lo tanto, no se ha desarrollado para uso médico en humanos; sin embargo, la modificación del fármaco ha dado lugar a compuestos más nuevos que actúan por vía oral, como el RB-120 y el RB-3007 , que tienen más probabilidades de ser adoptados para uso médico si los ensayos clínicos tienen éxito. [19] [20] [21] [22] [23]
Véase también
Referencias
- ^ Roques BP (abril de 1992). "Peptidomiméticos como agonistas de receptores o inhibidores de peptidasas: un enfoque estructural en el campo de las encefalinas, ANP y CCK". Biopolímeros . 32 (4): 407–10. doi :10.1002/bip.360320417. PMID 1320419.
- ^ Noble F, Soleilhac JM, Soroca-Lucas E, Turcaud S, Fournie-Zaluski MC, Roques BP (abril de 1992). "La inhibición de las enzimas metabolizadoras de encefalina por el primer profármaco inhibidor mixto sistémicamente activo RB 101 induce respuestas analgésicas potentes en ratones y ratas". The Journal of Pharmacology and Experimental Therapeutics . 261 (1): 181–90. PMID 1560364.
- ^ Fournié-Zaluski MC, Coric P, Turcaud S, Lucas E, Noble F, Maldonado R, et al. (Junio de 1992). "Profármaco-inhibidor mixto" como un nuevo enfoque hacia inhibidores sistémicamente activos de enzimas que degradan encefalinas". Journal of Medicinal Chemistry . 35 (13): 2473–81. doi :10.1021/jm00091a016. PMID 1352352.
- ^ Noble F, Smadja C, Roques BP (diciembre de 1994). "El papel de la colecistoquinina endógena en la facilitación de la antinocicepción mediada por mu mediante agonistas delta-opioides". The Journal of Pharmacology and Experimental Therapeutics . 271 (3): 1127–34. PMID 7996417.
- ^ Valverde O, Maldonado R, Fournie-Zaluski MC, Roques BP (julio de 1994). "Los antagonistas de la colecistoquinina B potencian fuertemente la antinocicepción mediada por encefalinas endógenas". Revista de farmacología y terapéutica experimental . 270 (1): 77–88. PMID 8035345.
- ^ Honore P, Buritova J, Fournié-Zaluski MC, Roques BP, Besson JM (abril de 1997). "Los efectos antinociceptivos de RB101, un inhibidor completo de las enzimas catabolizadoras de encefalina, se ven potenciados por un antagonista del receptor de colecistoquinina tipo B, como se revela por la expresión de c-Fos espinal nocivamente evocada en ratas". The Journal of Pharmacology and Experimental Therapeutics . 281 (1): 208–17. PMID 9103499.
- ^ Jutkiewicz EM, Torregrossa MM, Sobczyk-Kojiro K, et al. (febrero de 2006). "Efectos conductuales y neurobiológicos del inhibidor de la encefalinasa RB101 en relación con sus efectos antidepresivos". Revista Europea de Farmacología . 531 (1–3): 151–9. doi :10.1016/j.ejphar.2005.12.002. PMC 1828120 . PMID 16442521.
- ^ Jutkiewicz EM (2007). "Protección de opioides endógenos mediada por RB101: ¿Potencial utilidad terapéutica?" (PDF) . CNS Drug Reviews . 13 (2): 192–205. doi :10.1111/j.1527-3458.2007.00011.x. PMC 6726351 . PMID 17627672.
- ^ Maldonado R, Valverde O, Ducos B, Blommaert AG, Fournie-Zaluski MC, Roques BP (marzo de 1995). "Inhibición de la abstinencia de morfina mediante la asociación de RB 101, un inhibidor del catabolismo de la encefalina, y el antagonista de CCKB PD-134,308". Revista británica de farmacología . 114 (5): 1031–9. doi :10.1111/j.1476-5381.1995.tb13309.x. PMC 1510310 . PMID 7780637.
- ^ Ruiz F, Fournié-Zaluski MC, Roques BP, Maldonado R (septiembre de 1996). "Disminución similar en la abstinencia espontánea de morfina por metadona y RB 101, un inhibidor del catabolismo de las encefalinas". British Journal of Pharmacology . 119 (1): 174–82. doi :10.1111/j.1476-5381.1996.tb15691.x. PMC 1915744 . PMID 8872371.
- ^ Roques BP, Noble F (noviembre de 1996). "Asociación de inhibidores del catabolismo de la encefalina y antagonistas de CCK-B: un uso potencial en el tratamiento del dolor y la adicción a los opioides". Neurochemical Research . 21 (11): 1397–410. doi :10.1007/bf02532381. PMID 8947930.
- ^ Cordonnier L, Sanchez M, Roques BP, Noble F (mayo de 2007). "Bloqueo de la sensibilización conductual inducida por morfina mediante una combinación de amisulprida y RB101, comparación con tratamientos de mantenimiento con opioides clásicos". British Journal of Pharmacology . 151 (1): 94–102. doi :10.1038/sj.bjp.0707195. PMC 2012985 . PMID 17351659.
- ^ Noble F, Turcaud S, Fournié-Zaluski MC, Roques BP (noviembre de 1992). "La administración sistémica repetida del inhibidor mixto de las enzimas que degradan la encefalina, RB101, no induce tolerancia antinociceptiva ni tolerancia cruzada con la morfina". Revista Europea de Farmacología . 223 (1): 83–9. doi :10.1016/0014-2999(92)90821-K. PMID 1478260.
- ^ Noble F, Coric P, Turcaud S, Fournié-Zaluski MC, Roques BP (marzo de 1994). "Evaluación de la dependencia física después de la perfusión continua en la vena yugular de la rata del inhibidor mixto de enzimas que degradan la encefalina, RB 101". Revista Europea de Farmacología . 253 (3): 283–7. doi :10.1016/0014-2999(94)90203-8. PMID 8200422.
- ^ Noble F, Fournié-Zaluski MC, Roques BP (enero de 1993). "A diferencia de la morfina, las encefalinas endógenas protegidas por RB101 no pueden establecer una preferencia de lugar condicionada en ratones". Revista Europea de Farmacología . 230 (2): 139–49. doi :10.1016/0014-2999(93)90796-K. PMID 8422896.
- ^ Stein C, ed. (1999). Opioides en el control del dolor: aspectos básicos y clínicos . Cambridge, Reino Unido: Cambridge University Press. ISBN 978-0521622691.
- ^ Boudinot E, Morin-Surun M, Foutz AS, Fournié-Zaluski M, Roques BP, Denavit-Saubié M (febrero de 2001). "Efectos de los potentes inhibidores de la enzima catabolizante de encefalina analgésica RB101 y kelatorfano sobre la respiración". Pain . 90 (1–2): 7–13. doi :10.1016/S0304-3959(00)00382-1. PMID 11166965.
- ^ Nieto MM, Wilson J, Walker J, Benavides J, Fournié-Zaluski MC, Roques BP, et al. (septiembre de 2001). "Facilitación de la antinocicepción inducida por inhibidores del catabolismo de las encefalinas mediante fármacos de uso clásico en el tratamiento del dolor". Neurofarmacología . 41 (4): 496–506. doi :10.1016/S0028-3908(01)00077-6. PMID 11543770.
- ^ Noble F, Smadja C, Valverde O, Maldonado R, Coric P, Turcaud S, et al. (diciembre de 1997). "Efectos supresores del dolor sobre diversos estímulos nociceptivos (térmicos, químicos, eléctricos e inflamatorios) del primer inhibidor de la enzima metabolizadora de encefalina activo por vía oral, RB 120". Pain . 73 (3): 383–391. doi :10.1016/S0304-3959(97)00125-5. PMID 9469529.
- ^ Le Guen S, Mas Nieto M, Canestrelli C, Chen H, Fournié-Zaluski MC, Cupo A, et al. (julio de 2003). "Manejo del dolor mediante una nueva serie de inhibidores duales de las enzimas que degradan la encefalina: propiedades antinociceptivas de larga duración y potenciación mediante antagonista de CCK2 o metadona". Pain . 104 (1–2): 139–148. doi :10.1016/S0304-3959(02)00486-4. PMID 12855323.
- ^ Le Guen S, Mas Nieto M, Canestrelli C, Chen H, Fournié-Zaluski MC, Cupo A, et al. (julio de 2003). "Manejo del dolor mediante una nueva serie de inhibidores duales de las enzimas que degradan la encefalina: propiedades antinociceptivas de larga duración y potenciación mediante antagonista de CCK2 o metadona". Pain . 104 (1–2): 139–148. doi :10.1016/S0304-3959(02)00486-4. PMID 12855323.
- ^ Noble F, Roques BP (febrero de 2007). "Protección del catabolismo endógeno de las encefalinas como enfoque natural para nuevos fármacos analgésicos y antidepresivos". Opinión de expertos sobre objetivos terapéuticos . 11 (2): 145–159. doi :10.1517/14728222.11.2.145. PMID 17227231.
- ^ Thanawala V, Kadam VJ, Ghosh R (octubre de 2008). "Inhibidores de la encefalinasa: agentes potenciales para el tratamiento del dolor". Current Drug Targets . 9 (10): 887–894. doi :10.2174/138945008785909356. PMID 18855623.
