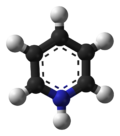
Piridinio
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Piridin-1-io | |||
| Identificadores | |||
| |||
Modelo 3D ( JSmol ) |
| ||
| Araña química | |||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| [ C5H5NH ] + | |||
| Masa molar | 80,110 g·mol −1 | ||
| Acidez (p K a ) | ~5 [1] [2] | ||
| Base conjugada | Piridina | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
El piridinio se refiere al catión [C 5 H 5 NH] + . Es el ácido conjugado de la piridina . Se conocen muchos cationes relacionados que involucran piridinas sustituidas, por ejemplo, picolinas, lutidinas, colidinas. Se preparan tratando la piridina con ácidos. [3]
Como la piridina se utiliza a menudo como base orgánica en reacciones químicas , las sales de piridinio se producen en muchas reacciones ácido-base . Sus sales suelen ser insolubles en el disolvente orgánico, por lo que la precipitación del complejo del grupo saliente de piridinio es una indicación del progreso de la reacción.
Los cationes piridinio son aromáticos , como se determina a través de la regla de Hückel . [4] Son isoelectrónicos con el benceno .
norte-Cationes alquilpiridinio
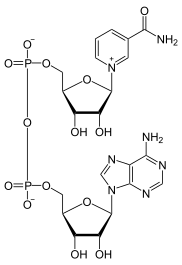
Cuando el protón ácido se reemplaza por alquilo , los compuestos se denominan N -alquilpiridinio. Un representante simple es el N -metilpiridinio ( [C 5 H 5 NCH 3 ] + ). Estos intermediarios de piridinio se han utilizado como electrófilos en la química orgánica sintética para construir congéneres desaromatizados llamados dihidropiridinas, como se demostró en un ejemplo de Smith en 2021. [5] Anteriormente, el mismo grupo de investigación también delineó las reglas que rodean las regioselectividades asociadas con la adición de nucleófilos a electrófilos de piridinio con sustituyentes variables. [6] Desde una perspectiva comercial, un compuesto de piridinio importante es el herbicida paraquat . [7]
Véase también
Referencias
- ^ Linnell, Robert (1960). "Notas: constantes de disociación de piridinas 2-sustituidas". Revista de química orgánica . 25 (2): 290. doi :10.1021/jo01072a623.
- ^ Pearson, Ralph G.; Williams, Forrest V. (1953). "Tasas de ionización de pseudoácidos.1V. Efectos estéricos en la ionización catalizada por bases del nitroetano". Journal of the American Chemical Society . 75 (13): 3073. doi :10.1021/ja01109a008.
- ^ George A. Olah; Michael Watkins (1978). "Fluoraciones con reactivo de fluoruro de polihidrógeno de piridinio: 1-fluoroadamantano". Org. Synth . 58 : 75. doi :10.15227/orgsyn.058.0075.
- ^ "Compuestos aromáticos" (PDF) . Alex Roche, Universidad Rutgers.
- ^ Grigolo, Thiago A.; Subhit, Ariana R.; Smith, Joel M. (3 de septiembre de 2021). "Alquinilación asimétrica regioselectiva de piridinios N-alquilo". Cartas orgánicas . 23 (17): 6703–6708. doi :10.1021/acs.orglett.1c02276. ISSN 1523-7060. PMID 34474575. S2CID 237401193.
- ^ Knight, Brian J.; Tolchin, Zachary A.; Smith, Joel M. (11 de marzo de 2021). "Un modelo predictivo para adiciones a N-alquilpiridinios". Chemical Communications . 57 (21): 2693–2696. doi :10.1039/D1CC00056J. ISSN 1364-548X. PMID 33595047. S2CID 231945207.
- ^ Shimizu, Shinkichi; Watanabe, Nanao; Kataoka, Toshiaki; Shoji, Takayuki; Abe, Nobuyuki; Morishita, Sinji; Ichimura, Hisao (2007). "Piridina y derivados de piridina". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a22_399. ISBN 978-3527306732.