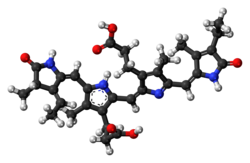
Ficocianobilina
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC Ácido 3-[(2Z,5E)-2-[[3-(2-carboxietil)-5-[(Z)-[(3R,4R)-3-etil-4-metil-5-oxopirrolidin-2-ilideno]metil]-4-metil-1H-pirrol-2-il]metilideno]-5-[(4-etil-3-metil-5-oxopirrol-2-il)metilideno]-4-metilpirrol-3-il]propanoico | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| 4285356 | |
| EBICh |
|
| Araña química |
|
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C33H38N4O6 | |
| Masa molar | 586,69 g/mol |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La ficocianobilina es una ficobilina azul , es decir, un cromóforo tetrapirrólico que se encuentra en las cianobacterias y en los cloroplastos de las algas rojas , las glaucófitas y algunas criptomonas . La ficocianobilina está presente únicamente en las ficobiliproteínas aloficocianina y ficocianina , de las que es el aceptor terminal de energía. Está unida covalentemente a estas ficobiliproteínas mediante un enlace tioéter .
La ficocianobilina (PCB) tiene la capacidad de unirse a la albúmina sérica humana (HSA), proteína que se encuentra principalmente en la sangre de los humanos. Este complejo PCB-HCA beneficia la estructura de la HSA, aumentando la estabilidad térmica de la HSA, así como su capacidad para prevenir la actividad proteolítica de otras proteínas. [1]
Vía biosintética

La vía biosintética de la ficocianobilina comienza con el ácido 5-aminolevulínico (5-ALA). [2] Dos moléculas de 5-ALA experimentan una reacción de condensación catalizada por la porfobilinógeno (PBG) sintasa para producir una molécula de porfobilinógeno (PBG) (no se muestra). [3] Cuatro moléculas de PBG se polimerizan en un tetrapirrol lineal por la porfobilinógeno desaminasa . Esta reacción libera cuatro moléculas de amoníaco en el proceso. La finalización del tetrapirrol es realizada por la uroporfirinógeno III sintasa que da como resultado el uroporfirinógeno III macrocíclico . El uroporfirinógeno III luego se convierte en un hemo por una uroporfirinógeno III descarboxilasa . La molécula de hemo se convierte en biliverdina IX α. Luego, la biliverdina se reduce finalmente a ficocianobilina (PCB) por la ficocianina ferredoxina oxidorreductasa PcyA. La literatura de alrededor de 1989 incluye la fitocromobilina como intermediario en esta conversión final. [2]
Referencias
- ^ Radibratovic M, Minic S, Stanic-Vucinic D, Nikolic M, Milcic M, Cirkovic Velickovic T (13 de diciembre de 2016). "Estabilización de la albúmina sérica humana mediante la unión de ficocianobilina, un cromóforo bioactivo de la alga verdeazulada espirulina: dinámica molecular y estudio experimental". PLOS ONE . 11 (12): e0167973. Bibcode :2016PLoSO..1167973R. doi : 10.1371/journal.pone.0167973 . PMC 5154526 . PMID 27959940.
- ^ ab Brown, Stanley B.; Houghton, Jennifer D.; Vernon, David I. (1990-04-01). "Nuevas tendencias en la biosíntesis de ficobilinas mediante fotobiología. Formación del cromóforo de fitocromo, ficocianina y ficoeritrina". Journal of Photochemistry and Photobiology B: Biology . 5 (1): 3–23. doi :10.1016/1011-1344(90)85002-E. ISSN 1011-1344. PMID 2111391. Archivado desde el original el 2024-03-20 . Consultado el 2023-07-10 .
- ^ Watanabe, Fumio; Yabuta, Yukinori; Bito, Tomohiro (1 de enero de 2014), Atta-ur-Rahman (ed.), Capítulo 11 - Compuestos tetrapirrólicos de cianobacterias, Estudios en química de productos naturales, vol. 42, Elsevier, págs. 341–351, doi :10.1016/b978-0-444-63281-4.00011-2, ISBN 9780444632814, archivado desde el original el 20 de marzo de 2024 , consultado el 8 de junio de 2023
Lectura adicional
- Cole WJ, Chapman DJ, Siegelman HW (1967). "Estructura de la ficocianobilina". Revista de la Sociedad Química Americana . 89 (14): 3643–3645. doi :10.1021/ja00990a055. ISSN 0002-7863.



