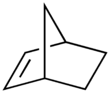
Norborneno
| |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Biciclo[2.2.1]hept-2-eno | |||
| Otros nombres Norbornileno Norcanfeno | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.007.152 | ||
| Número CE |
| ||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C7H10 | |||
| Masa molar | 94,157 g·mol −1 | ||
| Apariencia | Sólido blanco | ||
| Punto de fusión | 42 a 46 °C (108 a 115 °F; 315 a 319 K) | ||
| Punto de ebullición | 96 °C (205 °F; 369 K) | ||
| Peligros | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | -15 °C (5 °F; 258 K) | ||
| Compuestos relacionados | |||
Compuestos relacionados | Anhídrido nádico | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
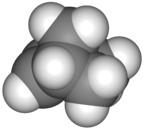
El norborneno , norbornileno o norcanfeno es un hidrocarburo cíclico con puentes muy deformados . Es un sólido blanco con un olor agrio y penetrante. La molécula consta de un anillo de ciclohexeno con un puente de metileno entre los carbonos 1 y 4. La molécula lleva un doble enlace que induce una deformación significativa del anillo y una reactividad significativa.
Producción
El norborneno se obtiene mediante una reacción de Diels-Alder de ciclopentadieno y etileno . Muchos norbornenos sustituidos se pueden preparar de manera similar. [2] [3] Los compuestos bicíclicos relacionados son el norbornadieno , que tiene el mismo esqueleto carbonado pero con dos dobles enlaces, y el norbornano , que se prepara mediante la hidrogenación del norborneno.
Reacciones
El norborneno sufre una reacción de hidratación catalizada por ácido para formar norborneol . Esta reacción fue de gran interés para la elucidación de la controversia sobre los carbocationes no clásicos .
El norborneno se utiliza en la reacción de Catellani y en la activación de meta -C−H mediada por norborneno . [4]
Ciertos norbornenos sustituidos experimentan reacciones de sustitución inusuales debido a la generación del catión 2-norbornilo .
Al ser un eno deformado, los norbornenos reaccionan fácilmente con tioles en la reacción tiol-eno para formar tioéteres . Esto hace que los monómeros funcionalizados con norborneno sean ideales para la polimerización con monómeros basados en tiol para formar redes tiol-eno. [5]
Polinorbornenos
Los norbornenos son monómeros importantes en las polimerizaciones por metátesis con apertura de anillo (ROMP). Normalmente, estas conversiones se efectúan con catalizadores poco definidos. Los polinorbornenos presentan altas temperaturas de transición vítrea y una gran claridad óptica. [6]

Reacción ROMP que produce polinorborneno. Como la mayoría de los procesos comerciales de metátesis de alquenos, esta reacción no utiliza un catalizador molecular bien definido.
Además de ROMP, los monómeros de norborneno también experimentan polimerización por adición de vinilo y es un monómero popular para usar en copolímeros de olefina cíclica .
El polinorborneno se utiliza principalmente en la industria del caucho para antivibración (ferrocarril, construcción, industria), antiimpacto (equipos de protección individual, piezas de calzado, parachoques) y mejora del agarre (neumáticos de juguete, neumáticos de competición, sistemas de transmisión, sistemas de transporte para fotocopiadoras, alimentadores, etc.)
El etilideno norborneno es un monómero relacionado derivado del ciclopentadieno y el butadieno .
Véase también
Referencias
- ^ MSDS de Norborneno
- ^ Binger, Paul; Wedemann, Petra; Brinker, Udo H. "Ciclopropeno: una nueva síntesis simple y su reacción de Diels-Alder con ciclopentadieno". Síntesis orgánicas; Volúmenes recopilados , vol. 10, pág. 231.
- ^ Oda, Masaji; Kawase, Takeshi; Okada, Tomoaki; Enomoto, Tetsuya. "2-ciclohexeno-1,4-diona". Síntesis orgánicas; Volúmenes recopilados , vol. 9, pág. 186.
- ^ Thansandote, Praew; Chong, Eugene; Feldmann, Kai-Oliver; Lautens, Mark (21 de mayo de 2010). "Acoplamiento dominó C−C/C−N catalizado por paladio utilizando una plantilla de norborneno: síntesis de benzomorfolinas sustituidas, fenoxazinas y dihidrodibenzoxazepinas". The Journal of Organic Chemistry . 75 (10): 3495–3498. doi :10.1021/jo100408p. PMID 20423091.
- ^ Hoyle, Charles E.; Bowman, Christopher N. (2010). "Química de clic de tiol-eno". Angewandte Chemie International Edition . 49 (9): 1540–1573. doi :10.1002/anie.200903924.
- ^ Delaude, Lionel; Noels, Alfred F. (2005). "Metátesis". Enciclopedia Kirk-Othmer de Tecnología Química . Weinheim: Wiley-VCH. doi :10.1002/0471238961.metanoel.a01. ISBN 978-0471238966.