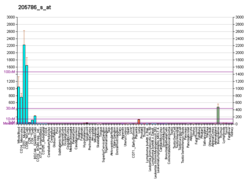
Integrina alfa M
| ITGAM | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificadores | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Alias | ITGAM , CD11B, CR3A, MAC-1, MAC1A, MO1A, SLEB6, subunidad alfa M de la integrina | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificaciones externas | OMIM : 120980; MGI : 96607; HomoloGene : 526; Tarjetas genéticas : ITGAM; OMA :ITGAM - ortólogos | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidatos | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
La integrina alfa M (ITGAM) es una subunidad proteica que forma la molécula heterodímera de integrina alfa-M beta-2 (α M β 2 ), también conocida como antígeno de macrófago-1 (Mac-1) o receptor de complemento 3 (CR3). [5] La ITGAM también se conoce como CR3A y grupo de moléculas de diferenciación 11B (CD11B). La segunda cadena de α M β 2 es la subunidad común de integrina β 2 conocida como CD18 , y la integrina α M β 2 pertenece, por lo tanto, a la subfamilia β 2 (o integrinas leucocitarias). [6]
La α M β 2 se expresa en la superficie de muchos leucocitos involucrados en el sistema inmune innato , incluyendo monocitos , granulocitos , macrófagos y células asesinas naturales [5] y subconjuntos de células T y B. [7] Media la inflamación regulando la adhesión y migración de leucocitos y ha sido implicada en varios procesos inmunes como la fagocitosis , la citotoxicidad mediada por células, la quimiotaxis y la activación celular. [5] Está involucrado en el sistema del complemento debido a su capacidad para unirse al componente 3b del complemento inactivado (iC3b). [8] La subunidad ITGAM (alfa) de la integrina α M β 2 está directamente involucrada en causar la adhesión y propagación de células, pero no puede mediar la migración celular sin la presencia de la subunidad β2 (CD18). [5]
En estudios de asociación del genoma completo, los polimorfismos de un solo nucleótido en ITGAM tuvieron la asociación más fuerte con el lupus eritematoso sistémico , con una razón de probabilidades de 1,65 para el alelo T de rs9888739 y el lupus. [9] [10]
En histopatología , la inmunohistoquímica con anticuerpos contra CD11B se utiliza con frecuencia para identificar macrófagos y microglía .
Función de CD11b
La CD11b, como molécula de integrina en la superficie de los leucocitos , desempeña un papel importante en la migración, adhesión y transmigración celular a través de los vasos sanguíneos , porque puede unirse a componentes de la matriz extracelular y moléculas de adhesión intracelular (ICAM) en la superficie endotelial . Este proceso es importante para el reclutamiento de leucocitos en el sitio de la inflamación . [7]
Además, existen otros procesos importantes en los que interviene CD11b, más precisamente la integrina Mac-1 en su conjunto. Uno de ellos es la fagocitosis de partículas opsonizadas por un componente del complemento iC3b. Dichas partículas opsonizadas podrían ser bacterias , células apoptóticas e incluso complejos inmunes . La unión de CD11b a iC3b conduce a la producción de citocinas antiinflamatorias , por ejemplo, interleucina 10 (IL-10) y factor de crecimiento tumoral beta (TGFβ) . Este proceso es importante para la regulación del entorno inflamatorio. [7] [11]
El CD11b también está involucrado en la diferenciación de los osteoclastos , células de remodelación ósea. Mac-1 se expresa en los progenitores de osteoclastos y parece ser que es parte de una retroalimentación negativa de la osteoclastogénesis. [11] El CD11b también modula otras funciones de los leucocitos, por ejemplo, el estallido oxidativo , la apoptosis , la unión del fibrinógeno , etc. [12]
En los leucocitos circulantes , CD11b se expresa en una conformación cerrada. El cambio a una conformación activa sigue rápidamente después de la estimulación de los receptores tipo Toll (TLR) de los leucocitos . [7] Una vez activado, CD11b puede unirse a sus ligandos con alta afinidad, por ejemplo, unión de moléculas ICAM-1 o ICAM-2 en el endotelio y posterior adhesión. También se sabe que la señalización de CD11b interfiere con la señalización de TLR en la célula. La estimulación de TLR da como resultado la producción de citocinas proinflamatorias , por ejemplo, IL-6 e IL-1β , a través de una serie de fosforilación de factores de señalización, uno de los cuales es el factor de transcripción NF-κB . [13] De hecho, esta señalización se ve afectada negativamente por la señalización de CD11b. En consecuencia, esto conduce a una activación reducida de NF-κB y una menor producción de las citocinas proinflamatorias mencionadas anteriormente . Para concluir, la señalización CD11b regula negativamente la activación de leucocitos después de la estimulación TLR . [7] [12] Además de la señalización TLR , CD11b también regula negativamente la señalización del receptor de células B (BCR) y suprime la activación de las células T y la maduración y función de las células dendríticas . [7]
Importancia terapéutica del CD11b
En cuanto a la función de CD11b, es evidente que desempeña un papel importante en la regulación de las células inmunitarias. Una vez que se altera esta regulación, puede conducir a una mayor susceptibilidad a enfermedades inflamatorias y autoinmunes . Algunos ejemplos serían el lupus eritematoso sistémico (LES) , la nefritis lúpica y ciertos tipos de cáncer . [12] [14]
Lupus eritematoso sistémico
Los estudios de asociación de todo el genoma ayudaron a descubrir 3 polimorfismos de un solo nucleótido (SNP) principales en CD11b, que están asociados con el riesgo de desarrollar LES , enfermedad cardiovascular y nefritis lúpica (una complicación que suele ocurrir junto con el LES ). Estos SNP son: rs1143679 (R77H), rs1143678 (P1146S) y rs1143683 (A858V) y dan como resultado una menor capacidad de CD11b para unirse adecuadamente a ICAM-1 e iC3b , lo que disminuye la adhesión celular y la fagocitosis . También se ha observado en estas mutaciones una capacidad reducida para regular negativamente la producción de citocinas proinflamatorias IL-6 , IL-1β y el factor de necrosis tumoral α (TNFα) después de la estimulación de TLR . [12]
El CD11b desempeña un papel protector durante el LES y la nefritis lúpica debido a sus propiedades antiinflamatorias . La nefritis lúpica se caracteriza por la acumulación de complejos inmunes en los riñones y la infiltración inmune general en los riñones, lo que resulta en daño renal. Esta complicación debilitante del LES está asociada con las mutaciones mencionadas anteriormente en CD11b. Los pacientes con SNP de ITGAM tienen niveles séricos más altos de interferón tipo I (IFN-I) , que es uno de los factores de riesgo para desarrollar LES y nefritis lúpica . Además, los niveles más altos de otras citocinas proinflamatorias IL-6 , IL-1β y TNFα después de la estimulación de TLR , observados en pacientes con SNP de ITGAM , impulsan aún más la inflamación durante esta enfermedad causando más daño tisular y creación de complejos inmunes . [7] [12]
Por lo tanto, el CD11b representa un posible objetivo terapéutico para el tratamiento del LES . De hecho, se han realizado muchos intentos de dirigirse al CD11b. En primer lugar, la terapia basada en anticuerpos que resultó ineficaz en el caso del CD11b. [15] Sin embargo, otras terapias que utilizan pequeños agonistas alostéricos del CD11b parecen ser una herramienta prometedora ya que su activación del CD11b conduce a una regulación de las vías proinflamatorias dependientes de TLR y a la protección contra el daño renal. [12]
Tumores
El CD11b parece ser un potente factor en el manejo de ciertos tipos de tumores sólidos . Aunque hoy en día existen muchas herramientas para el tratamiento del cáncer , múltiples factores de esta enfermedad siguen siendo un tema desafiante. Uno de ellos son las células supresoras derivadas de mieloides (MDSC) y los macrófagos asociados a tumores (TAM) , que son células mieloides presentes en el microambiente tumoral que poseen propiedades supresoras, favoreciendo así el crecimiento tumoral . Los TAM , sin embargo, no solo tienen propiedades promotoras de tumores, sino que también pueden mostrar propiedades inhibidoras de tumores. Depende de su estimulación. Las propiedades inhibidoras de tumores incluyen la producción de citocinas proinflamatorias y la capacidad de presentar antígenos . [14]
El uso de agonistas de CD11b parece ser importante en el tratamiento de tumores . Los agonistas que estabilizan CD11b en su conformación activa dan como resultado una mayor adhesión de CD11b a sus ligandos endoteliales, lo que en consecuencia perjudica la capacidad de migración transendotelial al sitio de la inflamación . Dicha terapia agonista está en desarrollo y un candidato prometedor, GB1275, se encuentra actualmente en su primera fase clínica a principios de 2023. Este agonista de CD11b muestra una transmigración alterada de TAM supresores en el sitio del tumor y una modulación de TAM hacia un fenotipo proinflamatorio con mayor presentación de antígenos y producción de citocinas proinflamatorias . Por lo tanto, promete una mejor inhibición tumoral. [14]
Véase también
Referencias
- ^ abc GRCh38: Lanzamiento de Ensembl 89: ENSG00000169896 – Ensembl , mayo de 2017
- ^ abc GRCm38: Lanzamiento de Ensembl 89: ENSMUSG00000030786 – Ensembl , mayo de 2017
- ^ "Referencia de PubMed humana:". Centro Nacional de Información Biotecnológica, Biblioteca Nacional de Medicina de EE. UU .
- ^ "Referencia de PubMed sobre ratón". Centro Nacional de Información Biotecnológica, Biblioteca Nacional de Medicina de EE. UU .
- ^ abcd Solovjov DA, Pluskota E, Plough EF (enero de 2005). "Distintas funciones de las subunidades alfa y beta en las funciones de la integrina alfaMbeta2". La Revista de Química Biológica . 280 (2): 1336-1345. doi : 10.1074/jbc.M406968200 . PMID 15485828.
- ^ Larson RS, Springer TA (abril de 1990). "Estructura y función de las integrinas leucocitarias". Reseñas inmunológicas . 114 : 181–217. doi :10.1111/j.1600-065X.1990.tb00565.x. PMID 2196220. S2CID 36709941.
- ^ abcdefg Khan SQ, Khan I, Gupta V (15 de marzo de 2018). "La actividad de CD11b modula la patogénesis de la nefritis lúpica". Frontiers in Medicine . 5 : 52. doi : 10.3389/fmed.2018.00052 . PMC 5862812 . PMID 29600248.
- ^ Arnaout MA, Todd RF, Dana N, Melamed J, Schlossman SF, Colten HR (julio de 1983). "Inhibición de la fagocitosis de partículas recubiertas de inmunoglobulina G o C3 del complemento y de la unión de C3bi por anticuerpos monoclonales a una glicoproteína de membrana de monocitos y granulocitos (Mol)". The Journal of Clinical Investigation . 72 (1): 171–179. doi :10.1172/JCI110955. PMC 1129172 . PMID 6874946.
- ^ Crow MK (febrero de 2008). "Colaboración, asociaciones genéticas y lupus eritematoso". The New England Journal of Medicine . 358 (9): 956–961. doi :10.1056/NEJMe0800096. PMID 18204099.
- ^ Hom G, Graham RR, Modrek B, Taylor KE, Ortmann W, Garnier S, et al. (febrero de 2008). "Asociación del lupus eritematoso sistémico con C8orf13-BLK e ITGAM-ITGAX". The New England Journal of Medicine . 358 (9): 900–909. doi : 10.1056/NEJMoa0707865 . PMID 18204098.
- ^ ab Bednarczyk M, Stege H, Grabbe S, Bros M (febrero de 2020). "Integrinas β2: receptores leucocitarios multifuncionales en la salud y la enfermedad". Revista internacional de ciencias moleculares . 21 (4): 1402. doi : 10.3390/ijms21041402 . PMC 7073085 . PMID 32092981.
- ^ abcdef Villanueva V, Li X, Jiménez V, Faridi HM, Gupta V (julio de 2022). "Los agonistas de CD11b ofrecen un nuevo enfoque para el tratamiento de la nefritis lúpica". Investigación Traslacional . 245 : 41–54. doi :10.1016/j.trsl.2022.03.001. PMC 9167730 . PMID 35288363.
- ^ Fitzgerald KA, Kagan JC (marzo de 2020). "Receptores tipo Toll y el control de la inmunidad". Cell . 180 (6): 1044–1066. doi :10.1016/j.cell.2020.02.041. PMC 9358771 . PMID 32164908.
- ^ abc DeNardo DG, Galkin A, Dupont J, Zhou L, Bendell J (agosto de 2021). "GB1275, un modulador de CD11b de primera clase: fundamentos para combinaciones inmunoterapéuticas en tumores sólidos". Revista de inmunoterapia del cáncer . 9 (8): e003005. doi :10.1136/jitc-2021-003005. PMC 8404448 . PMID 34452928.
- ^ Kabanov DS, Grachev SV, Prokhorenko IR (21 de noviembre de 2020). "Anticuerpo monoclonal contra CD14, TLR4 o CD11b: impacto de la especificidad del epítopo y el isotipo en la generación de ROS por granulocitos y monocitos humanos". Medicina oxidativa y longevidad celular . 2020 : 5708692. doi : 10.1155/2020/5708692 . PMC 7700042. PMID 33294123 .
Lectura adicional
- Stewart M, Thiel M, Hogg N (octubre de 1995). "Integrinas leucocitarias". Current Opinion in Cell Biology . 7 (5): 690–696. doi :10.1016/0955-0674(95)80111-1. PMID 8573344.
- Todd RF, Petty HR (mayo de 1997). "Las integrinas beta 2 (CD11/CD18) pueden servir como socios de señalización para otros receptores de leucocitos". The Journal of Laboratory and Clinical Medicine . 129 (5): 492–498. doi :10.1016/S0022-2143(97)90003-2. PMID 9142045.
- Schymeinsky J, Mócsai A, Walzog B (agosto de 2007). "Activación de neutrófilos a través de las integrinas beta2 (CD11/CD18): mecanismos moleculares e implicaciones clínicas". Trombosis y hemostasia . 98 (2): 262–273. doi :10.1160/th07-02-0156. PMID 17721605. S2CID 41094726.
Enlaces externos
- Integrina+alphaM en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
- Cuadro de antígenos CD de ratón
- Cuadro de antígenos CD humanos
- Información de ITGAM con enlaces en Cell Migration Gateway Archivado el 11 de diciembre de 2014 en Wayback Machine