Tomografía de coherencia óptica
This article may be too technical for most readers to understand. (April 2020) |

La tomografía de coherencia óptica ( OCT ) es una técnica de obtención de imágenes que utiliza interferometría con luz de longitud de coherencia corta para obtener una resolución de profundidad a nivel micrométrico y utiliza el escaneo transversal del haz de luz para formar imágenes bidimensionales y tridimensionales a partir de la luz reflejada desde el interior del tejido biológico u otros medios de dispersión . La luz de longitud de coherencia corta se puede obtener utilizando un diodo superluminiscente (SLD) con un ancho de banda espectral amplio o un láser ampliamente sintonizable con un ancho de línea estrecho . La primera demostración de imágenes OCT (in vitro) fue publicada por un equipo del MIT y la Facultad de Medicina de Harvard en un artículo de 1991 en la revista Science . [1] El artículo introdujo el término "OCT" para acreditar su derivación de la reflectometría de dominio de coherencia óptica , en la que la resolución axial se basa en la coherencia temporal . [2] Las primeras demostraciones de imágenes OCT in vivo siguieron rápidamente. [3] [4] [5]
Las primeras patentes estadounidenses sobre OCT del grupo MIT/Harvard describían un sistema OCT de dominio temporal (TD-OCT). [6] [7] Estas patentes fueron licenciadas por Zeiss y formaron la base de las primeras generaciones de productos OCT hasta 2006. Tanno et al. obtuvieron una patente sobre tomografía heterodina óptica (similar a TD-OCT) en Japón en el mismo año. [8]
En la década anterior a la invención de la OCT, se había investigado la interferometría con luz de longitud de coherencia corta para una variedad de aplicaciones. [9] [10] [11] [12] [13] [14] [15] [16] [17] [18] [19] [20] Se propuso el potencial de usar la interferometría para la obtención de imágenes, [20] y se había demostrado la medición del perfil de elevación y el grosor de la retina . [19]
Los primeros sistemas comerciales de OCT clínicos se basaban en la tecnología TD-OCT de escaneo puntual, que producía principalmente imágenes transversales debido a la limitación de velocidad (decenas a miles de escaneos axiales por segundo). La OCT de dominio de Fourier estuvo disponible clínicamente en 2006, lo que permitió una velocidad de adquisición de imágenes mucho mayor (decenas de miles a cientos de miles de escaneos axiales por segundo) sin sacrificar la intensidad de la señal. La mayor velocidad permitió la obtención de imágenes tridimensionales, que se pueden visualizar tanto en vistas frontales como transversales. También se hicieron posibles nuevos contrastes como la angiografía , la elastografía y la optorretinografía al detectar cambios de señal a lo largo del tiempo. Durante las últimas tres décadas, la velocidad de los sistemas comerciales de OCT clínicos aumentó más de 1000 veces, duplicándose cada tres años y rivalizando con la ley de Moore del rendimiento de los chips de computadora. El desarrollo de enfoques de adquisición de imágenes paralelas, como la tecnología de campo lineal y de campo completo, puede permitir que continúe la tendencia de mejora del rendimiento.
La OCT se utiliza más ampliamente en oftalmología , donde ha transformado el diagnóstico y el seguimiento de enfermedades de la retina, enfermedades del nervio óptico y enfermedades de la córnea . Ha mejorado enormemente el tratamiento de las tres principales causas de ceguera ( degeneración macular , retinopatía diabética y glaucoma ), previniendo así la pérdida de visión en muchos pacientes. En 2016, se estimó que la OCT se utilizaba en más de 30 millones de procedimientos de diagnóstico por imágenes al año en todo el mundo. [21]
La angioscopia OCT se utiliza en la evaluación intravascular de placas en la arteria coronaria y para guiar la colocación de stents . [22] Más allá de la oftalmología y la cardiología, también se están desarrollando aplicaciones en otras especialidades médicas como la dermatología , la gastroenterología (endoscopia), la neurología , la oncología y la odontología . [23] [24]
Introducción

La reflectometría interferométrica de tejido biológico, especialmente del ojo humano, utilizando luz de longitud de coherencia corta (también conocida como parcialmente coherente, de baja coherencia, de banda ancha, de amplio espectro o luz blanca) fue investigada en paralelo por múltiples grupos en todo el mundo desde la década de 1980. En 1991, David Huang, entonces estudiante en el laboratorio James Fujimoto en el Instituto Tecnológico de Massachusetts , trabajando con Eric Swanson en el Laboratorio Lincoln del MIT y colegas de la Facultad de Medicina de Harvard, demostró con éxito la obtención de imágenes y denominó a la nueva modalidad de obtención de imágenes "tomografía de coherencia óptica". [25] Desde entonces, la OCT con resolución micrométrica y capacidades de obtención de imágenes transversales se ha convertido en una importante técnica de obtención de imágenes biomédicas que ha mejorado continuamente en rendimiento técnico y rango de aplicaciones. La mejora en la tasa de adquisición de imágenes es particularmente espectacular, comenzando con la tasa de repetición de escaneo axial original de 0,8 Hz [1] hasta los sistemas OCT clínicos comerciales actuales que funcionan a varios cientos de kHz y prototipos de laboratorio a múltiples MHz. El rango de aplicaciones se ha expandido desde la oftalmología hasta la cardiología y otras especialidades médicas. Por su papel en la invención de la OCT, Fujimoto, Huang y Swanson recibieron el Premio de Investigación Médica Clínica Lasker-DeBakey 2023 y la Medalla Nacional de Tecnología e Innovación. [26] Estos avances se han analizado en artículos escritos para lectores generales [21] científicos [27] y médicos [28] .
Es particularmente adecuado para aplicaciones oftálmicas y otras imágenes de tejidos que requieren una resolución micrométrica y una profundidad de penetración milimétrica. [29] La OCT también se ha utilizado para varios proyectos de conservación de arte , donde se utiliza para analizar diferentes capas en una pintura. La OCT tiene ventajas interesantes sobre otros sistemas de imágenes médicas. La ecografía médica , la resonancia magnética (IRM), la microscopía confocal y la OCT son diferentes para las imágenes de tejidos morfológicos: mientras que las dos primeras tienen capacidad de imágenes de cuerpo completo pero de baja resolución (normalmente una fracción de milímetro), la tercera puede proporcionar imágenes con resoluciones muy por debajo de 1 micrómetro (es decir, subcelular), entre 0 y 100 micrómetros de profundidad, y la cuarta puede sondear hasta 500 micrómetros, pero con una resolución menor (es decir, arquitectónica) (alrededor de 10 micrómetros en lateral y unos pocos micrómetros de profundidad en oftalmología, por ejemplo, y 20 micrómetros en lateral en endoscopia). [30] [31]
La OCT se basa en la interferometría de baja coherencia. [32] [33] [34] En la interferometría convencional con longitud de coherencia larga (es decir, interferometría láser), la interferencia de la luz se produce a una distancia de metros. En la OCT, esta interferencia se acorta a una distancia de micrómetros, debido al uso de fuentes de luz de ancho de banda amplio (es decir, fuentes que emiten luz en un amplio rango de frecuencias). La luz con anchos de banda amplios se puede generar utilizando diodos superluminiscentes o láseres con pulsos extremadamente cortos ( láseres de femtosegundos ). La luz blanca es un ejemplo de una fuente de banda ancha con menor potencia.
La luz en un sistema OCT se divide en dos brazos: un brazo de muestra (que contiene el elemento de interés) y un brazo de referencia (normalmente un espejo). La combinación de la luz reflejada del brazo de muestra y la luz de referencia del brazo de referencia da lugar a un patrón de interferencia, pero solo si la luz de ambos brazos ha recorrido la "misma" distancia óptica ("misma" significa una diferencia de menos de una longitud de coherencia). Al escanear el espejo en el brazo de referencia, se puede obtener un perfil de reflectividad de la muestra (esto es OCT de dominio temporal). Las áreas de la muestra que reflejan mucha luz crearán una mayor interferencia que las áreas que no lo hacen. Cualquier luz que esté fuera de la corta longitud de coherencia no interferirá. [35] Este perfil de reflectividad, llamado A-scan , contiene información sobre las dimensiones espaciales y la ubicación de las estructuras dentro del elemento de interés. Se puede lograr un tomograma transversal ( B-scan ) combinando lateralmente una serie de estos escaneos de profundidad axial (A-scan). La obtención de imágenes en face a una profundidad adquirida es posible según el motor de imágenes utilizado.
Explicación para el profano
This section needs additional citations for verification. (March 2019) |


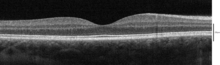
La tomografía de coherencia óptica (OCT) es una técnica para obtener imágenes subsuperficiales de materiales translúcidos u opacos con una resolución equivalente a la de un microscopio de baja potencia. Es en realidad una "ultrasonido óptico" que capta imágenes de los reflejos del interior del tejido para proporcionar imágenes transversales. [36]
La OCT ha atraído el interés de la comunidad médica porque proporciona imágenes de la morfología del tejido con una resolución mucho mayor (menos de 10 μm axialmente y menos de 20 μm lateralmente [37] ) que otras modalidades de imágenes como la resonancia magnética o la ecografía.
Los principales beneficios de la OCT son:
- Imágenes en vivo del subsuelo con una resolución casi microscópica
- Imágenes instantáneas y directas de la morfología del tejido.
- Sin preparación de la muestra ni del sujeto, sin contacto
- Sin radiación ionizante
La OCT ofrece una alta resolución porque se basa en la luz, en lugar del sonido o la radiofrecuencia. Se dirige un haz óptico al tejido y se recoge la pequeña parte de esta luz que se refleja directamente desde las características del subsuelo. Tenga en cuenta que la mayor parte de la luz se dispersa en ángulos grandes. En la obtención de imágenes convencionales, esta luz dispersa de forma difusa contribuye a crear un fondo que oscurece la imagen. Sin embargo, en la OCT se utiliza una técnica denominada interferometría para registrar la longitud del recorrido óptico de los fotones recibidos, lo que permite rechazar la mayoría de los fotones que se dispersan varias veces antes de ser detectados. Por tanto, la OCT puede generar imágenes 3D claras de muestras gruesas al rechazar la señal de fondo mientras recoge la luz reflejada directamente desde las superficies de interés.
Dentro de la gama de técnicas de imágenes tridimensionales no invasivas que se han introducido en la comunidad de investigación médica, la OCT como técnica de eco es similar a la ecografía . Otras técnicas de imágenes médicas como la tomografía axial computarizada, la resonancia magnética o la tomografía por emisión de positrones no utilizan el principio de ecolocalización. [38]
La técnica se limita a la obtención de imágenes de 1 a 2 mm por debajo de la superficie del tejido biológico, porque a mayores profundidades la proporción de luz que escapa sin dispersarse es demasiado pequeña para ser detectada. No se requiere una preparación especial de una muestra biológica y las imágenes se pueden obtener "sin contacto" o a través de una ventana o membrana transparente.
La salida láser de los instrumentos utilizados es baja (infrarrojo cercano o luz visible segura para los ojos [39] ) y, por lo tanto, no es probable que se produzcan daños en la muestra.
Teoría
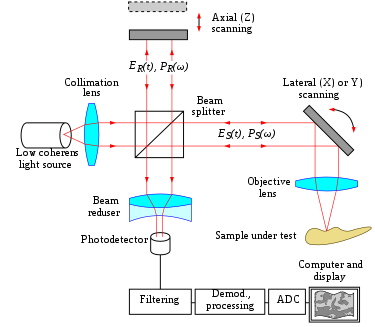
El principio de la OCT es la interferometría de luz blanca o de baja coherencia. La configuración óptica consiste típicamente en un interferómetro (Fig. 1, típicamente de tipo Michelson ) con una fuente de luz de ancho de banda amplio y baja coherencia. La luz se divide y se recombina a partir de los brazos de referencia y de muestra, respectivamente.
Dominio del tiempo
En la OCT en el dominio del tiempo, la longitud del recorrido del brazo de referencia varía en el tiempo (el espejo de referencia se traslada longitudinalmente). Una propiedad de la interferometría de baja coherencia es que la interferencia, es decir, la serie de franjas oscuras y brillantes, solo se logra cuando la diferencia de recorrido se encuentra dentro de la longitud de coherencia de la fuente de luz. Esta interferencia se denomina autocorrelación en un interferómetro simétrico (ambos brazos tienen la misma reflectividad) o correlación cruzada en el caso común. La envolvente de esta modulación cambia a medida que varía la diferencia de longitud del recorrido, donde el pico de la envolvente corresponde a la coincidencia de longitud del recorrido.
La interferencia de dos haces de luz parcialmente coherentes se puede expresar en términos de la intensidad de la fuente, , como
donde representa la relación de división del haz del interferómetro, y se denomina grado complejo de coherencia, es decir, la envolvente de interferencia y la portadora dependen del barrido del brazo de referencia o del retardo de tiempo , y cuya recuperación es de interés en la OCT. Debido al efecto de compuerta de coherencia de la OCT, el grado complejo de coherencia se representa como una función gaussiana expresada como [34]
donde representa el ancho espectral de la fuente en el dominio de frecuencia óptica, y es la frecuencia óptica central de la fuente. En la ecuación (2), la envolvente gaussiana es modulada en amplitud por una portadora óptica. El pico de esta envolvente representa la ubicación de la microestructura de la muestra bajo prueba, con una amplitud que depende de la reflectividad de la superficie. La portadora óptica se debe al efecto Doppler resultante del escaneo de un brazo del interferómetro, y la frecuencia de esta modulación está controlada por la velocidad de escaneo. Por lo tanto, trasladar un brazo del interferómetro tiene dos funciones; el escaneo de profundidad y una portadora óptica desplazada por Doppler se logran mediante la variación de la longitud del camino. En OCT, la portadora óptica desplazada por Doppler tiene una frecuencia expresada como
donde es la frecuencia óptica central de la fuente, es la velocidad de exploración de la variación de la longitud del camino y es la velocidad de la luz.
Las resoluciones axial y lateral de la OCT están desacopladas entre sí; la primera es equivalente a la longitud de coherencia de la fuente de luz y la segunda es una función de la óptica. La resolución axial de la OCT se define como
donde y son respectivamente la longitud de onda central y el ancho espectral de la fuente de luz. [40]
Dominio de Fourier

La OCT de dominio de Fourier (o dominio de frecuencia) (FD-OCT) tiene ventajas en cuanto a velocidad y relación señal-ruido (SNR) sobre la OCT de dominio temporal (TD-OCT) y se ha convertido en el estándar en la industria desde 2006. La idea de usar modulación de frecuencia y detección coherente para obtener información de alcance ya se demostró en la reflectometría de dominio de frecuencia óptica [9] y radar láser [14] en la década de 1980, aunque la resolución de distancia y el alcance eran mucho mayores que los de la OCT. Hay dos tipos de FD-OCT: OCT de fuente barrida (SS-OCT) y OCT de dominio espectral (SD-OCT), ambos adquieren interferogramas espectrales que luego se transforman en Fourier para obtener un escaneo axial de amplitud de reflectancia versus profundidad. En SS-OCT, el interferograma espectral se adquiere secuencialmente ajustando la longitud de onda de una fuente de luz láser. SD-OCT adquiere interferogramas espectrales simultáneamente en un espectrómetro. El grupo del MIT describió una implementación de SS-OCT ya en 1994. [6] [41] Un grupo con base en la Universidad de Viena describió la medición de la distancia intraocular utilizando interferometría basada en láser sintonizable y espectrómetro ya en 1995. [42] [43] La obtención de imágenes SD-OCT se demostró por primera vez tanto in vitro como in vivo mediante una colaboración entre el grupo de Viena y un grupo con base en la Universidad Nicolás Copérnico en una serie de artículos entre 2000 y 2002. [44] [45] [46] La ventaja de la relación señal/ruido de la FD-OCT sobre la TD-OCT se demostró por primera vez en imágenes oculares [47] y fue analizada posteriormente por varios grupos de investigadores en 2003. [48] [49] [50]
OCT de dominio espectral
La OCT de dominio espectral (OCT de dominio de frecuencia codificada espacialmente) extrae información espectral distribuyendo diferentes frecuencias ópticas en una franja de detector (CCD de matriz lineal o CMOS) a través de un elemento dispersivo (ver Figura 4). De este modo, la información de la exploración de profundidad completa se puede adquirir en una sola exposición. Sin embargo, la gran ventaja de la relación señal-ruido de la OCT de dominio espectral se reduce debido al rango dinámico más bajo de los detectores de franja con respecto a los diodos fotosensibles individuales, lo que da como resultado una ventaja de relación señal-ruido de ~10 dB a velocidades mucho más altas. Sin embargo, esto no es un gran problema cuando se trabaja a 1300 nm, ya que el rango dinámico no es un problema grave en este rango de longitud de onda. [40]
Las desventajas de esta tecnología se encuentran en una fuerte caída de la relación señal-ruido, que es proporcional a la distancia desde el retardo cero y una reducción de tipo sinc de la sensibilidad dependiente de la profundidad debido al ancho de línea de detección limitado. (Un píxel detecta una porción cuasi-rectangular de un rango de frecuencia óptica en lugar de una sola frecuencia, la transformada de Fourier conduce al comportamiento sinc(z)). Además, los elementos dispersivos en el detector espectroscópico normalmente no distribuyen la luz de manera uniforme en frecuencia en el detector, sino que en su mayoría tienen una dependencia inversa. Por lo tanto, la señal debe ser remuestreada antes del procesamiento, lo que no puede ocuparse de la diferencia en el ancho de banda local (píxel por píxel), lo que resulta en una reducción adicional de la calidad de la señal. Sin embargo, la caída no es un problema grave con el desarrollo de CCD de nueva generación o matriz de fotodiodos con un mayor número de píxeles.
La detección heterodina mediante matriz sintética ofrece otro enfoque para este problema sin necesidad de alta dispersión.
OCT de fuente barrida
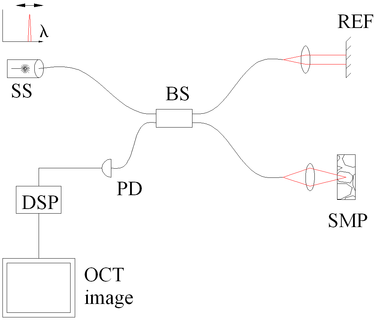
La OCT de fuente barrida (OCT de dominio de frecuencia codificada en el tiempo) intenta combinar algunas de las ventajas de la TD estándar y la OCT de dominio espectral. Aquí los componentes espectrales no se codifican por separación espacial, sino que se codifican en el tiempo. El espectro se filtra o se genera en pasos de frecuencia sucesivos individuales y se reconstruye antes de la transformación de Fourier. Al acomodar una fuente de luz de escaneo de frecuencia (es decir, láser de escaneo de frecuencia), la configuración óptica (ver Figura 3) se vuelve más simple que la OCT de dominio espectral, pero el problema del escaneo se traslada esencialmente del brazo de referencia TD-OCT a la fuente de luz OCT de fuente barrida. Aquí la ventaja radica en la tecnología de detección de alta relación señal-ruido probada, mientras que las fuentes láser de barrido logran anchos de banda instantáneos muy pequeños (anchos de línea) a frecuencias muy altas (20–200 kHz). Las desventajas son las no linealidades en la longitud de onda (especialmente a altas frecuencias de escaneo), el ensanchamiento del ancho de línea a altas frecuencias y una alta sensibilidad a los movimientos de la geometría de escaneo o la muestra (por debajo del rango de nanómetros dentro de los pasos de frecuencia sucesivos).
Esquemas de escaneo
Al enfocar el haz de luz hacia un punto de la superficie de la muestra en prueba y recombinar la luz reflejada con la de referencia, se obtendrá un interferograma con información de la muestra correspondiente a un único escaneo A (solo eje Z). El escaneo de la muestra se puede lograr escaneando la muestra con la luz o moviendo la muestra en prueba. Un escaneo lineal producirá un conjunto de datos bidimensionales correspondientes a una imagen transversal (escaneo de ejes XZ), mientras que un escaneo de área logra un conjunto de datos tridimensionales correspondientes a una imagen volumétrica (escaneo de ejes XYZ).
Punto único
Los sistemas basados en OCT de dominio temporal de punto único, confocal o de punto volante deben escanear la muestra en dos dimensiones laterales y reconstruir una imagen tridimensional utilizando información de profundidad obtenida mediante control de coherencia a través de un brazo de referencia de escaneo axial (Fig. 2). El escaneo lateral bidimensional se ha implementado electromecánicamente moviendo la muestra [51] utilizando una platina de traslación y utilizando un novedoso escáner de sistema microelectromecánico. [52]
OCT de línea-campo
La tomografía de coherencia óptica confocal de campo lineal (LC-OCT) es una técnica de obtención de imágenes basada en el principio de OCT de dominio temporal con iluminación de línea utilizando un láser de banda ancha y detección de línea utilizando una cámara de escaneo de línea. [53] La LC-OCT produce escaneos B en tiempo real a partir de múltiples escaneos A adquiridos en paralelo. También se pueden obtener imágenes en face y tridimensionales escaneando la línea de iluminación lateralmente. [54] [55] El enfoque se ajusta continuamente durante el escaneo de la profundidad de la muestra, utilizando un objetivo de microscopio de alta apertura numérica (NA) para obtener imágenes con alta resolución lateral. Al utilizar un láser supercontinuo como fuente de luz, se logra una resolución espacial cuasi isotrópica de ~ 1 μm a una longitud de onda central de ~ 800 nm. Por otro lado, la iluminación y detección de línea, combinadas con el uso de un objetivo de microscopio de alta NA, producen una compuerta confocal que evita que la cámara detecte la mayor parte de la luz dispersa que no contribuye a la señal. Esta puerta confocal, que está ausente en la técnica OCT de campo completo, le da a la LC-OCT una ventaja en términos de sensibilidad de detección y penetración en medios de alta dispersión como los tejidos de la piel. [56] Hasta ahora, esta técnica se ha utilizado principalmente para imágenes de la piel en los campos de la dermatología [57] [58] [59 ] [60] [61] [62] y la cosmetología. [63]
OCT de campo completo

En 1998, el equipo de Claude Boccara desarrolló un método de obtención de imágenes para la OCT temporal [64] , con una adquisición de imágenes sin escaneo del haz. En esta técnica, denominada OCT de campo completo (FF-OCT), a diferencia de otras técnicas de OCT que adquieren secciones transversales de la muestra, las imágenes son aquí "en-face", es decir, como imágenes de microscopía clásica: ortogonales al haz de luz de iluminación. [65]
Más precisamente, las imágenes interferométricas se crean mediante un interferómetro de Michelson donde la diferencia de longitud de trayectoria varía mediante un componente eléctrico rápido (generalmente un espejo piezoeléctrico en el brazo de referencia). Estas imágenes adquiridas por una cámara CCD se combinan en el postratamiento (o en línea) mediante el método de interferometría de desplazamiento de fase, donde generalmente se adquieren 2 o 4 imágenes por período de modulación, según el algoritmo utilizado. [66] [67] Más recientemente, se desarrollaron enfoques que permiten la obtención rápida de imágenes de un solo disparo para capturar simultáneamente múltiples imágenes desplazadas de fase necesarias para la reconstrucción, utilizando una sola cámara. [68] La OCM de dominio temporal de disparo único está limitada solo por la velocidad de cuadros de la cámara y la iluminación disponible.
Las imágenes tomográficas "en-face" se producen así mediante una iluminación de campo amplio, asegurada por la configuración Linnik del interferómetro de Michelson, donde se utiliza un objetivo de microscopio en ambos brazos. Además, si bien la coherencia temporal de la fuente debe permanecer baja como en la OCT clásica (es decir, un espectro amplio), la coherencia espacial también debe ser baja para evitar interferencias parásitas (es decir, una fuente con un tamaño grande). [69]
Aplicaciones seleccionadas
La tomografía de coherencia óptica es una técnica de imágenes médicas establecida y se utiliza en varias especialidades médicas, incluidas la oftalmología y la cardiología, y se utiliza ampliamente en aplicaciones de investigación científica básica.
Oftalmología
La OCT ocular (u oftálmica) es ampliamente utilizada por oftalmólogos y optometristas para obtener imágenes de alta resolución de la retina y el segmento anterior . Debido a la capacidad de la OCT para mostrar secciones transversales de capas de tejido con resolución micrométrica, la OCT proporciona un método sencillo para evaluar la organización celular , la integridad de los fotorreceptores, [70] [71] [72] [73] y el espesor axonal en el glaucoma , [74] la degeneración macular , [75] el edema macular diabético , [76] la esclerosis múltiple , [77] la neuritis óptica, [78] y otras enfermedades oculares o patologías sistémicas que presentan signos oculares. [79] Además, los oftalmólogos aprovechan la OCT para evaluar la salud vascular de la retina a través de una técnica llamada angiografía OCT (OCTA). [80] En la cirugía oftalmológica , especialmente la cirugía de retina, se puede montar una OCT en el microscopio. Este sistema se denomina OCT intraoperatoria (iOCT) y proporciona apoyo durante la cirugía con beneficios clínicos. [81] [82] [83] La OCT sensible a la polarización se aplicó recientemente en la retina humana para determinar las propiedades de polarización óptica de las paredes de los vasos cerca del nervio óptico. [84]
Las imágenes de retina con PS-OCT demostraron cómo se podía cuantificar in vivo el grosor y la birrefringencia del tejido de la pared de los vasos sanguíneos de sujetos sanos. [85] Posteriormente, se aplicó la PS-OCT a pacientes con diabetes y sujetos sanos de la misma edad, y mostró un aumento de casi el 100 % en la birrefringencia de la pared de los vasos debido a la diabetes, sin un cambio significativo en el grosor de la pared de los vasos. [86] Sin embargo, en pacientes con hipertensión, el grosor de la pared de los vasos de la retina aumentó un 60 %, mientras que la birrefringencia de la pared de los vasos disminuyó un 20 %, en promedio. [87] Las grandes diferencias medidas en sujetos sanos y pacientes sugieren que las mediciones de retina con PS-OCT podrían usarse como una herramienta de detección de hipertensión y diabetes. [86] [87] [88]
La OCT se puede utilizar para medir el grosor de la capa de fibras nerviosas de la retina (RNFL) . [89]
Cardiología
En el ámbito de la cardiología, la OCT se utiliza para obtener imágenes de las arterias coronarias y visualizar la morfología y la microestructura de la luz de la pared vascular con una resolución aproximadamente 10 veces mayor que otras modalidades existentes, como las ecografías intravasculares y la angiografía por rayos X ( tomografía de coherencia óptica intracoronaria ). Para este tipo de aplicación, se utilizan catéteres de fibra óptica de 1 mm de diámetro o menos para acceder a la luz de la arteria a través de intervenciones semiinvasivas, como las intervenciones coronarias percutáneas .
La primera demostración de OCT endoscópica fue reportada en 1997 por investigadores del laboratorio de Fujimoto en el Instituto Tecnológico de Massachusetts. [90] El primer catéter y sistema de imágenes TD-OCT fue comercializado por LightLab Imaging, Inc., una empresa con sede en Massachusetts en 2006. El primer estudio de imágenes FD-OCT fue reportado por el Hospital General de Massachusetts en 2008. [91] La FD-OCT intracoronaria fue introducida por primera vez en el mercado en 2009 por LightLab Imaging, Inc. [92] seguida por Terumo Corporation en 2012 y por Gentuity LLC en 2020. [93] La mayor velocidad de adquisición de FD-OCT permitió la adopción generalizada de esta tecnología de imágenes para imágenes de la arteria coronaria. Se estima que se realizan más de 100.000 casos de imágenes coronarias FD-OCT al año y que el mercado está aumentando aproximadamente un 20% cada año. [94]
Otros avances de la OCT intracoronaria incluyen la combinación con otras modalidades de imágenes ópticas para la obtención de imágenes multimodales. La OCT intravascular se ha combinado con la obtención de imágenes moleculares por fluorescencia en el infrarrojo cercano (NIRF) para mejorar su capacidad de detectar información molecular/funcional y morfológica tisular simultáneamente. [95] [96] De manera similar, se ha implementado la combinación con la espectroscopia de infrarrojo cercano (NIRS). [97]
Neurovascular
La OCT endoscópica/intravascular se ha desarrollado aún más para su uso en aplicaciones neurovasculares, incluida la obtención de imágenes para guiar el tratamiento endovascular del accidente cerebrovascular isquémico y los aneurismas cerebrales. [98]
Las investigaciones clínicas iniciales con los catéteres de OCT coronaria existentes se han limitado a la anatomía intracraneal proximal de pacientes con tortuosidad limitada, ya que la tecnología de OCT coronaria no fue diseñada para la cerebrovasculatura tortuosa que se encuentra en el cerebro. Sin embargo, a pesar de estas limitaciones, demostró el potencial de la OCT para la obtención de imágenes de enfermedades neurovasculares. [99] En 2020 se propuso un diseño de catéter de obtención de imágenes de OCT intravascular adaptado para su uso en anatomía neurovascular tortuosa. [100] En 2024 se informó de un primer estudio en humanos utilizando OCT neuro endovascular ( n OCT) . [101] [102]
Oncología
La OCT endoscópica se ha aplicado a la detección y diagnóstico de cáncer y lesiones precancerosas , como el esófago de Barrett y la displasia esofágica . [103] [104] [105]
Dermatología
El primer uso de OCT en dermatología se remonta a 1997. [106] Desde entonces, la OCT se ha aplicado al diagnóstico de varias lesiones cutáneas, incluidos los carcinomas. [107] [108] [109] Sin embargo, el diagnóstico de melanoma mediante OCT convencional es difícil, especialmente debido a la resolución insuficiente de las imágenes. [110] Las técnicas emergentes de OCT de alta resolución, como la LC-OCT, tienen el potencial de mejorar el proceso de diagnóstico clínico, permitiendo la detección temprana de tumores malignos de la piel, incluido el melanoma, y una reducción en el número de escisiones quirúrgicas de lesiones benignas. [111] Otras áreas de aplicación prometedoras incluyen la obtención de imágenes de lesiones en las que las escisiones son peligrosas o imposibles y la guía de intervenciones quirúrgicas mediante la identificación de los márgenes del tumor.
Odontología
Los investigadores de la Universidad Médica y Dental de Tokio pudieron detectar lesiones de manchas blancas en el esmalte alrededor y debajo de los brackets de ortodoncia utilizando OCT de fuente barrida. [112]
Aplicaciones de investigación
Los investigadores han utilizado OCT para producir imágenes detalladas de cerebros de ratones, a través de una "ventana" hecha de zirconia que ha sido modificada para ser transparente e implantada en el cráneo. [113] [114] La tomografía de coherencia óptica también es aplicable y se utiliza cada vez más en aplicaciones industriales , como pruebas no destructivas (NDT), mediciones de espesor de materiales, [115] y en particular obleas delgadas de silicio [116] [117] y mediciones de espesor de obleas de semiconductores compuestos [118] [119] caracterización de rugosidad superficial, imágenes de superficie y sección transversal [120] [121] y mediciones de pérdida de volumen. [122] Los sistemas OCT con retroalimentación se pueden utilizar para controlar procesos de fabricación. Con adquisición de datos de alta velocidad, [123] y resolución submicrónica, la OCT es adaptable para funcionar tanto en línea como fuera de línea. [124] Debido al alto volumen de píldoras producidas, un campo de aplicación interesante es en la industria farmacéutica para controlar el recubrimiento de tabletas. [125] Los sistemas OCT basados en fibra son particularmente adaptables a entornos industriales. [126] Estos pueden acceder y escanear interiores de espacios difíciles de alcanzar, [127] y pueden operar en entornos hostiles, ya sean radiactivos, criogénicos o muy calientes. [128] Actualmente se están desarrollando nuevas tecnologías de diagnóstico e imagenología biomédica óptica para resolver problemas en biología y medicina. [129] A partir de 2014, se han realizado intentos de utilizar la tomografía de coherencia óptica para identificar conductos radiculares en los dientes, específicamente conductos en los molares superiores, sin embargo, no hay diferencia con los métodos actuales de microscopio operatorio dental. [130] [131] [ fuente no primaria necesaria ] La investigación realizada en 2015 tuvo éxito en la utilización de un teléfono inteligente como plataforma OCT, aunque aún queda mucho trabajo por hacer antes de que dicha plataforma sea comercialmente viable. [132] Los circuitos integrados fotónicos pueden ser una opción prometedora para la OCT miniaturizada. De manera similar a los circuitos integrados, las técnicas de fabricación basadas en silicio se pueden utilizar para producir sistemas fotónicos miniaturizados. Recientemente se ha informado sobre la primera obtención de imágenes de retina humana in vivo. [133] En la microfabricación 3D , la OCT permite realizar pruebas no destructivas e inspecciones en tiempo real durante la fabricación aditiva. Su obtención de imágenes de alta resolución detecta defectos, caracteriza las propiedades del material y garantiza la integridad de las geometrías internas sin dañar la pieza. [122]
Véase también
- Interferometría de baja coherencia con resolución angular
- Fotón balístico
- Microscopía confocal
- Tomografía de coherencia óptica de doble eje
- Interferometría
- Tomografía de coherencia óptica intracoronaria
- Microsistemas Leica
- Imágenes médicas
- Tecnologías Novacam
- Detección heterodina óptica
- Tomografía de proyección óptica
- Tomografía de coherencia óptica espectroscópica
- Tomografía de terahercios
- Tomografía
Referencias
- ^ ab Huang D, Swanson EA, Lin CP, Schuman JS, Stinson WG, Chang W, et al. (noviembre de 1991). "Tomografía de coherencia óptica". Science . 254 (5035): 1178–1181. Bibcode :1991Sci...254.1178H. doi :10.1126/science.1957169. PMC 4638169 . PMID 1957169.
- ^ Youngquist RC, Carr S, Davies DE (marzo de 1987). "Reflectometría en el dominio de la coherencia óptica: una nueva técnica de evaluación óptica". Optics Letters . 12 (3): 158–160. Bibcode :1987OptL...12..158Y. doi :10.1364/ol.12.000158. PMID 19738824.
- ^ Izatt JA, Hee MR, Huang D, Fujimoto JG, Swanson EA, Lin CP, Shuman JS, Puliafito CA (24 de junio de 1993). Parel JM, Ren Q (eds.). "Diagnóstico oftálmico mediante tomografía de coherencia óptica". Ophthalmic Technologies III . 1877 . SPIE: 136–144. Código Bibliográfico :1993SPIE.1877..136I. doi :10.1117/12.147520. S2CID 121094027.
- ^ Swanson EA, Izatt JA, Hee MR, Huang D, Lin CP, Schuman JS, et al. (noviembre de 1993). "Obtención de imágenes retinianas in vivo mediante tomografía de coherencia óptica". Optics Letters . 18 (21): 1864–1866. Bibcode :1993OptL...18.1864S. doi :10.1364/ol.18.001864. PMID 19829430.
- ^ Fercher AF, Hitzenberger CK, Drexler W, Kamp G, Sattmann H (julio de 1993). "Tomografía de coherencia óptica in vivo". American Journal of Ophthalmology . 116 (1): 113–114. doi :10.1016/s0002-9394(14)71762-3. PMID 8328536.
- ^ ab US 5321501A, Swanson EA, Huang D, Fujimoto JG, Puliafito CA, "Método y aparato para la formación de imágenes ópticas con medios para controlar el rango longitudinal de la muestra", publicado el 14 de junio de 1994
- ^ US 5459570A, Swanson EA, Huang D, Fujimoto JG, Puliafito CA, "Método y aparato para realizar mediciones ópticas", publicado el 17 de octubre de 1995
- ^ JA 2010042, Tanno N, Ichikawa T, Saeki A, "Medición de la reflexión de las ondas de luz", publicado en 1990
- ^ ab Eickhoff W, Ulrich R (noviembre de 1981). "Reflectometría del dominio de frecuencia óptica en fibra monomodo". Applied Physics Letters . 39 (9): 693–695. Bibcode :1981ApPhL..39..693E. doi :10.1063/1.92872. ISSN 0003-6951.
- ^ Gillard CW, Buholz NE (1983). "Progreso en interferometría de distancia absoluta". Ingeniería óptica . 22 (3): 348–353. Código Bibliográfico :1983OptEn..22..348G. doi :10.1117/12.7973117. ISSN 0091-3286.
- ^ Fercher AF, Roth E (15 de septiembre de 1986). "Interferometría láser oftálmica". En Mueller GJ (ed.). Instrumentación óptica para aplicaciones láser biomédicas . Vol. 0658. SPIE. pág. 48. Bibcode :1986SPIE..658...48F. doi :10.1117/12.938523. S2CID 122883903.
{{cite book}}:|journal=ignorado ( ayuda ) - ^ Youngquist RC, Carr S, Davies DE (marzo de 1987). "Reflectometría en el dominio de la coherencia óptica: una nueva técnica de evaluación óptica". Optics Letters . 12 (3): 158–160. Bibcode :1987OptL...12..158Y. doi :10.1364/OL.12.000158. PMID 19738824.
- ^ Takada K, Yokohama I, Chida K, Noda J (mayo de 1987). "Nuevo sistema de medición para la localización de fallos en dispositivos de guía de ondas ópticas basado en una técnica interferométrica". Applied Optics . 26 (9): 1603–1606. Bibcode :1987ApOpt..26.1603T. doi :10.1364/AO.26.001603. PMID 20454375.
- ^ ab Kachelmyer AL (18 de febrero de 1989). Becherer RJ (ed.). "Formas de onda de imágenes de rango-Doppler y diseño de receptor". Laser Radar III . 0999 . SPIE: 138–161. Código Bibliográfico :1989SPIE..999..138K. doi :10.1117/12.960231. S2CID 110631959.
- ^ Fercher AF, Mengedoht K, Werner W (marzo de 1988). "Medición de la longitud del ojo mediante interferometría con luz parcialmente coherente". Optics Letters . 13 (3): 186–188. Bibcode :1988OptL...13..186F. doi :10.1364/OL.13.000186. PMID 19742022.
- ^ Gilgen HH, Novak RP, Salathe RP, Hodel W, Beaud P (1989). "Reflectometría óptica submilimétrica". Revista de tecnología de ondas de luz . 7 (8): 1225–1233. Código Bibliográfico :1989JLwT....7.1225G. doi :10.1109/50.32387. ISSN 1558-2213.
- ^ Huang D, Wang J, Lin CP, Puliafito CA, Fujimoto JG (1991). "Determinación de la resolución micrométrica de la cámara anterior de la córnea mediante reflectometría óptica". Láseres en cirugía y medicina . 11 (5): 419–425. doi :10.1002/lsm.1900110506. PMID 1816476. S2CID 19888483.
- ^ Hitzenberger CK (marzo de 1991). "Medición óptica de la longitud axial del ojo mediante interferometría láser Doppler". Oftalmología investigativa y ciencia visual . 32 (3): 616–624. PMID 2001935.
- ^ ab Fercher AF (12-16 de agosto de 1990). "Interferometría oftálmica". En von Bally G, Khanna S (eds.). Actas de la Conferencia Internacional sobre Óptica en Ciencias de la Vida . Garmisch-Partenkirchen, Alemania. págs. 221-228. ISBN 0-444-89860-3.
- ^ por Shinji Chiba; Naohiro Tanno (1991). Tomografía heterodina óptica por retrodispersión . XIV Simposio sobre detección láser (en japonés).
- ^ ab Fujimoto J, Swanson E (julio de 2016). "El desarrollo, la comercialización y el impacto de la tomografía de coherencia óptica". Oftalmología de investigación y ciencia visual . 57 (9): OCT1–OCT13. doi :10.1167/iovs.16-19963. PMC 4968928 . PMID 27409459.
- ^ Pereira, Vitor M.; Lylyk, Pedro; Cancelliere, Nicole; Lylyk, Pedro N.; Lylyk, Ivan; Anagnostakou, Vania; Bleise, Carlos; Nishi, Hidehisa; Epshtein, Mark; King, Robert M.; Shazeeb, Mohammed Salman; Puri, Ajit S.; Liang, Conrad W.; Hanel, Ricardo A.; Spears, Julian (15 de mayo de 2024). "Microscopía volumétrica de arterias cerebrales con una sonda de imágenes de tomografía de coherencia óptica miniaturizada". Science Translational Medicine . 16 (747): eadl4497. doi :10.1126/scitranslmed.adl4497. ISSN 1946-6234. PMID 38748771.
- ^ Wijns W, Shite J, Jones MR, Lee SW, Price MJ, Fabbiocchi F, et al. (diciembre de 2015). "La tomografía de coherencia óptica durante la intervención coronaria percutánea afecta la toma de decisiones del médico: estudio ILUMIEN I". Revista Europea del Corazón . 36 (47): 3346–3355. doi :10.1093/eurheartj/ehv367. PMC 4677272 . PMID 26242713.
- ^ Fujimoto J, Huang D (julio de 2016). "Prólogo: 25 años de tomografía de coherencia óptica". Oftalmología de investigación y ciencia visual . 57 (9): OCTi–OCTii. doi : 10.1167/iovs.16-20269 . hdl : 1721.1/105905 . PMID 27419359.
- ^ Huang D, Swanson EA, Lin CP, Schuman JS, Stinson WG, Chang W, et al. (noviembre de 1991). "Tomografía de coherencia óptica". Science . 254 (5035): 1178–1181. Bibcode :1991Sci...254.1178H. doi :10.1126/science.1957169. PMC 4638169 . PMID 1957169.
- ^ Davis TH (septiembre de 2023). "Preguntas y respuestas con James G. Fujimoto, David Huang y Eric A. Swanson: ganadores del premio de investigación médica clínica Lasker~DeBakey 2023". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 120 (39): e2313883120. Bibcode :2023PNAS..12013883D. doi :10.1073/pnas.2313883120. PMC 10523481 . PMID 37732757.
- ^ Nathans J (septiembre de 2023). "Ver para creer: el desarrollo de la tomografía de coherencia óptica". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 120 (39): e2311129120. Bibcode :2023PNAS..12011129N. doi :10.1073/pnas.2311129120. PMC 10523475 . PMID 37732756.
- ^ Toth CA (octubre de 2023). Phimister EG (ed.). "Tomografía de coherencia óptica y cuidado ocular". The New England Journal of Medicine . 389 (16): 1526–1529. doi :10.1056/NEJMcibr2307733. PMID 37732605. S2CID 262085371.
- ^ Zysk AM, Nguyen FT, Oldenburg AL, Marks DL, Boppart SA (2007). "Tomografía de coherencia óptica: una revisión del desarrollo clínico desde el laboratorio hasta la cabecera del paciente". Journal of Biomedical Optics . 12 (5): 051403. Bibcode :2007JBO....12e1403Z. doi : 10.1117/1.2793736 . PMID 17994864. S2CID 20621284.
- ^ Drexler W, Morgner U, Ghanta RK, Kärtner FX, Schuman JS, Fujimoto JG (abril de 2001). "Tomografía de coherencia óptica oftálmica de ultraalta resolución". Nature Medicine . 7 (4): 502–507. doi :10.1038/86589. PMC 1950821 . PMID 11283681.
- ^ Kaufman SC, Musch DC, Belin MW, Cohen EJ, Meisler DM, Reinhart WJ, et al. (febrero de 2004). "Microscopía confocal: un informe de la Academia Estadounidense de Oftalmología". Oftalmología . 111 (2): 396–406. doi :10.1016/j.ophtha.2003.12.002. PMID 15019397.
- ^ Riederer SJ (2000). "Desarrollo técnico actual de la resonancia magnética". Revista IEEE de Ingeniería en Medicina y Biología . 19 (5): 34–41. doi :10.1109/51.870229. PMID 11016028.
- ^ M. Born; E. Wolf (2000). Principios de óptica: teoría electromagnética de la propagación, interferencia y difracción de la luz . Cambridge University Press. ISBN 978-0-521-78449-8.
- ^ ab Fercher AF, Mengedoht K, Werner W (marzo de 1988). "Medición de la longitud del ojo mediante interferometría con luz parcialmente coherente". Optics Letters . 13 (3): 186–188. Bibcode :1988OptL...13..186F. doi :10.1364/OL.13.000186. PMID 19742022.
- ^ Fujimoto JG, Pitris C, Boppart SA, Brezinski ME (2000). "Tomografía de coherencia óptica: una tecnología emergente para la obtención de imágenes biomédicas y la biopsia óptica". Neoplasia . 2 (1–2): 9–25. doi :10.1038/sj.neo.7900071. PMC 1531864 . PMID 10933065.
- ^ Michelessi M, Lucenteforte E, Oddone F, Brazzelli M, Parravano M, Franchi S, et al. (noviembre de 2015). "Imágenes de la cabeza del nervio óptico y de la capa de fibras para el diagnóstico del glaucoma". Base de datos Cochrane de revisiones sistemáticas . 2015 (11): CD008803. doi :10.1002/14651858.CD008803.pub2. PMC 4732281. PMID 26618332.
- ^ Drexler W, Morgner U, Kärtner FX, Pitris C, Boppart SA, Li XD, et al. (septiembre de 1999). "Tomografía de coherencia óptica de ultraalta resolución in vivo". Optics Letters . 24 (17). OSA: 1221–1223. doi :10.1364/bio.1999.jwa2. PMID 18073990.
- ^ "La tomografía de coherencia óptica ofrece una mejor resolución que una resonancia magnética y ayuda a diagnosticar enfermedades de la retina y la córnea y el glaucoma, parte II". mastereyeassociates.com . mastereyeassociates. 13 de junio de 2017 . Consultado el 13 de junio de 2017 .
- ^ Shu X, Beckmann L, Zhang H (diciembre de 2017). "Tomografía de coherencia óptica con luz visible: una revisión". Revista de óptica biomédica . 22 (12). spiedigitallibrary: 1–14. Bibcode :2017JBO....22l1707S. doi :10.1117/1.JBO.22.12.121707. PMC 5745673 . PMID 29218923.
- ^ ab Garg A (2014). OCT de segmento anterior y posterior: tecnología actual y aplicaciones futuras, 1.ª edición .
- ^ Chinn SR, Swanson EA, Fujimoto JG (marzo de 1997). "Tomografía de coherencia óptica utilizando una fuente óptica sintonizable en frecuencia". Optics Letters . 22 (5): 340–342. Bibcode :1997OptL...22..340C. doi :10.1364/OL.22.000340. PMID 18183195.
- ^ Fercher AF, Hitzenberger CK, Kamp G, El-Zaiat SY (15 de mayo de 1995). "Medición de distancias intraoculares mediante interferometría espectral de retrodispersión". Optics Communications . 117 (1): 43–48. Bibcode :1995OptCo.117...43F. doi :10.1016/0030-4018(95)00119-S. ISSN 0030-4018.
- ^ Lexer F, Hitzenberger CK, Fercher AF, Kulhavy M (septiembre de 1997). "Interferometría de distancias intraoculares con ajuste de longitud de onda". Applied Optics . 36 (25): 6548–6553. Bibcode :1997ApOpt..36.6548L. doi :10.1364/AO.36.006548. PMID 18259516.
- ^ Leitgeb R, Wojtkowski M, Kowalczyk A, Hitzenberger CK, Sticker M, Fercher AF (junio de 2000). "Medición espectral de la absorción mediante tomografía de coherencia óptica espectroscópica en el dominio de la frecuencia". Optics Letters . 25 (11): 820–822. Bibcode :2000OptL...25..820L. doi :10.1364/OL.25.000820. PMID 18064195.
- ^ Wojtkowski M, Leitgeb R, Kowalczyk A, Bajraszewski T, Fercher AF (julio de 2002). "Obtención de imágenes de retina humana in vivo mediante tomografía de coherencia óptica de dominio de Fourier". Journal of Biomedical Optics . 7 (3): 457–463. Bibcode :2002JBO.....7..457W. doi : 10.1117/1.1482379 . PMID 12175297. S2CID 40844236.
- ^ Wojtkowski M, Kowalczyk A, Leitgeb R, Fercher AF (agosto de 2002). "Técnica de tomografía de coherencia óptica espectral compleja de rango completo en la obtención de imágenes oculares". Optics Letters . 27 (16): 1415–1417. Bibcode :2002OptL...27.1415W. doi :10.1364/OL.27.001415. PMID 18026464.
- ^ Wojtkowski M, Bajraszewski T, Targowski P, Kowalczyk A (abril de 2003). "Imágenes in vivo en tiempo real mediante tomografía de coherencia óptica espectral de alta velocidad". Optics Letters . 28 (19): 1745–1747. Bibcode :2003OptL...28.1745W. doi :10.1364/OL.28.001745. PMID 14514087.
- ^ Leitgeb R, Hitzenberger C, Fercher A (abril de 2003). "Rendimiento de la tomografía de coherencia óptica en el dominio de Fourier frente a la del dominio del tiempo". Optics Express . 11 (8): 889–894. Bibcode :2003OExpr..11..889L. doi : 10.1364/oe.11.000889 . PMID 19461802.
- ^ Choma M, Sarunic M, Yang C, Izatt J (septiembre de 2003). "Ventaja de sensibilidad de la tomografía de coherencia óptica de dominio de Fourier y fuente barrida". Optics Express . 11 (18): 2183–2189. Bibcode :2003OExpr..11.2183C. doi : 10.1364/oe.11.002183 . PMID 19466106.
- ^ de Boer JF, Cense B, Park BH, Pierce MC, Tearney GJ, Bouma BE (noviembre de 2003). "Mejora de la relación señal-ruido en la tomografía de coherencia óptica en el dominio espectral en comparación con la tomografía de coherencia óptica en el dominio del tiempo". Optics Letters . 28 (21): 2067–2069. Bibcode :2003OptL...28.2067D. doi :10.1364/ol.28.002067. PMID 14587817.
- ^ Fercher AF, Hitzenberger CK, Kamp G, El-Zaiat SY (1995). "Medición de distancias intraoculares mediante interferometría espectral de retrodispersión". Optics Communications . 117 (1–2): 43–48. Bibcode :1995OptCo.117...43F. doi :10.1016/0030-4018(95)00119-S.
- ^ Yeow JT, Yang VX, Chahwan A, Gordon ML, Qi B, Vitkin IA, Wilson BC, Goldenberg AA (2005). "Escáner 2-D micromaquinado para tomografía de coherencia óptica 3-D". Sensores y actuadores A: Física . 117 (2): 331–340. Código Bibliográfico :2005SeAcA.117..331Y. doi :10.1016/j.sna.2004.06.021.
- ^ Dubois A, Levecq O, Azimani H, Davis A, Ogien J, Siret D, Barut A (diciembre de 2018). "Tomografía de coherencia óptica confocal de dominio temporal de campo lineal con enfoque dinámico". Optics Express . 26 (26): 33534–33542. Bibcode :2018OExpr..2633534D. doi : 10.1364/OE.26.033534 . PMID 30650800.
- ^ Ogien J, Levecq O, Azimani H, Dubois A (marzo de 2020). "Tomografía de coherencia óptica confocal de campo lineal de modo dual para imágenes de cortes verticales y horizontales de ultraalta resolución de la piel humana in vivo". Biomedical Optics Express . 11 (3): 1327–1335. doi :10.1364/BOE.385303. PMC 7075601 . PMID 32206413.
- ^ Ogien J, Daures A, Cazalas M, Perrot JL, Dubois A (diciembre de 2020). "Tomografía de coherencia óptica confocal de campo lineal para imágenes tridimensionales de la piel". Frontiers of Optoelectronics . 13 (4): 381–392. doi :10.1007/s12200-020-1096-x. PMC 9743950 . PMID 36641566. S2CID 234456595.
- ^ Chen Y, Huang SW, Aguirre AD, Fujimoto JG (julio de 2007). "Microscopía de coherencia óptica de barrido lineal de alta resolución". Optics Letters . 32 (14): 1971–1973. Bibcode :2007OptL...32.1971C. doi :10.1364/OL.32.001971. PMID 17632613.
- ^ Dubois A, Levecq O, Azimani H, Siret D, Barut A, Suppa M, et al. (octubre de 2018). "Tomografía de coherencia óptica confocal de campo lineal para la obtención de imágenes no invasivas de alta resolución de tumores cutáneos". Journal of Biomedical Optics . 23 (10): 1–9. Bibcode :2018JBO....23j6007D. doi : 10.1117/1.JBO.23.10.106007 . PMID 30353716.
- ^ Ruini C, Schuh S, Gust C, Kendziora B, Frommherz L, French LE, et al. (diciembre de 2021). "Tomografía de coherencia óptica de campo lineal: diagnóstico in vivo de subtipos de carcinoma basocelular en comparación con la histopatología". Dermatología clínica y experimental . 46 (8): 1471–1481. doi : 10.1111/ced.14762 . hdl : 11380/1259112 . PMID 34047380. S2CID 235232158.
- ^ Suppa M, Fontaine M, Dejonckheere G, Cinotti E, Yélamos O, Diet G, et al. (mayo de 2021). "Tomografía de coherencia óptica confocal de campo lineal del carcinoma basocelular: un estudio descriptivo". Revista de la Academia Europea de Dermatología y Venereología . 35 (5): 1099–1110. doi :10.1111/jdv.17078. PMID 33398911. S2CID 230583854.
- ^ Cinotti E, Tognetti L, Cartocci A, Lamberti A, Gherbassi S, Orte Cano C, et al. (diciembre de 2021). "Tomografía de coherencia óptica confocal de campo lineal para queratosis actínica y carcinoma de células escamosas: un estudio descriptivo". Dermatología clínica y experimental . 46 (8): 1530–1541. doi :10.1111/ced.14801. PMC 9293459 . PMID 34115900. S2CID 235411841.
- ^ Lenoir C, Cinotti E, Tognetti L, Orte Cano C, Diet G, Miyamoto M, et al. (diciembre de 2021). "Tomografía de coherencia óptica confocal de campo lineal de queratosis actínica: una serie de casos". Revista de la Academia Europea de Dermatología y Venereología . 35 (12): e900–e902. doi :10.1111/jdv.17548. PMID 34310768. S2CID 236452537.
- ^ Ruini C, Schuh S, Gust C, Kendziora B, Frommherz L, French LE, et al. (diciembre de 2021). "Tomografía de coherencia óptica confocal de campo lineal para el diagnóstico in vivo en tiempo real de diferentes estadios del cáncer de piel de queratinocitos: un estudio preliminar". Revista de la Academia Europea de Dermatología y Venereología . 35 (12): 2388–2397. doi : 10.1111/jdv.17603 . hdl : 11380/1259110 . PMID 34415646. S2CID 237241412.
- ^ Pedrazzani M, Breugnot J, Rouaud-Tinguely P, Cazalas M, Davis A, Bordes S, et al. (mayo de 2020). "Comparación de imágenes de tomografía de coherencia óptica confocal de campo lineal con secciones histológicas: validación de un nuevo método para la cuantificación in vivo y no invasiva del espesor de la dermis superficial". Investigación y tecnología de la piel . 26 (3): 398–404. doi :10.1111/srt.12815. PMID 31799766. S2CID 208622348.
- ^ Beaurepaire E, Boccara AC, Lebec M, Blanchot L, Saint-Jalmes H (febrero de 1998). "Microscopía de coherencia óptica de campo completo". Optics Letters . 23 (4): 244–246. Bibcode :1998OptL...23..244B. doi :10.1364/ol.23.000244. PMID 18084473.
- ^ Dubois A, Boccara C (octubre de 2006). «[OCT de campo completo]». Médecine/Sciences (en francés). 22 (10): 859–864. doi : 10.1051/medsci/20062210859 . PMID 17026940.
- ^ Dubois A, Moneron G, Boccara C (2006). "Tomografía de coherencia óptica de campo completo con luz térmica en la región de longitud de onda de 1,2 micrones" (PDF) . Optics Communications . 266 (2): 738–743. Bibcode :2006OptCo.266..738D. doi :10.1016/j.optcom.2006.05.016. S2CID 120323507.
- ^ Boccara AC, Harms F, Latrive A (2013). "OCT de campo completo: una herramienta no invasiva para el diagnóstico y la selección de tejidos". Sala de prensa del SPIE . doi :10.1117/2.1201306.004933. S2CID 123478275.
- ^ Žurauskas M, Iyer RR, Boppart SA (febrero de 2021). "Microscopía de coherencia óptica de campo completo con desplazamiento simultáneo de 4 fases". Biomedical Optics Express . 12 (2). The Optical Society: 981–992. doi : 10.1364/boe.417183 . PMC 7901320 . PMID 33680554.
- ^ Boccara AC, Dubois A (2013). "Tomografía de coherencia óptica". Óptica en instrumentos . págs. 101–123. doi :10.1002/9781118574386.ch3. ISBN 9781118574386.
- ^ "El ABC de la OCT". Revista de Optometría .
- ^ Sherman J (junio de 2009). "La línea de integridad de los fotorreceptores se une a la capa de fibras nerviosas como clave para el diagnóstico clínico". Optometría . 80 (6): 277–278. doi :10.1016/j.optm.2008.12.006. PMID 19465337.
- ^ "Capas externas de la retina como predictores de pérdida de visión". Revista de Oftalmología .
- ^ Cuenca N, Ortuño-Lizarán I, Pinilla I (marzo de 2018). "Caracterización celular de OCT y bandas externas de la retina mediante marcadores inmunohistoquímicos específicos e implicaciones clínicas". Oftalmología . 125 (3): 407–422. doi :10.1016/j.ophtha.2017.09.016. hdl : 10045/74474 . PMID 29037595.
- ^ Grewal DS, Tanna AP (marzo de 2013). "Diagnóstico del glaucoma y detección de la progresión del glaucoma mediante tomografía de coherencia óptica de dominio espectral". Current Opinion in Ophthalmology . 24 (2): 150–161. doi :10.1097/ICU.0b013e32835d9e27. PMID 23328662. S2CID 39039199.
- ^ Keane PA, Patel PJ, Liakopoulos S, Heussen FM, Sadda SR, Tufail A (septiembre de 2012). "Evaluación de la degeneración macular relacionada con la edad con tomografía de coherencia óptica". Encuesta de Oftalmología . 57 (5): 389–414. doi :10.1016/j.survophthal.2012.01.006. PMID 22898648.
- ^ Virgili G, Menchini F, Casazza G, Hogg R, Das RR, Wang X, Michelessi M (enero de 2015). "Tomografía de coherencia óptica (OCT) para la detección del edema macular en pacientes con retinopatía diabética". Base de datos Cochrane de revisiones sistemáticas . 1 (4): CD008081. doi :10.1002/14651858.CD008081.pub3. PMC 4438571 . PMID 25564068.
- ^ Dörr J, Wernecke KD, Bock M, Gaede G, Wuerfel JT, Pfueller CF, et al. (abril de 2011). "Asociación del daño retiniano y macular con la atrofia cerebral en la esclerosis múltiple". PLOS ONE . 6 (4): e18132. Bibcode :2011PLoSO...618132D. doi : 10.1371/journal.pone.0018132 . PMC 3072966 . PMID 21494659.

- ^ Petzold A, Fraser CL, Abegg M, Alroughani R, Alshowaeir D, Alvarenga R, et al. (diciembre de 2022). "Diagnóstico y clasificación de la neuritis óptica". La lanceta. Neurología . 21 (12): 1120-1134. doi :10.1016/s1474-4422(22)00200-9. PMID 36179757. S2CID 252564095.
- ^ Aik Kah T (2018). "Síndrome de CuRRL: una serie de casos" (PDF) . Acta Scientific Ophthalmology . 1 : 9–13.
- ^ Kashani AH, Chen CL, Gahm JK, Zheng F, Richter GM, Rosenfeld PJ, et al. (septiembre de 2017). "Angiografía por tomografía de coherencia óptica: una revisión exhaustiva de los métodos actuales y las aplicaciones clínicas". Progreso en la investigación de la retina y los ojos . 60 : 66–100. doi :10.1016/j.preteyeres.2017.07.002. PMC 5600872. PMID 28760677 .
- ^ Ehlers JP, Tao YK, Srivastava SK (mayo de 2014). "El valor de la tomografía de coherencia óptica intraoperatoria en la cirugía vitreorretiniana". Current Opinion in Ophthalmology . 25 (3): 221–227. doi :10.1097/ICU.0000000000000044. PMC 4119822 . PMID 24614147.
- ^ Pfau M, Michels S, Binder S, Becker MD (2015). "Experiencia clínica con el primer sistema de tomografía de coherencia óptica intraoperatoria disponible comercialmente". Cirugía oftálmica, láseres e imágenes de retina . 46 (10): 1001–1008. doi :10.3928/23258160-20151027-03. PMID 26599241.
- ^ Neuhann R, Neuhann T, Hörster R, Cursiefen C, Guell J, Siebelmann S (diciembre de 2021). "OCT en tiempo real integrado con láser en procedimientos del segmento anterior". Revista de cirugía refractiva y de cataratas . 47 (12): e88–e92. doi : 10.1097/j.jcrs.0000000000000773 . PMID 34393183.
- ^ Neuhann R, Neuhann T, Hörster R, Cursiefen C, Guell J, Siebelmann S (diciembre de 2021). "OCT en tiempo real integrado con láser en procedimientos del segmento anterior". Revista de cirugía refractiva y de cataratas . 47 (12): e88–e92. doi : 10.1364/BOE.426079 . PMC 8367251 . PMID 34393183.
- ^ Afsharan, Hadi; Hackmann, Michael J.; Wang, Qiang; Navaeipour, Farzaneh; Jayasree, Stephy Vijaya Kumar; Zawadzki, Robert J.; Silva, Dilusha; Joo, Chulmin; Cense, Barry (1 de julio de 2021). "Propiedades de polarización de las paredes de los vasos sanguíneos de la retina medidas con tomografía de coherencia óptica sensible a la polarización". Biomedical Optics Express . 12 (7): 4340–4362. doi :10.1364/BOE.426079. ISSN 2156-7085. PMC 8367251 . PMID 34457418.
- ^ ab Afsharan, Hadi; Silva, Dilusha; Joo, Chulmin; Cense, Barry (agosto de 2023). "Mediciones no invasivas de la pared de los vasos sanguíneos de la retina con tomografía de coherencia óptica sensible a la polarización para la evaluación de la diabetes: un estudio cuantitativo". Biomolecules . 13 (8): 1230. doi : 10.3390/biom13081230 . ISSN 2218-273X. PMC 10452597 . PMID 37627295.
- ^ ab Afsharan, Hadi; Anilkumar, Vidyalakshmi; Silva, Dilusha; Dwivedi, Girish; Joo, Chulmin; Cense, Barry (1 de enero de 2024). "Cambios asociados a la hipertensión en las paredes de los vasos sanguíneos de la retina medidos in vivo con tomografía de coherencia óptica sensible a la polarización". Óptica y láseres en ingeniería . 172 : 107838. Bibcode :2024OptLE.17207838A. doi : 10.1016/j.optlaseng.2023.107838 . ISSN 0143-8166.
- ^ "Una prueba ocular básica podría diagnosticar diabetes e hipertensión". PerthNow . 2023-09-20 . Consultado el 2024-01-24 .
- ^ https://eyewiki.org/Optic_Nerve_and_Retinal_Nerve_Fiber_Imaging
- ^ Tearney GJ, Brezinski ME, Bouma BE, Boppart SA, Pitris C, Southern JF, Fujimoto JG (junio de 1997). "Biopsia óptica endoscópica in vivo con tomografía de coherencia óptica". Science . 276 (5321): 2037–2039. doi :10.1126/science.276.5321.2037. PMID 9197265. S2CID 43035300.
- ^ Tearney GJ, Waxman S, Shishkov M, Vakoc BJ, Suter MJ, Freilich MI, et al. (noviembre de 2008). "Microscopía tridimensional de la arteria coronaria mediante imágenes intracoronarias de dominio de frecuencia óptica". JACC. Cardiovascular Imaging . 1 (6): 752–761. doi :10.1016/j.jcmg.2008.06.007. PMC 2852244 . PMID 19356512.
- ^ "LightLab lanza FD-OCT en Europa" (Nota de prensa) . Consultado el 9 de septiembre de 2016 .
- ^ Bezerra HG, Quimby DL, Matar F, Mohanty BD, Bassily E, Ughi GJ (julio de 2023). "Tomografía de coherencia óptica de alta frecuencia (OCT-HF) para imágenes coronarias previas a la intervención: un estudio pionero en humanos". JACC. Imágenes cardiovasculares . 16 (7): 982–984. doi :10.1016/j.jcmg.2023.01.013. PMID 37407126. S2CID 258115402.
- ^ Swanson E (13 de junio de 2016). "Tomografía de coherencia óptica: más allá de una mejor atención clínica: el impacto económico de la OCT". BioOptics World . Consultado el 9 de septiembre de 2016 .
- ^ Ughi GJ, Wang H, Gerbaud E, Gardecki JA, Fard AM, Hamidi E, et al. (noviembre de 2016). "Caracterización clínica de la aterosclerosis coronaria con OCT de modalidad dual e imágenes de autofluorescencia en el infrarrojo cercano". JACC. Imágenes cardiovasculares . 9 (11): 1304–1314. doi :10.1016/j.jcmg.2015.11.020. PMC 5010789 . PMID 26971006.
- ^ Hara T, Ughi GJ, McCarthy JR, Erdem SS, Mauskapf A, Lyon SC, et al. (febrero de 2017). "La obtención de imágenes moleculares de fibrina intravascular mejora la detección de stents no cicatrizados evaluados mediante tomografía de coherencia óptica in vivo". European Heart Journal . 38 (6): 447–455. doi :10.1093/eurheartj/ehv677. PMC 5837565 . PMID 26685129.
- ^ Fard AM, Vacas-Jacques P, Hamidi E, Wang H, Carruth RW, Gardecki JA, Tearney GJ (diciembre de 2013). "Tomografía de coherencia óptica: sistema de espectroscopia de infrarrojo cercano y catéter para imágenes intravasculares". Optics Express . 21 (25): 30849–30858. Bibcode :2013OExpr..2130849F. doi :10.1364/OE.21.030849. PMC 3926541 . PMID 24514658.
- ^ Chen CJ, Kumar JS, Chen SH, Ding D, Buell TJ, Sur S, et al. (abril de 2018). "Tomografía de coherencia óptica: aplicaciones futuras en imágenes cerebrovasculares". Stroke . 49 (4): 1044–1050. doi : 10.1161/STROKEAHA.117.019818 . PMID 29491139.
- ^ Xu X, Li M, Liu R, Yin Q, Shi X, Wang F, et al. (agosto de 2020). "Evaluación de la estenosis de la arteria vertebrobasilar mediante tomografía de coherencia óptica: serie de casos y revisión de la literatura". Revista de cirugía neurointervencionista . 12 (8): 809–813. doi :10.1136/neurintsurg-2019-015660. PMID 32066569. S2CID 211159079.
- ^ Ughi GJ, Marosfoi MG, King RM, Caroff J, Peterson LM, Duncan BH, et al. (julio de 2020). "Un sistema de tomografía de coherencia óptica de alta frecuencia neurovascular permite la microscopía volumétrica cerebrovascular in situ". Nature Communications . 11 (1): 3851. Bibcode :2020NatCo..11.3851U. doi :10.1038/s41467-020-17702-7. PMC 7395105 . PMID 32737314.
- ^ Pereira, Vitor M.; Lylyk, Pedro; Cancelliere, Nicole; Lylyk, Pedro N.; Lylyk, Ivan; Anagnostakou, Vania; Bleise, Carlos; Nishi, Hidehisa; Epshtein, Mark; King, Robert M.; Shazeeb, Mohammed Salman; Puri, Ajit S.; Liang, Conrad W.; Hanel, Ricardo A.; Spears, Julian (15 de mayo de 2024). "Microscopía volumétrica de arterias cerebrales con una sonda de imágenes de tomografía de coherencia óptica miniaturizada". Science Translational Medicine . 16 (747): eadl4497. doi :10.1126/scitranslmed.adl4497. ISSN 1946-6234. PMID 38748771.
- ^ "Una sonda "con forma de serpiente" capta imágenes de las arterias desde dentro - IEEE Spectrum". IEEE . Consultado el 17 de mayo de 2024 .
- ^ "OCT de última generación para el esófago". BioOptics World . 1 de mayo de 2013 . Consultado el 9 de septiembre de 2016 .
- ^ Gora MJ, Sauk JS, Carruth RW, Gallagher KA, Suter MJ, Nishioka NS, et al. (febrero de 2013). "La endomicroscopía con cápsula atada permite obtener imágenes menos invasivas de la microestructura del tracto gastrointestinal". Nature Medicine . 19 (2): 238–240. doi :10.1038/nm.3052. PMC 3567218 . PMID 23314056.
- ^ Ughi GJ, Gora MJ, Swager AF, Soomro A, Grant C, Tiernan A, et al. (febrero de 2016). "Segmentación y caracterización automatizadas de la pared esofágica in vivo mediante tomografía de coherencia óptica endoscópica con cápsula atada". Biomedical Optics Express . 7 (2): 409–419. doi :10.1364/BOE.7.000409. PMC 4771459 . PMID 26977350.
- ^ Welzel J, Lankenau E, Birngruber R, Engelhardt R (diciembre de 1997). "Tomografía de coherencia óptica de la piel humana". Revista de la Academia Estadounidense de Dermatología . 37 (6): 958–963. doi :10.1016/S0190-9622(97)70072-0. PMID 9418764. S2CID 20078741.
- ^ Boone MA, Norrenberg S, Jemec GB, Del Marmol V (octubre de 2012). "Obtención de imágenes del carcinoma basocelular mediante tomografía de coherencia óptica de alta definición: correlación histomorfológica. Un estudio piloto". The British Journal of Dermatology . 167 (4): 856–864. doi :10.1111/j.1365-2133.2012.11194.x. PMID 22862425. S2CID 24965088.
- ^ Coleman AJ, Richardson TJ, Orchard G, Uddin A, Choi MJ, Lacy KE (febrero de 2013). "Correlaciones histológicas de la tomografía de coherencia óptica en el cáncer de piel no melanoma". Investigación y tecnología de la piel . 19 (1): 10–19. doi :10.1111/j.1600-0846.2012.00626.x. PMID 22738357. S2CID 26084419.
- ^ Ulrich M, von Braunmuehl T, Kurzen H, Dirschka T, Kellner C, Sattler E, et al. (agosto de 2015). "La sensibilidad y especificidad de la tomografía de coherencia óptica para el diagnóstico asistido del carcinoma basocelular no pigmentado: un estudio observacional". The British Journal of Dermatology . 173 (2): 428–435. doi : 10.1111/bjd.13853 . PMID 25904111.
- ^ Levine A, Wang K, Markowitz O (octubre de 2017). "Tomografía de coherencia óptica en el diagnóstico del cáncer de piel". Clínicas dermatológicas . 35 (4): 465–488. doi :10.1016/j.det.2017.06.008. PMID 28886803.
- ^ Dubois A, Levecq O, Azimani H, Siret D, Barut A, Suppa M, et al. (octubre de 2018). "Tomografía de coherencia óptica confocal de campo lineal para la obtención de imágenes no invasivas de alta resolución de tumores cutáneos". Journal of Biomedical Optics . 23 (10): 1–9. Bibcode :2018JBO....23j6007D. doi : 10.1117/1.JBO.23.10.106007 . PMID 30353716. S2CID 53023955.
 Este artículo contiene citas de esta fuente, que está disponible bajo la licencia Creative Commons Atribución 3.0 Unported (CC BY 3.0).
Este artículo contiene citas de esta fuente, que está disponible bajo la licencia Creative Commons Atribución 3.0 Unported (CC BY 3.0). - ^ Velusamy P, Shimada Y, Kanno Z, Ono T, Tagami J (febrero de 2019). "Evaluación óptica de las lesiones de manchas blancas del esmalte alrededor de los brackets de ortodoncia mediante tomografía de coherencia óptica de fuente barrida (SS-OCT): un estudio in vitro". Revista de materiales dentales . 38 (1): 22–27. doi : 10.4012/dmj.2017-262 . PMID 30158348.
- ^ Damestani Y, Reynolds CL, Szu J, Hsu MS, Kodera Y, Binder DK, et al. (noviembre de 2013). "Prótesis de calota de zirconio estabilizado con itrio nanocristalino transparente". Nanomedicina . 9 (8): 1135–1138. doi :10.1016/j.nano.2013.08.002. PMID 23969102. S2CID 14212180.
- ^ Mohan G (4 de septiembre de 2013). "¿Una ventana al cerebro? Está aquí, dice el equipo de UC Riverside". Los Angeles Times .
- ^ Patente de EE. UU. 7116429, Walecki WJ, Van P, "Determinación del espesor de losas de materiales", emitida el 3 de octubre de 2006 .
- ^ Walecki WJ, Szondy F (2008). Novak EL, Wolfgang O, Gorecki C (eds.). "Eficiencia cuántica integrada, reflectancia, topografía y metrología de tensión para la fabricación de células solares". Proc. SPIE . Interferometría XIV: Aplicaciones. 7064 : 70640A. Bibcode :2008SPIE.7064E..0AW. doi :10.1117/12.797541. S2CID 120257179.
- ^ Walecki WJ, Lai K, Pravdivtsev A, Souchkov V, Van P, Azfar T, Wong T, Lau SH, Koo A (2005). Tanner DM, Ramesham R (eds.). "Medidor de distancia absoluta interferométrico de baja coherencia para el estudio de estructuras MEMS". Proc. SPIE . Fiabilidad, empaquetado, pruebas y caracterización de MEMS/MOEMS IV. 5716 : 182. Bibcode :2005SPIE.5716..182W. doi :10.1117/12.590013. S2CID 110785119.
- ^ Walecki WJ, Lai K, Souchkov V, Van P, Lau SH, Koo A (2005). "Nueva metrología de espesor sin contacto para la fabricación de dispositivos emisores de luz de banda ancha". Physica Status Solidi C . 2 (3): 984–989. Bibcode :2005PSSCR...2..984W. doi :10.1002/pssc.200460606.
- ^ Walecki W, Wei F, Van P, Lai K, Lee T, Lau SH, Koo A (2004). Tanner DM, Rajeshuni R (eds.). "Nueva metrología de baja coherencia para la caracterización no destructiva de estructuras microfabricadas y micromaquinadas de alta relación de aspecto". Proc. SPIE . Fiabilidad, pruebas y caracterización de MEMS/MOEMS III. 5343 : 55. doi :10.1117/12.530749. S2CID 123249666.
- ^ Guss G, Bass I, Hackel R, Demos SG (6 de noviembre de 2007). Imágenes tridimensionales de alta resolución de sitios de daño superficial en sílice fundida con tomografía de coherencia óptica (PDF) (informe). Laboratorio Nacional Lawrence Livermore . UCRL-PROC-236270. Archivado desde el original (PDF) el 11 de febrero de 2017. Consultado el 14 de diciembre de 2010 .
- ^ Walecki W, Wei F, Van P, Lai K, Lee T, Lau SH, Koo A (2004). Metrología interferométrica para estructuras de semiconductores compuestos delgadas y ultradelgadas montadas sobre soportes aislantes (PDF) . Conferencia CS Mantech.
- ^ ab Zvagelsky, Roman; Mayer, Frederik; Beutel, Dominik; Rockstuhl, Carsten; Gomard, Guillaume; Wegener, Martin (12 de diciembre de 2022). "Hacia el diagnóstico in situ de la impresión láser 3D multifotónica mediante tomografía de coherencia óptica". Light: Advanced Manufacturing . 3 (3): 466–480. doi :10.37188/lam.2022.039. ISSN 2689-9620.
- ^ Walecki WJ, Pravdivtsev A, Santos II M, Koo A (agosto de 2006). "Interferometría de fibra óptica de baja coherencia, alta precisión y alta velocidad para el control de procesos de grabado y pulido in situ". Proc. SPIE . Interferometría XIII: Aplicaciones. 6293 : 62930D. Código Bibliográfico : 2006SPIE.6293E..0DW. doi : 10.1117/12.675592. S2CID 121209439.
- ^ Véase, por ejemplo: "ZebraOptical Optoprofiler: sonda interferométrica".
- ^ Solicitud EP 2799842, Markl, Daniel; Hannesschläger, Günther & Leitner, Michael et al., "Un dispositivo y un método para monitorear una propiedad de un recubrimiento de una forma de dosificación sólida durante un proceso de recubrimiento que forma el recubrimiento de la forma de dosificación sólida", publicada el 5 de noviembre de 2014 ; solicitud GB 2513581 ; solicitud US 20140322429 A1 .
- ^ Walecki WJ, Szondy F, Wang A (30 de abril de 2009). Xiao H, Fan S (eds.). "Interferometría IR de baja coherencia con fibra óptica para la fabricación de sensores de defensa" (PDF) . Proc. SPIE . Photonic Microdevices/Microstructures for Sensing. 7322 : 73220K. Bibcode :2009SPIE.7322E..0KW. doi :10.1117/12.818381. S2CID 120168355. Archivado desde el original (PDF) el 20 de agosto de 2011 . Consultado el 25 de mayo de 2011 .
- ^ Dufour M, Lamouche G, Gauthier B, Padioleau C, Monchalin JP (13 de diciembre de 2006). "Inspección de piezas industriales de difícil acceso utilizando sondas de diámetro pequeño" (PDF) . Sala de prensa de SPIE . doi :10.1117/2.1200610.0467. S2CID 120476700. Consultado el 15 de diciembre de 2010 .
- ^ Dufour ML, Lamouche G, Detalle V, Gauthier B, Sammut P (abril de 2005). "Interferometría de baja coherencia, una técnica avanzada para la metrología óptica en la industria". Insight: Ensayos no destructivos y monitoreo de condiciones . 47 (4): 216–219. CiteSeerX 10.1.1.159.5249 . doi :10.1784/insi.47.4.216.63149. ISSN 1354-2575. S2CID 15657288.
- ^ Boppart S (11 de junio de 2014). "Desarrollo de nuevas técnicas de obtención de imágenes ópticas para uso clínico". Sala de prensa de SPIE . doi :10.1117/2.3201406.03.
- ^ Al-Azri K, Melita LN, Strange AP, Festy F, Al-Jawad M, Cook R, et al. (marzo de 2016). "Uso de la tomografía de coherencia óptica en el diagnóstico de defectos del esmalte". Journal of Biomedical Optics . 21 (3): 36004. Bibcode :2016JBO....21c6004A. doi : 10.1117/1.jbo.21.3.036004 . PMID 26968386.
- ^ Iino Y, Ebihara A, Yoshioka T, Kawamura J, Watanabe S, Hanada T, et al. (noviembre de 2014). "Detección de un segundo canal mesiovestibular en molares superiores mediante tomografía de coherencia óptica de fuente de barrido". Revista de Endodoncia . 40 (11): 1865–1868. doi :10.1016/j.joen.2014.07.012. PMID 25266471.
- ^ Subhash HM, Hogan JN, Leahy MJ (mayo de 2015). "Tomografía de coherencia óptica de referencia múltiple para aplicaciones de teléfonos inteligentes". Sala de prensa de SPIE . doi :10.1117/2.1201503.005807.
- ^ Rank EA, Sentosa R, Harper DJ, Salas M, Gaugutz A, Seyringer D, et al. (enero de 2021). "Hacia la tomografía de coherencia óptica en un chip: obtención de imágenes tridimensionales de la retina humana in vivo utilizando rejillas de guía de ondas en matriz basadas en circuitos integrados fotónicos". Light: Science & Applications . 10 (1): 6. Bibcode :2021LSA....10....6R. doi :10.1038/s41377-020-00450-0. PMC 7785745 . PMID 33402664.






![{\displaystyle I=k_{1}I_{S}+k_{2}I_{S}+2{\sqrt {\left(k_{1}I_{S}\right)\cdot \left(k_{2}I_{S}\right)}}\cdot Re\left[\gamma \left(\tau \right)\right]\qquad (1)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e90b482fe73988b986f3ebc89f0ff288bf6d67d9)



![{\displaystyle \gamma \left(\tau \right)=\exp \left[-\left({\frac {\pi \Delta \nu \tau }{2{\sqrt {\ln 2}}}}\right)^{2}\right]\cdot \exp \left(-j2\pi \nu _{0}\tau \right)\qquad \quad (2)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/83da0d10e1049d9b461ab144e7b9dd7e58e85c45)










