Rancidificación
En este artículo falta información sobre detección y cuantificación: índice de peróxido, índice de acidez, índice de carbonilo, materiales polares totales; niveles legales. ( Noviembre de 2021 ) |
La rancidificación es el proceso de autooxidación o hidrólisis completa o incompleta de grasas y aceites cuando se exponen al aire, la luz, la humedad o la acción bacteriana, produciendo aldehídos de cadena corta , cetonas y ácidos grasos libres . [1]
Cuando estos procesos ocurren en los alimentos, pueden producirse olores y sabores indeseables. En el caso de las carnes procesadas, estos sabores se conocen colectivamente como sabor a recalentado . Sin embargo, en ciertos casos, los sabores pueden ser deseables (como en el caso de los quesos curados ). [2]
La rancidificación también puede restar valor nutricional a los alimentos, ya que algunas vitaminas son sensibles a la oxidación. [3] De manera similar a la rancidificación, la degradación oxidativa también ocurre en otros hidrocarburos, como aceites lubricantes , combustibles y fluidos de corte mecánico . [4]
Caminos
Se reconocen cinco vías de rancidificación: [5]
Hidrolítico
La rancidez hidrolítica se refiere al olor que se desarrolla cuando los triglicéridos se hidrolizan y se liberan ácidos grasos libres. Esta reacción de los lípidos con el agua puede requerir un catalizador (como una lipasa , [6] o condiciones ácidas o alcalinas) que conduce a la formación de ácidos grasos libres y glicerol . En particular, los ácidos grasos de cadena corta , como el ácido butírico , son malolientes . [7] Cuando se producen ácidos grasos de cadena corta, estos mismos sirven como catalizadores, acelerando aún más la reacción, una forma de autocatálisis . [7]
Oxidativo
La rancidez oxidativa está asociada a la degradación por el oxígeno del aire.
Oxidación por radicales libres
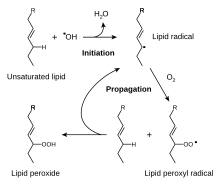
Los enlaces dobles de un ácido graso insaturado pueden romperse mediante reacciones de radicales libres que involucran oxígeno molecular. Esta reacción provoca la liberación de aldehídos y cetonas malolientes y altamente volátiles . Debido a la naturaleza de las reacciones de radicales libres, la reacción es catalizada por la luz solar. [7] La oxidación ocurre principalmente con grasas insaturadas. Por ejemplo, aunque la carne se mantenga refrigerada o congelada, la grasa poliinsaturada continuará oxidándose y se volverá rancia lentamente. El proceso de oxidación de la grasa, que potencialmente resulta en rancidez, comienza inmediatamente después de que el animal es sacrificado y la grasa muscular, intramuscular, intermuscular y superficial queda expuesta al oxígeno del aire. Este proceso químico continúa durante el almacenamiento congelado, aunque más lentamente a temperatura más baja. La rancidez oxidativa se puede prevenir mediante un empaque a prueba de luz, una atmósfera libre de oxígeno (recipientes herméticos) y mediante la adición de antioxidantes . [7]
Oxidación catalizada por enzimas
Un doble enlace de un ácido graso insaturado puede oxidarse con oxígeno del aire en reacciones catalizadas por enzimas lipoxigenasas de plantas o animales , [6] produciendo un hidroperóxido como intermediario reactivo, como en la peroxidación por radicales libres. Los productos finales dependen de las condiciones: el artículo sobre la lipoxigenasa muestra que si está presente una enzima hidroperóxido liasa , puede escindir el hidroperóxido para producir ácidos grasos de cadena corta y ácidos dicarboxílicos (varios de los cuales se descubrieron por primera vez en grasas rancias).
Microbiano
La rancidez microbiana se refiere a un proceso dependiente del agua en el que los microorganismos, como las bacterias o los mohos , utilizan sus enzimas, como las lipasas, para descomponer la grasa. [6] La pasteurización y/o la adición de ingredientes antioxidantes , como la vitamina E , pueden reducir este proceso al destruir o inhibir los microorganismos. [6]
Seguridad alimentaria
A pesar de las preocupaciones de la comunidad científica, hay pocos datos sobre los efectos de la rancidez o la oxidación de lípidos en la salud de los seres humanos. [8] [9] Los estudios realizados en animales muestran evidencia de daño orgánico, inflamación, carcinogénesis y aterosclerosis avanzada, aunque normalmente la dosis de lípidos oxidados es mayor que la que consumirían los seres humanos. [10] [11] [12]
Los antioxidantes se utilizan a menudo como conservantes en alimentos que contienen grasa para retrasar la aparición o ralentizar el desarrollo de la rancidez debido a la oxidación. Los antioxidantes naturales incluyen ácido ascórbico (vitamina C) y tocoferoles (vitamina E). Los antioxidantes sintéticos incluyen hidroxianisol butilado (BHA), hidroxitolueno butilado (BHT), TBHQ , galato de propilo y etoxiquina . Los antioxidantes naturales tienden a tener una vida útil corta, [13] por lo que se utilizan antioxidantes sintéticos cuando se prefiere una vida útil más larga. La eficacia de los antioxidantes solubles en agua es limitada en la prevención de la oxidación directa dentro de las grasas, pero es valiosa para interceptar los radicales libres que viajan a través de las partes acuosas de los alimentos. Una combinación de antioxidantes solubles en agua y liposolubles es ideal, generalmente en la proporción de grasa a agua.
Además, la rancidez puede reducirse almacenando las grasas y los aceites en un lugar fresco y oscuro con poca exposición al oxígeno o a los radicales libres, ya que el calor y la luz aceleran la velocidad de reacción de las grasas con el oxígeno. Los agentes antimicrobianos también pueden retrasar o prevenir la rancidez al inhibir el crecimiento de bacterias u otros microorganismos que afectan el proceso. [1]
La tecnología de eliminación de oxígeno se puede utilizar para eliminar el oxígeno de los envases de alimentos y así evitar la rancidificación oxidativa.
Medición de la estabilidad oxidativa
La estabilidad oxidativa es una medida de la resistencia del aceite o la grasa a la oxidación. Debido a que el proceso se lleva a cabo mediante una reacción en cadena , la reacción de oxidación tiene un período en el que es relativamente lenta, antes de acelerarse repentinamente. El tiempo que tarda en ocurrir esto se denomina "tiempo de inducción" y es repetible en condiciones idénticas (temperatura, flujo de aire, etc.). Hay varias formas de medir el progreso de la reacción de oxidación. Uno de los métodos más populares que se utilizan actualmente es el método Rancimat.
El método Rancimat se lleva a cabo utilizando una corriente de aire a temperaturas entre 50 y 220 °C. Los productos volátiles de oxidación (en gran parte ácido fórmico [14] ) son transportados por la corriente de aire al recipiente de medición, donde son absorbidos (disueltos) en el fluido de medición ( agua destilada ). Mediante la medición continua de la conductividad de esta solución, se pueden generar curvas de oxidación. El punto cúspide de la curva de oxidación (el punto donde comienza un aumento rápido de la conductividad) proporciona el tiempo de inducción de la reacción de rancidificación, [15] y puede tomarse como una indicación de la estabilidad oxidativa de la muestra.
El método Rancimat, el instrumento de estabilidad oxidativa (OSI) y el oxigrafista fueron desarrollados como versiones automáticas del más complicado método AOM (método de oxígeno activo), que se basa en la medición de los valores de peróxido [15] para determinar el tiempo de inducción de grasas y aceites. Con el tiempo, el método Rancimat se ha consolidado y ha sido aceptado en una serie de normas nacionales e internacionales, por ejemplo, AOCS Cd 12b-92 e ISO 6886.
Véase también
- Fritura § Deterioro del aceite y cambios químicos
- Fermentación
- Conservación de alimentos
- Peroxidación lipídica
- Preservativo
- Putrefacción
Referencias
- ^ ab Lück, Erich; von Rymon Lipinski, Gert-Wolfhard (2000). "Alimentos, 3. Aditivos alimentarios". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a11_561. ISBN 3527306730.
- ^ Thomas, Alfred (2000). "Grasas y aceites grasos". Ullmann's Encyclopedia of Industrial Chemistry . Weinheim: Wiley-VCH. doi :10.1002/14356007.a10_173. ISBN 3527306730.
- ^ Termes, Waldemar (1990). Naturwissenschaftliche Grundlagen der Lebensmittelzubereitung . Hamburgo: Behr's Verlag. págs. 50–37. ISBN 978-3-925673-84-9.
- ^ Klemchuk, Peter P. (2000). "Antioxidantes". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a03_091. ISBN 3527306730.
- ^ Freeman, IP (2000). "Margarinas y mantecas". Ullmann's Encyclopedia of Industrial Chemistry . doi :10.1002/14356007.a16_145. ISBN 978-3-527-30673-2.
- ^ abcd Robin Koon (4 de agosto de 2009). «Entender la rancidez de los lípidos nutricionales». Natural Products Insider . Consultado el 7 de abril de 2019 .
- ^ abcd Sergey, Bylikin (enero de 2014). Química: compañero de curso . Horner, Gary; Murphy, Brian; Tarcy, David (edición de 2014). Oxford. ISBN 978-0-19-839212-5.OCLC 862091138 .
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace ) - ^ Cameron-Smith, David; Albert, Benjamin B.; Cutfield, Wayne S. (23 de noviembre de 2015). "Buscando respuestas: ¿es un problema la oxidación de los suplementos de aceite de pescado?". Journal of Nutritional Science . 4 : e36. doi :10.1017/jns.2015.26. ISSN 2048-6790. PMC 4681158 . PMID 26688722.
- ^ Panel de la EFSA sobre riesgos biológicos (2010). «Opinión científica sobre el aceite de pescado para consumo humano. Higiene alimentaria, incluida la rancidez». Revista de la EFSA . 8 (10): 1874. doi : 10.2903/j.efsa.2010.1874 .
- ^ Albert, Benjamin B.; Cameron-Smith, David; Hofman, Paul L.; Cutfield, Wayne S. (2013). "Oxidación de suplementos de omega-3 marinos y salud humana". BioMed Research International . 2013 : 464921. doi : 10.1155/2013/464921 . PMC 3657456. PMID 23738326 .
- ^ Kanner, Joseph (2007). "Los productos finales de la oxidación avanzada de lípidos en la dieta son factores de riesgo para la salud humana". Molecular Nutrition & Food Research . 51 (9): 1094–1101. doi :10.1002/mnfr.200600303. PMID 17854006.
- ^ Falade, AO; Oboh, G.; Okoh, AI (2017). "Potenciales consecuencias para la salud del consumo de aceites de cocina oxidados térmicamente: una revisión". Revista polaca de ciencias de la alimentación y la nutrición (en polaco). 67 (2): 95–105. doi : 10.1515/pjfns-2016-0028 .
- ^ Rahmawati S, Bundjali B (2009). "Cinética de la oxidación de la vitamina C". Seminario invitado Kimia Bersama UKM-ITB . VIII (9–11): 535–546.
- ^ Allen, JC; Hamilton, RJ (1994). Rancidez en los alimentos. Springer Verlag GmbH. pag. 47.ISBN 978-0-8342-1287-9.
- ^ ab Miraliakbari, H. (2007). Aceites de frutos secos: características químicas, oxidación y antioxidantes. Biblioteca y Archivos de Canadá. p. 31. ISBN 978-0-494-19381-5.[ enlace muerto permanente ]
Lectura adicional
- Imark, Christian; Kneubühl, Markus; Bodmer, Stefan (diciembre de 2000). "Presencia y actividad de antioxidantes naturales en bebidas espirituosas a base de hierbas". Ciencia alimentaria innovadora y tecnologías emergentes . 1 (4): 239–243. doi :10.1016/S1466-8564(00)00018-7.

