Lisdexanfetamina
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Vyvanse, Tyvense, Elvanse, otros |
| Otros nombres | L -Lisina-d-anfetamina; (2 S )-2,6-Diamino- N -[(2 S )-1-fenilpropan-2-il]hexanamida N -[(2 S )-1-Fenil-2-propanil]- L -lisinamida |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a607047 |
| Datos de licencia |
|
Categoría de embarazo |
|
Responsabilidad por dependencia | Moderado [1] [2] |
Responsabilidad por adicción | Moderado [1] [2] |
| Vías de administración | Por la boca |
| Código ATC |
|
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | Oral : 96,4% [9] |
| Unión de proteínas | 20% (como dextroanfetamina ) [10] |
| Metabolismo | Inicialmente, la hidrólisis la realizan las enzimas en los glóbulos rojos y luego sigue el metabolismo. |
| Metabolitos | Dextroanfetamina (y sus metabolitos) y L -lisina |
| Inicio de la acción | Oral : <2 horas [11] [12] |
| Vida media de eliminación | Lisdexanfetamina: <1 hora [13] Dextroanfetamina: 10–12 h [13] [7] |
| Duración de la acción | 10–14 horas [14] [11] [12] |
| Excreción | Riñón : ~2% |
| Identificadores | |
| |
| Número CAS |
|
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL |
|
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Datos químicos y físicos | |
| Fórmula | C15H25N3O |
| Masa molar | 263,385 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| Quiralidad | Enantiómero dextrógiro |
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La lisdexanfetamina , que se vende bajo las marcas Vyvanse y Elvanse , entre otras, es un medicamento estimulante que se utiliza para tratar el trastorno por déficit de atención con hiperactividad (TDAH) en niños y adultos y para el trastorno por atracón moderado a severo en adultos. [15] La lisdexanfetamina se toma por vía oral . Sus efectos generalmente comienzan dentro de las dos horas y duran hasta 14 horas. [15]
Los efectos secundarios comunes de la lisdexanfetamina incluyen pérdida de apetito , ansiedad , diarrea , dificultad para dormir , irritabilidad y náuseas . [15] Los efectos secundarios raros pero graves incluyen manía , muerte cardíaca súbita en aquellos con problemas cardíacos subyacentes y psicosis . [15] Tiene un alto potencial de abuso de sustancias . [7] [15] El síndrome serotoninérgico puede ocurrir si se usa con ciertos otros medicamentos. [15] Su uso durante el embarazo puede resultar en daño al bebé y el fabricante no recomienda su uso durante la lactancia . [16] [15] [17]
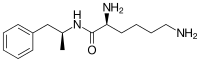
La lisdexanfetamina es un profármaco inactivo que actúa después de ser convertido por el cuerpo en dextroanfetamina , un estimulante del sistema nervioso central (SNC) . [15] [18] Químicamente, la lisdexanfetamina está compuesta por el aminoácido L -lisina , unido a la dextroanfetamina. [19]
La lisdexanfetamina fue aprobada para uso médico en los Estados Unidos en 2007 y en la Unión Europea en 2012. [15] [20] En 2022, fue el 69.º medicamento más recetado en los Estados Unidos, con más de 9 millones de recetas. [21] [22] Es una sustancia controlada de Clase B en el Reino Unido, una droga controlada de la Lista 8 en Australia y una sustancia controlada de la Lista II en los Estados Unidos. [16] [23]
Usos
Médico

La lisdexanfetamina se utiliza principalmente como tratamiento para el trastorno por déficit de atención con hiperactividad (TDAH) y el trastorno por atracones ; [7] tiene usos no aprobados similares a los de otras anfetaminas farmacéuticas. [14] Las personas mayores de 65 años no fueron evaluadas comúnmente en ensayos clínicos de lisdexanfetamina para el TDAH. [7] Según una revisión sistemática de 2019, la lisdexanfetamina fue el tratamiento más eficaz para el TDAH en adultos . [24]
TDAH
Se sabe que la exposición prolongada a dosis suficientemente altas de anfetaminas en algunas especies animales produce un desarrollo anormal del sistema de dopamina o daño nervioso, [25] [26] pero, en humanos con TDAH, el uso prolongado de anfetaminas farmacéuticas en dosis terapéuticas parece mejorar el desarrollo cerebral y el crecimiento nervioso. [27] [28] [29] Las revisiones de estudios de imágenes por resonancia magnética (IRM) sugieren que el tratamiento a largo plazo con anfetaminas disminuye las anomalías en la estructura y función cerebral encontradas en sujetos con TDAH y mejora la función en varias partes del cerebro, como el núcleo caudado derecho de los ganglios basales . [27] [28] [29]
Las revisiones de la investigación clínica sobre estimulantes han establecido la seguridad y eficacia del uso continuo de anfetaminas a largo plazo para el tratamiento del TDAH. [30] [31] [32] Los ensayos controlados aleatorios de terapia estimulante continua para el tratamiento del TDAH que abarcan 2 años han demostrado la eficacia y seguridad del tratamiento. [30] [31] Dos revisiones han indicado que la terapia estimulante continua a largo plazo para el TDAH es eficaz para reducir los síntomas centrales del TDAH (es decir, hiperactividad, falta de atención e impulsividad), mejorar la calidad de vida y el rendimiento académico, y producir mejoras en una gran cantidad de resultados funcionales [nota 1] en 9 categorías de resultados relacionados con lo académico, el comportamiento antisocial , la conducción, el uso de drogas no medicinales, la obesidad, la ocupación, la autoestima , el uso de servicios (es decir, académicos, ocupacionales, de salud, financieros y legales) y la función social. [30] [32] Una revisión destacó un ensayo controlado aleatorio de nueve meses de tratamiento con anfetaminas para el TDAH en niños que encontró un aumento promedio de 4,5 puntos de CI , aumentos continuos en la atención y disminuciones continuas en conductas disruptivas e hiperactividad. [31] Otra revisión indicó que, con base en los estudios de seguimiento más largos realizados hasta la fecha, la terapia estimulante de por vida que comienza durante la infancia es continuamente efectiva para controlar los síntomas del TDAH y reduce el riesgo de desarrollar un trastorno por consumo de sustancias en la edad adulta. [30]
Los modelos actuales del TDAH sugieren que está asociado con deterioros funcionales en algunos de los sistemas de neurotransmisores del cerebro ; [33] estos deterioros funcionales implican una alteración de la neurotransmisión de dopamina en la proyección mesocorticolímbica y de la neurotransmisión de noradrenalina en las proyecciones noradrenérgicas desde el locus coeruleus hasta la corteza prefrontal . [33] Los estimulantes como el metilfenidato y la anfetamina son eficaces en el tratamiento del TDAH porque aumentan la actividad de los neurotransmisores en estos sistemas. [34] [33] [35] Aproximadamente el 80% de los que usan estos estimulantes ven mejoras en los síntomas del TDAH. [36] Los niños con TDAH que usan medicamentos estimulantes generalmente tienen mejores relaciones con sus compañeros y familiares, tienen un mejor desempeño en la escuela, son menos distraídos e impulsivos y tienen períodos de atención más largos. [37] [38] Las revisiones Cochrane [nota 2] sobre el tratamiento del TDAH en niños, adolescentes y adultos con anfetaminas farmacéuticas afirmaron que los estudios a corto plazo han demostrado que estos fármacos disminuyen la gravedad de los síntomas, pero tienen tasas de interrupción más altas que los medicamentos no estimulantes debido a sus efectos secundarios adversos . [40] [41] Una revisión Cochrane sobre el tratamiento del TDAH en niños con trastornos de tics como el síndrome de Tourette indicó que los estimulantes en general no empeoran los tics , pero las dosis altas de dextroanfetamina podrían exacerbar los tics en algunos individuos. [42]
Trastorno por atracón
El trastorno por atracón (BED) se caracteriza por episodios recurrentes y persistentes de atracones compulsivos. [43] Estos episodios suelen ir acompañados de una angustia marcada y una sensación de pérdida de control sobre la alimentación. [43] La fisiopatología del BED no se entiende completamente, pero se cree que implica un circuito de recompensa dopaminérgico disfuncional a lo largo del circuito cortico-estriatal-tálamo-cortical . [44] [45] A partir de julio de 2024, la lisdexanfetamina es la única farmacoterapia aprobada por la USFDA y la TGA para el BED. [46] [47] La evidencia sugiere que la eficacia del tratamiento con lisdexanfetamina en el BED está respaldada al menos en parte por una superposición psicopatológica entre el BED y el TDAH, y este último se conceptualiza como un trastorno del control cognitivo que también se beneficia del tratamiento con lisdexanfetamina. [44] [45]

Los efectos terapéuticos de la lisdexanfetamina para el trastorno por atracón implican principalmente una acción directa en el sistema nervioso central después de la conversión a su metabolito farmacológicamente activo, la dextroanfetamina. [47] A nivel central, la dextroanfetamina aumenta la actividad neurotransmisora de la dopamina y la noradrenalina en las regiones corticales prefrontales que regulan el control cognitivo del comportamiento. [44] [47] De manera similar a su efecto terapéutico en el TDAH, la dextroanfetamina mejora el control cognitivo y puede reducir la impulsividad en pacientes con trastorno por atracón al mejorar los procesos cognitivos responsables de anular las respuestas de alimentación prepotentes que preceden a los episodios de atracones. [44] [49] [50] Además, las acciones de la dextroanfetamina fuera del sistema nervioso central también pueden contribuir a sus efectos terapéuticos en el trastorno por atracón. Periféricamente, la dextroanfetamina desencadena la lipólisis a través de la señalización noradrenérgica en las células grasas adiposas , lo que lleva a la liberación de triglicéridos en el plasma sanguíneo para ser utilizados como sustrato de combustible. [45] [51] La dextroanfetamina también activa TAAR1 en órganos periféricos a lo largo del tracto gastrointestinal que están involucrados en la regulación de la ingesta de alimentos y el peso corporal. [48] En conjunto, estas acciones confieren un efecto anorexigénico que promueve la saciedad en respuesta a la alimentación y puede disminuir los atracones como efecto secundario. [50] [48]
Las revisiones médicas de ensayos controlados aleatorios han demostrado que la lisdexanfetamina, en dosis entre 50 y 70 mg, es segura y eficaz para el tratamiento del trastorno por atracón moderado a grave en adultos. [fuentes 1] Estas revisiones sugieren que la lisdexanfetamina es persistentemente eficaz en el tratamiento del trastorno por atracón y se asocia con reducciones significativas en el número de días de atracones y episodios de atracones por semana. [fuentes 1] Además, una revisión sistemática metaanalítica destacó un estudio de seguridad y tolerabilidad de extensión de 12 meses de etiqueta abierta que informó que la lisdexanfetamina siguió siendo eficaz para reducir el número de días de atracones durante la duración del estudio. [50] Además, tanto una revisión como una revisión sistemática metaanalítica encontraron que la lisdexanfetamina era superior al placebo en varias medidas de resultados secundarios, incluido el cese persistente de los atracones, la reducción de los síntomas de atracones relacionados con el trastorno obsesivo-compulsivo, la reducción del peso corporal y la reducción de los triglicéridos. [45] [50] La lisdexanfetamina, como todas las anfetaminas farmacéuticas, tiene efectos supresores directos del apetito que pueden ser terapéuticamente útiles tanto en el trastorno por atracón como en sus comorbilidades. [46] [50] Según las revisiones de estudios de neuroimagen que involucraron a participantes diagnosticados con trastorno por atracón, la neuroplasticidad terapéutica en las vías dopaminérgicas y noradrenérgicas del uso a largo plazo de lisdexanfetamina puede estar implicada en mejoras duraderas en la regulación de las conductas alimentarias que se observan incluso después de suspender el medicamento. [46] [47] [50]
Narcolepsia
La narcolepsia es un trastorno crónico del sueño y la vigilia que se asocia con somnolencia diurna excesiva, cataplejía y parálisis del sueño . [53] Los pacientes con narcolepsia son diagnosticados como tipo 1 o tipo 2, y solo los primeros presentan síntomas de cataplejía. [54] La narcolepsia tipo 1 resulta de la pérdida de aproximadamente 70.000 neuronas liberadoras de orexina en el hipotálamo lateral , lo que conduce a niveles significativamente reducidos de orexina cerebroespinal ; [55] [56] esta reducción es un biomarcador diagnóstico para la narcolepsia tipo 1. [54] Las neuronas de orexina del hipotálamo lateral inervan cada componente del sistema activador reticular ascendente (ARAS), que incluye núcleos noradrenérgicos , dopaminérgicos , histaminérgicos y serotoninérgicos que promueven la vigilia . [56] [57]
El modo de acción terapéutico de la anfetamina en la narcolepsia implica principalmente aumentar la actividad del neurotransmisor monoamínico en el ARAS. [55] [58] [59] Esto incluye neuronas noradrenérgicas en el locus coeruleus , neuronas dopaminérgicas en el área tegmental ventral , neuronas histaminérgicas en el núcleo tuberomamilar y neuronas serotoninérgicas en el núcleo del rafe dorsal . [57] [59] La dextroanfetamina, el enantiómero más dopaminérgico de la anfetamina, es particularmente eficaz para promover la vigilia porque la liberación de dopamina tiene la mayor influencia en la activación cortical y la excitación cognitiva, en relación con otras monoaminas. [55] Por el contrario, la levoanfetamina puede tener un mayor efecto en la cataplejía, un síntoma más sensible a los efectos de la noradrenalina y la serotonina. [55] Los núcleos noradrenérgicos y serotoninérgicos en el ARAS están involucrados en la regulación del ciclo del sueño REM y funcionan como células "REM-off", con el efecto de la anfetamina sobre la noradrenalina y la serotonina contribuyendo a la supresión del sueño REM y una posible reducción de la cataplejía en dosis altas. [55] [54] [57]
La guía de práctica clínica de 2021 de la Academia Estadounidense de Medicina del Sueño (AASM) recomienda condicionalmente la dextroanfetamina para el tratamiento de la narcolepsia tipo 1 y tipo 2. [60] El tratamiento con anfetaminas farmacéuticas generalmente es menos preferido en relación con otros estimulantes (p. ej., modafinilo ) y se considera una opción de tratamiento de tercera línea . [61] [62] [63] Las revisiones médicas indican que la anfetamina es segura y eficaz para el tratamiento de la narcolepsia. [55] [61] [60] La anfetamina parece ser más eficaz para mejorar los síntomas asociados con la hipersomnolencia , y tres revisiones encontraron reducciones clínicamente significativas en la somnolencia diurna en pacientes con narcolepsia. [55] [61] [60] Además, estas revisiones sugieren que la anfetamina puede mejorar de forma dosis-dependiente los síntomas de cataplejía. [55] [61] [60] Sin embargo, la calidad de la evidencia de estos hallazgos es baja y, en consecuencia, se refleja en la recomendación condicional de la AASM de la dextroanfetamina como una opción de tratamiento para la narcolepsia. [60]
Mejorar el rendimiento
Rendimiento cognitivo
En 2015, una revisión sistemática y un metaanálisis de ensayos clínicos de alta calidad encontraron que, cuando se usa en dosis bajas (terapéuticas), la anfetamina produce mejoras modestas pero inequívocas en la cognición, incluida la memoria de trabajo , la memoria episódica a largo plazo , el control inhibitorio y algunos aspectos de la atención , en adultos sanos normales; [64] [65] Se sabe que estos efectos de mejora de la cognición de la anfetamina están parcialmente mediados por la activación indirecta tanto del receptor de dopamina D 1 como del receptor α 2 -adrenérgico en la corteza prefrontal . [34] [64] Una revisión sistemática de 2014 encontró que las dosis bajas de anfetamina también mejoran la consolidación de la memoria , lo que a su vez conduce a una mejor recuperación de la información . [66] Las dosis terapéuticas de anfetamina también mejoran la eficiencia de la red cortical, un efecto que media las mejoras en la memoria de trabajo en todos los individuos. [34] [67] La anfetamina y otros estimulantes del TDAH también mejoran la relevancia de la tarea (motivación para realizar una tarea) y aumentan la excitación (vigilia), lo que a su vez promueve el comportamiento dirigido a objetivos. [34] [68] [69] Los estimulantes como la anfetamina pueden mejorar el rendimiento en tareas difíciles y aburridas y algunos estudiantes los utilizan como ayuda para estudiar y realizar exámenes. [34] [69] [70] Según estudios sobre el uso de estimulantes ilícitos autodeclarado, entre el 5 y el 35 % de los estudiantes universitarios utilizan estimulantes desviados para el TDAH, que se utilizan principalmente para mejorar el rendimiento académico en lugar de como drogas recreativas. [71] [72] [73] Sin embargo, las dosis altas de anfetamina que están por encima del rango terapéutico pueden interferir con la memoria de trabajo y otros aspectos del control cognitivo. [34] [69]
Rendimiento físico
La anfetamina es utilizada por algunos atletas por sus efectos psicológicos y de mejora del rendimiento atlético , como el aumento de la resistencia y el estado de alerta; [74] [75] sin embargo, el uso no médico de anfetamina está prohibido en eventos deportivos que están regulados por agencias antidopaje universitarias, nacionales e internacionales. [76] [77] En personas sanas en dosis terapéuticas orales, se ha demostrado que la anfetamina aumenta la fuerza muscular , la aceleración, el rendimiento atlético en condiciones anaeróbicas y la resistencia (es decir, retrasa la aparición de la fatiga ), al tiempo que mejora el tiempo de reacción . [74] [78] [79] La anfetamina mejora la resistencia y el tiempo de reacción principalmente a través de la inhibición de la recaptación y la liberación de dopamina en el sistema nervioso central. [78] [79] [80] La anfetamina y otras drogas dopaminérgicas también aumentan la potencia de salida a niveles fijos de esfuerzo percibido al anular un "interruptor de seguridad", lo que permite que el límite de temperatura central aumente para acceder a una capacidad de reserva que normalmente está fuera de los límites. [79] [81] [82] En dosis terapéuticas, los efectos adversos de la anfetamina no impiden el rendimiento atlético; [74] [78] sin embargo, en dosis mucho más altas, la anfetamina puede inducir efectos que perjudican gravemente el rendimiento, como la rápida degradación muscular y la temperatura corporal elevada . [83] [78]
Formularios disponibles
La lisdexanfetamina está disponible como sal de dimesilato en forma de cápsulas orales y tabletas masticables . [7] Una dosis de 50 mg de dimesilato de lisdexanfetamina es aproximadamente equimolar a una dosis de 20 mg de sulfato de dextroanfetamina o a 15 mg de base libre de dextroanfetamina en términos de la cantidad de dextroanfetamina contenida. [13] [84] [85] Las cápsulas de lisdexanfetamina se pueden tragar intactas, o se pueden abrir y mezclar en agua, yogur o puré de manzana y consumir de esa manera. [7] [86]
Contraindicaciones
La lisdexanfetamina farmacéutica está contraindicada en personas con hipersensibilidad a los productos de anfetamina o a cualquiera de los ingredientes inactivos de la formulación . [7] También está contraindicada en pacientes que han usado un inhibidor de la monoaminooxidasa (IMAO) en los últimos 14 días. [7] [87] Los productos de anfetamina están contraindicados por la Administración de Alimentos y Medicamentos de los Estados Unidos (USFDA) en personas con antecedentes de abuso de drogas , enfermedad cardíaca o agitación o ansiedad graves, o en aquellos que actualmente experimentan arteriosclerosis , glaucoma , hipertiroidismo o hipertensión grave . [88] Sin embargo, una declaración de consenso europea sobre el TDAH en adultos señaló que los estimulantes no empeoran el abuso de sustancias en adultos con TDAH y trastorno por consumo de sustancias comórbido y no deben evitarse en estos individuos. [89] En cualquier caso, la declaración señaló que los estimulantes de liberación inmediata deben evitarse en aquellos con TDAH y trastorno por consumo de sustancias y que las formulaciones estimulantes de liberación más lenta como OROSSistema de administración oral con liberación controlada por ósmosis Se debe preferir el metilfenidato (Concerta) y la lisdexanfetamina debido a su menor potencial de mal uso. [89] La información de prescripción aprobada por la Administración Australiana de Productos Terapéuticos contraindica además la anorexia . [90]
Efectos adversos
Los productos que contienen lisdexanfetamina tienen un perfil de seguridad comparable al de los que contienen anfetamina . [19] Los principales efectos secundarios de la lisdexanfetamina en ensayos clínicos a corto plazo (incidencia ≥5%) han incluido disminución del apetito , insomnio , sequedad de boca , pérdida de peso , irritabilidad , dolor abdominal superior , náuseas , vómitos , diarrea , estreñimiento , aumento de la frecuencia cardíaca , ansiedad , mareos y sensación de nerviosismo . [7] [15] Las tasas de efectos secundarios pueden variar en adultos, adolescentes y niños. [7] Los efectos secundarios raros pero graves de la lisdexanfetamina pueden incluir manía , muerte cardíaca súbita en aquellos con problemas cardíacos subyacentes , psicosis estimulante y síndrome serotoninérgico . [15] [7]
Interacciones
- Agentes acidificantes : Los fármacos o alimentos que acidifican la orina, como el ácido ascórbico , aumentan la excreción urinaria de dextroanfetamina, disminuyendo así la vida media y la eficacia de la dextroanfetamina en el organismo. [7] [88]
- Agentes alcalinizantes : Los medicamentos o alimentos que alcalinizan la orina, como el bicarbonato de sodio , disminuyen la excreción urinaria de dextroanfetamina, aumentando así la vida media y la eficacia de la dextroanfetamina en el cuerpo. [7] [88]
- Inhibidores del CYP2D6 : La hidroxilación a través de la enzima citocromo P450 CYP2D6 es la principal vía metabólica de la dextroanfetamina. [91] Los inhibidores potentes del CYP2D6, como la paroxetina , la fluoxetina , el bupropión y la duloxetina , entre otros, pueden inhibir el metabolismo de la dextroanfetamina y, por lo tanto, aumentar la exposición a ella. [91] [7] Actualmente, faltan estudios que caractericen esta posible interacción. [91] El uso concomitante de lisdexanfetamina con inhibidores del CYP2D6 puede aumentar el riesgo de síndrome serotoninérgico debido a una mayor exposición al fármaco. [7]
- Inhibidores de la monoaminooxidasa : el uso concomitante de IMAO y estimulantes del sistema nervioso central como la lisdexanfetamina puede causar una crisis hipertensiva. [7]
Farmacología
Mecanismo de acción
Farmacodinamia de la anfetamina en una neurona dopaminérgica a través de AADC La anfetamina entra en la neurona presináptica a través de la membrana neuronal o a través de DAT . [92] Una vez dentro, se une a TAAR1 o entra en vesículas sinápticas a través de VMAT2 . [92] [93] Cuando la anfetamina entra en vesículas sinápticas a través de VMAT2, colapsa el gradiente de pH vesicular, lo que a su vez hace que la dopamina se libere en el citosol (área de color tostado claro) a través de VMAT2. [93] [94] Cuando la anfetamina se une a TAAR1, reduce la tasa de disparo de la neurona dopaminérgica a través de los canales de potasio rectificadores internos acoplados a proteína G (GIRK) y activa la proteína quinasa A (PKA) y la proteína quinasa C (PKC), que posteriormente fosforilan DAT. [92] [95] [96] La fosforilación de PKA hace que DAT se retire a la neurona presináptica ( internalizar ) y cese el transporte. [92] La DAT fosforilada por PKC puede funcionar a la inversa o, como la DAT fosforilada por PKA , internalizarse y dejar de transportarse. [92] También se sabe que la anfetamina aumenta el calcio intracelular, un efecto que está asociado con la fosforilación de DAT a través de una vía dependiente de CAMKIIα , que a su vez produce un eflujo de dopamina. [97] [98] |
La lisdexanfetamina es un profármaco inactivo que se convierte en el cuerpo en dextroanfetamina, un compuesto farmacológicamente activo que es responsable de la actividad del fármaco. [99] Después de la ingestión oral, la lisdexanfetamina es descompuesta por enzimas en los glóbulos rojos para formar L -lisina , un aminoácido esencial natural, y dextroanfetamina. [7] La vida media de esta conversión es de aproximadamente 1 hora. La conversión de lisdexanfetamina en dextroanfetamina no se ve afectada por el pH gastrointestinal y es poco probable que se vea afectada por alteraciones en los tiempos de tránsito gastrointestinal normales. [7] [100] Los estudios muestran una relación lineal entre la concentración plasmática máxima de dextroanfetamina y la dosis de lisdexanfetamina hasta dosis de lisdexanfetamina de 250 mg. [101]
Los isómeros ópticos de la anfetamina , es decir, dextroanfetamina y levoanfetamina , son agonistas de TAAR1 e inhibidores del transportador de monoamina vesicular 2 que pueden ingresar a las neuronas monoaminérgicas ; [92] [93] esto les permite liberar neurotransmisores monoaminérgicos ( dopamina , noradrenalina y serotonina , entre otros) de sus sitios de almacenamiento en la neurona presináptica , así como prevenir la recaptación de estos neurotransmisores de la hendidura sináptica . [92] [93]
La lisdexanfetamina se desarrolló con el objetivo de proporcionar una larga duración del efecto que sea constante a lo largo del día, con un potencial reducido de abuso. La unión del aminoácido lisina reduce la cantidad relativa de dextroanfetamina disponible en el torrente sanguíneo. Debido a que no hay dextroanfetamina libre presente en las cápsulas de lisdexanfetamina, la dextroanfetamina no se vuelve disponible a través de la manipulación mecánica, como el triturado o la extracción simple. Se necesita un proceso bioquímico relativamente sofisticado para producir dextroanfetamina a partir de lisdexanfetamina. [100] A diferencia de Adderall , que contiene sales de anfetamina en una proporción dextro:levo de 3:1, la lisdexanfetamina es una fórmula de dextroanfetamina de un solo enantiómero . [99] [88] Los estudios realizados muestran que el dimesilato de lisdexanfetamina puede tener un potencial de abuso menor que la dextroanfetamina y un perfil de abuso similar al dietilpropión en dosis aprobadas por la FDA para el tratamiento del TDAH , pero aún tiene un alto potencial de abuso cuando se excede esta dosis en más del 100%. [100]
Farmacocinética

La biodisponibilidad oral de la anfetamina varía con el pH gastrointestinal; [83] se absorbe bien en el intestino y la biodisponibilidad es típicamente del 90%. [103] La anfetamina es una base débil con un p K a de 9,9; [104] en consecuencia, cuando el pH es básico, más del fármaco está en su forma de base libre soluble en lípidos y más se absorbe a través de las membranas celulares ricas en lípidos del epitelio intestinal . [104] [83] Por el contrario, un pH ácido significa que el fármaco está predominantemente en una forma catiónica (sal) soluble en agua y se absorbe menos. [104] Aproximadamente el 20% de la anfetamina que circula en el torrente sanguíneo está unida a las proteínas plasmáticas . [10] Después de la absorción, la anfetamina se distribuye fácilmente en la mayoría de los tejidos del cuerpo, con altas concentraciones en el líquido cefalorraquídeo y el tejido cerebral . [105]
Las vidas medias de los enantiómeros de anfetamina difieren y varían con el pH de la orina. [104] A un pH urinario normal, las vidas medias de la dextroanfetamina y la levoanfetamina son de 9 a 11 horas y de 11 a 14 horas, respectivamente. [104] La orina muy ácida reducirá las vidas medias de los enantiómeros a 7 horas; [105] La orina muy alcalina aumentará las vidas medias hasta 34 horas. [105] Las variantes de liberación inmediata y liberación prolongada de las sales de ambos isómeros alcanzan concentraciones plasmáticas máximas a las 3 y 7 horas después de la dosis respectivamente. [104] La anfetamina se elimina por los riñones , y entre el 30 y el 40 % de la droga se excreta sin cambios a un pH urinario normal. [104] Cuando el pH urinario es básico, la anfetamina está en su forma de base libre, por lo que se excreta menos. [104] Cuando el pH de la orina es anormal, la recuperación urinaria de anfetamina puede variar desde un mínimo de 1% hasta un máximo de 75%, dependiendo principalmente de si la orina es demasiado básica o ácida, respectivamente. [104] Después de la administración oral, la anfetamina aparece en la orina dentro de las 3 horas. [105] Aproximadamente el 90% de la anfetamina ingerida se elimina 3 días después de la última dosis oral. [105]
La lisdexanfetamina es un profármaco de la dextroanfetamina. [13] [106] No es tan sensible al pH como la anfetamina cuando se absorbe en el tracto gastrointestinal. [106] Después de la absorción en el torrente sanguíneo, la lisdexanfetamina es completamente convertida por los glóbulos rojos en dextroanfetamina y el aminoácido L -lisina por hidrólisis a través de enzimas aminopeptidasas indeterminadas . [106] [13] [84] Este es el paso limitante de la velocidad en la bioactivación de la lisdexanfetamina. [13] La vida media de eliminación de la lisdexanfetamina es generalmente inferior a 1 hora. [106] [13] Debido a la conversión necesaria de lisdexanfetamina en dextroanfetamina, los niveles de dextroanfetamina con lisdexanfetamina alcanzan su punto máximo aproximadamente una hora más tarde que con una dosis equivalente de dextroanfetamina de liberación inmediata. [13] [84] Presumiblemente debido a su activación limitada por la velocidad por los glóbulos rojos, la administración intravenosa de lisdexanfetamina muestra un tiempo muy retrasado hasta el pico y niveles máximos reducidos en comparación con la administración intravenosa de una dosis equivalente de dextroanfetamina. [13] La farmacocinética de la lisdexanfetamina es similar independientemente de si se administra por vía oral, intranasal o intravenosa. [13] [84] Por lo tanto, a diferencia de la dextroanfetamina, el uso parenteral no mejora los efectos subjetivos de la lisdexanfetamina. [13] [84] Debido a su comportamiento como profármaco y sus diferencias farmacocinéticas, la lisdexanfetamina tiene una mayor duración del efecto terapéutico que la dextroanfetamina de liberación inmediata y muestra un potencial de mal uso reducido. [13] [84]
CYP2D6 , dopamina β-hidroxilasa (DBH), monooxigenasa que contiene flavina 3 (FMO3), butirato-CoA ligasa (XM-ligasa) y glicina N -aciltransferasa (GLYAT) son las enzimas conocidas por metabolizar la anfetamina o sus metabolitos en humanos. [fuentes 2] La anfetamina tiene una variedad de productos metabólicos excretados, incluyendo 4-hidroxianfetamina , 4-hidroxinorefedrina , 4-hidroxifenilacetona , ácido benzoico , ácido hipúrico , norefedrina y fenilacetona . [104] [107] Entre estos metabolitos, los simpaticomiméticos activos son 4-hidroxianfetamina , [108] 4-hidroxinorefedrina , [109] y norefedrina. [110] Las principales vías metabólicas implican la parahidroxilación aromática, la alfa y beta hidroxilación alifática, la N -oxidación, la N -desalquilación y la desaminación. [104] [111] Las vías metabólicas conocidas, los metabolitos detectables y las enzimas metabolizadoras en humanos incluyen los siguientes:
Vías metabólicas de la anfetamina en humanos [fuentes 2] Para- hidroxilación Para- hidroxilación Para- hidroxilación no identificado Beta- hidroxilación Beta- hidroxilación DBH [nota 3] Desaminación oxidativa Oxidación no identificado Conjugación de glicina Los metabolitos activos primarios de la anfetamina son la 4-hidroxianfetamina y la norefedrina; [107] a un pH urinario normal, alrededor del 30-40% de la anfetamina se excreta sin cambios y aproximadamente el 50% se excreta como metabolitos inactivos (fila inferior). [104] El 10-20% restante se excreta como metabolitos activos. [104] El ácido benzoico es metabolizado por la XM-ligasa en un producto intermedio, benzoil-CoA , que luego es metabolizado por GLYAT en ácido hipúrico. [117] |
Química
La lisdexanfetamina es una anfetamina sustituida con un enlace amida formado por la condensación de la dextroanfetamina con el grupo carboxilato del aminoácido esencial L -lisina . [19] La reacción ocurre con retención de la estereoquímica , por lo que el producto lisdexanfetamina existe como un solo estereoisómero . Hay muchos nombres posibles para la lisdexanfetamina según la nomenclatura de la IUPAC , pero generalmente se la nombra como N -[(2 S )-1-fenil-2-propanil] -L- lisinamida o (2 S )-2,6-diamino- N -[(1 S )-1-metil-2-feniletil]hexanamida . [121] La reacción de condensación ocurre con pérdida de agua:
- ( S ) -Farmacia
2C(CH
3)NUEVA HAMPSHIRE
2 + ( S )- HOOCCH(NH
2)CH
2es
2es
2es
2NUEVA HAMPSHIRE
2 → ( S , S ) -Fosfato de cromo (CCH)
2C(CH
3)NHC(O)CH(NH
2)CH
2es
2es
2es
2NUEVA HAMPSHIRE
2 + H
2Oh
Los grupos funcionales de amina son vulnerables a la oxidación en el aire, por lo que los productos farmacéuticos que los contienen suelen formularse como sales en las que esta fracción se ha protonado . Esto aumenta la estabilidad, la solubilidad en agua y, al convertir un compuesto molecular en un compuesto iónico , aumenta el punto de fusión y, por lo tanto, garantiza un producto sólido. [122] En el caso de la lisdexanfetamina, esto se logra al reaccionar con dos equivalentes de ácido metanosulfónico para producir la sal de di mesilato , un polvo soluble en agua (792 mg mL −1 ) con un color blanco a blanquecino. [7]
- PhCH
2C(CH
3)NHC(O)CH(NH
2)CH
2es
2es
2es
2NUEVA HAMPSHIRE
2 + 2 canales
3ENTONCES
3H → [PhCH
2C(CH
3)NHC(O)CH(NH+
3)CH
2es
2es
2es
2NUEVA HAMPSHIRE+
3] [ES
3ENTONCES−
3]
2
Comparación con otras formulaciones
El dimesilato de lisdexanfetamina es una formulación comercializada que contiene dextroanfetamina. La siguiente tabla compara el fármaco con otros fármacos anfetamínicos.
| droga | fórmula | masa molar [nota 4] | base de anfetamina [nota 5] | base de anfetamina en dosis iguales | Dosis con igual contenido de base [nota 6] | |||||
|---|---|---|---|---|---|---|---|---|---|---|
| (g/mol) | (por ciento) | (Dosis de 30 mg) | ||||||||
| total | base | total | dextro- | levo- | dextro- | levo- | ||||
| sulfato de dextroanfetamina [124] [125] | ( C9H13N ) 2 • H2SO4 | 368,49 | 270.41 | 73,38% | 73,38% | — | 22,0 mg | — | 30,0 mg | |
| sulfato de anfetamina [126] | ( C9H13N ) 2 • H2SO4 | 368,49 | 270.41 | 73,38% | 36,69% | 36,69% | 11,0 mg | 11,0 mg | 30,0 mg | |
| Aderall | 62,57% | 47,49% | 15,08% | 14,2 mg | 4,5 mg | 35,2 mg | ||||
| 25% | sulfato de dextroanfetamina [124] [125] | ( C9H13N ) 2 • H2SO4 | 368,49 | 270.41 | 73,38% | 73,38% | — | |||
| 25% | sulfato de anfetamina [126] | ( C9H13N ) 2 • H2SO4 | 368,49 | 270.41 | 73,38% | 36,69% | 36,69% | |||
| 25% | sacarato de dextroanfetamina [127] | ( C9H13N ) 2 · C6H10O8 | 480,55 | 270.41 | 56,27% | 56,27% | — | |||
| 25% | aspartato de anfetamina monohidrato [128] | ( C9H13N ) • C4H7NO4 • H2O | 286.32 | 135.21 | 47,22% | 23,61% | 23,61% | |||
| dimesilato de lisdexanfetamina [106] | C15H25N3O • ( CH4O3S ) 2 | 455,49 | 135.21 | 29,68% | 29,68% | — | 8,9 mg | — | 74,2 mg | |
| Suspensión de base de anfetamina [129] | C9H13N | 135.21 | 135.21 | 100% | 76,19% | 23,81% | 22,9 mg | 7,1 mg | 22,0 mg | |
Historia
La lisdexanfetamina fue desarrollada por New River Pharmaceuticals, que fue adquirida por Takeda Pharmaceuticals a través de su adquisición de Shire Pharmaceuticals , poco antes de que comenzara a comercializarse. Se desarrolló con la intención de crear una versión de la dextroanfetamina de mayor duración y menos fácil de abusar, ya que el requisito de conversión en dextroanfetamina a través de enzimas en los glóbulos rojos retrasa su inicio de acción, independientemente de la vía de administración. [130]
En febrero de 2007, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) aprobó la lisdexanfetamina para el tratamiento del TDAH. [131] En agosto de 2009, Health Canada aprobó la comercialización de lisdexanfetamina para uso con receta médica. [132]
En enero de 2015, la FDA aprobó la lisdexanfetamina para el tratamiento del trastorno por atracón en adultos. [133]
La FDA dio aprobación provisional a formulaciones genéricas de lisdexanfetamina en 2015. [134] La fecha de vencimiento de la protección de patente de lisdexanfetamina en los EE. UU. fue el 24 de febrero de 2023. [134] La patente canadiense expiró 20 años después de la fecha de presentación del 1 de junio de 2004. [135]
Las cuotas de producción para 2016 en Estados Unidos fueron de 29.750 kg. [136]
Sociedad y cultura
Nombre

Lisdexanfetamina es la Denominación Común Internacional (DCI) y es una contracción de L -lisina - dextroanfetamina . [137]
A partir de noviembre de 2020, la lisdexanfetamina se vende bajo las siguientes marcas: Aduvanz, Elvanse, Juneve, Samexid, Tyvense, Venvanse y Vyvanse. [138]
Investigación
Depresión
La anfetamina se ha utilizado para tratar la depresión a partir de la década de 1930 y se ha descrito como el primer antidepresivo . [139] En estudios clínicos realizados en las décadas de 1970 y 1980, se descubrió que los psicoestimulantes, incluida la anfetamina y el metilfenidato , mejoraban transitoriamente el estado de ánimo en la mayoría de las personas con depresión y aumentaban la activación psicomotora en casi todos los individuos. [140]
Algunos ensayos clínicos que utilizaron lisdexanfetamina como terapia complementaria con un inhibidor selectivo de la recaptación de serotonina (ISRS) o un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) para la depresión resistente al tratamiento indicaron que esto no es más eficaz que el uso de un ISRS o un IRSN solo. [141] Otros estudios indicaron que los psicoestimulantes potenciaban los antidepresivos y se prescribían de forma insuficiente para la depresión resistente al tratamiento. En esos estudios, los pacientes mostraron una mejora significativa en la energía, el estado de ánimo y la actividad psicomotora. [142] Las directrices clínicas recomiendan precaución en el uso de estimulantes para la depresión y los recomiendan solo como agentes complementarios de segunda o tercera línea . [143]
En febrero de 2014, Shire anunció que dos ensayos clínicos en etapa avanzada habían descubierto que Vyvanse no era un tratamiento eficaz para la depresión, y se interrumpió el desarrollo para esta indicación. [144] [145] Un metanálisis de 2018 de ensayos controlados aleatorios de lisdexanfetamina para la potenciación de los antidepresivos en personas con trastorno depresivo mayor (el primero que se realizó) descubrió que la lisdexanfetamina no era significativamente mejor que el placebo para mejorar las puntuaciones de la Escala de calificación de depresión de Montgomery-Åsberg , las tasas de respuesta o las tasas de remisión . [146] Sin embargo, hubo indicios de un pequeño efecto en la mejora de los síntomas depresivos que se acercó a la significación a nivel de tendencia. [146] La lisdexanfetamina fue bien tolerada en el metanálisis. [146] La cantidad de evidencia fue limitada, con solo cuatro ensayos incluidos. [146] En un metanálisis en red posterior de 2022 , la lisdexanfetamina fue significativamente eficaz como complemento antidepresivo para la depresión resistente al tratamiento. [143]
Aunque la lisdexanfetamina ha demostrado una eficacia limitada en el tratamiento de la depresión en ensayos clínicos, un estudio clínico de fase II encontró que la adición de lisdexanfetamina a un antidepresivo mejoraba la disfunción ejecutiva en personas con trastorno depresivo mayor leve pero disfunción ejecutiva persistente. [147] [148]
Notas explicativas
- ^ Los dominios de resultados relacionados con el TDAH con la mayor proporción de resultados significativamente mejorados de la terapia estimulante continua a largo plazo incluyen lo académico (≈55% de los resultados académicos mejoraron), la conducción (100% de los resultados de conducción mejoraron), el uso de drogas no médicas (47% de los resultados relacionados con la adicción mejoraron), la obesidad (≈65% de los resultados relacionados con la obesidad mejoraron), la autoestima (50% de los resultados de autoestima mejoraron) y la función social (67% de los resultados de la función social mejoraron). [32]
Los tamaños de efecto más grandes para las mejoras de los resultados de la terapia estimulante a largo plazo ocurren en los dominios que involucran lo académico (p. ej., promedio de calificaciones , puntajes de pruebas de rendimiento, duración de la educación y nivel educativo), la autoestima (p. ej., evaluaciones del cuestionario de autoestima, número de intentos de suicidio y tasas de suicidio) y la función social (p. ej., puntajes de nominación de pares, habilidades sociales y calidad de las relaciones entre pares, familiares y románticas). [32]
La terapia combinada a largo plazo para el TDAH (es decir, el tratamiento con un estimulante y una terapia conductual) produce tamaños de efecto aún mayores para las mejoras de los resultados y mejora una mayor proporción de resultados en cada dominio en comparación con la terapia estimulante a largo plazo sola. [32] - ^ Las revisiones Cochrane son revisiones sistemáticas metaanalíticas de alta calidad de ensayos controlados aleatorios. [39]
- ^ Se ha demostrado que la 4-hidroxianfetamina se metaboliza en 4-hidroxinorefedrina por la dopamina beta-hidroxilasa (DBH) in vitro y se presume que se metaboliza de manera similar in vivo . [112] [116] La evidencia de estudios que midieron el efecto de las concentraciones séricas de DBH en el metabolismo de la 4-hidroxianfetamina en humanos sugiere que una enzima diferente puede mediar la conversión de 4-hidroxianfetamina en 4-hidroxinorefedrina ; [116] [118] sin embargo, otra evidencia de estudios en animales sugiere que esta reacción es catalizada por la DBH en vesículas sinápticas dentro de las neuronas noradrenérgicas en el cerebro. [119] [120]
- ^ Para lograr uniformidad, las masas molares se calcularon utilizando la calculadora de peso molecular de Lenntech [123] y estaban dentro de 0,01 g/mol de los valores farmacéuticos publicados.
- ^ Porcentaje de base de anfetamina = masa molecular base / masa molecular total . Porcentaje de base de anfetamina para Adderall = suma de los porcentajes de los componentes / 4.
- ^ dosis = (1/porcentaje de base de anfetamina) × factor de escala = (masa molecular total /masa molecular base ) × factor de escala. Los valores de esta columna se escalaron a una dosis de 30 mg de sulfato de dextroanfetamina. Debido a las diferencias farmacológicas entre estos medicamentos (por ejemplo, diferencias en la liberación, absorción, conversión, concentración, diferentes efectos de los enantiómeros, vida media, etc.), los valores enumerados no deben considerarse dosis equipotentes.
Notas de referencia
- ^ ab [45] [46] [50] [47] [52]
- ^ ab [104] [112] [113] [114] [115] [107] [116] [117]
Referencias
- ^ ab "Adderall vs Vyvanse: ¿cuál es la diferencia entre ellos?". Drugs.com . Consultado el 12 de marzo de 2022 .
- ^ ab Goodman DW (mayo de 2010). "Dimesilato de lisdexanfetamina (vyvanse), un profármaco estimulante para el trastorno por déficit de atención e hiperactividad". P & T . 35 (5): 273–287. PMC 2873712 . PMID 20514273.
- ^ "Lista de todos los medicamentos con advertencias de recuadro negro obtenida por la FDA (use los enlaces Descargar resultados completos y Ver consulta)". nctr-crs.fda.gov . FDA . Consultado el 22 de octubre de 2023 .
- ^ "Información sobre el producto australiano Vyanse® (dimesilato de lisdexanfetamina)" (PDF) . Departamento de Salud y Atención a Personas Mayores . Archivado (PDF) del original el 22 de enero de 2023.
- ^ Anvisa (31 de marzo de 2023). "RDC Nº 784 - Listas de Substâncias Entorpecentes, Psicotrópicas, Precursoras e Outras sob Controle Especial" [Resolución del Consejo Colegiado N° 784 - Listas de Sustancias Estupefacientes, Psicotrópicas, Precursoras y Otras Sustancias Bajo Control Especial] (en portugués brasileño). Diário Oficial da União (publicado el 4 de abril de 2023). Archivado desde el original el 3 de agosto de 2023 . Consultado el 3 de agosto de 2023 .
- ^ "Información del producto Vyvanse". Health Canada . 15 de diciembre de 2021 . Consultado el 18 de marzo de 2024 .
- ^ abcdefghijklmnopqrst "Vyvanse- cápsula de dimesilato de lisdexanfetamina; Vyvanse- comprimido de dimesilato de lisdexanfetamina, masticable". DailyMed . 10 de marzo de 2022 . Consultado el 19 de diciembre de 2022 .
- ^ "Lista de medicamentos autorizados a nivel nacional: Principio(s) activo(s): lisdexanfetamina: Número de procedimiento PSUSA/00010289/202002" (PDF) . Ema.europa.eu . Consultado el 12 de marzo de 2022 .
- ^ "Procedimiento descentralizado para el informe de evaluación pública" (PDF) . MHRA. pág. 14. Archivado desde el original (PDF) el 26 de agosto de 2014 . Consultado el 23 de agosto de 2014 .
- ^ ab Wishart DS , Djombou Feunang Y, Guo AC, Lo EJ, Marcu A, Grant JR, et al. "Anfetamina | DrugBank Online". Banco de medicamentos . 5.0.
- ^ ab Millichap JG (2010). "Capítulo 9: Medicamentos para el TDAH". En Millichap JG (ed.). Manual del trastorno por déficit de atención con hiperactividad: guía para el médico sobre el TDAH (2.ª ed.). Nueva York, EE. UU.: Springer. pág. 112. ISBN 978-1-4419-1396-8Tabla 9.2
Formulaciones de dextroanfetamina de medicamentos estimulantes
Dexedrine [Pico: 2-3 h] [Duración: 5-6 h] ...
Adderall [Pico: 2-3 h] [Duración: 5-7 h]
Dexedrine spansules [Pico: 7-8 h] [Duración: 12 h] ...
Adderall XR [Pico: 7-8 h] [Duración: 12 h]
Vyvanse [Pico: 3-4 h] [Duración: 12 h] - ^ ab Brams M, Mao AR, Doyle RL (septiembre de 2008). "Inicio de eficacia de los psicoestimulantes de acción prolongada en el trastorno por déficit de atención e hiperactividad pediátrico". Medicina de posgrado . 120 (3): 69–88. doi :10.3810/pgm.2008.09.1909. PMID 18824827. S2CID 31791162.
El inicio de eficacia fue más temprano para d-MPH-ER a las 0,5 horas, seguido de d, l-MPH-LA a las 1 a 2 horas, MCD a las 1,5 horas, d, l-MPH-OR a las 1 a 2 horas, MAS-XR a las 1,5 a 2 horas, MTS a las 2 horas y LDX a las 2 horas aproximadamente. ... MAS-XR y LDX tienen una larga duración de acción a las 12 horas posteriores a la dosis.
- ^ abcdefghijkl Ermer JC, Pennick M, Frick G (mayo de 2016). "Dimesilato de lisdexanfetamina: administración de profármacos, exposición a la anfetamina y duración de la eficacia". Clinical Drug Investigation . 36 (5): 341–356. doi :10.1007/s40261-015-0354-y. PMC 4823324 . PMID 27021968.
- ^ ab Stahl SM (marzo de 2017). "Lisdexanfetamina". Guía del prescriptor: Psicofarmacología esencial de Stahl (6.ª ed.). Cambridge, Reino Unido: Cambridge University Press. págs. 379–384. ISBN 978-1-108-22874-9.
- ^ abcdefghijk "Monografía sobre dimesilato de lisdexanfetamina para profesionales". Drugs.com . Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud . Consultado el 15 de abril de 2019 .
- ^ Formulario nacional británico: BNF 76 (76.ª edición). Pharmaceutical Press. 2018. págs. 348-349. ISBN 978-0-85711-338-2.
- ^ "Uso de lisdexanfetamina (Vyvanse) durante el embarazo". Drugs.com . Consultado el 16 de abril de 2019 .
- ^ Heal DJ, Smith SL, Gosden J, Nutt DJ (junio de 2013). "Anfetamina, pasado y presente: una perspectiva farmacológica y clínica". Revista de psicofarmacología . 27 (6): 479–496. doi :10.1177/0269881113482532. PMC 3666194 . PMID 23539642.
- ^ abc Blick SK, Keating GM (2007). "Lisdexanfetamina". Medicamentos pediátricos . 9 (2): 129–135, discusión 136–138. doi :10.2165/00148581-200709020-00007. PMID 17407369. S2CID 260863254.
- ^ "La anfetamina para el TDAH de Shire obtiene el respaldo británico". Reuters . 12 de diciembre de 2012 . Consultado el 14 de diciembre de 2023 .
- ^ "Los 300 mejores de 2022". ClinCalc . Archivado desde el original el 30 de agosto de 2024 . Consultado el 30 de agosto de 2024 .
- ^ "Estadísticas de uso de la droga lisdexanfetamina, Estados Unidos, 2013-2022". ClinCalc . Consultado el 30 de agosto de 2024 .
- ^ Drogas de abuso (PDF) . Administración para el Control de Drogas • Departamento de Justicia de los EE. UU. 2017. p. 22 . Consultado el 16 de abril de 2019 .
- ^ Stuhec M, Lukić P, Locatelli I (febrero de 2019). "Eficacia, aceptabilidad y tolerabilidad de la lisdexanfetamina, sales mixtas de anfetamina, metilfenidato y modafinilo en el tratamiento del trastorno por déficit de atención e hiperactividad en adultos: una revisión sistemática y un metanálisis". Anales de farmacoterapia . 53 (2): 121–133. doi :10.1177/1060028018795703. PMID 30117329. S2CID 52019992.
- ^ Carvalho M, Carmo H, Costa VM, Capela JP, Pontes H, Remião F, et al. (Agosto de 2012). "Toxicidad de las anfetaminas: una actualización". Archivos de Toxicología . 86 (8): 1167-1231. Código Bib : 2012ArTox..86.1167C. doi :10.1007/s00204-012-0815-5. PMID 22392347. S2CID 2873101.
- ^ Berman S, O'Neill J, Fears S, Bartzokis G, London ED (octubre de 2008). "Abuso de anfetaminas y anomalías estructurales en el cerebro". Anales de la Academia de Ciencias de Nueva York . 1141 (1): 195–220. doi :10.1196/annals.1441.031. PMC 2769923 . PMID 18991959.
- ^ ab Hart H, Radua J, Nakao T, Mataix-Cols D, Rubia K (febrero de 2013). "Metaanálisis de estudios de imágenes por resonancia magnética funcional sobre inhibición y atención en el trastorno por déficit de atención e hiperactividad: exploración de los efectos específicos de la tarea, de la medicación estimulante y de la edad". JAMA Psychiatry . 70 (2): 185–198. doi : 10.1001/jamapsychiatry.2013.277 . PMID 23247506.
- ^ ab Spencer TJ, Brown A, Seidman LJ, Valera EM, Makris N, Lomedico A, et al. (septiembre de 2013). "Efecto de los psicoestimulantes en la estructura y función cerebral en el TDAH: una revisión bibliográfica cualitativa de estudios de neuroimagen basados en imágenes por resonancia magnética". The Journal of Clinical Psychiatry . 74 (9): 902–917. doi :10.4088/JCP.12r08287. PMC 3801446 . PMID 24107764.
- ^ ab Frodl T, Skokauskas N (febrero de 2012). "Metaanálisis de estudios de resonancia magnética estructural en niños y adultos con trastorno por déficit de atención con hiperactividad indica efectos del tratamiento". Acta Psychiatrica Scandinavica . 125 (2): 114–126. doi : 10.1111/j.1600-0447.2011.01786.x . PMID 22118249. S2CID 25954331.
Las regiones de los ganglios basales como el globo pálido derecho, el putamen derecho y el núcleo caudado se ven afectadas estructuralmente en niños con TDAH. Estos cambios y alteraciones en las regiones límbicas como la corteza cerebral anterior y la amígdala son más pronunciados en poblaciones no tratadas y parecen disminuir con el tiempo desde la infancia hasta la edad adulta. El tratamiento parece tener efectos positivos en la estructura cerebral.
- ^ abcd Huang YS, Tsai MH (julio de 2011). "Resultados a largo plazo con medicamentos para el trastorno por déficit de atención con hiperactividad: estado actual del conocimiento". CNS Drugs . 25 (7): 539–554. doi :10.2165/11589380-000000000-00000. PMID 21699268. S2CID 3449435.
Varios otros estudios,
[97-101]
incluyendo una revisión metaanalítica
[98]
y un estudio retrospectivo,
[97]
sugirieron que la terapia estimulante en la niñez está asociada con un riesgo reducido de uso posterior de sustancias, tabaquismo y trastornos por consumo de alcohol. ... Estudios recientes han demostrado que los estimulantes, junto con los no estimulantes atomoxetina y guanfacina de liberación prolongada, son continuamente efectivos durante más de períodos de tratamiento de 2 años con pocos y tolerables efectos adversos. La eficacia de la terapia a largo plazo incluye no sólo los síntomas principales del TDAH, sino también una mejor calidad de vida y logros académicos. Los efectos adversos a corto plazo más preocupantes de los estimulantes, como la presión arterial y la frecuencia cardíaca elevadas, disminuyeron en los estudios de seguimiento a largo plazo. ... Los datos actuales no respaldan el impacto potencial de los estimulantes en el empeoramiento o desarrollo de tics o abuso de sustancias en la edad adulta. En el estudio de seguimiento más largo (de más de 10 años), el tratamiento de por vida con estimulantes para el TDAH fue eficaz y protector contra el desarrollo de trastornos psiquiátricos adversos.
- ^ abc Millichap JG (2010). "Capítulo 9: Medicamentos para el TDAH". En Millichap JG (ed.). Manual del trastorno por déficit de atención con hiperactividad: guía para el médico sobre el TDAH (2.ª ed.). Nueva York, EE. UU.: Springer. págs. 121–123, 125–127. ISBN 9781441913968Las
investigaciones en curso han proporcionado respuestas a muchas de las preocupaciones de los padres y han confirmado la eficacia y seguridad del uso a largo plazo de la medicación.
- ^ abcde Arnold LE, Hodgkins P, Caci H, Kahle J, Young S (febrero de 2015). "Efecto de la modalidad de tratamiento en los resultados a largo plazo en el trastorno por déficit de atención e hiperactividad: una revisión sistemática". PLOS ONE . 10 (2): e0116407. doi : 10.1371/journal.pone.0116407 . PMC 4340791 . PMID 25714373.
La mayor proporción de resultados mejorados se informó con el tratamiento combinado (83% de los resultados). Entre los resultados significativamente mejorados, los mayores tamaños de efecto se encontraron para el tratamiento combinado. Las mayores mejoras se asociaron con los resultados académicos, de autoestima o de función social.
Figura 3: Beneficio del tratamiento por tipo de tratamiento y grupo de resultados - ^ abc Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 6: Sistemas de proyección amplia: monoaminas, acetilcolina y orexina". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2.ª ed.). Nueva York, EE. UU.: McGraw-Hill Medical. págs. 154-157. ISBN 9780071481274.
- ^ abcdef Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 13: Función cognitiva superior y control conductual". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2.ª ed.). Nueva York, EE. UU.: McGraw-Hill Medical. págs. 318, 321. ISBN 9780071481274.
Las dosis terapéuticas (relativamente bajas) de psicoestimulantes, como el metilfenidato y la anfetamina, mejoran el rendimiento en tareas de memoria de trabajo tanto en sujetos normales como en aquellos con TDAH. ... los estimulantes actúan no sólo sobre la función de la memoria de trabajo, sino también sobre los niveles generales de excitación y, dentro del núcleo accumbens, mejoran la relevancia de las tareas. Por lo tanto, los estimulantes mejoran el rendimiento en tareas que requieren esfuerzo pero son tediosas ... a través de la estimulación indirecta de los receptores de dopamina y noradrenalina. ...
Más allá de estos efectos permisivos generales, la dopamina (que actúa a través de los receptores D1) y la noradrenalina (que actúa en varios receptores) pueden, en niveles óptimos, mejorar la memoria de trabajo y aspectos de la atención. - ^ Bidwell LC, McClernon FJ, Kollins SH (agosto de 2011). "Potenciadores cognitivos para el tratamiento del TDAH". Farmacología, bioquímica y comportamiento . 99 (2): 262–274. doi :10.1016/j.pbb.2011.05.002. PMC 3353150. PMID 21596055 .
- ^ Parker J, Wales G, Chalhoub N, Harpin V (septiembre de 2013). "Los resultados a largo plazo de las intervenciones para el tratamiento del trastorno por déficit de atención con hiperactividad en niños y adolescentes: una revisión sistemática de ensayos controlados aleatorios". Psychology Research and Behavior Management . 6 : 87–99. doi : 10.2147/PRBM.S49114 . PMC 3785407 . PMID 24082796.
Solo un artículo
53
que examinaba los resultados más allá de los 36 meses cumplió con los criterios de revisión. ... Hay evidencia de alto nivel que sugiere que el tratamiento farmacológico puede tener un efecto beneficioso importante sobre los síntomas centrales del TDAH (hiperactividad, falta de atención e impulsividad) en aproximadamente el 80% de los casos en comparación con los controles de placebo, a corto plazo.
- ^ Millichap JG (2010). "Capítulo 9: Medicamentos para el TDAH". En Millichap JG (ed.). Manual del trastorno por déficit de atención con hiperactividad: guía para el médico sobre el TDAH (2.ª ed.). Nueva York, EE. UU.: Springer. págs. 111–113. ISBN 9781441913968.
- ^ "Estimulantes para el trastorno por déficit de atención e hiperactividad". WebMD . Healthwise. 12 de abril de 2010 . Consultado el 12 de noviembre de 2013 .
- ^ Scholten RJ, Clarke M, Hetherington J (agosto de 2005). "La Colaboración Cochrane". Revista Europea de Nutrición Clínica . 59 (Supl 1): S147–S149, discusión S195–S196. doi : 10.1038/sj.ejcn.1602188 . PMID 16052183. S2CID 29410060.
- ^ Castells X, Blanco-Silvente L, Cunill R (agosto de 2018). "Anfetaminas para el trastorno por déficit de atención e hiperactividad (TDAH) en adultos". Base de Datos Cochrane de Revisiones Sistemáticas . 2018 (8): CD007813. doi :10.1002/14651858.CD007813.pub3. PMC 6513464. PMID 30091808 .
- ^ Punja S, Shamseer L, Hartling L, Urichuk L, Vandermeer B, Nikles J, et al. (febrero de 2016). "Anfetaminas para el trastorno por déficit de atención e hiperactividad (TDAH) en niños y adolescentes". Base de datos Cochrane de revisiones sistemáticas . 2016 (2): CD009996. doi :10.1002/14651858.CD009996.pub2. PMC 10329868. PMID 26844979 .
- ^ Osland ST, Steeves TD, Pringsheim T (junio de 2018). "Tratamiento farmacológico para el trastorno por déficit de atención e hiperactividad (TDAH) en niños con trastornos de tics comórbidos". Base de datos Cochrane de revisiones sistemáticas . 2018 (6): CD007990. doi :10.1002/14651858.CD007990.pub3. PMC 6513283. PMID 29944175 .
- ^ ab Giel KE, Bulik CM, Fernandez-Aranda F, Hay P, Keski-Rahkonen A, Schag K, et al. (marzo de 2022). "Trastorno por atracón". Nature Reviews. Disease Primers . 8 (1): 16. doi :10.1038/s41572-022-00344-y. PMC 9793802. PMID 35301358 .
- ^ abcd Heal DJ, Smith SL (junio de 2022). "Perspectivas de nuevos fármacos para tratar el trastorno por atracón: perspectivas desde la psicopatología y la neurofarmacología". Revista de psicofarmacología . 36 (6): 680–703. doi :10.1177/02698811211032475. PMC 9150143 . PMID 34318734.
Los sujetos con trastorno por atracón presentan disminuciones sustanciales en sus vías de recompensa estriatales ventrales y una capacidad reducida para reclutar circuitos de control de impulsos frontocorticales para implementar la restricción dietética. ...
No solo existe una superposición sustancial entre la psicopatología del trastorno por atracón y el TDAH, sino también una clara asociación entre estos dos trastornos. La capacidad de la lisdexanfetamina para reducir la impulsividad y aumentar el control cognitivo en el TDAH respalda la hipótesis de que la eficacia en el trastorno por atracón depende del tratamiento de sus conductas obsesivas, compulsivas e impulsivas centrales.
- ^ abcde McElroy SL (2017). "Tratamientos farmacológicos para el trastorno por atracón". The Journal of Clinical Psychiatry . 78 Suppl 1: 14–19. doi :10.4088/JCP.sh16003su1c.03. PMID 28125174.
Se han encontrado polimorfismos genéticos asociados con la señalización dopaminérgica anormal en individuos que presentan un comportamiento de atracones, y los episodios de atracones, que a menudo implican el consumo de alimentos muy sabrosos, estimulan aún más el sistema dopaminérgico. Esta estimulación continua puede contribuir a alteraciones progresivas en la señalización de la dopamina. Se plantea la hipótesis de que la lisdexanfetamina reduce el comportamiento de atracones al normalizar la actividad dopaminérgica. ...
Después de 12 semanas, ambos estudios encontraron reducciones significativas en el número de días de atracones por semana en el grupo de tratamiento activo en comparación con placebo (P < .001 para ambos estudios; Figura 1). También se encontró que la lisdexanfetamina era superior al placebo en una serie de medidas de resultados secundarios, incluyendo la mejoría global, el cese de los atracones durante 4 semanas y la reducción de los síntomas de atracones obsesivo-compulsivos, el peso corporal y los triglicéridos.
- ^ abcd Rodan SC, Bryant E, Le A, Maloney D, Touyz S, McGregor IS, et al. (julio de 2023). "Farmacoterapia, terapias alternativas y complementarias para los trastornos alimentarios: hallazgos de una revisión rápida". Journal of Eating Disorders . 11 (1): 112. doi : 10.1186/s40337-023-00833-9 . PMC 10327007 . PMID 37415200.
La LDX se usa comúnmente en el tratamiento del TDAH y es el único tratamiento para el trastorno por atracón que actualmente está aprobado por la Administración de Alimentos y Medicamentos (FDA) y la Administración de Productos Terapéuticos (TGA). La LDX, como todos los estimulantes anfetamínicos, tiene efectos supresores directos del apetito que pueden ser terapéuticamente útiles en el trastorno por atracón, aunque las neuroadaptaciones a largo plazo en los sistemas dopaminérgico y noradrenérgico causadas por la LDX también pueden ser relevantes, lo que lleva a una mejor regulación de las conductas alimentarias, los procesos de atención y las conductas dirigidas a objetivos. ...
Evidentemente, existe un volumen sustancial de ensayos con evidencia de alta calidad que respalda la eficacia de la LDX en la reducción de la frecuencia de los atracones en el tratamiento de adultos con trastorno por atracón moderado a grave a dosis de 50 a 70 mg/día.
- ^ abcde Boswell RG, Potenza MN, Grilo CM (enero de 2021). "La neurobiología del trastorno por atracón en comparación con la obesidad: implicaciones para la terapéutica diferencial". Terapéutica clínica . 43 (1): 50–69. doi :10.1016/j.clinthera.2020.10.014. PMC 7902428 . PMID 33257092.
Los medicamentos estimulantes pueden ser especialmente eficaces para las personas con trastorno por atracón debido a sus efectos duales sobre los sistemas de recompensa y función ejecutiva. De hecho, la única farmacoterapia aprobada por la FDA para el trastorno por atracón es la LDX, un profármaco de d-anfetamina. ...
En humanos, los ECA encontraron que la LDX redujo los atracones y los síntomas de impulsividad/compulsividad. Cabe destacar que existe una fuerte correlación entre los síntomas de compulsividad y la gravedad/frecuencia de los episodios de atracones observados en los ensayos con LDX. Además, en individuos con trastorno por atracón, los cambios en los sistemas cerebrales prefrontales asociados con el tratamiento con LDX se relacionaron con el resultado del tratamiento.
- ^ abcd Berry MD, Gainetdinov RR, Hoener MC, Shahid M (diciembre de 2017). "Farmacología de los receptores humanos asociados a aminas traza: oportunidades y desafíos terapéuticos". Farmacología y terapéutica . 180 : 161–180. doi : 10.1016/j.pharmthera.2017.07.002 . PMID 28723415.
- ^ Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Capítulo 14: Función cognitiva superior y control conductual". Neurofarmacología molecular: una base para la neurociencia clínica (3.ª ed.). Nueva York: McGraw-Hill Medical. ISBN 9780071827706.
Debido a que las respuestas conductuales en los seres humanos no están dictadas rígidamente por las entradas y los impulsos sensoriales, las respuestas conductuales pueden guiarse en cambio de acuerdo con objetivos a corto o largo plazo, la experiencia previa y el contexto ambiental. La respuesta a un postre de aspecto delicioso es diferente dependiendo de si una persona está sola mirando su refrigerador, está en una cena formal a la que asiste su jefe puntilloso, o acaba de formular el objetivo de perder 10 libras. ...
Las respuestas adaptativas dependen de la capacidad de inhibir respuestas automáticas o prepotentes (p. ej., comer vorazmente el postre o huir de la serpiente) dados ciertos contextos sociales o ambientales o metas elegidas y, en esas circunstancias, seleccionar respuestas más apropiadas. En condiciones en las que las respuestas prepotentes tienden a dominar el comportamiento, como en la adicción a las drogas, donde las señales de las drogas pueden provocar la búsqueda de la droga (Capítulo 16), o el trastorno por déficit de atención con hiperactividad (TDAH; descrito a continuación), pueden resultar consecuencias negativas significativas. - ^ abcdefg Schneider E, Higgs S, Dourish CT (diciembre de 2021). "Lisdexanfetamina y trastorno por atracón: una revisión sistemática y un metaanálisis de los datos preclínicos y clínicos con un enfoque en el mecanismo de acción del fármaco en el tratamiento del trastorno" (PDF) . Neuropsicofarmacología europea . 53 : 49–78. doi :10.1016/j.euroneuro.2021.08.001. PMID 34461386.
Nuestro metaanálisis de los cuatro conjuntos de datos de ECA (Guerdjikova et al., 2016; McElroy et al., 2015b; McElroy et al., 2016a) mostró un efecto significativo general de LDX en el cambio de los síntomas de atracones. ...
El trastorno por atracón se ha descrito como un trastorno del control de los impulsos, ya que uno de los síntomas clave del trastorno es la falta de control sobre la alimentación (American Psychiatric Association, 2013) y es posible que la LDX pueda ser eficaz en el tratamiento del trastorno por atracón, al menos en parte, al reducir la impulsividad, la compulsividad y la naturaleza repetitiva de los atracones. Existe amplia evidencia de que la pérdida del control de los impulsos en el trastorno por atracón es un factor causal en la provocación de los síntomas de atracones (Colles et al., 2008; Galanti et al., 2007; Giel et al., 2017; McElroy et al., 2016a; Nasser et al., 2004; Schag et al., 2013). Más específicamente, el trastorno por atracón se asocia con la impulsividad motora y la impulsividad no planificada, que podrían iniciar y mantener los atracones (Nasser et al., 2004). Los estudios de neuroimagen que utilizan la tarea Stroop para medir el control de los impulsos han demostrado que los pacientes con trastorno por atracón tienen una actividad fMRI BOLD disminuida en las áreas cerebrales involucradas en la autorregulación y el control de los impulsos, incluyendo VMPFC, giro frontal inferior (IFG) e ínsula durante la ejecución de la tarea en comparación con los controles delgados y obesos (Balodis et al., 2013b). ...
Es concebible que en pacientes con trastorno por atracón una dosis baja de 30 mg de LDX podría reducir la ingesta de alimentos suprimiendo el apetito o mejorando la saciedad y dosis más altas (50 y 70 mg) del fármaco pueden tener un doble efecto supresor sobre la ingesta de alimentos y la frecuencia de los atracones.
- ^ Branis NM, Wittlin SD (2015). "Análogos similares a las anfetaminas en la diabetes: acelerando hacia la cetogénesis". Informes de casos en endocrinología . 2015 : 917869. doi : 10.1155/2015/917869 . PMC 4417573. PMID 25960894. La concentración periférica de noradrenalina también aumenta. Como se demostró después de
la administración de dextroanfetamina, la noradrenalina plasmática puede aumentar hasta 400 pg/ml, un nivel comparable al alcanzado durante la actividad física leve. Es probable que se produzca un efecto acumulativo en la concentración de noradrenalina cuando se administran medicamentos de tipo anfetamínico en el contexto de una enfermedad aguda o combinados con actividades que conducen a la liberación de catecolaminas, como el ejercicio. ... El efecto principal de la noradrenalina en la cetogénesis está mediado por una mayor disponibilidad de sustrato. Como lo demostraron Krentz et al., en concentraciones fisiológicas altas, la noradrenalina induce una lipólisis acelerada y aumenta significativamente la formación de NEFA. En segundo lugar, la noradrenalina estimula la cetogénesis directamente a nivel de los hepatocitos. Como informaron Keller et al., la infusión de noradrenalina aumentó la concentración de cuerpos cetónicos en mayor grado en comparación con la concentración de NEFA (155 ± 30 versus 57 ± 16 %), lo que sugiere un efecto cetogénico hepático directo.
- ^ Muratore AF, Attia E (julio de 2022). "Manejo psicofarmacológico de los trastornos alimentarios". Current Psychiatry Reports . 24 (7): 345–351. doi :10.1007/s11920-022-01340-5. PMC 9233107 . PMID 35576089.
Un ensayo clínico aleatorizado doble ciego de 11 semanas examinó los efectos de tres dosis de lisdexanfetamina (30 mg/día, 50 mg/día, 70 mg/día) y placebo sobre la frecuencia de los atracones. Los resultados indicaron que las dosis de 50 mg y 70 mg fueron superiores al placebo para reducir los atracones. Dos ECA de seguimiento de 12 semanas confirmaron la superioridad de las dosis de 50 y 70 mg frente al placebo para mejorar los atracones y las medidas de resultados secundarios, incluidos los síntomas obsesivo-compulsivos, el peso corporal y la mejoría global. ... Estudios posteriores de lisdexanfetamina brindaron más respaldo a la seguridad y eficacia del medicamento y brindaron evidencia adicional de que el uso continuo puede ser mejor que el placebo para prevenir las recaídas. Si bien se considera seguro y eficaz, el perfil de efectos secundarios de la lisdexanfetamina y el riesgo de uso indebido pueden hacer que no sea adecuado para ciertos pacientes.
- ^ Mahlios J, De la Herrán-Arita AK, Mignot E (octubre de 2013). "La base autoinmune de la narcolepsia". Opinión actual en neurobiología . 23 (5): 767–773. doi :10.1016/j.conb.2013.04.013. PMC 3848424 . PMID 23725858.
- ^ abc Barateau L, Pizza F, Plazzi G, Dauvilliers Y (agosto de 2022). "Narcolepsia". Revista de investigación del sueño . 31 (4): e13631. doi :10.1111/jsr.13631. PMID 35624073.
La narcolepsia tipo 1 se denominaba "narcolepsia con cataplejía" antes de 2014 (AASM, 2005), pero pasó a denominarse NT1 en la tercera y última clasificación internacional de los trastornos del sueño (AASM, 2014). ... Un nivel bajo de Hcrt-1 en el LCR es muy sensible y específico para el diagnóstico de NT1. ...
Todos los pacientes con niveles bajos de Hcrt-1 en LCR se consideran pacientes NT1, incluso si no informan cataplejía (en alrededor del 10-20% de los casos), y todos los pacientes con niveles normales de Hcrt-1 en LCR (o sin cataplejía cuando no se realiza la punción lumbar) como pacientes NT2 (Baumann et al., 2014). ...
En pacientes con NT1, la ausencia de Hcrt conduce a la inhibición de regiones que suprimen el sueño REM, permitiendo así la activación de vías descendentes que inhiben las neuronas motoras, lo que lleva a la cataplejía.
- ^ abcdefgh Mignot EJ (octubre de 2012). "Una guía práctica para la terapia de los síndromes de narcolepsia e hipersomnia". Neurotherapeutics . 9 (4): 739–752. doi :10.1007/s13311-012-0150-9. PMC 3480574 . PMID 23065655.
A nivel fisiopatológico, ahora está claro que la mayoría de los casos de narcolepsia con cataplejía, y una minoría de casos (5-30 %) sin cataplejía o con síntomas atípicos similares a la cataplejía, son causados por una falta de hipocretina (orexina) de probable origen autoinmune. En estos casos, una vez establecida la enfermedad, la mayoría de las 70.000 células productoras de hipocretina han sido destruidas y el trastorno es irreversible. ...
Las anfetaminas son excepcionalmente promotoras del estado de vigilia y, en dosis altas, también reducen la cataplejía en pacientes narcolépticos, un efecto que se explica mejor por su acción sobre las sinapsis adrenérgicas y serotoninérgicas. ...
El isómero D es más específico para la transmisión de DA y es un compuesto estimulante mejor. Algunos efectos sobre la cataplejía (especialmente para el isómero L), secundarios a los efectos adrenérgicos, ocurren en dosis más altas. ...
Numerosos estudios han demostrado que el aumento de la liberación de dopamina es la propiedad principal que explica la promoción del estado de vigilia, aunque los efectos de la noradrenalina también contribuyen.
- ^ ab Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Capítulo 10: Control neural y neuroendocrino del medio interno". Neurofarmacología molecular: una base para la neurociencia clínica (3.ª ed.). Nueva York: McGraw-Hill Medical. págs. 456–457. ISBN 9780071827706Más recientemente ,
se descubrió que el hipotálamo lateral también desempeña un papel central en la excitación. Las neuronas de esta región contienen cuerpos celulares que producen los péptidos orexina (también llamados hipocretina) (Capítulo 6). Estas neuronas se proyectan ampliamente por todo el cerebro y están involucradas en el sueño, la excitación, la alimentación, la recompensa, aspectos de la emoción y el aprendizaje. De hecho, se cree que la orexina promueve la alimentación principalmente al promover la excitación. Las mutaciones en los receptores de orexina son responsables de la narcolepsia en un modelo canino, la eliminación del gen de la orexina produce narcolepsia en ratones y los humanos con narcolepsia tienen niveles bajos o nulos de péptidos de orexina en el líquido cefalorraquídeo (Capítulo 13). Las neuronas del hipotálamo lateral tienen conexiones recíprocas con neuronas que producen neurotransmisores monoamínicos (Capítulo 6).
- ^ abc Malenka RC, Nestler EJ, Hyman SE, Holtzman DM (2015). "Capítulo 13: Sueño y despertar". Neurofarmacología molecular: una base para la neurociencia clínica (3.ª ed.). McGraw-Hill Medical. pág. 521. ISBN 9780071827706El ARAS consta de varios circuitos diferentes ,
incluidas las cuatro vías monoaminérgicas principales analizadas en el Capítulo 6. La vía de la noradrenalina se origina en el LC y los núcleos relacionados del tronco encefálico; las neuronas serotoninérgicas se originan también en el RN dentro del tronco encefálico; las neuronas dopaminérgicas se originan en el área tegmental ventral (VTA); y la vía histaminérgica se origina en neuronas en el núcleo tuberomamilar (TMN) del hipotálamo posterior. Como se analiza en el Capítulo 6, estas neuronas se proyectan ampliamente por todo el cerebro desde grupos restringidos de cuerpos celulares. La noradrenalina, la serotonina, la dopamina y la histamina tienen funciones moduladoras complejas y, en general, promueven la vigilia. El PT en el tronco encefálico también es un componente importante del ARAS. La actividad de las neuronas colinérgicas del PT (células REM-on) promueve el sueño REM, como se señaló anteriormente. Durante la vigilia, las células REM activas son inhibidas por un subconjunto de neuronas de noradrenalina y serotonina ARAS llamadas células REM desactivadas.
- ^ Shneerson JM (2009). Medicina del sueño: una guía sobre el sueño y sus trastornos (2.ª ed.). John Wiley & Sons. pág. 81. ISBN 9781405178518Todas las anfetaminas aumentan la actividad en las sinapsis de
dopamina, noradrenalina y 5HT. Provocan la liberación presináptica de transmisores preformados y también inhiben la recaptación de dopamina y noradrenalina. Estas acciones son más prominentes en el sistema activador reticular ascendente del tronco encefálico y la corteza cerebral.
- ^ ab Schwartz JR, Roth T (2008). "Neurofisiología del sueño y la vigilia: ciencia básica e implicaciones clínicas". Neurofarmacología actual . 6 (4): 367–378. doi :10.2174/157015908787386050. PMC 2701283. PMID 19587857. El
estado de alerta y la excitación cortical y del prosencéfalo asociadas están mediadas por varias vías ascendentes con componentes neuronales distintos que se proyectan desde el tronco encefálico superior cerca de la unión de la protuberancia y el mesencéfalo. ...
Las poblaciones celulares clave de la vía ascendente de excitación incluyen neuronas colinérgicas, noradrenérgicas, serotoninérgicas, dopaminérgicas e histaminérgicas ubicadas en el núcleo tegmental pedunculopontino y laterodorsal (PPT/LDT), el locus coeruleus, el núcleo del rafe dorsal y medio y el núcleo tuberomamilar (TMN), respectivamente. ...
El mecanismo de acción de los fármacos de alerta simpaticomiméticos (p. ej., dextro- y metanfetamina, metilfenidato) es la estimulación directa o indirecta de los núcleos dopaminérgicos y noradrenérgicos, lo que a su vez aumenta la eficacia del área gris periacueductal ventral y el locus coeruleus, ambos componentes de la rama secundaria del sistema ascendente de excitación. ...
Los fármacos simpaticomiméticos se han utilizado durante mucho tiempo para tratar la narcolepsia .
- ^ abcde Maski K, Trotti LM, Kotagal S, Robert Auger R, Rowley JA, Hashmi SD, et al. (septiembre de 2021). "Tratamiento de los trastornos centrales de la hipersomnia: una guía de práctica clínica de la Academia Estadounidense de Medicina del Sueño". Revista de Medicina Clínica del Sueño . 17 (9): 1881–1893. doi :10.5664/jcsm.9328. PMC 8636351. PMID 34743789. El
TF identificó 1 ECA doble ciego, 1 ECA simple ciego y 1 serie de casos retrospectiva observacional a largo plazo autoinformada que evaluaban la eficacia de la dextroanfetamina en pacientes con narcolepsia tipo 1 y narcolepsia tipo 2. Estos estudios demostraron mejoras clínicamente significativas en la somnolencia diurna excesiva y la cataplejía.
- ^ abcd Barateau L, Lopez R, Dauvilliers Y (octubre de 2016). "Manejo de la narcolepsia". Opciones actuales de tratamiento en neurología . 18 (10): 43. doi :10.1007/s11940-016-0429-y. PMID 27549768.
La utilidad de las anfetaminas está limitada por un riesgo potencial de abuso y sus efectos adversos cardiovasculares (Tabla 1). Es por eso que, aunque son más baratas que otros medicamentos y eficientes, siguen siendo una terapia de tercera línea en la narcolepsia. Tres estudios de clase II mostraron una mejoría del EDS en esa enfermedad. ...
A pesar del potencial de abuso o tolerancia de drogas usando estimulantes, los pacientes con narcolepsia rara vez muestran adicción a su medicación. ...
Algunos estimulantes, como el mazindol, las anfetaminas y el pitolisant, también pueden tener algunos efectos anticatapléjicos.
- ^ Dauvilliers Y, Barateau L (agosto de 2017). "Narcolepsia y otras hipersomnias centrales". Continuum . 23 (4, Neurología del sueño): 989–1004. doi :10.1212/CON.0000000000000492. PMID 28777172.
Ensayos clínicos y guías de práctica recientes han confirmado que los estimulantes como el modafinilo, el armodafinilo o el oxibato de sodio (como primera línea); el metilfenidato y el pitolisant (como segunda línea [pitolisant actualmente solo está disponible en Europa]); y las anfetaminas (como tercera línea) son medicamentos apropiados para la somnolencia diurna excesiva.
- ^ Thorpy MJ, Bogan RK (abril de 2020). "Actualización sobre el tratamiento farmacológico de la narcolepsia: mecanismos de acción e implicaciones clínicas". Medicina del sueño . 68 : 97–109. doi :10.1016/j.sleep.2019.09.001. PMID 32032921.
Los primeros agentes utilizados para tratar el SED (es decir, anfetaminas, metilfenidato) ahora se consideran opciones de segunda o tercera línea porque se han desarrollado medicamentos más nuevos con mejor tolerabilidad y menor potencial de abuso (p. ej., modafinilo/armodafinilo, solriamfetol, pitolisant)
- ^ ab Spencer RC, Devilbiss DM, Berridge CW (junio de 2015). "Los efectos potenciadores cognitivos de los psicoestimulantes implican una acción directa en la corteza prefrontal". Psiquiatría biológica . 77 (11): 940–950. doi :10.1016/j.biopsych.2014.09.013. PMC 4377121 . PMID 25499957.
Las acciones procognitivas de los psicoestimulantes solo se asocian con dosis bajas. Sorprendentemente, a pesar de casi 80 años de uso clínico, la neurobiología de las acciones procognitivas de los psicoestimulantes solo se ha investigado sistemáticamente recientemente. Los hallazgos de esta investigación demuestran inequívocamente que los efectos potenciadores cognitivos de los psicoestimulantes implican la elevación preferencial de las catecolaminas en la corteza prefrontal y la posterior activación de los receptores de noradrenalina α2 y dopamina D1. ... Esta modulación diferencial de los procesos dependientes de la corteza prefrontal en función de la dosis parece estar asociada con la participación diferencial de los receptores noradrenérgicos α2 frente a los α1. En conjunto, esta evidencia indica que en dosis bajas y clínicamente relevantes, los psicoestimulantes carecen de las acciones conductuales y neuroquímicas que definen a esta clase de fármacos y, en cambio, actúan en gran medida como potenciadores cognitivos (mejorando la función dependiente de la corteza prefrontal). ... En particular, tanto en animales como en humanos, las dosis más bajas mejoran al máximo el rendimiento en pruebas de memoria de trabajo e inhibición de la respuesta, mientras que la supresión máxima de la conducta manifiesta y la facilitación de los procesos de atención se produce en dosis más altas.
- ^ Ilieva IP, Hook CJ, Farah MJ (junio de 2015). "Efectos de los estimulantes recetados en el control inhibitorio saludable, la memoria de trabajo y la memoria episódica: un metaanálisis". Journal of Cognitive Neuroscience . 27 (6): 1069–1089. doi :10.1162/jocn_a_00776. PMID 25591060. S2CID 15788121.
Específicamente, en un conjunto de experimentos limitados a diseños de alta calidad, encontramos una mejora significativa de varias habilidades cognitivas. ... Los resultados de este metaanálisis ... confirman la realidad de los efectos de mejora cognitiva para adultos sanos normales en general, al tiempo que indican que estos efectos son de tamaño modesto.
- ^ Bagot KS, Kaminer Y (abril de 2014). "Eficacia de los estimulantes para la mejora cognitiva en jóvenes sin trastorno por déficit de atención e hiperactividad: una revisión sistemática". Adicción . 109 (4): 547–557. doi :10.1111/add.12460. PMC 4471173 . PMID 24749160.
Se ha demostrado que la anfetamina mejora la consolidación de la información (0,02 ≥ P ≤ 0,05), lo que conduce a una mejor recuperación.
- ^ Devous MD, Trivedi MH, Rush AJ (abril de 2001). "Respuesta del flujo sanguíneo cerebral regional a la exposición oral a anfetaminas en voluntarios sanos". Journal of Nuclear Medicine . 42 (4): 535–542. PMID 11337538.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). "Capítulo 10: Control neural y neuroendocrino del medio interno". En Sydor A, Brown RY (eds.). Neurofarmacología molecular: una base para la neurociencia clínica (2.ª ed.). Nueva York, EE. UU.: McGraw-Hill Medical. pág. 266. ISBN 9780071481274
La dopamina actúa en el núcleo accumbens para otorgar significado motivacional a los estímulos asociados con la recompensa
. - ^ abc Wood S, Sage JR, Shuman T, Anagnostaras SG (enero de 2014). "Psicoestimulantes y cognición: un continuo de activación conductual y cognitiva". Pharmacological Reviews . 66 (1): 193–221. doi :10.1124/pr.112.007054. PMC 3880463 . PMID 24344115.
- ^ Twohey M (26 de marzo de 2006). "Las pastillas se convierten en una ayuda de estudio adictiva". JS Online . Archivado desde el original el 15 de agosto de 2007. Consultado el 2 de diciembre de 2007 .
- ^ Teter CJ, McCabe SE, LaGrange K, Cranford JA, Boyd CJ (octubre de 2006). "Uso ilícito de estimulantes específicos sujetos a prescripción médica entre estudiantes universitarios: prevalencia, motivos y vías de administración". Farmacoterapia . 26 (10): 1501–1510. doi :10.1592/phco.26.10.1501. PMC 1794223 . PMID 16999660.
- ^ Weyandt LL, Oster DR, Marraccini ME, Gudmundsdottir BG, Munro BA, Zavras BM, et al. (septiembre de 2014). "Intervenciones farmacológicas para adolescentes y adultos con TDAH: medicamentos estimulantes y no estimulantes y uso indebido de estimulantes recetados". Psychology Research and Behavior Management . 7 : 223–249. doi : 10.2147/PRBM.S47013 . PMC 4164338 . PMID 25228824.
El uso indebido de estimulantes recetados se ha convertido en un problema grave en los campus universitarios de los EE. UU. y también se ha documentado recientemente en otros países. ... De hecho, un gran número de estudiantes afirman haber participado en el uso no médico de estimulantes recetados, lo que se refleja en las tasas de prevalencia de por vida del uso indebido de estimulantes recetados que van del 5% a casi el 34% de los estudiantes.
- ^ Clemow DB, Walker DJ (septiembre de 2014). "El potencial de uso indebido y abuso de medicamentos en el TDAH: una revisión". Medicina de posgrado . 126 (5): 64–81. doi :10.3810/pgm.2014.09.2801. PMID 25295651. S2CID 207580823.
En general, los datos sugieren que el uso indebido y el desvío de medicamentos para el TDAH son problemas de atención médica comunes para los medicamentos estimulantes, con una prevalencia que se cree que es aproximadamente del 5% al 10% de los estudiantes de secundaria y del 5% al 35% de los estudiantes universitarios, según el estudio.
- ^ abc Liddle DG, Connor DJ (junio de 2013). "Suplementos nutricionales y ayuda ergogénica". Atención primaria: clínicas en la práctica de oficina . 40 (2): 487–505. doi : 10.1016/j.pop.2013.02.009. PMID 23668655.
Las anfetaminas y la cafeína son estimulantes que aumentan el estado de alerta, mejoran la concentración, disminuyen el tiempo de reacción y retrasan la fatiga, lo que permite una mayor intensidad y duración del entrenamiento ...
Efectos fisiológicos y de rendimiento
• Las anfetaminas aumentan la liberación de dopamina/norepinefrina e inhiben su recaptación, lo que conduce a la estimulación del sistema nervioso central (SNC)
• Las anfetaminas parecen mejorar el rendimiento atlético en condiciones anaeróbicas 39 40
• Tiempo de reacción mejorado
• Mayor fuerza muscular y fatiga muscular retrasada
• Mayor aceleración
• Mayor estado de alerta y atención a la tarea
- ^ Westfall DP, Westfall TC (2010). "Agonistas simpaticomiméticos diversos". En Brunton LL, Chabner BA, Knollmann BC (eds.). Goodman & Gilman's Pharmacological Basis of Therapeutics (12.ª ed.). Nueva York, EE. UU.: McGraw-Hill. ISBN 9780071624428.
- ^ Bracken NM (enero de 2012). «Estudio nacional sobre las tendencias de consumo de sustancias entre los estudiantes-atletas universitarios de la NCAA» (PDF) . Publicaciones de la NCAA . Asociación Nacional de Atletismo Universitario. Archivado (PDF) del original el 9 de octubre de 2022. Consultado el 8 de octubre de 2013 .
- ^ Docherty JR (junio de 2008). "Farmacología de los estimulantes prohibidos por la Agencia Mundial Antidopaje (AMA)". British Journal of Pharmacology . 154 (3): 606–622. doi :10.1038/bjp.2008.124. PMC 2439527 . PMID 18500382.
- ^ abcd Parr JW (julio de 2011). "Trastorno por déficit de atención con hiperactividad y el deportista: nuevos avances y comprensión". Clinics in Sports Medicine . 30 (3): 591–610. doi :10.1016/j.csm.2011.03.007. PMID 21658550.
En 1980, Chandler y Blair
47
demostraron aumentos significativos en la fuerza de extensión de la rodilla, la aceleración, la capacidad anaeróbica, el tiempo hasta el agotamiento durante el ejercicio, las frecuencias cardíacas previas al ejercicio y máximas, y el tiempo hasta el agotamiento durante la prueba de consumo máximo de oxígeno (VO2 máx.) después de la administración de 15 mg de dextroanfetamina frente a placebo. La mayor parte de la información para responder a esta pregunta se ha obtenido en la última década a través de estudios sobre la fatiga en lugar de un intento de investigar sistemáticamente el efecto de los fármacos para el TDAH en el ejercicio.
- ^ abc Roelands B, de Koning J, Foster C, Hettinga F, Meeusen R (mayo de 2013). "Determinantes neurofisiológicos de los conceptos teóricos y mecanismos implicados en el ritmo". Medicina deportiva . 43 (5): 301–311. doi :10.1007/s40279-013-0030-4. PMID 23456493. S2CID 30392999.
En temperaturas ambientales altas, las manipulaciones dopaminérgicas mejoran claramente el rendimiento. La distribución de la potencia de salida revela que después de la inhibición de la recaptación de dopamina, los sujetos pueden mantener una mayor potencia de salida en comparación con el placebo. ... Los fármacos dopaminérgicos parecen anular un interruptor de seguridad y permitir a los atletas utilizar una capacidad de reserva que está "fuera de los límites" en una situación normal (placebo).
- ^ Parker KL, Lamichhane D, Caetano MS, Narayanan NS (octubre de 2013). "Disfunción ejecutiva en la enfermedad de Parkinson y déficits de sincronización". Frontiers in Integrative Neuroscience . 7 : 75. doi : 10.3389/fnint.2013.00075 . PMC 3813949 . PMID 24198770.
Las manipulaciones de la señalización dopaminérgica influyen profundamente en la sincronización del intervalo, lo que lleva a la hipótesis de que la dopamina influye en la actividad del marcapasos interno o "reloj". Por ejemplo, la anfetamina, que aumenta las concentraciones de dopamina en la hendidura sináptica, adelanta el inicio de la respuesta durante la sincronización del intervalo, mientras que los antagonistas de los receptores de dopamina de tipo D2 suelen ralentizar la sincronización;... El agotamiento de dopamina en voluntarios sanos altera la sincronización, mientras que la anfetamina libera dopamina sináptica y acelera la sincronización.
- ^ Rattray B, Argus C, Martin K, Northey J, Driller M (marzo de 2015). "¿Es hora de dirigir nuestra atención hacia los mecanismos centrales de las estrategias y el rendimiento de recuperación posterior al esfuerzo?". Frontiers in Physiology . 6 : 79. doi : 10.3389/fphys.2015.00079 . PMC 4362407 . PMID 25852568.
Además de tener en cuenta el rendimiento reducido de los participantes con fatiga mental, este modelo racionaliza la RPE reducida y, por lo tanto, el rendimiento mejorado en la prueba contrarreloj de ciclismo de los atletas que usan un enjuague bucal de glucosa (Chambers et al., 2009) y la mayor producción de potencia durante una prueba contrarreloj de ciclismo con RPE igualado después de la ingestión de anfetaminas (Swart, 2009). ... Se sabe que los fármacos estimulantes de la dopamina mejoran aspectos del rendimiento deportivo (Roelands et al., 2008)
- ^ Roelands B, De Pauw K, Meeusen R (junio de 2015). "Efectos neurofisiológicos del ejercicio en el calor". Scandinavian Journal of Medicine & Science in Sports . 25 (Suppl 1): 65–78. doi : 10.1111/sms.12350 . PMID 25943657. S2CID 22782401.
Esto indica que los sujetos no sintieron que estaban produciendo más potencia y, en consecuencia, más calor. Los autores concluyeron que el "interruptor de seguridad" o los mecanismos existentes en el cuerpo para prevenir efectos nocivos son anulados por la administración del fármaco (Roelands et al., 2008b). En conjunto, estos datos indican fuertes efectos ergogénicos de una mayor concentración de DA en el cerebro, sin ningún cambio en la percepción del esfuerzo.
- ^ abc "Adderall XR: cápsula de sulfato de dextroanfetamina, sacarato de dextroanfetamina, sulfato de anfetamina y aspartato de anfetamina, liberación prolongada". DailyMed . Shire US Inc. 17 de julio de 2019 . Consultado el 22 de diciembre de 2019 .
- ^ abcdefgh Dolder PC, Strajhar P, Vizeli P, Hammann F, Odermatt A, Liechti ME (2017). "Farmacocinética y farmacodinamia de la lisdexanfetamina en comparación con la D-anfetamina en sujetos sanos". Front Pharmacol . 8 : 617. doi : 10.3389/fphar.2017.00617 . PMC 5594082 . PMID 28936175.
La lisdexanfetamina inactiva se convierte completamente (>98%) en su metabolito activo D-anfetamina en la circulación (Pennick, 2010; Sharman y Pennick, 2014). Cuando se hace un uso indebido de la lisdexanfetamina por vía intranasal o intravenosa, la farmacocinética es similar a la del uso oral (Jasinski y Krishnan, 2009b; Ermer et al., 2011), y los efectos subjetivos no se potencian con la administración parenteral en contraste con la D-anfetamina (Lile et al., 2011), lo que reduce el riesgo de uso indebido parenteral de la lisdexanfetamina en comparación con la D-anfetamina. El uso intravenoso de lisdexanfetamina también produjo aumentos significativamente menores en el "gusto por la droga" y los "efectos estimulantes" en comparación con la D-anfetamina en los usuarios de sustancias intravenosas (Jasinski y Krishnan, 2009a).
- ^ "Elvanse Adultos 30mg Cápsulas Duras" . Consultado el 26 de febrero de 2022 .
2. Composición cualitativa y cuantitativa. Cápsulas de 30 mg: Cada cápsula contiene 30 mg de lisdexanfetamina dimesilato, equivalente a 8,9 mg de dexanfetamina. Cápsulas de 50 mg: Cada cápsula contiene 50 mg de lisdexanfetamina dimesilato, equivalente a 14,8 mg de dexanfetamina. Cápsulas de 70 mg: Cada cápsula contiene 70 mg de lisdexanfetamina dimesilato, equivalente a 20,8 mg de dexanfetamina.
- ^ Ermer J, Corcoran M, Lasseter K, Martin PT (diciembre de 2016). "Biodisponibilidad relativa de dimesilato de lisdexanfetamina y D-anfetamina en adultos sanos en un estudio abierto, aleatorizado y cruzado después de mezclar dimesilato de lisdexanfetamina con alimentos o bebidas". Ther Drug Monit . 38 (6): 769–776. doi :10.1097/FTD.0000000000000343. PMC 5158093 . PMID 27661399.
- ^ Heedes G, Ailakis J. "Anfetamina (PIM 934)". INCHEM . Programa Internacional de Seguridad Química . Consultado el 24 de junio de 2014 .
- ^ abcd «Adderall XR: cápsula de sulfato de dextroanfetamina, sacarato de dextroanfetamina, sulfato de anfetamina y aspartato de anfetamina, liberación prolongada». DailyMed . 25 de octubre de 2023 . Consultado el 18 de marzo de 2024 .
- ^ ab Kooij JJ, Bijlenga D, Salerno L, Jaeschke R, Bitter I, Balázs J, et al. (febrero de 2019). "Declaración de consenso europea actualizada sobre el diagnóstico y el tratamiento del TDAH en adultos". Psiquiatría europea . 56 : 14–34. doi : 10.1016/j.eurpsy.2018.11.001 . hdl : 10067/1564410151162165141 . PMID 30453134. S2CID 53714228.
- ^ "Tabletas de dexanfetamina". Therapeutic Goods Administration . Consultado el 12 de abril de 2014 .
- ^ abc Schoretsanitis G, de Leon J, Eap CB, Kane JM, Paulzen M (diciembre de 2019). "Interacciones farmacológicas clínicamente significativas con agentes para el trastorno por déficit de atención e hiperactividad". CNS Drugs . 33 (12): 1201–1222. doi :10.1007/s40263-019-00683-7. PMID 31776871. S2CID 208330108.
- ^ abcdefg Miller GM (enero de 2011). "El papel emergente del receptor 1 asociado a trazas de aminas en la regulación funcional de los transportadores de monoaminas y la actividad dopaminérgica". Journal of Neurochemistry . 116 (2): 164–176. doi :10.1111/j.1471-4159.2010.07109.x. PMC 3005101 . PMID 21073468.
- ^ abcd Eiden LE, Weihe E (enero de 2011). "VMAT2: un regulador dinámico de la función neuronal monoaminérgica cerebral que interactúa con drogas de abuso". Anales de la Academia de Ciencias de Nueva York . 1216 (1): 86–98. Bibcode :2011NYASA1216...86E. doi :10.1111/j.1749-6632.2010.05906.x. PMC 4183197 . PMID 21272013.
VMAT2 es el transportador vesicular del SNC no solo para las aminas biógenas DA, NE, EPI, 5-HT y HIS, sino probablemente también para las aminas traza TYR, PEA y tironamina (THYR) ... Las neuronas [traza aminérgicas] en el SNC de los mamíferos serían identificables como neuronas que expresan VMAT2 para almacenamiento y la enzima biosintética descarboxilasa de aminoácidos aromáticos (AADC).
- ^ Sulzer D, Cragg SJ, Rice ME (agosto de 2016). "Neurotransmisión de dopamina estriatal: regulación de la liberación y captación". Ganglios basales . 6 (3): 123–148. doi :10.1016/j.baga.2016.02.001. PMC 4850498. PMID 27141430. A
pesar de los desafíos para determinar el pH de la vesícula sináptica, el gradiente de protones a través de la membrana de la vesícula es de importancia fundamental para su función. La exposición de vesículas de catecolaminas aisladas a protonóforos colapsa el gradiente de pH y redistribuye rápidamente el transmisor desde el interior hacia el exterior de la vesícula. ... La anfetamina y sus derivados como la metanfetamina son compuestos de base débil que son la única clase de drogas ampliamente utilizada que se sabe que provoca la liberación del transmisor mediante un mecanismo no exocítico. Como sustratos tanto para DAT como para VMAT, las anfetaminas pueden llegar al citosol y luego secuestrarse en vesículas, donde actúan para colapsar el gradiente de pH vesicular.
- ^ Ledonne A, Berretta N, Davoli A, Rizzo GR, Bernardi G, Mercuri NB (julio de 2011). "Efectos electrofisiológicos de las aminas traza en las neuronas dopaminérgicas mesencefálicas". Front. Syst. Neurosci . 5 : 56. doi : 10.3389/fnsys.2011.00056 . PMC 3131148 . PMID 21772817.
Recientemente han surgido tres nuevos aspectos importantes de la acción de los TA: (a) inhibición de la activación debido al aumento de la liberación de dopamina; (b) reducción de las respuestas inhibidoras mediadas por los receptores D2 y GABAB (efectos excitatorios debido a la desinhibición); y (c) una activación directa mediada por el receptor TA1 de los canales GIRK que producen hiperpolarización de la membrana celular.
- ^ "TAAR1". GenAtlas . Universidad de París. 28 de enero de 2012 . Consultado el 29 de mayo de 2014 .
• activa tónicamente los canales de K(+) rectificadores internos, lo que reduce la frecuencia de activación basal de las neuronas dopaminérgicas (DA) del área tegmental ventral (VTA)
- ^ Underhill SM, Wheeler DS, Li M, Watts SD, Ingram SL, Amara SG (julio de 2014). "La anfetamina modula la neurotransmisión excitatoria a través de la endocitosis del transportador de glutamato EAAT3 en neuronas dopaminérgicas". Neuron . 83 (2): 404–416. doi :10.1016/j.neuron.2014.05.043. PMC 4159050 . PMID 25033183.
La AMPH también aumenta el calcio intracelular (Gnegy et al., 2004) que está asociado con la activación de calmodulina/CamKII (Wei et al., 2007) y la modulación y el tráfico del DAT (Fog et al., 2006; Sakrikar et al., 2012). ... Por ejemplo, el AMPH aumenta el glutamato extracelular en varias regiones cerebrales, incluido el cuerpo estriado, el ATV y el NAc (Del Arco et al., 1999; Kim et al., 1981; Mora y Porras, 1993; Xue et al., 1996), pero no se ha establecido si este cambio puede explicarse por una mayor liberación sináptica o por una menor eliminación del glutamato. ... La captación de EAAT2 sensible a DHK no se vio alterada por el AMPH (Figura 1A). El transporte de glutamato restante en estos cultivos de mesencéfalo probablemente esté mediado por EAAT3 y este componente se redujo significativamente por el AMPH.
- ^ Vaughan RA, Foster JD (septiembre de 2013). "Mecanismos de regulación del transportador de dopamina en estados normales y patológicos". Trends Pharmacol. Sci . 34 (9): 489–496. doi :10.1016/j.tips.2013.07.005. PMC 3831354 . PMID 23968642.
El AMPH y la metanfetamina también estimulan el eflujo de DA, que se cree que es un elemento crucial en sus propiedades adictivas [80], aunque los mecanismos no parecen ser idénticos para cada droga [81]. Estos procesos dependen de PKCβ y CaMK [72, 82], y los ratones knock-out de PKCβ muestran una disminución del eflujo inducido por AMPH que se correlaciona con una locomoción reducida inducida por AMPH [72].
- ^ ab Wishart DS , Djombou Feunang Y, Guo AC, Lo EJ, Marcu A, Grant JR, et al. "Lisdexanfetamina | DrugBank Online". Banco de medicamentos . 5.0.
- ^ abc Jasinski DR, Krishnan S (junio de 2009). "Abuso de riesgo y seguridad del dimesilato de lisdexanfetamina oral en individuos con antecedentes de abuso de estimulantes". Journal of Psychopharmacology . 23 (4): 419–427. doi :10.1177/0269881109103113. PMID 19329547. S2CID 6138292.
- ^ Ermer J, Homolka R, Martin P, Buckwalter M, Purkayastha J, Roesch B (septiembre de 2010). "Dimesilato de lisdexanfetamina: proporcionalidad lineal de la dosis, baja variabilidad intersujeto e intrasujeto y seguridad en un estudio farmacocinético abierto de dosis única en voluntarios adultos sanos". Journal of Clinical Pharmacology . 50 (9): 1001–1010. doi :10.1177/0091270009357346. PMID 20173084.
- ^ Strajhar P, Vizeli P, Patt M, Dolder PC, Kratschmar DV, Liechti ME, et al. (febrero de 2019). "Efectos de la lisdexanfetamina en las concentraciones plasmáticas de esteroides en comparación con la d-anfetamina en sujetos sanos: un estudio aleatorizado, doble ciego y controlado con placebo" (PDF) . The Journal of Steroid Biochemistry and Molecular Biology . 186 : 212–225. doi :10.1016/j.jsbmb.2018.10.016. PMID 30381248. S2CID 53183893.
- ^ Patel VB, Preedy VR, eds. (2022). Manual sobre abuso de sustancias y adicciones. Cham: Springer International Publishing. pág. 2006. doi :10.1007/978-3-030-92392-1. ISBN 978-3-030-92391-4La anfetamina
se consume habitualmente por vía inhalatoria o por vía oral, ya sea en forma de mezcla racémica (levoanfetamina y dextroanfetamina) o dextroanfetamina sola (Childress et al. 2019). En general, todas las anfetaminas presentan una alta biodisponibilidad cuando se consumen por vía oral, y en el caso específico de la anfetamina, el 90% de la dosis consumida se absorbe en el tracto gastrointestinal, sin diferencias significativas en la velocidad y grado de absorción entre ambos enantiómeros (Carvalho et al. 2012; Childress et al. 2019). El inicio de la acción se produce aproximadamente entre 30 y 45 minutos después del consumo, dependiendo de la dosis ingerida y del grado de pureza o del consumo concomitante de determinados alimentos (Observatorio Europeo de las Drogas y las Toxicomanías 2021a; Steingard et al. 2019). Se describe que aquellas sustancias que promueven la acidificación del tracto gastrointestinal provocan una disminución en la absorción de anfetaminas, mientras que la alcalinización gastrointestinal puede estar relacionada con un aumento en la absorción del compuesto (Markowitz y Patrick 2017).
- ^ abcdefghijklmn "Información de prescripción de Adderall XR" (PDF) . Administración de Alimentos y Medicamentos de los Estados Unidos . Shire US Inc. Diciembre de 2013. págs. 12-13 . Consultado el 30 de diciembre de 2013 .
- ^ abcde "Metabolismo/farmacocinética". Anfetamina. Banco de datos de sustancias peligrosas. Biblioteca Nacional de Medicina de los Estados Unidos – Red de datos toxicológicos. Archivado desde el original el 2 de octubre de 2017 . Consultado el 2 de octubre de 2017 .
La duración del efecto varía según el agente y el pH de la orina. La excreción aumenta en orinas más ácidas. La vida media es de 7 a 34 horas y depende, en parte, del pH de la orina (la vida media es más larga con orina alcalina). ... Las anfetaminas se distribuyen en la mayoría de los tejidos corporales y se producen altas concentraciones en el cerebro y el LCR. La anfetamina aparece en la orina aproximadamente 3 horas después de la administración oral. ... Tres días después de una dosis de (+ o -)-anfetamina, los sujetos humanos habían excretado el 91% del (14)C en la orina.
- ^ abcde "Vyvanse- cápsula de dimesilato de lisdexanfetamina Vyvanse- comprimido masticable de dimesilato de lisdexanfetamina". DailyMed . Shire US Inc. 30 de octubre de 2019 . Consultado el 22 de diciembre de 2019 .
- ^ abc Santagati NA, Ferrara G, Marrazzo A, Ronsisvalle G (septiembre de 2002). "Determinación simultánea de anfetamina y uno de sus metabolitos por HPLC con detección electroquímica". Journal of Pharmaceutical and Biomedical Analysis . 30 (2): 247–255. doi :10.1016/S0731-7085(02)00330-8. PMID 12191709.
- ^ "Resumen de compuestos". p-Hidroxianfetamina. Base de datos de compuestos de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos – Centro Nacional de Información Biotecnológica . Consultado el 15 de octubre de 2013 .
- ^ "Resumen de compuestos". p-Hidroxinorefedrina. Base de datos de compuestos de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos – Centro Nacional de Información Biotecnológica . Consultado el 15 de octubre de 2013 .
- ^ "Resumen de compuestos". Fenilpropanolamina. Base de datos de compuestos de PubChem . Biblioteca Nacional de Medicina de los Estados Unidos – Centro Nacional de Información Biotecnológica . Consultado el 15 de octubre de 2013 .
- ^ "Farmacología y bioquímica". Anfetamina. Base de datos de compuestos de Pubchem . Biblioteca Nacional de Medicina de los Estados Unidos – Centro Nacional de Información Biotecnológica . Consultado el 12 de octubre de 2013 .
- ^ ab Glennon RA (2013). "Estimulantes de fenilisopropilamina: agentes relacionados con las anfetaminas". En Lemke TL, Williams DA, Roche VF, Zito W (eds.). Principios de química medicinal de Foye (7.ª ed.). Filadelfia, EE. UU.: Wolters Kluwer Health/Lippincott Williams & Wilkins. págs. 646–648. ISBN 9781609133450.
La fenilisopropilamina no sustituida más simple, 1-fenil-2-aminopropano, o anfetamina, sirve como una plantilla estructural común para alucinógenos y psicoestimulantes. La anfetamina produce acciones estimulantes centrales, anoréxicas y simpaticomiméticas, y es el miembro prototipo de esta clase (39). ... El metabolismo de fase 1 de los análogos de anfetamina es catalizado por dos sistemas: citocromo P450 y flavina monooxigenasa. ... La anfetamina también puede sufrir hidroxilación aromática a p -hidroxianfetamina. ... La oxidación posterior en la posición bencílica por DA β-hidroxilasa produce p -hidroxinorefedrina. Alternativamente, la oxidación directa de la anfetamina por DA β-hidroxilasa puede producir norefedrina.
- ^ Taylor KB (enero de 1974). "Dopamina-beta-hidroxilasa. Curso estereoquímico de la reacción" (PDF) . Journal of Biological Chemistry . 249 (2): 454–458. doi : 10.1016/S0021-9258(19)43051-2 . PMID 4809526. Consultado el 6 de noviembre de 2014.
La dopamina-β-hidroxilasa catalizó la eliminación del átomo de hidrógeno pro-
R
y la producción de 1-norefedrina, (2
S
, 1
R
)-2-amino-1-hidroxil-1-fenilpropano, a partir de
d
-anfetamina.
- ^ Krueger SK, Williams DE (junio de 2005). "Monooxigenasas que contienen flavina en mamíferos: estructura/función, polimorfismos genéticos y papel en el metabolismo de fármacos". Farmacología y terapéutica . 106 (3): 357–387. doi :10.1016/j.pharmthera.2005.01.001. PMC 1828602 . PMID 15922018.
Tabla 5: Medicamentos que contienen N y xenobióticos oxigenados por FMO - ^ Cashman JR, Xiong YN, Xu L, Janowsky A (marzo de 1999). "N-oxigenación de anfetamina y metanfetamina por la monooxigenasa humana que contiene flavina (forma 3): papel en la bioactivación y la desintoxicación". Revista de farmacología y terapéutica experimental . 288 (3): 1251–1260. PMID 10027866.
- ^ abc Sjoerdsma A, von Studnitz W (abril de 1963). "Actividad de la dopamina-beta-oxidasa en el hombre, utilizando hidroxianfetamina como sustrato". British Journal of Pharmacology and Chemotherapy . 20 (2): 278–284. doi :10.1111/j.1476-5381.1963.tb01467.x. PMC 1703637 . PMID 13977820.
Se administró hidroxianfetamina por vía oral a cinco sujetos humanos ... Dado que la conversión de hidroxianfetamina en hidroxinorefedrina ocurre in vitro por la acción de la dopamina-β-oxidasa, se sugiere un método simple para medir la actividad de esta enzima y el efecto de sus inhibidores en el hombre. ... La falta de efecto de la administración de neomicina a un paciente indica que la hidroxilación ocurre en los tejidos corporales. ... una parte importante de la β-hidroxilación de la hidroxianfetamina se produce en el tejido no suprarrenal. Lamentablemente, en la actualidad no se puede estar completamente seguro de que la hidroxilación de la hidroxianfetamina in vivo se lleve a cabo por la misma enzima que convierte la dopamina en noradrenalina.
- ^ ab Badenhorst CP, van der Sluis R, Erasmus E, van Dijk AA (septiembre de 2013). "Conjugación de glicina: importancia en el metabolismo, el papel de la glicina N-aciltransferasa y factores que influyen en la variación interindividual". Opinión de expertos sobre metabolismo y toxicología de fármacos . 9 (9): 1139–1153. doi :10.1517/17425255.2013.796929. PMID 23650932. S2CID 23738007.
Figura 1. Conjugación de glicina del ácido benzoico. La vía de conjugación de glicina consta de dos pasos. Primero, el benzoato se liga a CoASH para formar el tioéster de benzoil-CoA de alta energía. Esta reacción es catalizada por las ligasas de cadena media de ácido:CoA HXM-A y HXM-B y requiere energía en forma de ATP. ... El benzoil-CoA se conjuga luego con glicina por GLYAT para formar ácido hipúrico, liberando CoASH. Además de los factores enumerados en los recuadros, los niveles de ATP, CoASH y glicina pueden influir en la velocidad general de la vía de conjugación de glicina.
- ^ Horwitz D, Alexander RW, Lovenberg W, Keiser HR (mayo de 1973). "Dopamina-β-hidroxilasa sérica humana. Relación con la hipertensión y la actividad simpática". Circulation Research . 32 (5): 594–599. doi :10.1161/01.RES.32.5.594. PMID 4713201. S2CID 28641000.
La importancia biológica de los diferentes niveles de actividad sérica de DβH se estudió de dos maneras. En primer lugar, se comparó la capacidad in vivo para β-hidroxilar el sustrato sintético hidroxianfetamina en dos sujetos con baja actividad sérica de DβH y dos sujetos con actividad media. ... En un estudio, se administró hidroxianfetamina (Paredrine), un sustrato sintético para DβH, a sujetos con niveles bajos o medios de actividad sérica de DβH. El porcentaje del fármaco hidroxilado a hidroxinorefedrina fue comparable en todos los sujetos (6,5-9,62) (Tabla 3).
- ^ Freeman JJ, Sulser F (diciembre de 1974). "Formación de p-hidroxinorefedrina en el cerebro tras la administración intraventricular de p-hidroxianfetamina". Neurofarmacología . 13 (12): 1187–1190. doi :10.1016/0028-3908(74)90069-0. PMID 4457764.
En especies en las que la hidroxilación aromática de la anfetamina es la principal vía metabólica,
la p
-hidroxianfetamina (POH) y
la p
-hidroxinorefedrina (PHN) pueden contribuir al perfil farmacológico de la droga original. ... La ubicación de las reacciones de
p
-hidroxilación y β-hidroxilación es importante en especies en las que la hidroxilación aromática de la anfetamina es la vía predominante del metabolismo. Tras la administración sistémica de anfetamina a ratas, se ha encontrado POH en la orina y en el plasma.
La falta observada de una acumulación significativa de PHN en el cerebro después de la administración intraventricular de (+)-anfetamina y la formación de cantidades apreciables de PHN a partir de (+)-POH en el tejido cerebral in vivo apoya la opinión de que la hidroxilación aromática de la anfetamina después de su administración sistémica ocurre predominantemente en la periferia, y que luego la POH es transportada a través de la barrera hematoencefálica, captada por las neuronas noradrenérgicas en el cerebro, donde la (+)-POH es convertida en las vesículas de almacenamiento por la dopamina β-hidroxilasa a PHN.
- ^ Matsuda LA, Hanson GR, Gibb JW (diciembre de 1989). "Efectos neuroquímicos de los metabolitos de la anfetamina en los sistemas dopaminérgicos y serotoninérgicos centrales". Journal of Pharmacology and Experimental Therapeutics . 251 (3): 901–908. PMID 2600821.
El metabolismo de
p
-OHA a
p
-OHNor está bien documentado y la dopamina-β hidroxilasa presente en las neuronas noradrenérgicas podría convertir fácilmente
p
-OHA a
p
-OHNor después de la administración intraventricular.
- ^ "Lisdexanfetamina". ChemSpider . Royal Society of Chemistry . 2015 . Consultado el 22 de abril de 2019 .
- ^ Stahl PH, Wermuth DG , eds. (2011). Sales farmacéuticas: propiedades, selección y uso (2.ª ed.). John Wiley & Sons . ISBN 978-3-906390-51-2.
- ^ "Calculadora de peso molecular". Lenntech . Consultado el 19 de agosto de 2015 .
- ^ ab "Sulfato de dextroanfetamina USP". Mallinckrodt Pharmaceuticals. Marzo de 2014. Consultado el 19 de agosto de 2015 .
- ^ ab "Sulfato de D-anfetamina". Tocris. 2015. Consultado el 19 de agosto de 2015 .
- ^ ab "Sulfato de anfetamina USP". Mallinckrodt Pharmaceuticals. Marzo de 2014. Consultado el 19 de agosto de 2015 .
- ^ "Dextroamphetamine Saccharate". Mallinckrodt Pharmaceuticals. Marzo de 2014. Consultado el 19 de agosto de 2015 .
- ^ "Aspartato de anfetamina". Mallinckrodt Pharmaceuticals. Marzo de 2014. Consultado el 19 de agosto de 2015 .
- ^ Mattingly G (mayo de 2010). "Dimesilato de lisdexanfetamina: un profármaco estimulante para el tratamiento del TDAH en niños y adultos". Espectros del sistema nervioso central . 15 (5): 315–325. doi :10.1017/S1092852900027541. PMID 20448522. S2CID 46435024.
- ^ "Paquete de aprobación de medicamentos: Vyvanse (dimesilato de lisdexanfetamina) NDA n.º 021977". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) . Consultado el 18 de marzo de 2024 .
- ^ "Base resumida de la decisión (SBD) para Vyvanse". Health Canada . 10 de junio de 2010 . Consultado el 18 de marzo de 2024 .
- ^ "La FDA amplía los usos de Vyvanse para tratar el trastorno por atracón". Administración de Alimentos y Medicamentos de Estados Unidos (FDA) (Comunicado de prensa). 30 de enero de 2015. Archivado desde el original el 26 de enero de 2018. Consultado el 19 de marzo de 2023 .
- ^ ab "Aprobación provisional" (PDF) . 3 de marzo de 2023. Archivado (PDF) del original el 3 de marzo de 2023. Consultado el 24 de abril de 2022 .
- ^ "Base de datos de patentes canadienses / Base de données sur les brevets canadiens". www.ic.gc.ca. Consultado el 4 de mayo de 2023 .
- ^ "Oficina de Control de Desvíos de la DEA" (PDF) . DEA. Archivado desde el original (PDF) el 27 de mayo de 2016 . Consultado el 7 de noviembre de 2023 .
- ^ Buoli M, Serati M, Cahn W (2016). "Estrategias farmacológicas alternativas para el tratamiento del TDAH en adultos: una revisión sistemática". Expert Review of Neurotherapeutics . 16 (2): 131–144. doi :10.1586/14737175.2016.1135735. PMID 26693882. S2CID 33004517.
- ^ "Marcas internacionales de lisdexanfetamina". Drugs.com. Archivado desde el original el 11 de noviembre de 2020. Consultado el 11 de noviembre de 2020 .
- ^ Rasmussen N (julio de 2006). "Fabricación del primer antidepresivo: la anfetamina en la medicina estadounidense, 1929-1950". J Hist Med Allied Sci . 61 (3): 288–323. doi :10.1093/jhmas/jrj039. PMID 16492800.
- ^ Brown AS, Gershon S (1993). "Dopamina y depresión". J Neural Transm Gen Sect . 91 (2–3): 75–109. doi :10.1007/BF01245227. PMID 8099801.
- ^ Dale E, Bang-Andersen B, Sánchez C (mayo de 2015). "Mecanismos emergentes y tratamientos para la depresión más allá de los ISRS y los IRSN". Farmacología bioquímica . 95 (2): 81–97. doi : 10.1016/j.bcp.2015.03.011 . PMID 25813654.
- ^ Stotz G, Woggon B, Angst J (diciembre de 1999). "Psicoestimulantes en la terapia de la depresión resistente al tratamiento. Revisión de la literatura y hallazgos de un estudio retrospectivo en 65 pacientes deprimidos". Diálogos en neurociencia clínica . 1 (3): 165–174. doi :10.31887/DCNS.1999.1.3/gstotz. PMC 3181580 . PMID 22034135.
- ^ ab Nuñez NA, Joseph B, Pahwa M, Kumar R, Resendez MG, Prokop LJ, et al. (abril de 2022). "Estrategias de aumento para la depresión mayor resistente al tratamiento: una revisión sistemática y un metanálisis en red". Journal of Affective Disorders . 302 : 385–400. doi :10.1016/j.jad.2021.12.134. PMC 9328668 . PMID 34986373. S2CID 245657964.
- ^ Hirschler B (7 de febrero de 2014). "ACTUALIZACIÓN 2: Shire descarta el uso de Vyvanse para la depresión tras ensayos fallidos". Reuters. Archivado desde el original el 10 de marzo de 2016. Consultado el 13 de febrero de 2014 .
- ^ "Lisdexanfetamina - Shionogi/Takeda". Adisinsight.springer.com . Consultado el 12 de marzo de 2022 .
El desarrollo clínico está en marcha en los EE. UU. para los trastornos del estado de ánimo en niños y adolescentes, el trastorno por atracón y el TDAH.
- ^ abcd Giacobbe P, Rakita U, Lam R, Milev R, Kennedy SH, McIntyre RS (enero de 2018). "Eficacia y tolerabilidad de la lisdexanfetamina como estrategia de potenciación de los antidepresivos: un metaanálisis de ensayos controlados aleatorizados". Journal of Affective Disorders . 226 : 294–300. doi :10.1016/j.jad.2017.09.041. PMID 29028590.
- ^ Pan Z, Grovu RC, McIntyre RS (2019). "Estrategias de medicina traslacional en el desarrollo de fármacos para trastornos del estado de ánimo". Medicina traslacional en el desarrollo de fármacos para el sistema nervioso central . Manual de neurociencia conductual. Vol. 29. Elsevier. págs. 333–347. doi :10.1016/B978-0-12-803161-2.00023-0. ISBN . 978-0-12-803161-2. ISSN 1569-7339. S2CID 196561249.
- ^ Madhoo M, Keefe RS, Roth RM, Sambunaris A, Wu J, Trivedi MH, et al. (mayo de 2014). "Aumento de la lisdexanfetamina dimesilato en adultos con disfunción ejecutiva persistente después de la remisión parcial o total del trastorno depresivo mayor". Neuropsicofarmacología . 39 (6): 1388–1398. doi :10.1038/npp.2013.334. PMC 3988542 . PMID 24309905.

