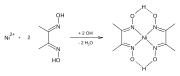
- Reacción de formación de Ni-dmg
- Muestra de Ni(dmgH) 2
- Estructura de la cloro(piridina)cobaloxima
Dimetilglioxima
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC N , N ′ -Dihidroxi-2,3-butanodiimina | |
Otros nombres
| |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| Química biológica |
|
| Araña química | |
| Tarjeta informativa de la ECHA | 100.002.201 |
| Número CE |
|
Identificador de centro de PubChem |
|
| Número RTECS |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C4H8N2O2 | |
| Masa molar | 116,120 g·mol −1 |
| Apariencia | Polvo blanco/blanquecino |
| Densidad | 1,37 g/ cm3 |
| Punto de fusión | 240 a 241 °C (464 a 466 °F; 513 a 514 K) |
| Punto de ebullición | se descompone |
| bajo | |
| Estructura | |
| 0 | |
| Peligros | |
| Seguridad y salud en el trabajo (SST/OHS): | |
Principales peligros | Tóxico, irritante para la piel y los ojos |
| Etiquetado SGA : | |
  | |
| Peligro | |
| H228 , H301 | |
| P210 , P240 , P241 , P264 , P270 , P280 , P301+P310 , P321 , P330 , P370+P378 , P405 , P501 | |
| NFPA 704 (rombo cortafuegos) | |
| Ficha de datos de seguridad (FDS) | Hoja de datos de seguridad externa |
| Compuestos relacionados | |
Compuestos relacionados | Salicilaldoxima de hidroxilamina |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La dimetilglioxima es un compuesto químico descrito por la fórmula CH 3 C(NOH)C(NOH)CH 3 . Su abreviatura es dmgH 2 para la forma neutra, y dmgH − para la forma aniónica, donde H representa el hidrógeno. Este sólido incoloro es el derivado dioxima de la dicetona butano-2,3-diona (también conocida como diacetilo ). El DmgH 2 se utiliza en el análisis del paladio o el níquel . Sus complejos de coordinación son de interés teórico como modelos para enzimas y como catalizadores. Muchos ligandos relacionados se pueden preparar a partir de otras dicetonas, por ejemplo, el bencilo .
Preparación y reacciones
La dimetilglioxima se puede preparar a partir de butanona primero por reacción con nitrito de etilo para dar biacetil monoxima . La segunda oxima se prepara utilizando monosulfonato de hidroxilamina de sodio : [1]
La 2,3-butanodiamina se produce mediante la reducción de dimetilglioxima con hidruro de litio y aluminio . [2]
Complejos
La dimetilglioxima forma complejos con metales como el níquel , [3] el paladio y el cobalto . [4] Estos complejos se utilizan para separar esos cationes de soluciones de sales metálicas y en análisis gravimétricos . También se utiliza en la refinación de metales preciosos para precipitar el paladio de soluciones de cloruro de paladio .
Referencias
- ^ Semon, WL; Damerell, VR (1930). "Dimetilglioxima". Síntesis orgánicas . 10 : 22. doi :10.15227/orgsyn.010.0022.
- ^ Hilleary, Christopher J.; Them, Theodore F.; Tapscott, Robert E. (1980). "Estudios estereoquímicos sobre diastereómeros de tris(2,3-butanediamina)cobalto(III)". Química inorgánica . 19 : 102–107. doi :10.1021/ic50203a022.
- ^ Lev Tschugaeff (1905). "Über ein neues, empfindliches Reagens auf Nickel" [Acerca de un reactivo nuevo y sensible sobre níquel]. Berichte der Deutschen Chemischen Gesellschaft (en alemán). 38 (3): 2520–2522. doi :10.1002/cber.19050380317.
- ^ Girolami, GS; Rauchfuss, TB; Angelici, RJ (1999). Síntesis y técnica en química inorgánica: manual de laboratorio (3.ª ed.). págs. 213-215. ISBN 0-935702-48-2– vía Internet Archive.