Ubenimex
 | |
 | |
| Nombres | |
|---|---|
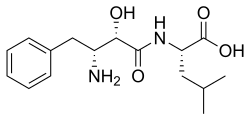
| Nombre IUPAC N -[(2 S ,3 R )-3-amino-2-hidroxi-4-fenilbutanoil] -L -leucina | |
| Nombre sistemático de la IUPAC Ácido (2 S )-2-[(2 S ,3 R )-3-amino-2-hidroxi-4-fenilbutanamido]-4-metilpentanoico | |
| Otros nombres Bestatina; N -[(2 S ,3 R )-3-amino-2-hidroxi-4-fenilbutiril] -L -leucina | |
| Identificadores | |
| |
Modelo 3D ( JSmol ) |
|
| Química biológica | |
| Araña química |
|
| Banco de medicamentos |
|
| Tarjeta informativa de la ECHA | 100.055.917 |
| Número CE |
|
| BARRIL |
|
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C16H24N2O4 | |
| Masa molar | 308,378 g·mol −1 |
| Punto de fusión | 245 °C (473 °F; 518 K) (se descompone) |
| Peligros | |
| Etiquetado SGA : [2] | |
 | |
| Advertencia | |
| H315 , H319 , H335 | |
| P261 , P264 , P271 , P280 , P302+P352 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313 , P337+P313 , P362 , P403+P233 , P405 | |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
Ubenimex ( DCI ), también conocido más comúnmente como bestatina , es un inhibidor de proteasa reversible competitivo . Es un inhibidor de la arginil aminopeptidasa (aminopeptidasa B), [3] leucotrieno A 4 hidrolasa (una metaloproteasa de zinc que muestra actividades tanto de epóxido hidrolasa como de aminopeptidasa ), [4] alanil aminopeptidasa (aminopeptidasa M/N), [5] leucil/cistinil aminopeptidasa (oxitocinasa/vasopresinasa), [6] [7] y dipeptidasa de membrana (leucotrieno D 4 hidrolasa). Se está estudiando para su uso en el tratamiento de la leucemia mielocítica aguda [8] y el linfedema . [9] Se deriva de Streptomyces olivoreticuli . [10] Se ha descubierto que el ubenimex inhibe la degradación enzimática de la oxitocina , la vasopresina , las encefalinas y varios otros péptidos y compuestos. [ cita requerida ]

Véase también
Referencias
- ^ N-((2S,3R)-3-Amino-2-hidroxi-4-fenilbutiril)-L-leucina en Sigma-Aldrich
- ^ "Ubenimex". pubchem.ncbi.nlm.nih.gov . Consultado el 12 de diciembre de 2021 .
- ^ Umezawa, H.; Aoyagi, T.; Suda, H.; Hamada, M.; Takeuchi, T. (1976). "Bestatina, un inhibidor de la aminopeptidasa B, producida por actinomicetos". The Journal of Antibiotics . 29 (29): 97–99. doi : 10.7164/antibiotics.29.97 . PMID 931798.
- ^ Muskardin, DT; Voelkel, NF; Fitzpatrick, FA (1994). "Modulación de la formación de leucotrienos pulmonares y la presión de perfusión por bestatina, un inhibidor de la hidrolasa del leucotrieno A4". Farmacología bioquímica . 48 (48): 131–137. doi :10.1016/0006-2952(94)90232-1. PMID 8043014.
- ^ K Sekine; H Fujii; F Abe (1999). "Inducción de apoptosis por bestatina (ubenimex) en líneas celulares leucémicas humanas". Leucemia . 13 (5): 729–734. doi : 10.1038/sj.leu.2401388 . PMID 10374877.
- ^ Nakanishi Y, Nomura S, Okada M, Ito T, Katsumata Y, Kikkawa F, Hattori A, Tsujimoto M, Mizutani S (2000). "Purificación por inmunoafinidad y caracterización de la leucina aminopeptidasa/oxitocinasa placentaria nativa de la placenta humana". Placenta . 21 (7): 628–34. doi :10.1053/plac.2000.0564. PMID 10985965.
- ^ Naruki M, Mizutani S, Goto K, Tsujimoto M, Nakazato H, Itakura A, Mizuno K, Kurauchi O, Kikkawa F, Tomoda Y (1996). "La oxitocina es hidrolizada por una enzima de la placenta humana que es idéntica a la oxitocinasa del suero del embarazo". Péptidos . 17 (2): 257–61. doi :10.1016/0196-9781(95)02124-8. PMID 8801531. S2CID 28486489.
- ^ Hirayama, Y; Sakamaki, S; Takayanagi, N; Tsuji, Y; Sagawa, T; Chiba, H; Matsunaga, T; Niitsu, Y (2003). "Quimioterapia con ubenimex correspondiente a la edad del paciente y al trastorno orgánico en 18 casos de leucemia mieloide aguda en pacientes ancianos: efectos, complicaciones y supervivencia a largo plazo". Gan a Kagaku Ryoho. Cáncer y quimioterapia . 30 (8): 1113–8. PMID 12938265.
- ^ Tian, W; Rockson, S; Jiang, X; Kim, J; Begaye, A; Shuffle, EM; Tu, AB; Cribb, M; Nepiyushchikh, Z; Feroze, AH; Zamanian, RT; Dhillon, RT; Voelkel, NF; Peters-Golden, M; Kitajewski, J; Dixon, JB; Nicolls, MR (2017). "El antagonismo del leucotrieno B4 mejora el linfedema experimental". Science Translational Medicine . 9 (389): eaal3920. doi : 10.1126/scitranslmed.aal3920 . PMID 28490670.
- ^ Bauvois, B; Dauzonne, D (enero de 2006). "Inhibidores de la aminopeptidasa-N/CD13 (EC 3.4.11.2): química, evaluaciones biológicas y perspectivas terapéuticas". Medicinal Research Reviews . 26 (1): 88–130. doi :10.1002/med.20044. PMC 7168514 . PMID 16216010.
Enlaces externos
- Base de datos en línea MEROPS para peptidasas y sus inhibidores: Bestatin



