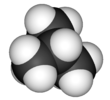
Isobutano
| |||
| |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido 2-Metilpropano [1] | |||
Otros nombres
| |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| 1730720 | |||
| EBICh | |||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.000.780 | ||
| Número CE |
| ||
| Número E | E943b (agentes de recubrimiento, ...) | ||
| 1301 | |||
| BARRIL | |||
Identificador de centro de PubChem |
| ||
| Número RTECS |
| ||
| UNIVERSIDAD | |||
| Número de la ONU | 1969 | ||
Panel de control CompTox ( EPA ) |
| ||
| |||
| Propiedades | |||
| C4H10 | |||
| Masa molar | 58,124 g·mol −1 | ||
| Apariencia | Gas incoloro | ||
| Olor | Inodoro | ||
| Densidad |
| ||
| Punto de fusión | -159,42 °C (-254,96 °F; 113,73 K) [4] | ||
| Punto de ebullición | -11,7 °C (10,9 °F; 261,4 K) [4] | ||
| 48,9 mg⋅L −1 (a 25 °C (77 °F)) [2] | |||
| Presión de vapor | 3,1 atm (310 kPa) (a 21 °C (294 K; 70 °F)) [3] | ||
Constante de la ley de Henry ( k H ) | 8,6 nmol⋅Pa − 1⋅kg −1 | ||
| Ácido conjugado | Isobutanio | ||
| −51,7·10 −6 cm3 / mol | |||
| Termoquímica | |||
Capacidad calorífica ( C ) | 96,65 J⋅K −1 ⋅mol −1 | ||
Entalpía estándar de formación (Δ f H ⦵ 298 ) | −134,8 – −133,6 kJ⋅mol −1 | ||
Entalpía estándar de combustión (Δ c H ⦵ 298 ) | −2,86959 – −2,86841 MJ⋅mol −1 | ||
| Peligros | |||
| Etiquetado SGA : | |||
 | |||
| Peligro | |||
| H220 | |||
| P210 | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | -83 °C (-117 °F; 190 K) | ||
| 460 °C (860 °F; 733 K) | |||
| Límites de explosividad | 1,4–8,3% | ||
| NIOSH (límites de exposición a la salud en EE. UU.): | |||
PEL (Permisible) | Ninguno [5] | ||
REL (recomendado) | TWA 800 ppm (1900 mg/m3 ) [ 5] | ||
IDLH (Peligro inmediato) | En Dakota del Norte [5] | ||
| Ficha de datos de seguridad (FDS) | lindeus.com | ||
| Compuestos relacionados | |||
Alcanos relacionados | Isopentano | ||
| Página de datos complementarios | |||
| Isobutano (página de datos) | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||

El isobutano , también conocido como i -butano , 2-metilpropano o metilpropano , es un compuesto químico con fórmula molecular HC(CH3 ) 3 . Es un isómero del butano . El isobutano es un gas incoloro e inodoro. Es el alcano más simple con un átomo de carbono terciario . El isobutano se utiliza como molécula precursora en la industria petroquímica , por ejemplo en la síntesis de isooctano . [6]
Producción
El isobutano se obtiene por isomerización del butano .

Usos
El isobutano es la principal materia prima en las unidades de alquilación de las refinerías. Con él se generan "combustibles de mezcla" de calidad para gasolina con una alta ramificación para lograr buenas características de combustión. Los productos típicos creados con isobutano son el 2,4-dimetilpentano y, especialmente, el 2,2,4-trimetilpentano . [7]

Solvente
En el proceso de lechada de Chevron Phillips para fabricar polietileno de alta densidad , se utiliza isobutano como diluyente. A medida que se retira el polietileno en lechada, el isobutano se "evapora" y se condensa, y se recicla nuevamente en el reactor de bucle para este propósito. [8]
Precursor deterc-hidroperóxido de butilo
El isobutano se oxida a hidroperóxido de terc -butilo , que posteriormente reacciona con propileno para producir óxido de propileno . El terc-butanol que resulta como subproducto se utiliza normalmente para fabricar aditivos para gasolina, como el metil terc-butil éter (MTBE).
Usos varios
El isobutano también se utiliza como propulsor para aerosoles .
El isobutano se utiliza como parte de combustibles mezclados, especialmente común en los botes de combustible utilizados para acampar . [9]
Refrigerante
El isobutano se utiliza como refrigerante . [10] Su uso en refrigeradores comenzó en 1993 cuando Greenpeace presentó el proyecto Greenfreeze con la antigua empresa de Alemania del Este Foron . [11] [12] En este sentido, las mezclas de "isobutano" puro y seco (R-600a) (es decir, mezclas de isobutano) tienen un potencial insignificante de agotamiento de la capa de ozono y un potencial de calentamiento global muy bajo (tienen un valor de 3,3 veces el GWP del dióxido de carbono) y pueden servir como un reemplazo funcional para el R-12 , R-22 (ambos conocidos comúnmente por la marca registrada Freon ), R-134a y otros refrigerantes clorofluorocarbonados o hidrofluorocarbonados en sistemas convencionales de refrigeración estacionarios y aire acondicionado.
Como refrigerante, el isobutano plantea un riesgo de incendio y explosión, además de los peligros asociados a los refrigerantes CFC no inflamables. La sustitución de este refrigerante en sistemas de aire acondicionado de vehículos de motor que no hayan sido diseñados originalmente para isobutano está ampliamente prohibida o desaconsejada. [13] [14] [15] [16] [17] [18] [19]
Los vendedores y defensores de refrigerantes de hidrocarburos argumentan contra tales prohibiciones con el argumento de que ha habido muy pocos incidentes de ese tipo en relación con el número de sistemas de aire acondicionado de vehículos llenos de hidrocarburos. [20] [21]
Una fuga de isobutano en el sistema de refrigeración de un frigorífico inició el incendio del complejo residencial Valencia 2024 en España , que se cobró 10 vidas. [22]
Nomenclatura
El nombre tradicional isobutano todavía se mantuvo en las recomendaciones de la IUPAC de 1993 , [23] pero ya no se recomienda según las recomendaciones de 2013. [1] Dado que la cadena continua más larga del isobutano contiene solo tres átomos de carbono, el nombre IUPAC preferido es 2-metilpropano, pero el localizador (2-) generalmente se omite en la nomenclatura general por ser redundante; C2 es la única posición en una cadena de propano donde se puede ubicar un sustituyente de metilo sin alterar la cadena principal y formar el isómero constitucional n -butano.
Referencias
- ^ ab Nomenclatura de la química orgánica: recomendaciones de la IUPAC y nombres preferidos 2013 (Libro azul) . Cambridge: The Royal Society of Chemistry . 2014. pág. 652. doi :10.1039/9781849733069-FP001. ISBN . 978-0-85404-182-4Los nombres
'isobutano', 'isopentano' y 'neopentano' ya no se recomiendan.
- ^ "Solubilidad en agua". PubChem . Centro Nacional de Información Biotecnológica . Consultado el 6 de abril de 2017 .
- ^ "CDC - NIOSH Pocket Guide to Chemical Hazards - Isobutane" ( Guía de bolsillo de los CDC y NIOSH sobre los peligros químicos: isobutano) . CDC . Consultado el 28 de diciembre de 2018 .
- ^ ab Registro en la base de datos de sustancias GESTIS del Instituto de Seguridad y Salud Ocupacional
- ^ abc Guía de bolsillo del NIOSH sobre peligros químicos. "#0350". Instituto Nacional de Seguridad y Salud Ocupacional (NIOSH).
- ^ "Patent Watch, 31 de julio de 2006". Archivado desde el original el 11 de marzo de 2007. Consultado el 8 de agosto de 2006 .
- ^ Bipin V. Vora; Joseph A. Kocal; Paul T. Barger; Robert J. Schmidt; James A. Johnson (2003). "Alquilación". Enciclopedia Kirk-Othmer de tecnología química . doi :10.1002/0471238961.0112112508011313.a01.pub2. ISBN 0471238961.
- ^ Kenneth S. Whiteley. "Polietileno". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a21_487.pub2. ISBN 978-3527306732.
- ^ Rietveld, Will (8 de febrero de 2005). "Preguntas frecuentes sobre estufas y combustibles livianos con cartucho" . Backpacking Light (se requiere suscripción) . Consultado el 3 de junio de 2022 .
- ^ "Reunión técnica sobre la eliminación gradual de los HCFC: descripción general de las ventajas y desventajas de las alternativas (Montreal, Canadá; Comisión Europea sobre refrigerantes de reacondicionamiento para aplicaciones estacionarias)" (PDF) . Abril de 2008. Archivado (PDF) desde el original el 2009-08-05 . Consultado el 21 de mayo de 2021 .
- ^ "GreenFreeze". Greenpeace. 15 de marzo de 2010. Archivado desde el original el 5 de octubre de 2010. Consultado el 2 de enero de 2013 .
- ^ Wolfgang Lohbeck (junio de 2004). «Greenfreeze: de una bola de nieve a una avalancha industrial» (PDF) . Consultado el 21 de mayo de 2021 .
- ^ "Preguntas frecuentes de la EPA sobre refrigerantes de hidrocarburos". Epa.gov . Consultado el 29 de octubre de 2010 .
- ^ "Compendio de declaraciones de política sobre hidrocarburos y refrigerantes, octubre de 2006" (PDF) . Archivado desde el original (PDF) el 8 de agosto de 2014. Consultado el 1 de agosto de 2014 .
- ^ "Boletín MACS: uso de refrigerantes de hidrocarburos en vehículos" (PDF) . Archivado desde el original (PDF) el 2011-01-05 . Consultado el 2010-10-29 .
- ^ "Boletín de refrigerantes de hidrocarburos de la Sociedad de Ingenieros Automotrices". Sae.org. 27 de abril de 2005. Archivado desde el original el 5 de mayo de 2005. Consultado el 29 de octubre de 2010 .
- ^ "Boletín del Partido Laborista de Saskatchewan sobre refrigerantes de hidrocarburos en vehículos". Labour.gov.sk.ca. 29 de junio de 2010. Archivado desde el original el 1 de julio de 2009. Consultado el 29 de octubre de 2010 .
- ^ VASA sobre la legalidad y conveniencia de los refrigerantes Archivado el 13 de enero de 2009 en Wayback Machine
- ^ "Advertencia del gobierno de Queensland (Australia) sobre los refrigerantes de hidrocarburos" (PDF) . Energy.qld.gov.au. Archivado desde el original (PDF) el 2008-12-17 . Consultado el 2010-10-29 .
- ^ "Registro parlamentario de Nueva Gales del Sur (Australia), 16 de octubre de 1997". Parliament.nsw.gov.au. 16 de octubre de 1997. Archivado desde el original el 1 de julio de 2009. Consultado el 29 de octubre de 2010 .
- ^ "Registro parlamentario de Nueva Gales del Sur (Australia), 29 de junio de 2000". Parliament.nsw.gov.au. Archivado desde el original el 22 de mayo de 2005. Consultado el 29 de octubre de 2010 .
- ^ Domínguez, Teresa (3 de mayo de 2024). "Una fuga del gas refrigerante de la nevera del piso 86 propició el inicio del incendio de Campanar". Levante-EMV (en español europeo) . Consultado el 15 de octubre de 2024 .
- ^ Panico, R. y Powell, WH, eds. (1994). Una guía para la nomenclatura de compuestos orgánicos de la IUPAC 1993. Oxford: Blackwell Science. ISBN 0-632-03488-2.https://www.acdlabs.com/iupac/nomenclature/93/r93_679.htm
Enlaces externos
- Ficha internacional de seguridad química 0901
- Guía de bolsillo del NIOSH sobre peligros químicos