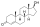Gonane
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC 5ξ-gonano | |
| Nombre sistemático de la IUPAC (3a R ,3b S ,5a Ξ ,9a S ,9b R ,11a S )-Hexadecahidro-1 H -ciclopenta[ a ]fenantreno | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| EBICh | |
| Araña química | |
| BARRIL | |
Identificador de centro de PubChem |
|
Panel de control CompTox ( EPA ) |
|
| |
| Propiedades | |
| C 17 H 28 | |
| Masa molar | 232,411 g·mol −1 |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
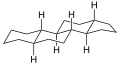
El gonano ( ciclopentanoperhidrofenantreno ) es un compuesto químico con fórmula C
17yo
28, cuya estructura consiste en cuatro anillos de hidrocarburos fusionados entre sí: tres unidades de ciclohexano y un ciclopentano . También puede considerarse como el resultado de la fusión de una molécula de ciclopentano con una molécula completamente hidrogenada de fenantreno , de ahí el nombre más descriptivo " perhidrociclopenta[a]fenantreno ". La versión no sistemática del nombre anterior es "ciclopentanoperhidrofenantreno". [1]
No tiene dobles enlaces, es decir, está completamente saturado y se considera la estructura principal de los esteroides , a menudo denominado núcleo esteroide . [1] Hay muchas formas de gonano, pero solo unas pocas se producen de forma natural en los organismos vivos. Algunas formas comunes incluyen 5α-gonano y 5β-gonano. El estrano , el androstano y el pregnano son derivados del gonano con grupos metilo o etilo adicionales unidos a ciertas posiciones de carbono. El término gonano también se utiliza para describir un grupo de progestinas que son similares al levonorgestrel pero que tienen una estructura ligeramente diferente a la de otras hormonas como los estranos.
Significado
El gonano es un compuesto químico importante en la familia de los esteroides porque su estructura comprende cuatro anillos de hidrocarburos fusionados entre sí, que constan de tres unidades de ciclohexano y un ciclopentano, al que a menudo se hace referencia como el "núcleo esteroide" y sirve como compuesto original de los esteroides.
El descubrimiento del gonano y su papel como núcleo esteroide ha sido fundamental para comprender la estructura y la función de varias hormonas esteroides . La numeración de los anillos esteroides se determina en función de la estructura esquelética del gonano, lo que proporciona un marco para la clasificación e identificación de diferentes esteroides.
Uso del término
El término gonano también se utiliza para referirse a un grupo de progestinas [2] que son derivados de la 19-nortestosterona homologados con carbono 18, incluyendo el levonorgestrel y sus análogos . [3] Este término se utiliza de esta manera para distinguirlos de los estranos , que también son derivados de la 19-nortestosterona. [3]
Estructura
El gonano es un hidrocarburo tetracíclico sin dobles enlaces. Es formalmente el compuesto original de los esteroides , por lo que se le denomina "núcleo esteroide". [1] [4] [5] Algunos derivados importantes del gonano son las hormonas esteroides , caracterizadas por grupos metilo en las posiciones C10 y C13 y una cadena lateral en la posición C17. [5]
Debido a que el gonano tiene seis centros de quiralidad , tiene 64 (2 6 ) estereoisómeros teóricamente posibles , [4] que difieren en la posición de los hidrógenos solitarios en los carbonos 5, 8, 9, 10, 13 y 14 en la dirección perpendicular al plano medio de los carbonos. Sin embargo, solo unos pocos de estos estereoisómeros ocurren en organismos vivos. [4] Los más comunes son el 5α-gonano y el 5β-gonano.
- 5α-gonano
- 5β-gonano
- 5α-Gonane, vista en perspectiva lateral
- 5β-Gonane, vista en perspectiva lateral
Variantes
El estrano (C18) es la variante 13β-metil del gonano, el androstano (C19) es la variante 10β,13β-dimetil del gonano, y el pregnano (C21) es la variante 10β,13β-dimetil, 17β- etilo del gonano. [6] [7]
Referencias
- ^ abc Yang, Yanqing; Krin, Anna; Cai, Xiaoli; Poopari, Mohammad Reza; Zhang, Yuefei; Cheeseman, James R.; Xu, Yunjie (12 de enero de 2023). "Conformaciones de hormonas esteroides: espectroscopia de dicroísmo circular infrarroja y vibracional". Moléculas (Basilea, Suiza) . 28 (2): 771. doi : 10.3390/molecules28020771 . ISSN: 1420-3049. PMC: 9864676. PMID : 36677830.
- ^ Loiseau, Camille; Cayetanot, Florence; Joubert, Fanny; Perrin-Terrin, Anne S.; Cardot, Philippe; Fiamma, Marie N.; Frugiere, Alain; Straus, Christian; Bodineau, Laurence (2018-11-02). "Perspectivas actuales para el uso de fármacos progesteronérgicos gonanos en el tratamiento de los síndromes de hipoventilación central". Neurofarmacología actual . 16 (10): 1433–1454. doi : 10.2174/1570159X15666170719104605 . PMC 6295933 . PMID 28721821.
- ^ ab Edgren, Richard A.; Stanczyk, Frank Z. (diciembre de 1999). "Nomenclatura de las progestinas gonanas". Anticoncepción . 60 (6): 313. doi :10.1016/S0010-7824(99)00101-8. PMID 10715364.
- ^ a b C Burkhard Fugmann; Susanne Lang-Fugmann; Wolfgang Steglich (28 de mayo de 2014). Enciclopedia RÖMPP Productos naturales, 1.ª edición, 2000. Thieme. págs. 1918–. ISBN 9783131795519.OCLC 1389366313 .
- ^ ab Speight, James G. (24 de diciembre de 2010). Manual de procesos industriales de hidrocarburos. Gulf Professional Publishing. pp. 474–. ISBN 9780080942711.OCLC 750151056 .
- ^ D. Sriram (1 de septiembre de 2010). Química medicinal. Pearson Education India. pp. 594–. ISBN 978-81-317-3144-4.
- ^ Etienne-Emile Baulieu; Paul A. Kelly (30 de noviembre de 1990). Hormonas: de las moléculas a la enfermedad. Springer Science & Business Media. pp. 391–. ISBN 978-0-412-02791-8.