Trifluorometanosulfonato de escandio (III)
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC Trifluorometanosulfonato de escandio | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| Araña química | |
| Tarjeta informativa de la ECHA | 100.157.499 |
Identificador de centro de PubChem |
|
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C3F9O9S3Sc | |
| Masa molar | 492,16 g/mol |
| Peligros | |
| Ficha de datos de seguridad (FDS) | Hoja de datos de seguridad de Oxford |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
El trifluorometanosulfonato de escandio , comúnmente llamado triflato de escandio , es un compuesto químico con fórmula Sc(SO 3 CF 3 ) 3 , una sal que consiste en cationes escandio Sc 3+ y triflato SO
3CF−
3 aniones .
El triflato de escandio se utiliza como reactivo en química orgánica como ácido de Lewis . [1] En comparación con otros ácidos de Lewis, este reactivo es estable frente al agua y a menudo se puede utilizar en reacciones orgánicas como un verdadero catalizador en lugar de uno utilizado en cantidades estequiométricas. El compuesto se prepara mediante la reacción del óxido de escandio con ácido trifluorometanosulfónico .
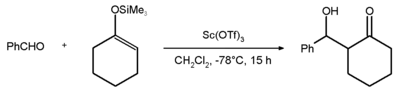
Un ejemplo del uso científico del triflato de escandio es la reacción de adición aldólica de Mukaiyama entre el benzaldehído y el éter enólico silílico de ciclohexanona con un rendimiento del 81% . [2]
Véase también
Referencias
- ^ Deborah Longbottom (1999). "SYNLETT Spotlight 12: Triflato de escandio". Synlett . 1999 (12): 2023. doi : 10.1055/s-1999-5997 .
- ^ S. Kobayashi (1999). "Triflato de escandio en síntesis orgánica". Eur. J. Org. Chem. 1999 : 15–27. doi :10.1002/(SICI)1099-0690(199901)1999:1<15::AID-EJOC15>3.0.CO;2-B. Archivado desde el original el 5 de enero de 2013.