Murexida
 | |
 | |
| Nombres | |
|---|---|
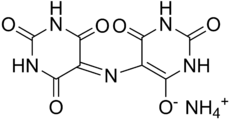
| Nombre IUPAC 2,6-dioxo-5-[(2,4,6-trioxo-5-hexahidropirimidinilideno)amino]-3H - pirimidin-4-olato de amonio | |
| Otros nombres Sal de amonio del ácido purpúrico | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| Araña química | |
| Tarjeta informativa de la ECHA | 100.019.334 |
| Número CE |
|
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C8H8N6O6 | |
| Masa molar | 284,188 g·mol −1 |
| Densidad | 1,72 g/cm 3 (hidrato de sal de amonio) |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
Murexida (NH 4 C 8 H 4 N 5 O 6 , o C 8 H 5 N 5 O 6 ·NH 3 ), también llamada purpurato de amonio o MX , es la sal de amonio del ácido purpúrico . Es un sólido púrpura que es soluble en agua. El compuesto alguna vez se usó como reactivo indicador . [1] Las soluciones acuosas son amarillas a pH bajo , púrpura rojizo en soluciones débilmente ácidas y púrpura azulado en soluciones alcalinas.
Preparación
La murexida se prepara tratando la aloxantina con amoníaco a 100 °C, o tratando el uramilo (ácido 5-aminobarbitúrico) con óxido de mercurio . [2] También se puede preparar digiriendo aloxano con amoníaco alcohólico .
Historia
En la década de 1830 , Justus von Liebig y Friedrich Wöhler , de Giessen (Alemania), habían investigado el producto púrpura, el murexida, obtenido a partir de excrementos de serpiente, pero no se trataba de una materia prima abundante y en esa época no se había establecido un método para utilizarlo como colorante. [3] En la década de 1850, coloristas y productores de tintes franceses, como Depoully en París, lograron fabricar murexida a partir del abundante guano sudamericano y aplicarla a fibras naturales. Luego fue ampliamente adoptada en Gran Bretaña, Francia y Alemania.
Usar
La murexida se utiliza en química analítica como indicador complexométrico para titulaciones complexométricas, con mayor frecuencia de iones de calcio , [4] pero también de cobre , níquel , cobalto , torio y tierras raras . Funciona como un ligando tridentado. [1]
Su uso ha sido eclipsado por los electrodos selectivos de iones de calcio .
Referencias
- ^ ab Martin, Raymond L.; White, Allan H.; Willis, Anthony C. (1977). "Estudios estructurales en complejos metal-purpurato. Parte 1. Estructuras cristalinas del purpurato de potasio trihidrato y del purpurato de amonio monohidrato (murexido)". J. Chem. Soc., Dalton Trans. (14): 1336–1342. doi :10.1039/DT9770001336.
- ^ Alguna información sobre el químico W. N. Hartley está disponible aquí Archivado el 26 de mayo de 2013 en Wayback Machine .
- ^ Peter JT Morris; Anthony S. Travis (noviembre de 1992), "A History of the International Dyestuff Industry", American Dyestuff Reporter , 81 (11), archivado desde el original el 11 de junio de 2007
{{citation}}: CS1 maint: URL no apta ( enlace ) - ^ Lewis, Michael J. (2011). "La medición y la importancia del calcio iónico en la leche: una revisión". Revista internacional de tecnología láctea . 64 : 1–13. doi : 10.1111/j.1471-0307.2010.00639.x .
Este artículo incorpora texto de una publicación que ahora es de dominio público : Chisholm, Hugh , ed. (1911). "Murexide". Encyclopædia Britannica . Vol. 19 (11.ª ed.). Cambridge University Press. pág. 36.



