Dolor fantasma
| Dolor fantasma | |
|---|---|
| Especialidad | Neurología |
El dolor fantasma es una percepción dolorosa que experimenta un individuo en relación con una extremidad o un órgano que no es físicamente parte del cuerpo, ya sea porque fue extirpado o nunca estuvo allí en primer lugar. [1]
Las sensaciones se informan con mayor frecuencia después de la amputación de una extremidad, pero también pueden ocurrir después de la extirpación de un seno , la lengua o un órgano interno. [2] El síndrome del ojo fantasma puede ocurrir después de la pérdida de un ojo. La sensación de dolor y su duración y frecuencia varían de un individuo a otro.
El dolor fantasma debe distinguirse de otras afecciones que pueden presentarse de manera similar, como la sensación de miembro fantasma y el dolor en el miembro residual. La sensación de miembro fantasma es cualquier fenómeno sensorial, excepto el dolor, que se siente en un miembro ausente o en una parte del miembro. [3] Se estima que hasta el 80% de los amputados experimentan sensaciones de miembro fantasma en algún momento de sus vidas. [4] Algunos experimentan algún nivel de esta sensación fantasma en el miembro faltante durante el resto de sus vidas. El dolor del miembro residual, también conocido como dolor del muñón, es una percepción dolorosa que se origina en el miembro residual, o muñón, en sí. [2] Por lo general, es una manifestación de una fuente subyacente, como un traumatismo quirúrgico, la formación de neuromas , una infección o un dispositivo protésico mal ajustado . [5] Aunque se trata de condiciones clínicas diferentes, es más probable que las personas con dolor fantasma también experimenten dolor en el miembro residual de forma concomitante. [6]
El término "miembro fantasma" fue acuñado por primera vez por el neurólogo estadounidense Silas Weir Mitchell en 1871. [7] Mitchell describió que "miles de miembros fantasmas acechaban a muchos buenos soldados, atormentándolos de vez en cuando". [8] Sin embargo, en 1551, el cirujano militar francés Ambroise Paré registró la primera documentación del dolor del miembro fantasma cuando informó que "los pacientes, mucho después de que se realiza la amputación, dicen que todavía sienten dolor en la parte amputada". [8]
Signos y síntomas
El curso sintomático del dolor fantasma es muy variable, pero el inicio suele presentarse dentro de la primera semana después de la amputación. [2] El dolor informado puede ser intermitente y durar segundos a minutos, pero puede ser continuo con exacerbaciones agudas. [9] La duración de los síntomas varía entre individuos, algunos informan una disminución del dolor con el tiempo y otros informan una trayectoria más estable o incluso creciente. [10] Las sensaciones pueden describirse como punzantes, punzantes, opresivas, palpitantes, hormigueantes o ardientes, y a veces se siente como si la parte fantasma estuviera siendo forzada a una posición incómoda. [11]
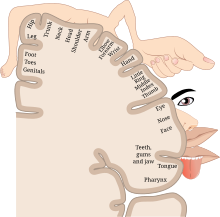
Si bien la sensación a menudo afecta la parte de la extremidad más alejada del cuerpo, como los dedos de las manos o de los pies, otras partes del cuerpo más cercanas al cerebro, como el brazo o la pierna, también pueden experimentar sensaciones similares. [12] Se cree que el dolor fantasma involucra más comúnmente la parte de la extremidad más alejada del cuerpo debido a su mayor representación cortical dentro de la corteza somatosensorial . [13]
En general, las sensaciones pueden ser provocadas por la presión en la parte restante de la extremidad, el estrés emocional o los cambios de temperatura. [14]
Causas
Las personas pueden experimentar dolor fantasma después de una amputación quirúrgica o traumática de una extremidad, la extracción de un órgano o en casos de deficiencia congénita de una extremidad. Se observa con mayor frecuencia después de una amputación, aunque se han informado casos menos frecuentes después de la extirpación de un seno, la lengua o un ojo. [2] El dolor fantasma se observa con mayor frecuencia en adultos mayores en comparación con personas con deficiencia congénita de una extremidad o amputación a una edad temprana. [15] También se ha informado que las personas con antecedentes de dolor crónico, ansiedad o depresión tienen más probabilidades de desarrollar dolor fantasma que aquellas sin estos factores de riesgo. [16]
Fisiopatología
La base neurológica y los mecanismos del dolor fantasma se derivan de teorías y observaciones experimentales. Se sabe poco sobre los verdaderos mecanismos que causan el dolor fantasma, y muchas teorías se superponen en gran medida. Históricamente, se pensaba que los dolores fantasma se originaban en neuromas ubicados en la punta del muñón. [1] Los neuromas traumáticos, o lesiones nerviosas no tumorales, a menudo surgen de cirugías y son el resultado del crecimiento anormal de las fibras nerviosas lesionadas . [11] Aunque los neuromas del muñón pueden contribuir a los dolores fantasma, no son la única causa. La razón es que los pacientes con deficiencia congénita de las extremidades a veces también pueden experimentar dolores fantasma. [15] Este hallazgo sugiere que también hay un mecanismo central responsable de generar sensaciones dolorosas. [17] Actualmente, las teorías se basan en vías neurológicas alteradas y cambios desadaptativos dentro del sistema nervioso periférico , la médula espinal y el cerebro .
Mecanismos periféricos
Los neuromas formados a partir de terminaciones nerviosas lesionadas en el sitio del muñón muestran una mayor expresión del canal de sodio y pueden disparar espontáneamente potenciales de acción anormales . [18] Esta mayor actividad de las fibras Aδ y C , que están involucradas en el dolor y la sensación de temperatura, puede contribuir al dolor fantasma. Sin embargo, se ha observado que el dolor persiste una vez que los neuromas han dejado de disparar potenciales de acción o cuando los nervios periféricos se tratan con agentes bloqueadores de la conducción. [17] Por lo tanto, se cree que el sistema nervioso periférico tiene como máximo un efecto de modulación sobre el dolor del miembro fantasma. [8]
Mecanismos espinales

Además de los mecanismos periféricos, se cree que los mecanismos espinales tienen un papel influyente en el desarrollo del dolor fantasma. La lesión de los nervios periféricos puede conducir a la degeneración de las fibras C en el asta dorsal de la médula espinal, y las fibras A terminales pueden posteriormente ramificarse en la misma lámina. [8] Si esto ocurre, las entradas de las fibras A podrían informarse como estímulos nocivos. La sustancia P , involucrada en la transmisión de señales de dolor, generalmente se expresa por fibras Aδ y C, pero después de un daño en los nervios periféricos, la sustancia P se expresa por fibras Aβ. [8] Esto conduce a la hiperexcitabilidad de la médula espinal, que generalmente ocurre solo en presencia de estímulos nocivos. Estos cambios en las entradas de las fibras nerviosas también pueden conducir a una expansión de los campos receptivos neuronales, de modo que los estímulos previamente no nocivos ahora se interpretan como nocivos. [11] Este proceso de hiperexcitabilidad y cambios en el campo receptivo se conoce ampliamente como sensibilización central . [1] También se sabe que el aumento de la expresión de glutamato y NMDA , junto con la disminución de la inhibición de las neuronas GABAérgicas , contribuye aún más al mecanismo de sensibilización central. [19] Sin embargo, debido a que los pacientes con lesión completa de la médula espinal han experimentado dolor fantasma, también debe haber un mecanismo central subyacente dentro del cerebro.
Mecanismos centrales
En circunstancias normales, el circuito cerebral determinado genéticamente permanece en gran medida estable durante toda la vida. Durante gran parte del siglo XX, se creyó que no se podían formar nuevos circuitos neuronales en el cerebro de los mamíferos adultos, pero los experimentos realizados a partir de la década de 1980 pusieron esto en duda. [17] Por ejemplo, los estudios de resonancia magnética funcional en amputados han demostrado que casi todos los pacientes han experimentado un remapeo cortical . [20] Después de la amputación, el remapeo cortical es el proceso por el cual las áreas de las cortezas somatosensorial y motora primaria que representan la extremidad perdida son invadidas por regiones cercanas. [21] Esto hace que las áreas del cerebro que antes recibían información de la extremidad perdida ahora puedan ser estimuladas por las regiones corticales invasoras cercanas.
La mayoría de los estudios que utilizan la resonancia magnética funcional para investigar la reorganización cortical en humanos se han realizado en amputados de miembros superiores. Después de la pérdida de un brazo, la mayor parte de la reorganización motora se produjo como un desplazamiento hacia abajo del área de la mano de la corteza sobre el área de representación de la cara, especialmente los labios. [21] En individuos con dolor de miembro fantasma, la reorganización fue lo suficientemente grande como para causar un cambio en la representación cortical de los labios en las áreas de la mano solo durante los movimientos de los labios. [17] Además, a medida que aumentaban los dolores fantasma en los amputados de las extremidades superiores, hubo un mayor grado de desplazamiento medial de la representación motora facial. [22] También se ha descubierto que existe una alta correlación entre la gravedad del dolor de miembro fantasma y el grado en que se ha producido la reorganización cortical. [22]
La neuromatriz
La teoría de la neuromatriz, acuñada inicialmente por el psicólogo Ronald Melzack en la década de 1990, propone que existe una red extensa que conecta el tálamo y la corteza, y la corteza y el sistema límbico . [8] Se extiende más allá de la teoría del esquema corporal y propone que la conciencia y la percepción de uno mismo se generan en el cerebro a través de patrones de entrada que pueden modificarse mediante diferentes entradas perceptivas. [23] La red está predeterminada genéticamente y se modifica a lo largo de la vida mediante diversas entradas sensoriales para crear una neurofirma. [24] Es la neurofirma de una parte específica del cuerpo la que determina cómo se percibe conscientemente. [8] Los sistemas de entrada que contribuyen a la neurofirma son principalmente los sistemas somatosensorial , límbico y talamocortical. La teoría de la neuromatriz tiene como objetivo explicar cómo ciertas actividades asociadas con el dolor conducen a la percepción consciente del dolor fantasma. Después de la amputación de una extremidad, los cambios en la neuromatriz y la neurofirma pueden ser la causa del dolor fantasma localizado en la extremidad perdida. [11] El dolor fantasma también puede surgir de una reorganización anormal en la neuromatriz a un estado de dolor preexistente. [25]
La teoría de la neuromatriz se apoya en gran medida en estudios en los que la cordotomía y, por lo tanto, la eliminación de las señales de dolor transmitidas al cerebro, no logran tratar los dolores fantasmas. [26] La oposición a la teoría existe en gran medida porque no logra explicar por qué el alivio de las sensaciones fantasma rara vez elimina los dolores fantasmas. Tampoco aborda cómo las sensaciones pueden terminar espontáneamente y cómo algunos amputados no experimentan sensaciones fantasmas en absoluto. [8] Además, una limitación importante de la teoría de la neuromatriz es que es difícil probarla empíricamente, especialmente cuando se prueban sensaciones fantasmas indoloras. [23]
Diagnóstico
El dolor fantasma es un diagnóstico clínico basado en los signos y síntomas que describe una persona. [2] No existen estudios de laboratorio específicos ni hallazgos de imagen que respalden su diagnóstico. [1] Sin embargo, es importante que un médico realice un examen físico completo para evaluar otras posibles causas del dolor. Se debe realizar una evaluación del miembro residual para inspeccionar si hay signos de infección, formación de bursa o úlceras por presión o lesión de tejido profundo. [2] Si una persona tiene una prótesis, también se debe realizar una evaluación del ajuste y la alineación. Se debe realizar un examen neurológico y musculoesquelético completo, que incluya una evaluación de la fuerza, el rango de movimiento y los reflejos, para descartar cualquier otra causa central o periférica del dolor. [12]
Gestión
Se han utilizado diversos métodos para tratar el dolor del miembro fantasma. Actualmente no existen pautas específicas de tratamiento ni enfoques terapéuticos escalonados. En cambio, el tratamiento implica un enfoque multimodal con una variedad de intervenciones disponibles. [27] Los médicos pueden recetar medicamentos, y se ha demostrado que algunos antidepresivos o antiepilépticos tienen un efecto beneficioso en la reducción del dolor del miembro fantasma. [28] Se han utilizado métodos físicos como masajes ligeros, estimulación eléctrica y terapia de frío y calor con resultados variables. [29] [30]
Existen muchas opciones de tratamiento diferentes para el dolor del miembro fantasma que se están investigando activamente. La mayoría de los tratamientos no tienen en cuenta los mecanismos subyacentes a los dolores fantasma y, por lo tanto, son difíciles de investigar. Sin embargo, hay algunas opciones de tratamiento que han demostrado aliviar el dolor en algunos pacientes, pero estas opciones de tratamiento suelen tener una tasa de éxito de menos del 30 %. [8] Es importante señalar que esta tasa de éxito no supera el efecto placebo .
Medicamento
Las técnicas farmacológicas a menudo se inician solas o junto con otras opciones de tratamiento. Las dosis de analgésicos necesarios a menudo disminuyen sustancialmente cuando se combinan con otras técnicas, pero rara vez se suspenden por completo. El uso de antiepilépticos, como gabapentina , pregabalina y topiramato , ha mostrado resultados mixtos en estudios clínicos. [31] [32] [28] Sin embargo, actualmente no hay ensayos aleatorios de alta calidad que respalden la eficacia de estos medicamentos. Los antidepresivos tricíclicos , como la amitriptilina , se utilizan a menudo para aliviar el dolor crónico y recientemente se han utilizado en un intento de reducir los dolores fantasma. Estudios recientes con amitriptilina tampoco han logrado proporcionar resultados concluyentes y no contradictorios. [33] [34] Se cree que los antagonistas del receptor N-metil-D-aspartato (NMDA), como la ketamina , funcionan revirtiendo el proceso de sensibilización central dentro de la médula espinal, que se ha propuesto como un posible mecanismo para el desarrollo del dolor fantasma. [11] Se ha demostrado que el uso de ketamina reduce el dolor fantasma, pero la memantina , un medicamento de la misma clase, no proporcionó ningún beneficio a los pacientes. [35] [36] El alivio del dolor también se puede lograr mediante el uso de opioides , calcitonina y lidocaína . [8]
Terapia del espejo

La terapia de la caja de espejo es una terapia sencilla y económica para el dolor fantasma que fue inventada por primera vez en la década de 1990 por el neurocientífico Vilayanur S. Ramachandran . Las personas colocan su miembro intacto frente al espejo y lo mueven voluntariamente, lo que les da la visión de que su miembro ausente también se está moviendo. Permite ilusiones de movimiento y tacto en un miembro fantasma al inducir el acoplamiento de la vía motora y somatosensorial entre el miembro fantasma y el real. [23] Muchos pacientes experimentan dolor como resultado de un miembro fantasma apretado, y debido a que los miembros fantasma no están bajo control voluntario, aflojarlos se vuelve imposible. [37] Esta teoría propone que el miembro fantasma se siente paralizado porque no hay retroalimentación del fantasma hacia el cerebro para informarle lo contrario. Ramachandran cree que si el cerebro recibiera retroalimentación visual de que el miembro fantasma se ha movido, entonces el miembro fantasma dejaría de estar paralizado. [37]
.jpg/440px-110613-N-YM336-079_(5880440625).jpg)
Aunque se ha demostrado que el uso de la terapia del espejo es eficaz en algunos casos, todavía no existe una teoría ampliamente aceptada sobre cómo funciona. Según un artículo de 2017 que revisó una amplia gama de estudios que utilizan la terapia del espejo, los pacientes pueden experimentar una reducción de los dolores fantasma después de cuatro semanas de tratamiento. [38] El estudio continúa diciendo que, si bien no se comprende por completo el mecanismo exacto de la terapia del espejo, es una opción segura y económica que los pacientes pueden considerar. [38]
Antes de 2009 se habían publicado pocas investigaciones sobre la terapia del espejo y, desde entonces, gran parte de las investigaciones han sido de baja calidad. [39] De 115 publicaciones entre 2012 y 2017 que investigaron el uso de la terapia del espejo para el dolor fantasma, una revisión de 2018 encontró solo 15 estudios cuyos resultados científicos deberían tenerse en cuenta. A partir de estos 15 estudios, los revisores concluyeron que la terapia del espejo es una herramienta eficaz para reducir tanto la duración como la intensidad del dolor fantasma. [40]
Las teorías actuales sobre cómo la terapia del espejo puede reducir el dolor fantasma provienen en gran medida de estudios que investigan los cambios en el cerebro mediante resonancia magnética funcional. Hay evidencia que muestra una reducción y reversión de la reorganización cortical dentro de la corteza somatosensorial después de la terapia del espejo. [41] Dado que se propone que los cambios desadaptativos dentro de las regiones corticales del cerebro son un mecanismo central del dolor fantasma, se cree que una reversión de esta reorganización alivia el dolor.
Imágenes motoras graduadas
La imaginería motora graduada se desarrolló inicialmente para ayudar a los pacientes que sufrían del síndrome de dolor regional complejo , pero desde entonces se ha ampliado a otras afecciones de dolor crónico, incluido el dolor fantasma. [42] Se cree que el tratamiento funciona de manera similar a la terapia de la caja de espejo, donde se revierte la reorganización cortical desadaptativa y ya no hay una conexión funcional entre el movimiento y el dolor. Una revisión sistemática y un metanálisis recientes respaldaron el uso de la imaginería motora graduada para ayudar a reducir la gravedad del dolor fantasma en los amputados. [43]
Ejecución motora con biofeedback
La ejecución motora fantasma con biorretroalimentación es una intervención terapéutica más reciente que aprovecha la realidad aumentada y virtual . [44] Durante estas sesiones, los pacientes usan gafas de realidad virtual que les permiten visualizar su miembro fantasma como un miembro normal e intacto. Luego pueden participar en diferentes juegos interactivos, como alcanzar y agarrar objetos. Se teoriza que al hacer esto, se produce una "coincidencia" entre los sistemas visual y somatosensorial, lo que puede conducir a una disminución del dolor fantasma. [45] Es importante destacar que, a diferencia de la terapia de caja de espejos convencional, la capacidad de interactuar con juegos de realidad virtual puede aumentar la participación de los pacientes y dar como resultado mejores resultados. [44] Numerosos informes de casos y series de casos han mostrado resultados prometedores, pero es probable que se necesite un análisis más sólido para corroborar estas afirmaciones. [46] [47] [48]
Estimulación cerebral profunda

La estimulación cerebral profunda es una técnica quirúrgica utilizada para aliviar el dolor de los miembros fantasmas en los pacientes. Normalmente se reserva para casos refractarios o cuando todas las demás intervenciones terapéuticas no han proporcionado alivio. Antes de la cirugía, los pacientes se someten a técnicas de imágenes cerebrales funcionales, como tomografías por emisión de positrones y resonancias magnéticas funcionales, para determinar una trayectoria adecuada del origen del dolor. [49] Luego, la cirugía se lleva a cabo con anestesia local , porque se necesita la retroalimentación del paciente durante la operación. En el estudio realizado por Bittar et al., se colocó un electrodo de radiofrecuencia con cuatro puntos de contacto en el cerebro. Una vez que el electrodo estaba en su lugar, las ubicaciones de contacto se modificaron ligeramente de acuerdo con el lugar donde el paciente sentía el mayor alivio del dolor. Una vez que se determinó la ubicación del alivio máximo, se implantó el electrodo y se aseguró al cráneo. Después de la cirugía primaria, se realizó una cirugía secundaria con anestesia general . Se implantó un generador de pulso subcutáneo en un bolsillo pectoral debajo de la clavícula para estimular el electrodo. [8] Se encontró que los tres pacientes estudiados habían obtenido un alivio satisfactorio del dolor con la estimulación cerebral profunda. El dolor no se había eliminado por completo, pero la intensidad se había reducido en más del 50% y el componente ardiente había desaparecido por completo. [8] Estudios adicionales han corroborado estos hallazgos, aunque se necesitan ensayos intervencionistas más rigurosos para dilucidar mejor la seguridad y eficacia de este procedimiento. [50] [51] Una revisión sistemática reciente encontró resultados mixtos, lo que también sugiere la necesidad de estudios controlados aleatorios adicionales. [49]
Epidemiología
Se estima que la prevalencia reportada de dolor fantasma puede ser tan alta como 80% entre amputados. [4] Se observa más comúnmente en la población adulta, con ocurrencias menos comunes observadas entre individuos con amputaciones a una edad temprana o en aquellos con deficiencia congénita de miembros. [15] No se ha demostrado que el género, el lado de la pérdida de la extremidad y la etiología de la amputación afecten la aparición del dolor del miembro fantasma. [2] Una investigación de amputación de miembros inferiores observó que a medida que la longitud del muñón disminuía, y por lo tanto la longitud del miembro fantasma aumentaba, había una mayor incidencia de dolor fantasma moderado y severo. [8] También se ha informado que los individuos con amputaciones bilaterales, especialmente en los miembros inferiores, experimentan dolor fantasma con mayor frecuencia. [52] [53]
Más de la mitad de las personas que experimentan dolor fantasma también experimentarán dolor en el miembro residual. [54]
Véase también
Referencias
- ^ abcd Hanyu-Deutmeyer, Aaron A.; Cascella, Marco; Varacallo, Matthew (2023), "Dolor en el miembro fantasma", StatPearls , Treasure Island (FL): StatPearls Publishing, PMID 28846343 , consultado el 19 de enero de 2024
- ^ abcdefg knadmin (3 de marzo de 2017). "Dolor fantasma". PM&R KnowledgeNow . Consultado el 19 de enero de 2024 .
- ^ Pobre Zamany Nejatkermany, Mahtab; Modirian, Ehsan; Soroush, Mohammadreza; Masoumi, Mehdi; Hosseini, Maryam (2016). "Sensación de miembro fantasma (PLS) y dolor de miembro fantasma (PLP) entre jóvenes amputados por minas terrestres". Revista iraní de neurología infantil . 10 (3): 42–47. ISSN 1735-4668. PMC 4928615 . PMID 27375755.
- ^ ab Kaur, Amreet; Guan, Yuxi (diciembre de 2018). "Dolor del miembro fantasma: una revisión de la literatura". Revista china de traumatología . 21 (6): 366–368. doi :10.1016/j.cjtee.2018.04.006. PMC 6354174 . PMID 30583983.
- ^ Stover, Gary; Prahlow, Nathan (2020). "Dolor en el miembro residual: una revisión basada en evidencia". NeuroRehabilitation . 47 (3): 315–325. doi :10.3233/NRE-208005. ISSN 1878-6448. PMID 32986622. S2CID 222156523.
- ^ Srivastava, Devjit (noviembre de 2017). "Dolor crónico postamputación: manejo perioperatorio - Revisión". British Journal of Pain . 11 (4): 192–202. doi :10.1177/2049463717736492. ISSN 2049-4637. PMC 5661696 . PMID 29123664.
- ^ Halligan, PW (2002). "Miembros fantasma: el cuerpo en la mente". Neuropsiquiatría cognitiva . 7 (3): 251–269. doi :10.1080/13546800244000111. PMID 16571541. S2CID 31375410.
- ^ abcdefghijklm Bittar, RG; Otero, S.; Carter, H.; Aziz, TZ (2005). "Estimulación cerebral profunda para el dolor del miembro fantasma". Revista de neurociencia clínica . 12 (4): 399–404. doi :10.1016/j.jocn.2004.07.013. PMID 15925769. S2CID 42653229.
- ^ Sherman, RA; Sherman, CJ (octubre de 1983). "Prevalencia y características del dolor crónico de miembro fantasma entre veteranos estadounidenses. Resultados de una encuesta de ensayo". American Journal of Physical Medicine . 62 (5): 227–238. ISSN 0002-9491. PMID 6624883.
- ^ Sherman, Richard A.; Sherman, Crystal J.; Parker, Laura (enero de 1984). "Dolor crónico fantasma y de muñón entre veteranos estadounidenses: resultados de una encuesta". Pain . 18 (1): 83–95. doi :10.1016/0304-3959(84)90128-3. ISSN 0304-3959. PMID 6709380. S2CID 21102803.
- ^ abcde Culp, Clayton J.; Abdi, Salahadin (octubre de 2022). "Comprensión actual del dolor fantasma y su tratamiento". Pain Physician . 25 (7): E941–E957. ISSN 2150-1149. PMID 36288580.
- ^ ab "Dolor en el miembro fantasma". Physiopedia . Consultado el 19 de enero de 2024 .
- ^ Flor, Herta (mayo de 2008). "Plasticidad desadaptativa, memoria para el dolor y dolor del miembro fantasma: revisión y sugerencias para nuevas terapias". Expert Review of Neurotherapeutics . 8 (5): 809–818. doi :10.1586/14737175.8.5.809. ISSN 1744-8360. PMID 18457537. S2CID 23797588.
- ^ "Dolor del miembro fantasma: qué es, causas, tratamiento y resultados". Cleveland Clinic . Consultado el 17 de enero de 2024 .
- ^ abc Diers, Martin; Fuchs, Xaver; Bekrater-Bodmann, Robin; Flor, Herta (marzo de 2023). "Prevalencia de fenómenos fantasmas en amputados congénitos y en etapas tempranas de la vida". The Journal of Pain . 24 (3): 502–508. doi : 10.1016/j.jpain.2022.10.010 . PMID 36273776. S2CID 253072027.
- ^ Larbig, Wolfgang; Andoh, Jamila; Huse, Ellena; Stahl-Corino, Dietlinde; Montoya, Pedro; Seltzer, Ze'ev; Flor, Herta (2019-05-29). "Predictores pre y postoperatorios del dolor del miembro fantasma". Neuroscience Letters . 702 : 44–50. doi :10.1016/j.neulet.2018.11.044. ISSN 1872-7972. PMID 30503915. S2CID 53864052.
- ^ abcd Ramachandran, VS; Hirstein, W. (1998). "La percepción de los miembros fantasma. La conferencia DO Hebb". Brain: A Journal of Neurology . 121 (9): 1603–1630. doi : 10.1093/brain/121.9.1603 . PMID 9762952.
- ^ Bennett, David L.; Clark, Alex J.; Huang, Jianying; Waxman, Stephen G.; Dib-Hajj, Sulayman D. (1 de abril de 2019). "El papel de los canales de sodio dependientes del voltaje en la señalización del dolor". Physiological Reviews . 99 (2): 1079–1151. doi :10.1152/physrev.00052.2017. ISSN 0031-9333. PMID 30672368.
- ^ Koga, Kohei; Li, Shermaine; Zhuo, Min (1 de junio de 2016). "Plasticidad cortical dependiente del receptor de glutamato metabotrópico en el dolor crónico". Neurofarmacología actual . 14 (5): 427–434. doi :10.2174/1570159X13666150425002304. PMC 4983748 . PMID 27296638.
- ^ Cruz, VT; Nunes, B.; Reis, AM; Pereira, JR (2003). "Remapeo cortical en pacientes amputados y dismélicos: un estudio de resonancia magnética funcional". NeuroRehabilitation . 18 (4): 299–305. doi :10.3233/NRE-2003-18404. PMID 14757926.
- ^ ab Makin, Tamar R. ; Flor, Herta (1 de septiembre de 2020). "(Re)organización cerebral tras una amputación: implicaciones para el dolor del miembro fantasma". NeuroImage . 218 : 116943. doi :10.1016/j.neuroimage.2020.116943. ISSN 1053-8119. PMC 7422832 . PMID 32428706.
- ^ ab Karl, A.; Birbaumer, N.; Lutzenberger, W.; Cohen, LG; Flor, H. (2001). "Reorganización de la corteza motora y somatosensorial en amputados de extremidades superiores con dolor de miembro fantasma". The Journal of Neuroscience . 21 (10): 3609–3618. doi :10.1523/JNEUROSCI.21-10-03609.2001. PMC 6762494 . PMID 11331390.
- ^ abc Giummarra, MJ; Gibson, SJ; Georgiou-Karistianis, N.; Bradshaw, JL (2007). "Mecanismos centrales en la percepción del miembro fantasma: el pasado, el presente y el futuro". Brain Research Reviews . 54 (1): 219–232. doi :10.1016/j.brainresrev.2007.01.009. PMID 17500095. S2CID 42209339.
- ^ Melzack, Ronald (agosto de 1999). "De la puerta a la neuromatriz". Pain . Suppl 6: S121–S126. doi :10.1016/S0304-3959(99)00145-1. ISSN 0304-3959. PMID 10491980. S2CID 20967995.
- ^ Melzack, R. (1992). "Miembros fantasma". Scientific American . 266 (4): 120–126. Código Bibliográfico :1992SciAm.266d.120M. doi :10.1038/scientificamerican0492-120. PMID 1566028.
- ^ Fonoff, Erich Talamoni; de Oliveira, Ywzhe Sifuentes Almeida; López, William Omar Contreras; Alho, Eduardo Joaquim Lopes; Lara, Nilton Alves; Teixeira, Manoel Jacobsen (septiembre de 2010). "Cordotomía por radiofrecuencia percutánea guiada por endoscopia". Revista de Neurocirugía . 113 (3): 524–527. doi :10.3171/2010.4.JNS091779. ISSN 1933-0693. PMID 20433282.
- ^ Erlenwein, Joaquín; Diers, Martín; Ernst, Jennifer; Schulz, Friederike; Petzke, Frank (2021). "Actualizaciones clínicas sobre el dolor del miembro fantasma". Informes DOLOR . 6 (1): e888. doi :10.1097/PR9.0000000000000888. ISSN 2471-2531. PMC 7813551 . PMID 33490849.
- ^ ab Spiegel, David R.; Lappinen, Erik; Gottlieb, Michael (2010). "Un presunto caso de dolor en el miembro fantasma tratado con éxito con duloxetina y pregabalina". Psiquiatría del Hospital General . 32 (2): 228.e5–7. doi :10.1016/j.genhosppsych.2009.05.012. ISSN 1873-7714. PMID 20303003.
- ^ Mulvey, Matthew R.; Radford, Helen E.; Fawkner, Helen J.; Hirst, Lynn; Neumann, Vera; Johnson, Mark I. (abril de 2013). "Estimulación nerviosa eléctrica transcutánea para el dolor fantasma y el dolor del muñón en amputados adultos". Pain Practice . 13 (4): 289–296. doi :10.1111/j.1533-2500.2012.00593.x. ISSN 1530-7085. PMID 22935086.
- ^ Subedi, Bishnu; Grossberg, George T. (14 de agosto de 2011). "Dolor del miembro fantasma: mecanismos y enfoques de tratamiento". Investigación y tratamiento del dolor . 2011 : 1–8. doi : 10.1155/2011/864605 . ISSN: 2090-1542. PMC : 3198614. PMID: 22110933.
- ^ Bone, Margaret; Critchley, Peter; Buggy, Donal J. (2002). "Gabapentina en el dolor del miembro fantasma postamputación: un estudio aleatorizado, doble ciego, controlado con placebo y cruzado". Anestesia regional y medicina del dolor . 27 (5): 481–486. doi :10.1053/rapm.2002.35169. ISSN 1098-7339. PMID 12373695. S2CID 26515957.
- ^ Harden, R. Norman; Houle, Tim T.; Remble, Thomas A.; Lin, Wendy; Wang, Kenten; Saltz, Samuel (2005). "Topiramato para el dolor del miembro fantasma: un análisis de series temporales". Medicina del dolor . 6 (5): 375–378. doi :10.1111/j.1526-4637.2005.00060.x. ISSN 1526-2375. PMID 16266358.
- ^ Robinson, Lawrence R.; Czerniecki, Joseph M.; Ehde, Dawn M.; Edwards, W. Thomas; Judish, David A.; Goldberg, Myron L.; Campbell, Kellye M.; Smith, Douglas G.; Jensen, Mark P. (enero de 2004). "Ensayo de amitriptilina para el alivio del dolor en amputados: resultados de un estudio controlado aleatorio". Archivos de Medicina Física y Rehabilitación . 85 (1): 1–6. doi :10.1016/s0003-9993(03)00476-3. ISSN 0003-9993. PMID 14970960.
- ^ Wilder-Smith, Clive H.; Hill, Lauren T.; Laurent, Sophie (septiembre de 2005). "Dolor postamputación y cambios sensoriales en pacientes sin tratamiento previo: características y respuestas al tratamiento con tramadol, amitriptilina y placebo". Anestesiología . 103 (3): 619–628. doi :10.1097/00000542-200509000-00027. ISSN 0003-3022. PMID 16129989.
- ^ Schwenkreis, P.; Maier, C.; Pleger, B.; Mansourian, N.; Dertwinkel, R.; Malin, J.-P.; Tegenthoff, M.; Zenz, M. (septiembre de 2003). "Mecanismos mediados por NMDA en los cambios de excitabilidad cortical después de la amputación de una extremidad". Acta Neurologica Scandinavica . 108 (3): 179–184. doi :10.1034/j.1600-0404.2003.00114.x. ISSN 0001-6314. PMID 12911461. S2CID 45858493.
- ^ Eichenberger, Urs; Neff, Frank; Sveticic, Gorazd; Björgo, Steinar; Petersen-Felix, Steen; Arendt-Nielsen, Lars; Curatolo, Michele (abril de 2008). "Dolor crónico del miembro fantasma: los efectos de la calcitonina, la ketamina y su combinación en los umbrales sensoriales y del dolor". Anestesia y analgesia . 106 (4): 1265–1273, tabla de contenidos. doi :10.1213/ane.0b013e3181685014. ISSN 1526-7598. PMID 18349204.
- ^ ab Ramachandran, VS; Rogers-Ramachandran, D. (1996). "Sinestesia en miembros fantasma inducida con espejos". Actas de la Royal Society B: Biological Sciences . 263 (1369): 377–386. Bibcode :1996RSPSB.263..377R. doi :10.1098/rspb.1996.0058. PMID 8637922. S2CID 4819370.
- ^ ab Terapia del espejo: una posible intervención para el manejo del dolor, Wittkopf, Johnson, noviembre de 2017;63(11):[1]
- ^ Jessie, Barbin; Seetha, Vanessa (2016). "Los efectos de la terapia del espejo en el dolor y el control motor del miembro fantasma en amputados: una revisión sistemática". Annals of Physical and Rehabilitation Medicine . 59 (4): 270–275. doi : 10.1016/j.rehab.2016.04.001 . PMID 27256539.
Hasta el 26 de noviembre de 2015, se recuperaron 85 artículos en las bases de datos Medline, Cochrane y Embase utilizando las palabras clave miembro fantasma y terapia del espejo. Se observó que a partir de 2009, el número de artículos aumentó notablemente (Fig. 1), lo que muestra un mayor interés en la terapia del espejo después de la amputación.
- ^ Campo-Prieto, P; Rodríguez-Fuentes, G (14 de noviembre de 2018). "Efectividad de la terapia del espejo en el dolor del miembro fantasma: una revisión de la literatura". Neurologia . 37 (8): 668–681. doi : 10.1016/j.nrl.2018.08.003 . PMID 30447854.
Es un tratamiento válido, sencillo y económico para el dolor del miembro fantasma. La calidad metodológica de la mayoría de las publicaciones en este campo es muy limitada, lo que pone de relieve la necesidad de estudios adicionales de alta calidad para desarrollar protocolos clínicos que puedan maximizar los beneficios de la terapia del espejo para los pacientes con dolor del miembro fantasma.
- ^ Foell, J.; Bekrater-Bodmann, R.; Diers, M.; Flor, H. (mayo de 2014). "Terapia con espejo para el dolor del miembro fantasma: cambios cerebrales y el papel de la representación corporal". Revista Europea del Dolor . 18 (5): 729–739. doi :10.1002/j.1532-2149.2013.00433.x. ISSN 1532-2149. PMID 24327313. S2CID 44669695.
- ^ "Graded Motor Imaginery" (Imágenes motoras graduadas). Physiopedia . Consultado el 26 de enero de 2024 .
- ^ Limakatso, Katleho; Cashin, Aidan G.; Williams, Sam; Devonshire, Jack; Parker, Romy; McAuley, James H. (2023). "La eficacia de la imaginería motora graduada y sus componentes en el dolor y la discapacidad del miembro fantasma: una revisión sistemática y un metaanálisis". Revista canadiense del dolor . 7 (1): 2188899. doi :10.1080/24740527.2023.2188899. ISSN 2474-0527. PMC 10193907 . PMID 37214633.
- ^ ab Boomgaardt, Jacob; Dastan, Kovosh; Chan, Tiffany; Shilling, Ashley; Abd-Elsayed, Alaa; Kohan, Lynn (26 de octubre de 2022). "Un enfoque algorítmico para el dolor del miembro fantasma". Revista de investigación del dolor . 15 : 3349–3367. doi : 10.2147/JPR.S355278 . PMC 9618240 . PMID 36320223.
- ^ Ichinose, Akimichi; Sano, Yuko; Osumi, Michihiro; Sumitani, Masahiko; Kumagaya, Shin-Ichiro; Kuniyoshi, Yasuo (agosto de 2017). "La retroalimentación somatosensorial en la mejilla durante la terapia de retroalimentación visual virtual mejora el alivio del dolor de los brazos fantasma". Neurorrehabilitación y Reparación Neural . 31 (8): 717–725. doi :10.1177/1545968317718268. ISSN 1552-6844. PMID 28691602.
- ^ Mercier, Catherine; Sirigu, Angela (julio de 2009). "Entrenamiento con retroalimentación visual virtual para aliviar el dolor del miembro fantasma". Neurorrehabilitación y reparación neuronal . 23 (6): 587–594. doi :10.1177/1545968308328717. ISSN 1545-9683. PMID 19171946. S2CID 22995879.
- ^ Cole, Jonathan; Crowle, Simon; Austwick, Greg; Henderson Slater, David (enero de 2009). "Hallazgos exploratorios con realidad virtual para el dolor de miembros fantasma; desde el movimiento del muñón hasta la capacidad de acción y la analgesia". Disability and Rehabilitation . 31 (10): 846–854. doi :10.1080/09638280802355197. ISSN 0963-8288. PMID 19191061. S2CID 4846236.
- ^ Murray, Craig D.; Patchick, Emma; Pettifer, Stephen; Caillette, Fabrice; Howard, Toby (abril de 2006). "Realidad virtual inmersiva como tecnología de rehabilitación para la experiencia del miembro fantasma: un protocolo". CyberPsychology & Behavior . 9 (2): 167–170. doi :10.1089/cpb.2006.9.167. ISSN 1094-9313. PMID 16640472.
- ^ ab Corbett, Mark; South, Emily; Harden, Melissa; Eldabe, Sam; Pereira, Erlick; Sedki, Imad; Hall, Neil; Woolacott, Nerys (noviembre de 2018). "Terapias de estimulación cerebral y espinal para el dolor del miembro fantasma: una revisión sistemática". Evaluación de tecnologías sanitarias . 22 (62): 1–94. doi :10.3310/hta22620. ISSN 1366-5278. PMC 6253324 . PMID 30407905.
- ^ Katayama, Yoichi; Yamamoto, Takamitsu; Kobayashi, Kazutaka; Kasai, Masahiko; Oshima, Hideki; Fukaya, Chikashi (2001). "Estimulación de la corteza motora para el dolor del miembro fantasma: terapia integral con estimulación de la médula espinal y del tálamo". Neurocirugía estereotáctica y funcional . 77 (1–4): 159–162. doi :10.1159/000064593. ISSN 1011-6125. PMID 12378068. S2CID 29788874.
- ^ Ahuja, Vanita; Thapa, Deepak; Ghai, Babita (2018). "Estrategias para la prevención del dolor postamputación de miembros inferiores: una revisión clínica narrativa". Revista de anestesiología y farmacología clínica . 34 (4): 439–449. doi : 10.4103/joacp.JOACP_126_17 . ISSN 0970-9185. PMC 6360885. PMID 30774224 .
- ^ Kehlet, Henrik; Jensen, Troels S.; Woolf, Clifford J. (13 de mayo de 2006). "Dolor posquirúrgico persistente: factores de riesgo y prevención". Lancet . 367 (9522): 1618–1625. doi :10.1016/S0140-6736(06)68700-X. ISSN 1474-547X. PMID 16698416. S2CID 38138668.
- ^ Dijkstra, Pieter U.; Geertzen, Jan HB; Stewart, Roy; van der Schans, Cees P. (diciembre de 2002). "Dolor fantasma y factores de riesgo: un análisis multivariado". Revista de manejo del dolor y los síntomas . 24 (6): 578–585. doi : 10.1016/s0885-3924(02)00538-9 . ISSN 0885-3924. PMID 12551807.
- ^ Hanyu-Deutmeyer, Aaron A.; Cascella, Marco; Varacallo, Matthew (2024), "Phantom Limb Pain", StatPearls , Treasure Island (FL): StatPearls Publishing, PMID 28846343 , consultado el 11 de junio de 2024
Enlaces externos
- MacLachlan, Malcolm; McDonald, Dympna; Waloch, Justine (2004), "Tratamiento con espejo del dolor fantasma en las extremidades inferiores: un estudio de caso" (PDF) , Disability and Rehabilitation , 26 (14/15): 901–904, doi :10.1080/09638280410001708913, PMID 15497919, S2CID 36325980
- Richardson, Cliff; Glenn, Sheila; Horgan, Maureen; Nurmikko, Turo (octubre de 2007), "Un estudio prospectivo de los factores asociados con la presencia de dolor en el miembro fantasma seis meses después de una amputación importante de un miembro inferior en pacientes con enfermedad vascular periférica", The Journal of Pain , 8 (10): 793–801, doi : 10.1016/j.jpain.2007.05.007 , PMID 17631056
- Reinervación muscular dirigida