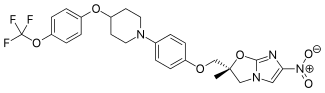
Delamanida
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Deltyba |
| Otros nombres | OPC-67683 |
| AHFS / Drogas.com | Información sobre medicamentos en el Reino Unido |
| Vías de administración | Por la boca |
| Código ATC |
|
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Unión de proteínas | ≥99,5% |
| Metabolismo | en el plasma por la albúmina, en el hígado por CYP3A4 (en menor medida) |
| Vida media de eliminación | 30–38 horas |
| Excreción | no se excreta en la orina [1] |
| Identificadores | |
| |
| Número CAS |
|
| Identificador de centro de PubChem |
|
| Banco de medicamentos |
|
| Araña química |
|
| UNIVERSIDAD |
|
| BARRIL |
|
| EBICh |
|
| Química biológica |
|
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.348.783 |
| Datos químicos y físicos | |
| Fórmula | C25H25F3N4O6 |
| Masa molar | 534,492 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| |
Delamanid se vende bajo la marca Deltyba y es un medicamento utilizado para tratar la tuberculosis . [2] En concreto, se utiliza, junto con otros medicamentos antituberculosos , para la tuberculosis multirresistente activa . [2] Se toma por vía oral . [2]
Existen efectos secundarios comunes que incluyen dolor de cabeza, mareos y náuseas. [3] Otros efectos secundarios incluyen prolongación del intervalo QT . [2] Delamanid actúa bloqueando la fabricación de ácidos micólicos, desestabilizando así la pared celular bacteriana . [4] Pertenece a la clase de medicamentos de nitroimidazol . [5]
La delamanida fue aprobada para uso médico en 2014 en Europa, Japón y Corea del Sur. [6] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [7] En 2016, la Alianza Alto a la Tuberculosis tenía un acuerdo para obtener el medicamento por US$1.700 por seis meses para su uso en más de 100 países. [8]
Usos médicos
La delamanida se utiliza, junto con otros medicamentos antituberculosos , para la tuberculosis multirresistente activa . [2]
Efectos adversos
Los efectos secundarios comunes incluyen dolor de cabeza, mareos y náuseas. [3] Otros efectos secundarios incluyen prolongación del intervalo QT . [2] El uso durante el embarazo no se ha estudiado ampliamente, pero ha habido informes de éxito [9] y actualmente se recomienda como parte del régimen de tratamiento estándar para mujeres embarazadas con tuberculosis resistente a la rifampicina en Sudáfrica. [10]
Interacciones
La delamanida se metaboliza por la enzima hepática CYP3A4 ; por lo tanto, los inductores fuertes de esta enzima pueden reducir su eficacia. [11]
Mecanismo de acción
La delamanida se activa en la micobacteria por la nitroreductasa dependiente de la deazaflavina ( Ddn ), una enzima que utiliza dihidro-F 420 (forma reducida), en óxido nítrico y un metabolito altamente reactivo. Este metabolito ataca a la enzima de síntesis DprE2 , que es importante para la síntesis del arabinogalactano de la pared celular , al que se uniría el ácido micólico. Este mecanismo es compartido con la pretomanida . Los aislados clínicos resistentes a este fármaco tienden a tener mutaciones en la vía biosintética de la coenzima F 420. [12]
Historia
En los ensayos clínicos de fase II , el fármaco se utilizó en combinación con tratamientos estándar, como cuatro o cinco de los fármacos etambutol , isoniazida , pirazinamida , rifampicina , antibióticos aminoglucósidos y quinolonas . Las tasas de curación (medidas como conversión del cultivo de esputo ) fueron significativamente mejores en los pacientes que tomaron además delamanida. [13] [14]
La Agencia Europea de Medicamentos (EMA) recomendó la autorización condicional de comercialización de delamanid en adultos con tuberculosis pulmonar resistente a múltiples fármacos sin otras opciones de tratamiento debido a la resistencia o la tolerabilidad. La EMA consideró que los datos muestran que los beneficios de delamanid superan los riesgos, pero que se necesitan estudios adicionales sobre la eficacia a largo plazo. [15]
Sociedad y cultura
Esta sección necesita ser actualizada . ( Marzo de 2020 ) |
En 2015, el medicamento no estaba disponible a nivel mundial. Se creía que el precio sería similar al de la bedaquilina , que por seis meses cuesta aproximadamente 900 dólares estadounidenses en países de bajos ingresos, 3000 dólares estadounidenses en países de ingresos medios y 30 000 dólares estadounidenses en países de ingresos altos. [2] En 2016, la Stop TB Partnership tenía un acuerdo para obtener el medicamento por 1700 dólares estadounidenses por seis meses. [8]
Referencias
- ^ "Deltyba (delamanid): Resumen de las características del producto. 5.2. Propiedades farmacocinéticas" (PDF) . Otsuka Novel Products GmbH. pág. 10. Archivado (PDF) del original el 17 de agosto de 2016 . Consultado el 9 de julio de 2016 .
- ^ abcdefg Organización Mundial de la Salud (2015). Selección y utilización de medicamentos esenciales. Vigésimo informe del Comité de Expertos de la OMS 2015 (incluida la 19.ª Lista Modelo de la OMS de Medicamentos Esenciales y la 5.ª Lista Modelo de la OMS de Medicamentos Pediátricos Esenciales) . Ginebra: Organización Mundial de la Salud. pp. 30–1. hdl : 10665/189763 . ISBN 9789241209946. ISSN 0512-3054. Serie de informes técnicos de la OMS;994.
- ^ ab Smith MR, Accinelli A, Tejada FR, Kharel MK (2016). "Medicamentos utilizados en la tuberculosis y la lepra". En Ray SD (ed.). Efectos secundarios de los medicamentos: una encuesta anual mundial de nuevos datos sobre reacciones adversas a los medicamentos . Elsevier. pág. 284. ISBN 978-0-444-63889-2. Archivado desde el original el 20 de diciembre de 2016.
- ^ Blair HA, Scott LJ (enero de 2015). "Delamanid: una revisión de su uso en pacientes con tuberculosis resistente a múltiples fármacos". Drugs . 75 (1): 91–100. doi :10.1007/s40265-014-0331-4. PMID 25404020. S2CID 34541500.
- ^ Alves de Oliverira TS, da Sliva Rabello MC (2017). "Vacunas contra la tuberculosis". En de Paiva Cavalcanti M, Pereira VR, Dessein AJ (eds.). Enfermedades tropicales: una visión general de las principales enfermedades que ocurren en las Américas . Editores científicos de Bentham. pag. 461. doi : 10.2174/9781681085876117010022. ISBN 978-1-68108-587-6.
- ^ Fischer J (2016). Descubrimiento exitoso de fármacos. John Wiley & Sons. pág. 139. ISBN 978-3-527-34115-3. Archivado desde el original el 20 de diciembre de 2016.
- ^ Organización Mundial de la Salud (2019). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 21.ª lista , 2019. Ginebra: Organización Mundial de la Salud. hdl : 10665/325771 . OMS/MVP/EMP/IAU/2019.06. Licencia: CC BY-NC-SA 3.0 IGO.
- ^ ab "Stop TB Partnership | "El mecanismo mundial de medicamentos de Stop TB Partnership impulsa el acceso a nuevos medicamentos para la tuberculosis multirresistente con innovadoras asociaciones público-privadas". www.stoptb.org . Archivado desde el original el 16 de enero de 2017 . Consultado el 15 de enero de 2017 .
- ^ Acquah R, Mohr-Holland E, Daniels J, Furin J, Loveday M, Mudaly V, et al. (mayo de 2021). "Resultados de los niños nacidos de mujeres embarazadas con tuberculosis resistente a los medicamentos tratados con nuevos fármacos en Khayelitsha, Sudáfrica: un informe de cinco pacientes". The Pediatric Infectious Disease Journal . 40 (5): e191–e192. doi : 10.1097/INF.0000000000003069 . PMC 8043512 . PMID 33847295.
- ^ "Manejo clínico de la tuberculosis resistente a la rifampicina: guía de referencia clínica actualizada" (PDF) . Departamento de Salud, República de Sudáfrica . Septiembre de 2023.
- ^ "Delamanid: Neuer Wirkstoff gegen tuberculosis multirresistente". Pharmazeutische Zeitung (en alemán). 9 de mayo de 2014. Archivado desde el original el 24 de septiembre de 2015.
- ^ Abrahams KA, Batt SM, Gurcha SS, Veerapen N, Bashiri G, Besra GS (junio de 2023). "DprE2 es un objetivo molecular de los compuestos antituberculosos nitroimidazólicos pretomanid y delamanid". Nature Communications . 14 (1): 3828. Bibcode :2023NatCo..14.3828A. doi : 10.1038/s41467-023-39300-z . PMC 10307805 . PMID 37380634.
- ^ Spreitzer H (18 de febrero de 2013). "Neue Wirkstoffe - Bedaquilin und Delamanid" . Österreichische Apothekerzeitung (en alemán) (4/2013): 22.
- ^ Gler MT, Skripconoka V, Sánchez-Garavito E, Xiao H, Cabrera-Rivero JL, Vargas-Vásquez DE, et al. (junio de 2012). "Delamanid para la tuberculosis pulmonar multirresistente". La Revista de Medicina de Nueva Inglaterra . 366 (23): 2151–2160. doi : 10.1056/NEJMoa1112433 . PMID 22670901.
- ^ "La Agencia Europea de Medicamentos recomienda dos nuevas opciones de tratamiento para la tuberculosis". Agencia Europea de Medicamentos . 22 de noviembre de 2013. Archivado desde el original el 3 de diciembre de 2013.

