Lisina
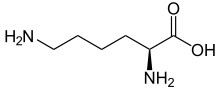 Fórmula esquelética de la L -lisina | |||
| |||
| Nombres | |||
|---|---|---|---|
| Nombres IUPAC L -lisina D -lisina | |||
| Nombre sistemático de la IUPAC Ácido (2 S )-2,6-diaminohexanoico ( L -lisina) Ácido (2 R )-2,6-diaminohexanoico ( D -lisina) | |||
| Otros nombres Lisina, D -lisina, L -lisina, LYS, h-Lys-OH | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.000.673 | ||
| |||
| BARRIL | |||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C6H14N2O2 | |||
| Masa molar | 146,190 g·mol −1 | ||
| 1,5 kg/l | |||
| Farmacología | |||
| B05XB03 ( QUIÉN ) | |||
| Página de datos complementarios | |||
| Lisina (página de datos) | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
La lisina ( símbolo Lys o K ) [2] es un α-aminoácido precursor de muchas proteínas . Contiene un grupo α-amino (que se encuentra en el −NH protonado +3forma cuando se disuelve en agua), un grupo ácido α-carboxílico (que está en la forma desprotonada −COO − cuando se disuelve en agua), y un lisilo de cadena lateral ( (CH 2 ) 4 NH 2 ), clasificándolo como un aminoácido alifático básico , cargado (a pH fisiológico ) . Está codificado por los codones AAA y AAG. Como casi todos los demás aminoácidos, el carbono α es quiral y la lisina puede referirse a un enantiómero o a una mezcla racémica de ambos. Para el propósito de este artículo, lisina se referirá al enantiómero biológicamente activo L -lisina, donde el carbono α está en la configuración S.
El cuerpo humano no puede sintetizar lisina, que es esencial para el ser humano y, por lo tanto, debe obtenerse a través de la dieta. En los organismos que sintetizan lisina, existen dos vías biosintéticas principales , las vías del diaminopimelato y del α-aminoadipato , que emplean enzimas y sustratos distintos y se encuentran en diversos organismos. El catabolismo de la lisina se produce a través de una de varias vías, la más común de las cuales es la vía de la sacaropina .
La lisina desempeña varias funciones en los seres humanos, la más importante de las cuales es la proteinogénesis , pero también en la reticulación de los polipéptidos de colágeno , la absorción de nutrientes minerales esenciales y en la producción de carnitina , que es clave en el metabolismo de los ácidos grasos . La lisina también suele estar implicada en las modificaciones de las histonas y, por tanto, afecta al epigenoma . El grupo ε-amino participa a menudo en la unión de hidrógeno y como base general en la catálisis . El grupo ε - amonio ( −NH+3) está unido al cuarto carbono desde el carbono α, que está unido al grupo carboxilo ( −COOH ). [3]
Debido a su importancia en varios procesos biológicos, la falta de lisina puede provocar varios estados patológicos, como defectos en el tejido conectivo, alteración del metabolismo de los ácidos grasos, anemia y deficiencia sistémica de proteína y energía. Por el contrario, una sobreabundancia de lisina, causada por un catabolismo ineficaz, puede causar trastornos neurológicos graves .
La lisina fue aislada por primera vez por el químico biológico alemán Ferdinand Heinrich Edmund Drechsel en 1889 a partir de la hidrólisis de la proteína caseína , [4] y por eso la llamó lisina, del griego λύσις (lisis) 'aflojamiento'. [5] [6] En 1902, los químicos alemanes Emil Fischer y Fritz Weigert determinaron la estructura química de la lisina sintetizándola. [7]
El símbolo de una letra K se asignó a la lisina por ser el más cercano alfabéticamente, mientras que L se asignó a la leucina estructuralmente más simple y M a la metionina. [8]
Biosíntesis
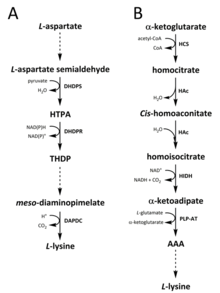
Se han identificado dos vías en la naturaleza para la síntesis de lisina. La vía del diaminopimelato (DAP) pertenece a la familia biosintética derivada del aspartato , que también está involucrada en la síntesis de treonina , metionina e isoleucina [9] [10] , mientras que la vía del α-aminoadipato (AAA) es parte de la familia biosintética del glutamato [11] [12] .
Ruta DAP
La vía DAP se encuentra tanto en procariotas como en plantas y comienza con la reacción de condensación catalizada por la dihidrodipicolinato sintasa (DHDPS) (EC 4.3.3.7) entre el derivado de aspartato, L -aspartato semialdehído, y el piruvato para formar ácido (4 S )-4-hidroxi-2,3,4,5-tetrahidro-(2 S )-dipicolínico (HTPA). [13] [14] [15] [16] [17] El producto es luego reducido por la dihidrodipicolinato reductasa (DHDPR) (EC 1.3.1.26), con NAD(P)H como donante de protones, para producir 2,3,4,5-tetrahidrodipicolinato (THDP). [18] A partir de este punto, se han encontrado cuatro variaciones de la vía, a saber, las vías de la acetilasa, la aminotransferasa, la deshidrogenasa y la succinilasa. [9] [19] Tanto la vía de la acetilasa como la de la succinilasa utilizan cuatro pasos catalizados por enzimas , la vía de la aminotransferasa utiliza dos enzimas y la vía de la deshidrogenasa utiliza una sola enzima. [20] Estas cuatro vías variantes convergen en la formación del penúltimo producto, meso -diaminopimelato, que posteriormente se descarboxila enzimáticamente en una reacción irreversible catalizada por la diaminopimelato descarboxilasa (DAPDC) (EC 4.1.1.20) para producir L -lisina. [21] [22] La vía DAP está regulada en múltiples niveles, incluyendo aguas arriba en las enzimas implicadas en el procesamiento del aspartato, así como en el paso inicial de condensación catalizada por DHDPS. [22] [23] La lisina imparte un fuerte ciclo de retroalimentación negativa en estas enzimas y, posteriormente, regula toda la vía. [23]
Vía AAA
La vía AAA implica la condensación de α-cetoglutarato y acetil-CoA a través del intermediario AAA para la síntesis de L -lisina. Se ha demostrado que esta vía está presente en varias especies de levaduras , así como en protistas y hongos superiores. [12] [24] [25] [26] [27] [28] [29] También se ha informado que se ha encontrado una variante alternativa de la ruta AAA en Thermus thermophilus y Pyrococcus horikoshii , lo que podría indicar que esta vía está más ampliamente extendida en procariotas de lo que se propuso originalmente. [30] [31] [32] El primer paso, y el que limita la velocidad, en la vía AAA es la reacción de condensación entre acetil-CoA y α-cetoglutarato catalizada por la homocitrato-sintasa (HCS) (EC 2.3.3.14) para dar el intermediario homocitril-CoA, que es hidrolizado por la misma enzima para producir homocitrato . [33] El homocitrato es deshidratado enzimáticamente por la homoaconitasa (HAc) (EC 4.2.1.36) para producir cis -homoaconitato . [34] Luego, la HAc cataliza una segunda reacción en la que el cis -homoaconitato sufre rehidratación para producir homoisocitrato . [12] El producto resultante sufre una descarboxilación oxidativa por la homoisocitrato deshidrogenasa (HIDH) (EC 1.1.1.87) para producir α-cetoadipato. [12] Luego, el AAA se forma a través de una aminotransferasa dependiente de piridoxal 5'-fosfato (PLP) (PLP-AT) (EC 2.6.1.39), utilizando glutamato como donante de amino. [33] A partir de este punto, la vía AAA varía con [¿Falta algo aquí? -> ¡al menos, encabezado de sección!] en el reino. En los hongos, el AAA se reduce a α-aminoadipato-semialdehído a través de la AAA reductasa (EC 1.2.1.95) en un proceso único que involucra tanto adenilación como reducción que es activado por una fosfopanteteinil transferasa (EC 2.7.8.7). [12] Una vez formado el semialdehído, la sacaropina reductasa (EC 1.5.1.10) cataliza una reacción de condensación con glutamato y NAD(P)H, como donante de protones, y la imina se reduce para producir el penúltimo producto, la sacaropina. [32] El paso final de la vía en los hongos implica la La sacaropina deshidrogenasa (SDH) (EC 1.5.1.8) catalizó la desaminación oxidativa de la sacaropina, lo que resultó en L -lisina. [12] En una vía variante de AAA encontrada en algunos procariotas, AAA primero se convierte en N -acetil-α-aminoadipato, que se fosforila y luego se desfosforila reductivamente al ε-aldehído. [32] [33] Luego, el aldehído se transamina a N -acetillisina, que se desacetila para dar L -lisina. [32] [33] Sin embargo, las enzimas involucradas en esta vía variante necesitan mayor validación.
Catabolismo

Al igual que con todos los aminoácidos, el catabolismo de la lisina se inicia a partir de la absorción de lisina dietética o de la descomposición de la proteína intracelular . El catabolismo también se utiliza como un medio para controlar la concentración intracelular de lisina libre y mantener un estado estable para prevenir los efectos tóxicos de la lisina libre excesiva. [35] Hay varias vías involucradas en el catabolismo de la lisina, pero la más comúnmente utilizada es la vía de la sacaropina, que tiene lugar principalmente en el hígado (y órganos equivalentes) en animales, específicamente dentro de las mitocondrias . [36] [35] [37] [38] Esta es la inversa de la vía AAA descrita anteriormente. [36] [39] En animales y plantas, los dos primeros pasos de la vía de la sacaropina son catalizados por la enzima bifuncional, α-aminoadípico semialdehído sintasa (AASS) , que posee actividades tanto de lisina-cetoglutarato reductasa (LKR) (EC 1.5.1.8) como de SDH, mientras que en otros organismos, como bacterias y hongos, ambas enzimas están codificadas por genes separados . [40] [41] El primer paso implica la reducción catalizada por LKR de L -lisina en presencia de α-cetoglutarato para producir sacaropina, con NAD(P)H actuando como donante de protones. [42] Luego, la sacaropina sufre una reacción de deshidratación, catalizada por SDH en presencia de NAD + , para producir AAS y glutamato. [43] La AAS deshidrogenasa (AASD) (EC 1.2.1.31) luego deshidrata aún más la molécula en AAA. [42] Posteriormente, PLP-AT cataliza la reacción inversa a la de la vía de biosíntesis de AAA, lo que da como resultado que AAA se convierta en α-cetoadipato. El producto, α-cetoadipato, se descarboxila en presencia de NAD + y coenzima A para producir glutaril-CoA, sin embargo, la enzima involucrada en esto aún debe dilucidarse por completo. [44] [45] Algunas evidencias sugieren que el complejo 2-oxoadipato deshidrogenasa (OADHc), que es estructuralmente homólogo a la subunidad E1 del complejo oxoglutarato deshidrogenasa (OGDHc) (EC 1.2.4.2), es responsable de la reacción de descarboxilación. [44] [46] Finalmente, la glutaril-CoA es descarboxilada oxidativamente a crotonil-CoA por la glutaril-CoA deshidrogenasa (EC 1.3.8.6), que luego es procesada a través de múltiples pasos enzimáticos para producir acetil-CoA; un metabolito de carbono esencial involucrado en el ciclo del ácido tricarboxílico (TCA) . [42][47] [48] [49]
Valor nutricional
La lisina es un aminoácido esencial en los seres humanos. [50] El requerimiento nutricional diario humano varía de ~60 mg/kg en la infancia a ~30 mg/kg en adultos. [36] Este requerimiento se satisface comúnmente en una sociedad occidental con la ingesta de lisina de fuentes de carne y vegetales muy por encima del requerimiento recomendado. [36] En las dietas vegetarianas, la ingesta de lisina es menor debido a la cantidad limitada de lisina en los cultivos de cereales en comparación con las fuentes de carne. [36]
Dada la concentración limitante de lisina en los cultivos de cereales, se ha especulado durante mucho tiempo que el contenido de lisina se puede aumentar a través de prácticas de modificación genética . [51] [52] A menudo, estas prácticas han implicado la desregulación intencional de la vía DAP mediante la introducción de ortólogos insensibles a la retroalimentación de la lisina de la enzima DHDPS. [51] [52] Estos métodos han tenido un éxito limitado probablemente debido a los efectos secundarios tóxicos del aumento de la lisina libre y los efectos indirectos en el ciclo del TCA. [53] Las plantas acumulan lisina y otros aminoácidos en forma de proteínas de almacenamiento de semillas , que se encuentran dentro de las semillas de la planta, y esto representa el componente comestible de los cultivos de cereales. [54] Esto resalta la necesidad no solo de aumentar la lisina libre, sino también de dirigir la lisina hacia la síntesis de proteínas de almacenamiento de semillas estables y, posteriormente, aumentar el valor nutricional del componente consumible de los cultivos. [55] [56] Si bien las prácticas de modificación genética han tenido un éxito limitado, las técnicas de crianza selectiva más tradicionales han permitido el aislamiento de " maíz de proteína de calidad ", que ha aumentado significativamente los niveles de lisina y triptófano , también un aminoácido esencial. Este aumento en el contenido de lisina se atribuye a una mutación opaca-2 que redujo la transcripción de proteínas de almacenamiento de semillas relacionadas con la zeína que carecen de lisina y, como resultado, aumentó la abundancia de otras proteínas que son ricas en lisina. [56] [57] Comúnmente, para superar la abundancia limitante de lisina en el alimento para el ganado , se agrega lisina producida industrialmente. [58] [59] El proceso industrial incluye el cultivo fermentativo de Corynebacterium glutamicum y la posterior purificación de la lisina. [58]
Fuentes dietéticas
Las buenas fuentes de lisina son los alimentos ricos en proteínas, como los huevos, la carne (en concreto, la carne roja, el cordero, el cerdo y las aves de corral), la soja , los frijoles y los guisantes, el queso (en particular el parmesano) y ciertos pescados (como el bacalao y las sardinas ). [60] La lisina es el aminoácido limitante (el aminoácido esencial que se encuentra en menor cantidad en el alimento en cuestión) en la mayoría de los cereales , pero es abundante en la mayoría de las legumbres. [61] Los frijoles contienen la lisina de la que carece el maíz , y en el registro arqueológico humano los frijoles y el maíz suelen aparecer juntos, como en las Tres Hermanas : frijoles, maíz y calabaza. [62]
Se considera que un alimento tiene suficiente lisina si tiene al menos 51 mg de lisina por gramo de proteína (de modo que la proteína es 5,1% lisina). [63] La L -lisina HCl se utiliza como suplemento dietético , aportando 80,03% de L -lisina. [64] Por tanto, 1 g de L -lisina está contenido en 1,25 g de L -lisina HCl.
Roles biológicos
El papel más común de la lisina es la proteinogénesis. La lisina juega frecuentemente un papel importante en la estructura de las proteínas . Dado que su cadena lateral contiene un grupo cargado positivamente en un extremo y una larga cola de carbono hidrofóbica cerca de la cadena principal, la lisina se considera algo anfipática . Por esta razón, la lisina se puede encontrar enterrada, así como más comúnmente en los canales de solventes y en el exterior de las proteínas, donde puede interactuar con el entorno acuoso. [65] La lisina también puede contribuir a la estabilidad de las proteínas, ya que su grupo ε-amino a menudo participa en la unión de hidrógeno , puentes salinos e interacciones covalentes para formar una base de Schiff . [65] [66] [67] [68]
Un segundo papel importante de la lisina es en la regulación epigenética por medio de la modificación de histonas . [69] [70] Hay varios tipos de modificaciones covalentes de histonas, que comúnmente involucran residuos de lisina encontrados en la cola saliente de las histonas. Las modificaciones a menudo incluyen la adición o eliminación de un acetilo (−CH 3 CO) formando acetil-lisina o revirtiendo a lisina, hasta tres metil (−CH 3 ) , ubiquitina o un grupo proteico sumo . [69] [71] [72] [73] [74] Las diversas modificaciones tienen efectos posteriores en la regulación genética , en la que los genes pueden ser activados o reprimidos.
La lisina también ha sido implicada en desempeñar un papel clave en otros procesos biológicos, incluyendo; proteínas estructurales de tejidos conectivos , homeostasis de calcio y metabolismo de ácidos grasos . [75] [76] [77] Se ha demostrado que la lisina está involucrada en la reticulación entre los tres polipéptidos helicoidales en colágeno , resultando en su estabilidad y resistencia a la tracción. [75] [78] Este mecanismo es similar al papel de la lisina en las paredes celulares bacterianas , en las que la lisina (y el meso -diaminopimelato) son críticos para la formación de reticulaciones, y por lo tanto, la estabilidad de la pared celular. [79] Este concepto ha sido explorado previamente como un medio para evitar la liberación no deseada de bacterias genéticamente modificadas potencialmente patógenas . Se propuso que una cepa auxotrófica de Escherichia coli ( X 1776) podría ser utilizada para todas las prácticas de modificación genética, ya que la cepa no puede sobrevivir sin la suplementación de DAP, y por lo tanto, no puede vivir fuera de un ambiente de laboratorio. [80] También se ha propuesto que la lisina está involucrada en la absorción intestinal de calcio y la retención renal y, por lo tanto, puede desempeñar un papel en la homeostasis del calcio . [76] Finalmente, se ha demostrado que la lisina es un precursor de la carnitina , que transporta ácidos grasos a las mitocondrias , donde pueden oxidarse para liberar energía. [77] [81] La carnitina se sintetiza a partir de la trimetillisina , que es un producto de la degradación de ciertas proteínas, por lo que la lisina primero debe incorporarse a las proteínas y metilarse antes de convertirse en carnitina. [77] Sin embargo, en los mamíferos, la fuente principal de carnitina es a través de fuentes dietéticas, en lugar de a través de la conversión de lisina. [ 77 ]
En opsinas como la rodopsina y las opsinas visuales (codificadas por los genes OPN1SW , OPN1MW y OPN1LW ), el retinaldehído forma una base de Schiff con un residuo de lisina conservado, y la interacción de la luz con el grupo retinilideno provoca la transducción de señales en la visión del color (ver el ciclo visual para más detalles).
Roles en disputa
Se ha debatido durante mucho tiempo que la lisina, cuando se administra por vía intravenosa u oral, puede aumentar significativamente la liberación de hormonas de crecimiento . [82] Esto ha llevado a los atletas a utilizar la lisina como un medio para promover el crecimiento muscular durante el entrenamiento, sin embargo, hasta la fecha no se ha encontrado evidencia significativa que respalde esta aplicación de la lisina. [82] [83]
Como las proteínas del virus del herpes simple (VHS) son más ricas en arginina y más pobres en lisina que las células que infectan, se han probado suplementos de lisina como tratamiento. Dado que los dos aminoácidos se absorben en el intestino, se recuperan en el riñón y se trasladan a las células por los mismos transportadores de aminoácidos , una abundancia de lisina, en teoría, limitaría la cantidad de arginina disponible para la replicación viral. [84] Los estudios clínicos no proporcionan buena evidencia de la eficacia como profiláctico o en el tratamiento de brotes de VHS. [85] [86] En respuesta a las afirmaciones del producto de que la lisina podría mejorar las respuestas inmunitarias al VHS, una revisión de la Autoridad Europea de Seguridad Alimentaria no encontró evidencia de una relación causa-efecto. La misma revisión, publicada en 2011, no encontró evidencia para apoyar las afirmaciones de que la lisina podría reducir el colesterol, aumentar el apetito, contribuir a la síntesis de proteínas en cualquier función que no sea como un nutriente ordinario, o aumentar la absorción o retención de calcio. [87]
Papeles en la enfermedad
Las enfermedades relacionadas con la lisina son el resultado del procesamiento posterior de la lisina, es decir, la incorporación a proteínas o la modificación en biomoléculas alternativas. El papel de la lisina en el colágeno se ha descrito anteriormente, sin embargo, la falta de lisina e hidroxilisina involucradas en la reticulación de los péptidos de colágeno se ha relacionado con un estado patológico del tejido conectivo. [88] Como la carnitina es un metabolito clave derivado de la lisina involucrado en el metabolismo de los ácidos grasos, una dieta deficiente que carezca de suficiente carnitina y lisina puede conducir a una disminución de los niveles de carnitina, lo que puede tener efectos en cascada significativos en la salud de un individuo. [81] [89] También se ha demostrado que la lisina desempeña un papel en la anemia , ya que se sospecha que la lisina tiene un efecto en la absorción de hierro y, posteriormente, en la concentración de ferritina en el plasma sanguíneo . [90] Sin embargo, aún no se ha dilucidado el mecanismo de acción exacto. [90] Más comúnmente, la deficiencia de lisina se observa en sociedades no occidentales y se manifiesta como desnutrición proteico-energética , que tiene efectos profundos y sistémicos en la salud del individuo. [91] [92] También existe una enfermedad genética hereditaria que implica mutaciones en las enzimas responsables del catabolismo de la lisina, a saber, la enzima bifuncional AASS de la vía de la sacaropina. [93] Debido a la falta de catabolismo de la lisina, el aminoácido se acumula en el plasma y los pacientes desarrollan hiperlisinemia , que puede presentarse como discapacidades neurológicas asintomáticas o graves , que incluyen epilepsia , ataxia , espasticidad y deterioro psicomotor . [93] [94] La importancia clínica de la hiperlisinemia es tema de debate en el campo y algunos estudios no encuentran correlación entre las discapacidades físicas o mentales y la hiperlisinemia. [95] Además de esto, las mutaciones en genes relacionados con el metabolismo de la lisina se han implicado en varios estados patológicos, incluyendo la epilepsia dependiente de piridoxina ( gen ALDH7A1 ), la aciduria α-cetoadípica y α-aminoadípica ( gen DHTKD1 ) y la aciduria glutárica tipo 1 ( gen GCDH ). [44] [96] [97] [98] [99]
La hiperlisinuria se caracteriza por la presencia de cantidades elevadas de lisina en la orina. [100] A menudo se debe a una enfermedad metabólica en la que una proteína implicada en la descomposición de la lisina no es funcional debido a una mutación genética. [101] También puede ocurrir debido a una falla del transporte tubular renal . [101]
Uso de lisina en la alimentación animal

La producción de lisina para la alimentación animal es una industria global importante, alcanzando en 2009 casi 700.000 toneladas por un valor de mercado de más de 1.220 millones de euros. [102] La lisina es un aditivo importante para la alimentación animal porque es un aminoácido limitante a la hora de optimizar el crecimiento de ciertos animales como cerdos y pollos para la producción de carne. La suplementación con lisina permite el uso de proteínas vegetales de menor costo (maíz, por ejemplo, en lugar de soja ) manteniendo al mismo tiempo altas tasas de crecimiento y limitando la contaminación por excreción de nitrógeno. [103] A su vez, sin embargo, la contaminación por fosfato es un importante coste ambiental cuando el maíz se utiliza como alimento para aves de corral y cerdos. [104]
La lisina se produce industrialmente mediante fermentación microbiana, a partir de una base principalmente de azúcar. La investigación en ingeniería genética está buscando activamente cepas bacterianas para mejorar la eficiencia de la producción y permitir que la lisina se produzca a partir de otros sustratos. [102] La bacteria más común utilizada es Corynebacterium glutamicum especialmente mutagenizada o modificada genéticamente para producir lisina, pero también se emplean cepas análogas de Escherichia coli .
En la cultura popular
La película de 1993 Jurassic Park , basada en la novela de 1990 Jurassic Park de Michael Crichton , presenta dinosaurios que fueron alterados genéticamente para que no pudieran producir lisina, un ejemplo de auxotrofia diseñada . [105] Esto se conocía como la "contingencia de lisina" y se suponía que evitaría que los dinosaurios clonados sobrevivieran fuera del parque, obligándolos a depender de suplementos de lisina proporcionados por el personal veterinario del parque. En realidad, ningún animal puede producir lisina; es un aminoácido esencial . [106]
En 1996, la lisina se convirtió en el foco de un caso de fijación de precios , el más grande en la historia de los Estados Unidos. La Archer Daniels Midland Company pagó una multa de 100 millones de dólares estadounidenses y tres de sus ejecutivos fueron condenados y cumplieron condena en prisión. También se encontraron culpables en el caso de fijación de precios dos empresas japonesas ( Ajinomoto , Kyowa Hakko) y una empresa surcoreana (Sewon). [107] Se pueden encontrar grabaciones de video secretas de los conspiradores fijando el precio de la lisina en línea o solicitando el video al Departamento de Justicia de los EE. UU. , División Antimonopolio. Este caso sirvió de base para el libro The Informant: A True Story , [108] y la película The Informant !.
Referencias
 Este artículo fue adaptado de la siguiente fuente bajo licencia CC BY 4.0 (2018) (informes de los revisores): Cody J Hall; Tatiana P. Soares da Costa (1 de junio de 2018). "Lisina: biosíntesis, catabolismo y funciones" (PDF) . WikiJournal of Science . 1 (1): 4. doi : 10.15347/WJS/2018.004 . ISSN 2470-6345. Wikidata Q55120301.
Este artículo fue adaptado de la siguiente fuente bajo licencia CC BY 4.0 (2018) (informes de los revisores): Cody J Hall; Tatiana P. Soares da Costa (1 de junio de 2018). "Lisina: biosíntesis, catabolismo y funciones" (PDF) . WikiJournal of Science . 1 (1): 4. doi : 10.15347/WJS/2018.004 . ISSN 2470-6345. Wikidata Q55120301.
- ^ ab Williams, PA; Hughes, CE; Harris, KD M (2015). "L-Lisina: Aprovechamiento de la difracción de rayos X en polvo para completar el conjunto de estructuras cristalinas de los 20 aminoácidos proteinogénicos codificados directamente". Angew. Chem. Int. Ed. 54 (13): 3973–3977. doi :10.1002/anie.201411520. PMID 25651303.
- ^ "IUPAC-IUB Joint Commission on Biochemical Nomenclature (JCBN). Nomenclatura y simbolismo para aminoácidos y péptidos. Recomendaciones 1983". Biochemical Journal . 219 (2): 345–373. 15 de abril de 1984. doi :10.1042/bj2190345. PMC 1153490 . PMID 6743224.
- ^ Lisina. Proyecto de Biología, Departamento de Bioquímica y Biofísica Molecular, Universidad de Arizona.
- ^ Drechsel E (1889). "Zur Kenntniss der Spaltungsprodukte des Caseïns" [[Contribución] a [nuestro] conocimiento de los productos de escisión de la caseína]. Revista para la química práctica . 2da serie (en alemán). 39 : 425–429. doi :10.1002/prac.18890390135. En la pág. 428, Drechsel presentó una fórmula empírica para la sal de cloroplatinato de lisina – C 8 H 16 N 2 O 2 Cl 2 · PtCl 4 + H 2 O – pero luego admitió que esta fórmula era errónea porque los cristales de la sal contenían etanol en lugar de agua. Véase: Drechsel E (1891). "Der Abbau der Eiweissstoffe" [El desmontaje de las proteínas]. Archiv für Anatomie und Physiologie (en alemán): 248–278; Drechsel E (1877). "Zur Kenntniss der Spaltungsproducte des Caseïns" [Contribución] a [nuestro] conocimiento de los productos de escisión de la caseína] (en alemán). págs. 254–260.
De la pág. 256:] "... die darin enthaltene Base hat die Formel C 6 H 14 N 2 O 2 . Der anfängliche Irrthum ist dadurch veranlasst worden, dass das Chloroplatinat nicht, wie angenommen ward, Krystallwasser, sondern Krystallalkohol enthält, … " (... la base [que] contiene tiene la fórmula [empírica] C 6 H 14 N 2 O 2 . El error inicial fue causado porque el cloroplatinato no contenía agua en el cristal (como se suponía), sino etanol...)
- ^ Vickery, Hubert Bradford.; Schmidt, Carl LA (1 de octubre de 1931). "La historia del descubrimiento de los aminoácidos". Chemical Reviews . 9 (2): 169–318. doi :10.1021/cr60033a001. ISSN 0009-2665.
- ^ Drechsel E (1891). "Der Abbau der Eiweissstoffe" [El desmontaje de proteínas]. Archiv für Anatomie und Physiologie (en alemán): 248–278.; Fischer E. (1891). "Ueber neue Spaltungsproducte des Leimes" [Sobre nuevos productos de escisión de gelatina]. Archiv für Anatomie und Physiologie (en alemán): 465–469.
De la pág. 469:]
"... die Base C
6
H 14 N 2 O 2 , welche mit dem Namen Lysin bezeichnet werden mag, … " (... la base C 6 H
14
N
2
O
2
,
que
puede
designarse
con
el
nombre
"
lisina
"
, … ) [Nota: Ernst Fischer era un estudiante de posgrado de Drechsel.]
- ^ Fischer E, Weigert F (1902). "Synthese der α,ε – Diaminocapronsäure (Lisina inactiva)" [Síntesis de ácido α,ε-diaminohexanoico (lisina [ópticamente] inactiva)]. Berichte der Deutschen Chemischen Gesellschaft (en alemán). 35 (3): 3772–3778. doi :10.1002/cber.190203503211.
- ^ Saffran, M. (abril de 1998). "Nombres de aminoácidos y juegos de salón: desde nombres triviales hasta códigos de una letra, los nombres de aminoácidos han puesto a prueba la memoria de los estudiantes. ¿Es posible una nomenclatura más racional?". Educación bioquímica . 26 (2): 116–118. doi :10.1016/S0307-4412(97)00167-2.
- ^ ab Hudson AO, Bless C, Macedo P, Chatterjee SP, Singh BK, Gilvarg C, Leustek T (enero de 2005). "Biosíntesis de lisina en plantas: evidencia de una variante de las vías bacterianas conocidas". Biochimica et Biophysica Acta (BBA) - Temas generales . 1721 (1–3): 27–36. doi :10.1016/j.bbagen.2004.09.008. PMID 15652176.
- ^ Velasco AM, Leguina JI, Lazcano A (octubre de 2002). "Evolución molecular de las vías biosintéticas de la lisina". Journal of Molecular Evolution . 55 (4): 445–459. Bibcode :2002JMolE..55..445V. doi :10.1007/s00239-002-2340-2. PMID 12355264. S2CID 19460256.
- ^ Miyazaki T, Miyazaki J, Yamane H, Nishiyama M (julio de 2004). "Alfa-aminoadipato aminotransferasa de una bacteria extremadamente termófila, Thermus thermophilus". Microbiología . 150 (Pt 7): 2327–2334. doi : 10.1099/mic.0.27037-0 . PMID 15256574. S2CID 25416966.
- ^ abcdef Xu H, Andi B, Qian J, West AH, Cook PF (2006). "La vía del alfa-aminoadipato para la biosíntesis de lisina en hongos". Bioquímica celular y biofísica . 46 (1): 43–64. doi :10.1385/CBB:46:1:43. PMID 16943623. S2CID 22370361.
- ^ Atkinson SC, Dogovski C, Downton MT, Czabotar PE, Dobson RC, Gerrard JA, Wagner J, Perugini MA (marzo de 2013). "Investigación estructural, cinética y computacional de la DHDPS de Vitis vinifera revela nuevos conocimientos sobre el mecanismo de inhibición alostérica mediada por lisina". Biología molecular de plantas . 81 (4–5): 431–446. doi :10.1007/s11103-013-0014-7. hdl : 11343/282680 . PMID: 23354837. S2CID : 17129774.
- ^ Griffin MD, Billakanti JM, Wason A, Keller S, Mertens HD, Atkinson SC, Dobson RC, Perugini MA, Gerrard JA, Pearce FG (2012). "Caracterización de las primeras enzimas comprometidas con la biosíntesis de lisina en Arabidopsis thaliana". PLOS ONE . 7 (7): e40318. Bibcode :2012PLoSO...740318G. doi : 10.1371/journal.pone.0040318 . PMC 3390394 . PMID 22792278.
- ^ Soares da Costa TP, Muscroft-Taylor AC, Dobson RC, Devenish SR, Jameson GB, Gerrard JA (julio de 2010). "¿Qué tan esencial es la lisina del sitio activo 'esencial' en la dihidrodipicolinato sintasa?". Biochimie . 92 (7): 837–845. doi :10.1016/j.biochi.2010.03.004. PMID 20353808.
- ^ Soares da Costa TP, Christensen JB, Desbois S, Gordon SE, Gupta R, Hogan CJ, Nelson TG, Downton MT, Gardhi CK, Abbott BM, Wagner J, Panjikar S, Perugini MA (2015). "Análisis de la estructura cuaternaria de una enzima oligomérica esencial". Ultracentrifugación analítica . Métodos en enzimología. Vol. 562. págs. 205–223. doi :10.1016/bs.mie.2015.06.020. ISBN 9780128029084. Número de identificación personal 26412653.
- ^ Muscroft-Taylor AC, Soares da Costa TP, Gerrard JA (marzo de 2010). "Nuevos conocimientos sobre el mecanismo de la dihidrodipicolinato sintasa mediante calorimetría de titulación isotérmica". Biochimie . 92 (3): 254–262. doi :10.1016/j.biochi.2009.12.004. PMID 20025926.
- ^ Christensen JB, Soares da Costa TP, Faou P, Pearce FG, Panjikar S, Perugini MA (noviembre de 2016). "Estructura y función de DHDPS y DHDPR de cianobacterias". Informes científicos . 6 (1): 37111. Código bibliográfico : 2016NatSR...637111C. doi :10.1038/srep37111. PMC 5109050 . PMID 27845445.
- ^ McCoy AJ, Adams NE, Hudson AO, Gilvarg C, Leustek T, Maurelli AT (noviembre de 2006). "L,L-diaminopimelato aminotransferasa, una enzima trans-reino compartida por Chlamydia y plantas para la síntesis de diaminopimelato/lisina". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 103 (47): 17909–17914. Bibcode :2006PNAS..10317909M. doi : 10.1073/pnas.0608643103 . PMC 1693846 . PMID 17093042.
- ^ Hudson AO, Gilvarg C, Leustek T (mayo de 2008). "Caracterización bioquímica y filogenética de una nueva vía de biosíntesis de diaminopimelato en procariotas que identifica una forma divergente de la aminotransferasa LL-diaminopimelato". Journal of Bacteriology . 190 (9): 3256–3263. doi :10.1128/jb.01381-07. PMC 2347407 . PMID 18310350.
- ^ Peverelli MG, Perugini MA (agosto de 2015). "Un ensayo acoplado optimizado para cuantificar la actividad de la diaminopimelato descarboxilasa". Biochimie . 115 : 78–85. doi :10.1016/j.biochi.2015.05.004. PMID 25986217.
- ^ ab Soares da Costa TP, Desbois S, Dogovski C, Gorman MA, Ketaren NE, Paxman JJ, Siddiqui T, Zammit LM, Abbott BM, Robins-Browne RM, Parker MW, Jameson GB, Hall NE, Panjikar S, Perugini MA (Agosto de 2016). "Determinantes estructurales que definen la inhibición alostérica de un objetivo antibiótico esencial". Estructura . 24 (8): 1282-1291. doi : 10.1016/j.str.2016.05.019 . PMID 27427481.
- ^ ab Jander G, Joshi V (1 de enero de 2009). "Biosíntesis de aminoácidos derivados del aspartato en Arabidopsis thaliana". The Arabidopsis Book . 7 : e0121. doi :10.1199/tab.0121. PMC 3243338 . PMID 22303247.
- ^ Andi B, West AH, Cook PF (septiembre de 2004). "Mecanismo cinético de la homocitrato sintasa marcada con histidina de Saccharomyces cerevisiae". Bioquímica . 43 (37): 11790–11795. doi :10.1021/bi048766p. PMID 15362863.
- ^ Bhattacharjee JK (1985). "Vía del alfa-aminoadipato para la biosíntesis de lisina en eucariotas inferiores". Critical Reviews in Microbiology . 12 (2): 131–151. doi :10.3109/10408418509104427. PMID 3928261.
- ^ Bhattacharjee JK, Strassman M (mayo de 1967). "Acumulación de ácidos tricarboxílicos relacionados con la biosíntesis de lisina en un mutante de levadura". The Journal of Biological Chemistry . 242 (10): 2542–2546. doi : 10.1016/S0021-9258(18)95997-1 . PMID 6026248.
- ^ Gaillardin CM, Ribet AM, Heslot H (noviembre de 1982). "Formas salvajes y mutantes de la deshidrogenasa homoisocítrica en la levadura Saccharomycopsis lipolytica". Revista Europea de Bioquímica . 128 (2–3): 489–494. doi : 10.1111/j.1432-1033.1982.tb06991.x . PMID 6759120.
- ^ Jaklitsch WM, Kubicek CP (julio de 1990). "Homocitrato sintasa de Penicillium chrysogenum. Localización, purificación de la isoenzima citosólica y sensibilidad a la lisina". The Biochemical Journal . 269 (1): 247–253. doi :10.1042/bj2690247. PMC 1131560 . PMID 2115771.
- ^ Ye ZH, Bhattacharjee JK (diciembre de 1988). "Vía de biosíntesis de lisina y bloqueos bioquímicos de los auxótrofos de lisina de Schizosaccharomyces pombe". Journal of Bacteriology . 170 (12): 5968–5970. doi :10.1128/jb.170.12.5968-5970.1988. PMC 211717 . PMID 3142867.
- ^ Kobashi N, Nishiyama M, Tanokura M (marzo de 1999). "Síntesis de lisina independiente de la aspartato quinasa en una bacteria extremadamente termófila, Thermus thermophilus: la lisina se sintetiza a través del ácido alfa-aminoadípico, no a través del ácido diaminopimélico". Journal of Bacteriology . 181 (6): 1713–1718. doi :10.1128/JB.181.6.1713-1718.1999. PMC 93567 . PMID 10074061.
- ^ Kosuge T, Hoshino T (1999). "La vía alfa-aminoadipato para la biosíntesis de lisina está ampliamente distribuida entre las cepas de Thermus". Journal of Bioscience and Bioengineering . 88 (6): 672–675. doi :10.1016/S1389-1723(00)87099-1. PMID 16232683.
- ^ abcd Nishida H, Nishiyama M, Kobashi N, Kosuge T, Hoshino T, Yamane H (diciembre de 1999). "Un grupo de genes procariotas involucrado en la síntesis de lisina a través de la vía del amino adipato: una clave para la evolución de la biosíntesis de aminoácidos". Genome Research . 9 (12): 1175–1183. doi : 10.1101/gr.9.12.1175 . PMID 10613839.
- ^ abcd Nishida H, Nishiyama M (septiembre de 2000). "¿Cuál es la característica de la síntesis de lisina fúngica a través de la vía del alfa-aminoadipato?". Journal of Molecular Evolution . 51 (3): 299–302. Bibcode :2000JMolE..51..299N. doi :10.1007/s002390010091. PMID 11029074. S2CID 1265909.
- ^ Zabriskie TM, Jackson MD (febrero de 2000). "Biosíntesis y metabolismo de la lisina en hongos". Natural Product Reports . 17 (1): 85–97. doi :10.1039/a801345d. PMID 10714900.
- ^ ab Zhu X, Galili G (mayo de 2004). "El metabolismo de la lisina está regulado simultáneamente por la síntesis y el catabolismo en los tejidos reproductivos y vegetativos". Fisiología vegetal . 135 (1): 129–136. doi :10.1104/pp.103.037168. PMC 429340 . PMID 15122025.
- ^ abcde Tomé D, Bos C (junio de 2007). "Requerimientos de lisina a lo largo del ciclo de vida humano". The Journal of Nutrition . 137 (6 Suppl 2): 1642S–1645S. doi : 10.1093/jn/137.6.1642S . PMID 17513440.
- ^ Blemings KP, Crenshaw TD, Swick RW, Benevenga NJ (agosto de 1994). "La lisina-alfa-cetoglutarato reductasa y la sacaropina deshidrogenasa se encuentran únicamente en la matriz mitocondrial del hígado de rata". The Journal of Nutrition . 124 (8): 1215–1221. doi : 10.1093/jn/124.8.1215 . PMID 8064371.
- ^ Galili G, Tang G, Zhu X, Gakiere B (junio de 2001). "Catabolismo de la lisina: una vía metabólica superregulada por el estrés y el desarrollo". Current Opinion in Plant Biology . 4 (3): 261–266. Bibcode :2001COPB....4..261G. doi :10.1016/s1369-5266(00)00170-9. PMID 11312138.
- ^ Arruda P, Kemper EL, Papes F, Leite A (agosto de 2000). "Regulación del catabolismo de la lisina en plantas superiores". Tendencias en la ciencia de las plantas . 5 (8): 324–330. doi :10.1016/s1360-1385(00)01688-5. PMID 10908876.
- ^ Sacksteder KA, Biery BJ, Morrell JC, Goodman BK, Geisbrecht BV, Cox RP, Gould SJ, Geraghty MT (junio de 2000). "Identificación del gen de la sintetasa de semialdehído alfa-aminoadípico, que es defectuoso en la hiperlisinemia familiar". American Journal of Human Genetics . 66 (6): 1736–1743. doi :10.1086/302919. PMC 1378037 . PMID 10775527.
- ^ Zhu X, Tang G, Galili G (diciembre de 2002). "La actividad de la enzima bifuncional lisina-cetoglutarato reductasa/sacaropina deshidrogenasa de Arabidopsis del catabolismo de la lisina está regulada por la interacción funcional entre sus dos dominios enzimáticos". The Journal of Biological Chemistry . 277 (51): 49655–49661. doi : 10.1074/jbc.m205466200 . PMID 12393892.
- ^ abc Kiyota E, Pena IA, Arruda P (noviembre de 2015). "La vía de la sacaropina en el desarrollo de las semillas y la respuesta al estrés del maíz". Plant, Cell & Environment . 38 (11): 2450–2461. doi : 10.1111/pce.12563 . PMID 25929294.
- ^ Serrano GC, Rezende e Silva Figueira T, Kiyota E, Zanata N, Arruda P (marzo de 2012). "Degradación de la lisina a través de la vía de la sacaropina en bacterias: LKR y SDH en bacterias y su relación con las enzimas vegetales y animales". FEBS Letters . 586 (6): 905–911. Bibcode :2012FEBSL.586..905D. doi : 10.1016/j.febslet.2012.02.023 . PMID 22449979. S2CID 32385212.
- ^ abc Danhauser K, Sauer SW, Haack TB, Wieland T, Staufner C, Graf E, Zschocke J, Strom TM, Traub T, Okun JG, Meitinger T, Hoffmann GF, Prokisch H, Kölker S (diciembre de 2012). "Las mutaciones de DHTKD1 causan aciduria 2-aminoadípica y 2-oxoadípica". Revista Estadounidense de Genética Humana . 91 (6): 1082–1087. doi :10.1016/j.ajhg.2012.10.006. PMC 3516599 . PMID 23141293.
- ^ Sauer SW, Opp S, Hoffmann GF, Koeller DM, Okun JG, Kölker S (enero de 2011). "Modulación terapéutica del metabolismo cerebral de la L-lisina en un modelo murino para la aciduria glutárica tipo I". Brain . 134 (Pt 1): 157–170. doi : 10.1093/brain/awq269 . PMID 20923787.
- ^ Goncalves RL, Bunik VI, Brand MD (febrero de 2016). "Producción de superóxido/peróxido de hidrógeno por el complejo mitocondrial 2-oxoadipato deshidrogenasa". Free Radical Biology & Medicine . 91 : 247–255. doi : 10.1016/j.freeradbiomed.2015.12.020 . PMID 26708453.
- ^ Goh DL, Patel A, Thomas GH, Salomons GS, Schor DS, Jakobs C, Geraghty MT (julio de 2002). "Caracterización del gen humano que codifica la alfa-aminoadipato aminotransferasa (AADAT)". Genética molecular y metabolismo . 76 (3): 172–180. doi :10.1016/s1096-7192(02)00037-9. PMID 12126930.
- ^ Härtel U, Eckel E, Koch J, Fuchs G, Linder D, Buckel W (1 de febrero de 1993). "Purificación de glutaril-CoA deshidrogenasa de Pseudomonas sp., una enzima implicada en la degradación anaeróbica del benzoato". Archivos de Microbiología . 159 (2): 174–181. Código Bibliográfico :1993ArMic.159..174H. doi :10.1007/bf00250279. PMID 8439237. S2CID 2262592.
- ^ Sauer SW (octubre de 2007). "Bioquímica y bioenergética de la deficiencia de glutaril-CoA deshidrogenasa". Journal of Inherited Metabolic Disease . 30 (5): 673–680. doi :10.1007/s10545-007-0678-8. PMID 17879145. S2CID 20609879.
- ^ Nelson DL, Cox MM, Lehninger AL (2013). Principios de bioquímica de Lehninger (6.ª ed.). Nueva York: WH Freeman and Company. ISBN 978-1-4641-0962-1.OCLC 824794893 .
- ^ ab Galili G, Amir R (febrero de 2013). "Fortificación de plantas con los aminoácidos esenciales lisina y metionina para mejorar la calidad nutricional". Revista de biotecnología vegetal . 11 (2): 211–222. doi : 10.1111/pbi.12025 . PMID 23279001.
- ^ ab Wang G, Xu M, Wang W, Galili G (junio de 2017). "Fortificación de cultivos hortícolas con aminoácidos esenciales: una revisión". Revista internacional de ciencias moleculares . 18 (6): 1306. doi : 10.3390/ijms18061306 . PMC 5486127 . PMID 28629176.
- ^ Angelovici R, Fait A, Fernie AR, Galili G (enero de 2011). "Un rasgo de alto contenido de lisina en las semillas está asociado negativamente con el ciclo del TCA y ralentiza la germinación de las semillas de Arabidopsis". The New Phytologist . 189 (1): 148–159. doi : 10.1111/j.1469-8137.2010.03478.x . PMID 20946418.
- ^ Edelman M, Colt M (2016). "Valor nutritivo de las hojas frente a las semillas". Frontiers in Chemistry . 4 : 32. doi : 10.3389/fchem.2016.00032 . PMC 4954856 . PMID 27493937.
- ^ Jiang SY, Ma A, Xie L, Ramachandran S (septiembre de 2016). "Mejora del contenido y la calidad de las proteínas mediante la sobreexpresión de proteínas de fusión sintéticas artificiales con un alto contenido de lisina y treonina en plantas de arroz". Scientific Reports . 6 (1): 34427. Bibcode :2016NatSR...634427J. doi :10.1038/srep34427. PMC 5039639 . PMID 27677708.
- ^ ab Shewry PR (noviembre de 2007). "Mejora del contenido proteico y la composición de los granos de cereales". Journal of Cereal Science . 46 (3): 239–250. doi :10.1016/j.jcs.2007.06.006.
- ^ Prasanna B, Vasal SK, Kassahun B, Singh NN (2001). "Maíz con proteína de calidad". Current Science . 81 (10): 1308–1319. JSTOR 24105845.
- ^ ab Kircher M, Pfefferle W (abril de 2001). "La producción fermentativa de L -lisina como aditivo para piensos animales". Chemosphere . 43 (1): 27–31. Bibcode :2001Chmsp..43...27K. doi :10.1016/s0045-6535(00)00320-9. PMID 11233822.
- ^ Junior L, Alberto L, Letti GV, Soccol CR, Junior L, Alberto L, Letti GV, Soccol CR (2016). "Desarrollo de un salvado enriquecido con L-lisina para nutrición animal mediante fermentación sumergida por Corynebacterium glutamicum utilizando sustratos agroindustriales". Archivos Brasileños de Biología y Tecnología . 59 . doi : 10.1590/1678-4324-2016150519 . ISSN 1516-8913.
- ^ Centro Médico de la Universidad de Maryland. "Lisina" . Consultado el 30 de diciembre de 2009 .
- ^ Young VR, Pellett PL (1994). "Proteínas vegetales en relación con la nutrición humana en proteínas y aminoácidos". American Journal of Clinical Nutrition . 59 (5 Suppl): 1203S–1212S. doi : 10.1093/ajcn/59.5.1203s . PMID 8172124. S2CID 35271281.
- ^ Landon, Amanda J. (2008). "El 'cómo' de las Tres Hermanas: los orígenes de la agricultura en Mesoamérica y el nicho humano". Nebraska Anthropologist : 110–124 . Consultado el 9 de agosto de 2022 .
- ^ Instituto de Medicina de las Academias Nacionales (2005). Ingesta dietética de referencia para macronutrientes. p. 589. doi :10.17226/10490. ISBN 978-0-309-08525-0. Recuperado el 29 de octubre de 2017 .
- ^ "Base de datos de suplementos dietéticos: información sobre mezclas (DSBI)".
L
-Lisina HCl 10000820 80,03 % lisina
- ^ ab Betts MJ, Russell RB (2003). Barnes MR, Gray IC (eds.). Bioinformática para genetistas . John Wiley & Sons, Ltd., págs. 289-316. doi :10.1002/0470867302.ch14. ISBN 978-0-470-86730-3.
- ^ Blickling S, Renner C, Laber B, Pohlenz HD, Holak TA, Huber R (enero de 1997). "Mecanismo de reacción de la sintasa de dihidrodipicolinato de Escherichia coli investigado mediante cristalografía de rayos X y espectroscopia de RMN". Bioquímica . 36 (1): 24–33. doi :10.1021/bi962272d. PMID 8993314. S2CID 23072673.
- ^ Kumar S, Tsai CJ, Nussinov R (marzo de 2000). "Factores que mejoran la termoestabilidad de las proteínas". Ingeniería de proteínas . 13 (3): 179–91. doi : 10.1093/protein/13.3.179 . PMID 10775659.
- ^ Sokalingam S, Raghunathan G, Soundrarajan N, Lee SG (9 de julio de 2012). "Un estudio sobre el efecto de la mutagénesis de la superficie de lisina a arginina en la estabilidad y estructura de las proteínas utilizando proteína fluorescente verde". PLOS ONE . 7 (7): e40410. Bibcode :2012PLoSO...740410S. doi : 10.1371/journal.pone.0040410 . PMC 3392243 . PMID 22792305.
- ^ ab Dambacher S, Hahn M, Schotta G (julio de 2010). "Regulación epigenética del desarrollo mediante la metilación de la lisina de la histona". Heredity . 105 (1): 24–37. doi : 10.1038/hdy.2010.49 . PMID 20442736.
- ^ Martin C, Zhang Y (noviembre de 2005). "Las diversas funciones de la metilación de la lisina de la histona". Nature Reviews. Molecular Cell Biology . 6 (11): 838–849. doi :10.1038/nrm1761. PMID 16261189. S2CID 31300025.
- ^ Black JC, Van Rechem C, Whetstine JR (noviembre de 2012). "Dinámica de la metilación de la lisina de la histona: establecimiento, regulación e impacto biológico". Molecular Cell . 48 (4): 491–507. doi :10.1016/j.molcel.2012.11.006. PMC 3861058 . PMID 23200123.
- ^ Choudhary C, Kumar C, Gnad F, Nielsen ML, Rehman M, Walther TC, Olsen JV, Mann M (agosto de 2009). "La acetilación de lisina actúa sobre complejos proteicos y co-regula las principales funciones celulares". Science . 325 (5942): 834–840. Bibcode :2009Sci...325..834C. doi : 10.1126/science.1175371 . PMID 19608861. S2CID 206520776.
- ^ Shiio Y, Eisenman RN (noviembre de 2003). "La sumoilación de histonas está asociada con la represión transcripcional". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 100 (23): 13225–13230. doi : 10.1073/pnas.1735528100 . PMC 263760 . PMID 14578449.
- ^ Wang H, Wang L, Erdjument-Bromage H, Vidal M, Tempst P, Jones RS, Zhang Y (octubre de 2004). "El papel de la ubiquitinación de la histona H2A en el silenciamiento de Polycomb". Nature . 431 (7010): 873–878. Bibcode :2004Natur.431..873W. doi :10.1038/nature02985. hdl :10261/73732. PMID 15386022. S2CID 4344378.
- ^ ab Shoulders MD, Raines RT (2009). "Estructura y estabilidad del colágeno". Revisión anual de bioquímica . 78 : 929–958. doi :10.1146/annurev.biochem.77.032207.120833. PMC 2846778. PMID 19344236.
- ^ ab Civitelli R, Villareal DT, Agnusdei D, Nardi P, Avioli LV, Gennari C (1992). " Metabolismo dietético de L -lisina y calcio en humanos". Nutrición . 8 (6): 400–405. PMID 1486246.
- ^ abcd Vaz FM, Wanders RJ (febrero de 2002). "Biosíntesis de carnitina en mamíferos". The Biochemical Journal . 361 (Pt 3): 417–429. doi :10.1042/bj3610417. PMC 1222323 . PMID 11802770.
- ^ Yamauchi M, Sricholpech M (25 de mayo de 2012). "Modificaciones postraduccionales de lisina en el colágeno". Ensayos en bioquímica . 52 : 113–133. doi :10.1042/bse0520113. PMC 3499978 . PMID 22708567.
- ^ Vollmer W, Blanot D, de Pedro MA (marzo de 2008). "Estructura y arquitectura de los peptidoglicanos". FEMS Microbiology Reviews . 32 (2): 149–167. doi : 10.1111/j.1574-6976.2007.00094.x . PMID 18194336.
- ^ Curtiss R (mayo de 1978). "Contención biológica y transmisibilidad del vector de clonación". The Journal of Infectious Diseases . 137 (5): 668–675. doi :10.1093/infdis/137.5.668. PMID 351084.
- ^ ab Flanagan JL, Simmons PA, Vehige J, Willcox MD, Garrett Q (abril de 2010). "El papel de la carnitina en la enfermedad". Nutrition & Metabolism . 7 : 30. doi : 10.1186/1743-7075-7-30 . PMC 2861661 . PMID 20398344.
- ^ ab Chromiak JA, Antonio J (2002). "Uso de aminoácidos como agentes liberadores de hormona de crecimiento por deportistas". Nutrition . 18 (7–8): 657–661. doi :10.1016/s0899-9007(02)00807-9. PMID 12093449.
- ^ Corpas E, Blackman MR, Roberson R, Scholfield D, Harman SM (julio de 1993). "La arginina-lisina oral no aumenta la hormona del crecimiento ni el factor de crecimiento similar a la insulina-I en hombres mayores". Journal of Gerontology . 48 (4): M128–M133. doi :10.1093/geronj/48.4.M128. PMID 8315224.
- ^ Gaby AR (2006). "Remedios naturales para el herpes simple". Altern Med Rev . 11 (2): 93–101. PMID 16813459.
- ^ Tomblin FA, Lucas KH (2001). "Lisina para el tratamiento del herpes labial". Am J Health Syst Pharm . 58 (4): 298–300, 304. doi : 10.1093/ajhp/58.4.298 . PMID 11225166.
- ^ Chi CC, Wang SH, Delamere FM, Wojnarowska F, Peters MC, Kanjirath PP (7 de agosto de 2015). "Intervenciones para la prevención del herpes labial (herpes labial)". Base de datos Cochrane de revisiones sistemáticas . 2016 (8): CD010095. doi :10.1002/14651858.CD010095.pub2. PMC 6461191. PMID 26252373 .
- ^ "Opinión científica sobre la fundamentación de las declaraciones de propiedades saludables relacionadas con la L -lisina y la defensa inmunitaria contra el virus del herpes (ID 453), el mantenimiento de concentraciones normales de colesterol LDL en sangre (ID 454, 4669), el aumento del apetito que conduce a un aumento de la energía". Revista EFSA . 9 (4): 2063. 2011. doi :10.2903/j.efsa.2011.2063. ISSN 1831-4732.
- ^ Pinnell SR, Krane SM, Kenzora JE, Glimcher MJ (mayo de 1972). "Un trastorno hereditario del tejido conectivo. Enfermedad del colágeno por deficiencia de hidroxilisina". The New England Journal of Medicine . 286 (19): 1013–1020. doi :10.1056/NEJM197205112861901. PMID 5016372.
- ^ Rudman D, Sewell CW, Ansley JD (septiembre de 1977). "Deficiencia de carnitina en pacientes cirróticos caquécticos". The Journal of Clinical Investigation . 60 (3): 716–723. doi :10.1172/jci108824. PMC 372417 . PMID 893675.
- ^ ab Rushton DH (julio de 2002). "Factores nutricionales y pérdida de cabello". Dermatología clínica y experimental . 27 (5): 396–404. doi :10.1046/j.1365-2230.2002.01076.x. PMID 12190640. S2CID 39327815.
- ^ Emery PW (octubre de 2005). "Cambios metabólicos en la desnutrición". Eye . 19 (10): 1029–1034. doi : 10.1038/sj.eye.6701959 . PMID 16304580.
- ^ Ghosh S, Smriga M, Vuvor F, Suri D, Mohammed H, Armah SM, Scrimshaw NS (octubre de 2010). "Efecto de la suplementación con lisina en la salud y la morbilidad en sujetos pertenecientes a hogares pobres periurbanos en Accra, Ghana". The American Journal of Clinical Nutrition . 92 (4): 928–939. doi : 10.3945/ajcn.2009.28834 . PMID 20720257.
- ^ ab Houten SM, Te Brinke H, Denis S, Ruiter JP, Knegt AC, de Klerk JB, Augoustides-Savvopoulou P, Häberle J, Baumgartner MR, Coşkun T, Zschocke J, Sass JO, Poll-The BT, Wanders RJ, Durán M (abril de 2013). "Bases genéticas de la hiperlisinemia". Revista Orphanet de Enfermedades Raras . 8 : 57. doi : 10.1186/1750-1172-8-57 . PMC 3626681 . PMID 23570448.
- ^ Hoffmann GF, Kölker S (2016). "Trastornos de los ácidos orgánicos cerebrales y otros trastornos del catabolismo de la lisina". Enfermedades metabólicas congénitas . Springer, Berlín, Heidelberg. págs. 333–348. doi :10.1007/978-3-662-49771-5_22. ISBN . 978-3-662-49769-2.
- ^ Dancis J, Hutzler J, Ampola MG, Shih VE, van Gelderen HH, Kirby LT, Woody NC (mayo de 1983). "El pronóstico de la hiperlisinemia: un informe provisional". American Journal of Human Genetics . 35 (3): 438–442. PMC 1685659 . PMID 6407303.
- ^ Mills PB, Struys E, Jakobs C, Plecko B, Baxter P, Baumgartner M, Willemsen MA, Omran H, Tacke U, Uhlenberg B, Weschke B, Clayton PT (marzo de 2006). "Mutaciones en antiquitina en individuos con convulsiones dependientes de piridoxina". Nature Medicine . 12 (3): 307–309. doi :10.1038/nm1366. PMID 16491085. S2CID 27940375.
- ^ Mills PB, Footitt EJ, Mills KA, Tuschl K, Aylett S, Varadkar S, Hemingway C, Marlow N, Rennie J, Baxter P, Dulac O, Nabbout R, Craigen WJ, Schmitt B, Feillet F, Christensen E, De Lonlay P, Pike MG, Hughes MI, Struys EA, Jakobs C, Zuberi SM, Clayton PT (julio de 2010). "Espectro genotípico y fenotípico de la epilepsia dependiente de piridoxina (deficiencia de ALDH7A1)". Brain . 133 (Pt 7): 2148–2159. doi :10.1093/brain/awq143. PMC 2892945 . PMID 20554659.
- ^ Hagen J, te Brinke H, Wanders RJ, Knegt AC, Oussoren E, Hoogeboom AJ, Ruijter GJ, Becker D, Schwab KO, Franke I, Duran M, Waterham HR, Sass JO, Houten SM (septiembre de 2015). "Base genética de la aciduria alfa-aminoadípica y alfa-cetoadípica". Revista de enfermedades metabólicas hereditarias . 38 (5): 873–879. doi : 10.1007/s10545-015-9841-9 . PMID 25860818. S2CID 20379124.
- ^ Hedlund GL, Longo N, Pasquali M (mayo de 2006). "Acidemia glutárica tipo 1". American Journal of Medical Genetics Part C: Seminars in Medical Genetics . 142C (2): 86–94. doi :10.1002/ajmg.c.30088. PMC 2556991 . PMID 16602100.
- ^ "Hiperlisinuria | Defina hiperlisinuria en Dictionary.com".
- ^ ab Walter, John; John Fernandes; Jean-Marie Saudubray; Georges van den Berghe (2006). Enfermedades metabólicas congénitas: diagnóstico y tratamiento . Berlín: Springer. pág. 296. ISBN 978-3-540-28783-4.
- ^ ab "Noruega recibe subvención por mejorar el proceso de producción de lisina". All About Feed . 26 de enero de 2010. Archivado desde el original el 11 de marzo de 2012.
- ^ Toride Y (2004). "Lisina y otros aminoácidos para piensos: producción y contribución a la utilización de proteínas en la alimentación animal". Fuentes de proteínas para la industria de piensos para animales; Consulta y taller de expertos de la FAO sobre fuentes de proteínas para la industria de piensos para animales; Bangkok, 29 de abril - 3 de mayo de 2002. Roma: Organización de las Naciones Unidas para la Agricultura y la Alimentación. ISBN 978-92-5-105012-5. Archivado desde el original el 1 de febrero de 2019.
- ^ Abelson PH (marzo de 1999). "Una posible crisis del fosfato". Science . 283 (5410): 2015. Bibcode : 1999Sci...283.2015A . doi : 10.1126/science.283.5410.2015 . PMID 10206902. S2CID 28106949 .
- ^ Coyne JA (10 de octubre de 1999). "La verdad está muy lejos" . The New York Times . Archivado desde el original el 10 de noviembre de 2012. Consultado el 6 de abril de 2008 .
- ^ Wu G (mayo de 2009). "Aminoácidos: metabolismo, funciones y nutrición". Aminoácidos . 37 (1): 1–17. doi :10.1007/s00726-009-0269-0. PMID 19301095. S2CID 1870305.
- ^ Connor JM (2008). Fijación de precios a nivel mundial (2.ª ed.). Heidelberg: Springer-Verlag. ISBN 978-3-540-78669-6.
- ^ Eichenwald K (2000). El informante: una historia real . Nueva York: Broadway Books. ISBN 978-0-7679-0326-4.


