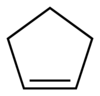
Ciclopenteno
| |||
 | |||
| Nombres | |||
|---|---|---|---|
| Nombre IUPAC preferido Ciclopenteno | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh | |||
| Química biológica | |||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.005.030 | ||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C5H8 | |||
| Masa molar | 68,11 g/mol | ||
| Densidad | 0,771 g/ cm3 | ||
| Punto de fusión | -135 °C (-211 °F; 138 K) | ||
| Punto de ebullición | 44 a 46 °C (111 a 115 °F; 317 a 319 K) | ||
| Peligros | |||
| NFPA 704 (rombo cortafuegos) | |||
| punto de inflamabilidad | -29 °C (-20 °F; 244 K) | ||
| Compuestos relacionados | |||
Compuestos relacionados | Ciclopentadieno Ciclobuteno | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
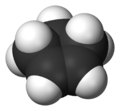
El ciclopenteno es un compuesto químico con la fórmula (CH2 ) 3 ( CH) 2 . Es un líquido incoloro con olor similar al de la gasolina . Tiene pocas aplicaciones, por lo que se utiliza principalmente como componente menor de la gasolina, presente en concentraciones inferiores al 1%. [1] [2] Es uno de los principales cicloalquenos .
Historia y síntesis
El ciclopenteno fue preparado por primera vez por Carl Gärtner en 1893 a partir de yodociclopentano con hidróxido de potasio . Lo llamó pentametenileno ( en alemán : Pentamethenylen ). [3]
El ciclopenteno se produce industrialmente en grandes cantidades mediante el craqueo a vapor de nafta . En el laboratorio, se prepara mediante la deshidratación del ciclopentanol . [4] Los ciclopentenos sustituidos son el producto de la transposición vinilciclopropano-ciclopenteno . [5]
También se puede producir mediante la hidrogenación catalítica del ciclopentadieno . [6]
Reacciones
La polimerización de ciclopenteno mediante catalizadores Ziegler-Natta produce enlaces 1,3, no el polímero con enlaces 1,2 más típico. [7]
La hidrocarboxilación de ciclopenteno catalizada por paladio produce ácido ciclopentanocarboxílico : [8]
- C5H8 + CO + H2O → C5H9CO2H
Referencias
- ^ Dieter Hönicke; Ringo Födisch; Pedro Claus; Michael Olson (2002). "Cicopentadieno y ciclopenteno". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a08_227. ISBN 978-3527306732.
- ^ "Composición de hidrocarburos de las emisiones de vapor de gasolina de los tanques de combustible cerrados". nepis.epa.gov . Agencia de Protección Ambiental de los Estados Unidos. 2011.
- ^ Gärtner, Carl (enero de 1893). "Das Pentamethenylen und sein Dibromür". Justus Liebigs Annalen der Chemie . 275 (2–3): 331–332. doi :10.1002/jlac.18932750217. ISSN 0075-4617.
- ^ BB Corson, VN Ipatieff (1939). "Ciclohexilbenceno". Síntesis orgánicas . 19 : 36. doi :10.15227/orgsyn.019.0036.
- ^ Baldwin, John E. (2003). "Reordenamientos térmicos de vinilciclopropanos a ciclopentenos". Chemical Reviews . 103 (4): 1197–212. doi :10.1021/cr010020z. PMID 12683781.
- ^ D. Hönicke, R. Födisch, P. Claus, M. Olson: ciclopentadieno y ciclopenteno , en: Ullmanns Enzyklopädie der Technischen Chemie 2002 , Wiley-VCH, Weinheim.
- ^ Collins, Scott; Kelly, W. Mark (1992). "La microestructura del poli(ciclopenteno) producido por polimerización de ciclopenteno con catalizadores Ziegler-Natta homogéneos". Macromolecules . 25 (1): 233–7. Bibcode :1992MaMol..25..233C. doi :10.1021/ma00027a039.
- ^ Sang, Rui; Kucmierczyk, Peter; Dühren, Ricarda; Razzaq, Rauf; Dong, Kaiwu; Liu, Jie; Franke, Robert; Jackstell, Ralf; Beller, Matthias (2019). "Síntesis de ácidos carboxílicos mediante hidroxicarbonilación catalizada por paladio". Angewandte Chemie International Edition . 58 (40): 14365–14373. doi : 10.1002/anie.201908451 . PMID 31390131. S2CID 199466915.