Antígeno leucocitario humano
| Antígeno leucocitario humano | |
|---|---|
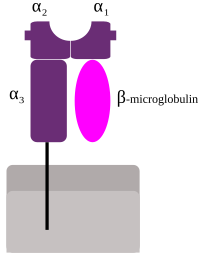 Representación esquemática del MHC de clase I | |
| Identificadores | |
| Símbolo | HLA |
| Interprofesional | IPR037055 |
| Membranoma | 63 |

El sistema del antígeno leucocitario humano ( HLA ) es un complejo de genes en el cromosoma 6 de los humanos que codifican proteínas de la superficie celular responsables de la regulación del sistema inmunológico . [1] El sistema HLA también se conoce como la versión humana del complejo mayor de histocompatibilidad (MHC) que se encuentra en muchos animales. [2]
Las mutaciones en los genes HLA pueden estar relacionadas con enfermedades autoinmunes como la diabetes tipo I y la enfermedad celíaca . El complejo de genes HLA se encuentra en un tramo de 3 Mbp dentro del cromosoma 6, brazo p en 21.3. Los genes HLA son altamente polimórficos , lo que significa que tienen muchos alelos diferentes , lo que les permite ajustar el sistema inmunológico adaptativo . Las proteínas codificadas por ciertos genes también se conocen como antígenos , como resultado de su descubrimiento histórico como factores en los trasplantes de órganos . [3]
Los HLA correspondientes a MHC clase I ( A , B y C ), todos los cuales son el grupo HLA clase 1, presentan péptidos desde el interior de la célula. Por ejemplo, si la célula está infectada por un virus, el sistema HLA lleva fragmentos del virus a la superficie de la célula para que la célula pueda ser destruida por el sistema inmunológico. Estos péptidos se producen a partir de proteínas digeridas que se descomponen en los proteasomas . En general, estos péptidos particulares son polímeros pequeños , de aproximadamente 8-10 aminoácidos de longitud. [4] Los antígenos extraños presentados por MHC clase I atraen a los linfocitos T llamados células T asesinas (también conocidas como células T CD8 -positivas o citotóxicas) que destruyen las células. Algunos trabajos nuevos han propuesto que los antígenos de más de 10 aminoácidos, 11-14 aminoácidos, pueden presentarse en MHC I, provocando una respuesta de células T citotóxicas. [5] Las proteínas MHC de clase I se asocian con la β2-microglobulina , que, a diferencia de las proteínas HLA, está codificada por un gen en el cromosoma 15 .
Los HLA correspondientes a la clase II del MHC ( DP , DM , DO , DQ y DR ) presentan antígenos desde el exterior de la célula a los linfocitos T. Estos antígenos particulares estimulan la multiplicación de las células T auxiliares (también llamadas células T CD4 -positivas), que a su vez estimulan a las células B productoras de anticuerpos para que produzcan anticuerpos contra ese antígeno específico. Los autoantígenos son suprimidos por las células T reguladoras . Predecir qué (fragmentos de) antígenos serán presentados al sistema inmunológico por un cierto tipo de HLA es difícil, pero la tecnología involucrada está mejorando. [6]
Los HLA correspondientes a la clase III del MHC codifican componentes del sistema del complemento .
Los HLA tienen otras funciones. Son importantes en la defensa contra enfermedades. Son la principal causa del rechazo de trasplantes de órganos . Pueden proteger contra el cáncer o no hacerlo (si se regulan a la baja por una infección). [7] El HLA también puede estar relacionado con la percepción que las personas tienen del olor de otras personas y puede estar involucrado en la selección de pareja, ya que al menos un estudio encontró una tasa menor de lo esperado de similitud de HLA entre cónyuges en una comunidad aislada. [8]
Además de los genes que codifican las seis principales proteínas presentadoras de antígenos, muchos otros genes, muchos de ellos implicados en la función inmunitaria, se encuentran en el complejo HLA. La diversidad de HLA en la población humana es un aspecto de la defensa contra las enfermedades y, como resultado, la probabilidad de que dos individuos no relacionados tengan moléculas de HLA idénticas en todos los loci es extremadamente baja. Los genes HLA se han identificado históricamente como resultado de la capacidad de trasplantar órganos con éxito entre individuos con HLA similares. [9]
Funciones
Las proteínas codificadas por los HLA son aquellas que se encuentran en la parte externa de las células del cuerpo y que son (de hecho) exclusivas de esa persona. El sistema inmunológico utiliza los HLA para diferenciar las células propias de las ajenas. Cualquier célula que muestre el tipo de HLA de esa persona pertenece a esa persona y, por lo tanto, no es un invasor.
En enfermedades infecciosas
Cuando un patógeno extraño entra en el cuerpo, unas células específicas llamadas células presentadoras de antígenos (APC) engullen al patógeno a través de un proceso llamado fagocitosis . Las proteínas del patógeno se digieren en pequeños fragmentos ( péptidos ) y se cargan en antígenos HLA (para ser específicos, MHC clase II ). Luego, las células presentadoras de antígenos las muestran a las células T auxiliares CD4+ , [10] que luego producen una variedad de efectos e interacciones de célula a célula para eliminar el patógeno.
Mediante un proceso similar, las proteínas (tanto nativas como extrañas, como las proteínas de los virus) producidas dentro de la mayoría de las células se muestran en los HLA (para ser más específicos, MHC clase I ) en la superficie celular. Las células infectadas pueden ser reconocidas y destruidas por las células T CD8+ . [10]
La imagen de al lado muestra un fragmento de una proteína bacteriana venenosa (péptido SEI) unido a la porción de la hendidura de unión de la molécula HLA-DR1. En la ilustración que se encuentra más abajo, una vista diferente, se puede ver un DQ completo con un péptido unido en una hendidura similar, visto desde un lado. Los péptidos relacionados con enfermedades encajan en estas "ranuras" de manera muy similar a como una mano encaja en un guante.
Cuando se unen, los péptidos se presentan a las células T. Las células T requieren presentación a través de moléculas MHC para reconocer antígenos extraños, un requisito conocido como restricción MHC . Las células T tienen receptores que son similares a los receptores de células B, y cada célula T reconoce solo unas pocas combinaciones de péptidos de clase II de MHC. Una vez que una célula T reconoce un péptido dentro de una molécula de clase II de MHC, puede estimular a las células B que también reconocen la misma molécula en sus receptores de células B. Por lo tanto, las células T ayudan a las células B a producir anticuerpos contra los mismos antígenos extraños. Cada HLA puede unirse a muchos péptidos, y cada persona tiene 3 tipos de HLA y puede tener 4 isoformas de DP, 4 isoformas de DQ y 4 isoformas de DR (2 de DRB1 y 2 de DRB3, DRB4 o DRB5) para un total de 12 isoformas. En tales heterocigotos, es difícil que las proteínas relacionadas con la enfermedad escapen a la detección.
En el rechazo del injerto
Cualquier célula que muestre algún otro tipo de HLA es "no propia" y es vista como un invasor por el sistema inmunológico del cuerpo, lo que resulta en el rechazo del tejido que contiene esas células. Esto es particularmente importante en el caso del tejido trasplantado, porque podría conducir al rechazo del trasplante . Debido a la importancia del HLA en el trasplante, los loci HLA son algunos de los más frecuentemente tipificados por serología y PCR. Se ha demostrado que la tipificación de HLA de alta resolución (HLA-A, HLA-B, HLA-C, HLA-DRB1, HLA-DQB1 y HLA-DPB1) puede ser relevante en el trasplante para identificar una compatibilidad completa, incluso cuando el donante está relacionado. [11]
| Alelo HLA | Enfermedades con mayor riesgo | Riesgo relativo |
|---|---|---|
| HLA-B27 | Espondiloartritis anquilosante | 12 [12] |
| Artritis reactiva | 14 [12] | |
| Uveítis anterior aguda | 15 [12] | |
| HLA-B47 | Deficiencia de 21-hidroxilasa | 15 [12] |
| HLA-B51 | Enfermedad de Behçet | |
| HLA-DR2 | Lupus eritematoso sistémico | 2 a 3 [13] |
| HLA-DR3 | Hepatitis autoinmune | 14 [12] |
| Síndrome de Sjögren primario | 10 [12] | |
| Diabetes mellitus tipo 1 | 5 [12] | |
| Lupus eritematoso sistémico | 2 a 3 [13] | |
| HLA-DR4 | Artritis reumatoide | 4 [12] |
| Diabetes mellitus tipo 1 | 6 [12] | |
| HLA-DR3 y -DR4 combinados | Diabetes mellitus tipo 1 | 15 [12] |
| HLA-DQ2 y HLA-DQ8 | Enfermedad celíaca | 7 [14] |
En autoinmunidad
Los tipos de HLA son hereditarios y algunos de ellos están relacionados con trastornos autoinmunes y otras enfermedades. Las personas con ciertos antígenos HLA tienen más probabilidades de desarrollar ciertas enfermedades autoinmunes, como diabetes tipo I , espondilitis anquilosante , artritis reumatoide , [15] enfermedad celíaca , LES (lupus eritematoso sistémico), miastenia gravis , miositis por cuerpos de inclusión , síndrome de Sjögren y narcolepsia . [16]
La tipificación de HLA ha permitido mejorar y acelerar el diagnóstico de la enfermedad celíaca y la diabetes tipo 1; sin embargo, para que la tipificación de DQ2 sea útil, se requiere una tipificación de B1* de alta resolución (que resuelva *02:01 a partir de *02:02), una tipificación de DQA1* o una serotipificación de DR . La serotipificación actual puede resolver, en un solo paso, DQ8. La tipificación de HLA en la autoinmunidad se utiliza cada vez más como herramienta de diagnóstico. En la enfermedad celíaca , es el único medio eficaz para discriminar entre familiares de primer grado que están en riesgo y aquellos que no lo están, antes de la aparición de síntomas a veces irreversibles, como alergias y enfermedades autoinmunes secundarias.
En el cáncer
Algunas enfermedades mediadas por HLA están directamente implicadas en la promoción del cáncer. La enteropatía sensible al gluten se asocia con una mayor prevalencia de linfoma de células T asociado a la enteropatía, y los homocigotos DR3-DQ2 se encuentran dentro del grupo de mayor riesgo, con cerca del 80% de los casos de linfoma de células T asociado a la enteropatía sensible al gluten. Sin embargo, con mayor frecuencia, las moléculas HLA desempeñan un papel protector, ya que reconocen aumentos de antígenos que no se toleran debido a niveles bajos en el estado normal. Las células anormales podrían ser el objetivo de la apoptosis, que se cree que media en muchos cánceres antes del diagnóstico.
En la selección de pareja
Hay evidencia de que la elección de pareja no es aleatoria con respecto a ciertas características genéticas. [17] [18] Esto ha dado lugar a un campo conocido como emparejamiento genético .
Clasificación
Las proteínas MHC de clase I forman un receptor funcional en la mayoría de las células nucleadas del cuerpo. [1]
Hay tres genes MHC de clase I principales y tres menores en HLA.
Clase I del MHC mayor
Los genes menores son HLA-E , HLA-F y HLA-G . La β 2 -microglobulina se une a las subunidades de los genes mayores y menores para producir un heterodímero.
Existen tres proteínas principales y dos secundarias de la clase II del MHC codificadas por el HLA. Los genes de la clase II se combinan para formar receptores proteicos heterodímeros (αβ) que se expresan típicamente en la superficie de las células presentadoras de antígenos .
Las principales proteínas MHC de clase II solo se encuentran en las células presentadoras de antígenos , las células B y las células T. [1 ]
- HLA-DP
- Cadena α codificada por el locus HLA-DPA1
- Cadena β codificada por el locus HLA-DPB1
- HLA-DQ
- HLA-DR
- Cadena α codificada por el locus HLA-DRA
- 4 cadenas β (solo 3 posibles por persona), codificadas por los loci HLA-DRB1, DRB3, DRB4, DRB5
Las otras proteínas MHC de clase II, DM y DO, se utilizan en el procesamiento interno de antígenos, cargando los péptidos antigénicos generados a partir de patógenos en las moléculas HLA de la célula presentadora de antígenos .
Nomenclatura
Los alelos HLA modernos se suelen anotar con distintos niveles de detalle. La mayoría de las designaciones comienzan con HLA- y el nombre del locus, luego * y un número (par) de dígitos que especifican el alelo. Los dos primeros dígitos especifican un grupo de alelos, también conocidos como supertipos. Las metodologías de tipificación más antiguas a menudo no podían distinguir completamente los alelos y, por lo tanto, se detenían en este nivel. Los dígitos tercero a cuarto especifican un alelo no sinónimo. Los dígitos cinco a seis denotan cualquier mutación sinónima dentro del marco codificante del gen. Los dígitos séptimo y octavo distinguen mutaciones fuera de la región codificante. Letras como L, N, Q o S pueden seguir a la designación de un alelo para especificar un nivel de expresión u otros datos no genómicos conocidos sobre él. Por lo tanto, un alelo completamente descrito puede tener hasta 9 dígitos de longitud, sin incluir el prefijo HLA y la notación del locus. [19]
Variabilidad

Los loci MHC son algunos de los loci codificantes genéticamente más variables en los mamíferos, y los loci HLA humanos no son una excepción. A pesar de que la población humana atravesó varias veces a lo largo de su historia una constricción que fue capaz de fijar muchos loci, los loci HLA parecen haber sobrevivido a dicha constricción con una gran cantidad de variación. [20] De los 9 loci mencionados anteriormente, la mayoría retuvo una docena o más de grupos de alelos para cada loci, una variación mucho más preservada que la gran mayoría de los loci humanos. Esto es consistente con un coeficiente de selección heterocigoto o de equilibrio para estos loci. Además, algunos loci HLA se encuentran entre las regiones codificantes de más rápida evolución en el genoma humano. Se ha observado un mecanismo de diversificación en el estudio de las tribus amazónicas de América del Sur que parecen haber experimentado una intensa conversión genética entre alelos variables y loci dentro de cada clase de gen HLA. [21] Con menor frecuencia, se han observado recombinaciones productivas de mayor alcance a través de genes HLA que producen genes quiméricos.
Se han detectado seis loci con más de 100 alelos en la población humana. De ellos, los más variables son HLA B y HLA DRB1. A partir de 2012, el número de alelos que se han determinado se enumera en la siguiente tabla. Para interpretar esta tabla, es necesario considerar que un alelo es una variante de la secuencia de nucleótidos (ADN) en un locus, de modo que cada alelo difiere de todos los demás alelos en al menos una posición (polimorfismo de un solo nucleótido, SNP). La mayoría de estos cambios dan lugar a un cambio en las secuencias de aminoácidos que dan lugar a diferencias funcionales leves o importantes en la proteína.
Existen cuestiones que limitan esta variación. Algunos alelos, como DQA1*05:01 y DQA1*05:05, codifican proteínas con productos procesados de manera idéntica. Otros alelos, como DQB1*0201 y DQB1*0202, producen proteínas que son funcionalmente similares. En el caso de la clase II (DR, DP y DQ), las variantes de aminoácidos dentro de la hendidura de unión del péptido del receptor tienden a producir moléculas con diferente capacidad de unión.
Sin embargo, las frecuencias genéticas de los alelos más comunes (>5%) de HLA-A, -B, -C y HLA-DPA1, -DPB1, -DQA1, -DQB1 y -DRB1 de Sudamérica se han reportado a partir de la tipificación y secuenciación llevada a cabo en estudios de diversidad genética y casos y controles. [22] Además, se ha compilado información sobre las frecuencias alélicas de los genes HLA-I y HLA-II para la población europea. [23] [24] En ambos casos la distribución de frecuencias alélicas revela una variación regional relacionada con la historia de las poblaciones.
Tablas de alelos variantes
Número de alelos variantes en loci de clase I según la base de datos IMGT-HLA, última actualización en octubre de 2018:
| MHC clase I | |
|---|---|
| lugar | # [25] [26] |
| Antígenos principales | |
| HLA-A | 4.340 |
| HLA-B | 5,212 |
| HLA-C | 3.930 |
| Antígenos menores | |
| HLA-E | 27 |
| HLA-F | 31 |
| HLA-G | 61 |
Número de alelos variantes en los loci de clase II (DM, DO, DP, DQ y DR):
| MHC clase II | ||||
|---|---|---|---|---|
| HLA | -A1 | -B1 | -B3 a -B5 1 | Teoría posible |
| lugar | # [26] | # [26] | # [26] | combinaciones |
| DM- | 7 | 13 | 91 | |
| HACER- | 12 | 13 | 156 | |
| DP- | 67 | 1.014 | 16.036 | |
| DQ- | 95 | 1.257 | 34.528 | |
| DR- | 7 | 2,593 | 312 | 11.431 |
| 1 DRB3, DRB4, DRB5 tienen presencia variable en humanos | ||||
Tipo de variante de característica de secuencia (SFVT)
La gran variabilidad de los genes HLA plantea desafíos importantes a la hora de investigar el papel de las variaciones genéticas de HLA en las enfermedades. Los estudios de asociación de enfermedades suelen tratar cada alelo HLA como una única unidad completa, lo que no ilumina las partes de la molécula asociadas con la enfermedad. Karp DR et al. describe un nuevo enfoque de tipo de variante de característica de secuencia (SFVT) para el análisis genético de HLA que clasifica las proteínas HLA en características de secuencia más pequeñas (SF) biológicamente relevantes y sus tipos de variantes (VT). [27] Las características de secuencia son combinaciones de sitios de aminoácidos definidos en función de la información estructural (p. ej., hoja beta 1), información funcional (p. ej., unión al antígeno del péptido) y polimorfismo. Estas características de secuencia pueden superponerse y ser continuas o discontinuas en la secuencia lineal. Los tipos de variantes para cada característica de secuencia se definen en función de todos los polimorfismos conocidos en el locus HLA que se describe. La categorización SFVT de HLA se aplica en el análisis de asociación genética para que se puedan identificar los efectos y funciones de los epítopos compartidos por varios alelos HLA. Se han descrito las características de la secuencia y sus tipos de variantes para todas las proteínas HLA clásicas; el repositorio internacional de SFVT de HLA se mantendrá en la base de datos IMGT/HLA. [28] Se puede encontrar una herramienta para convertir los alelos HLA en sus SFVT componentes en el sitio web del Portal de análisis y base de datos de inmunología (ImmPort). [29]
Alelos comunes, bien documentados y raros
Aunque el número de alelos HLA individuales que se han identificado es grande, aproximadamente el 40% de estos alelos parecen ser únicos, habiéndose identificado solamente en individuos individuales. [30] [31] Aproximadamente un tercio de los alelos se han reportado más de tres veces en individuos no relacionados. [31] [32] Debido a esta variación en la tasa a la que se detectan los alelos HLA individuales, se han hecho intentos para categorizar los alelos en cada locus HLA expresado en términos de su prevalencia. El resultado es un catálogo de alelos HLA comunes y bien documentados (CWD), [32] [33] y un catálogo de alelos HLA raros y muy raros. [30] [31]
Los alelos HLA comunes se definen como aquellos que se han observado con una frecuencia de al menos 0,001 en poblaciones de referencia de al menos 1500 individuos. [32] [33] Los alelos HLA bien documentados se definieron originalmente como aquellos que se habían notificado al menos tres veces en individuos no relacionados, [32] y ahora se definen como aquellos que se han detectado al menos cinco veces en individuos no relacionados mediante la aplicación de un método de tipificación basada en secuencias (SBT), o al menos tres veces mediante un método SBT y en un haplotipo específico en individuos no relacionados. [33] Los alelos raros se definen como aquellos que se han notificado de una a cuatro veces, y los alelos muy raros como aquellos que se notificaron solo una vez. [30] [31]
Tabla de alelos HLA en cada categoría de prevalencia
Si bien las designaciones actuales de CWD y de raro o muy raro se desarrollaron utilizando diferentes conjuntos de datos y diferentes versiones de la base de datos IMGT/HLA , [31] [33] la fracción aproximada de alelos en cada locus HLA en cada categoría se muestra a continuación.
Locus HLA | No. de alelos comunes [33] | % de alelos comunes [33] | No. de alelos bien documentados [33] | % de alelos bien documentados [33] | No. alelos raros [31] | % de alelos raros [31] | No. alelos muy raros [31] | % de alelos muy raros [31] | % alelos categorizados |
|---|---|---|---|---|---|---|---|---|---|
| A | 68 | 3,4% | 178 | 8,8% | 145 | 21,5% | 280 | 41,6% | ~75% |
| B | 125 | 4,8% | 242 | 9,3% | 190 | 17,6% | 468 | 43,5% | ~75% |
| do | 44 | 2,8% | 102 | 6,6% | 77 | 21,4% | 154 | 42,8% | ~74% |
| DRB1 | 79 | 6,8% | 147 | 12,7% | 133 | 22,7% | 206 | 35,2% | ~77% |
| DRB3 | 5 | 8,6% | 7 | 12,1% | ~21% | ||||
| DRB4 | 6 | 40,0% | 2 | 13,3% | ~53% | ||||
| DRB5 | 5 | 25,0% | 3 | 15,0% | ~40% | ||||
| DQA1 | 15 | 31,9% | 4 | 8,5% | 9 | 26,5% | 7 | 20,6% | ~88% |
| DQB1 | 22 | 12,5% | 8 | 4,5% | 26 | 28,9% | 42 | 45,2% | ~91% |
| DPA1 | 6 | 17,6% | 0 | 0,0% | 4 | 14,8% | 15 | 55,6% | ~88% |
| DPB1 | 40 | 28,8% | 14 | 9.0% | 29 | 22,7% | 29 | 32,8% | ~90% |
| Todos los lugares | 415 | 5,3% | 707 | 9.0% | 613 | 20,6% | 1214 | 40,8% | ~76% |
Examinando los tipos de HLA
Nombres de serotipos y alelos
Existen dos sistemas paralelos de nomenclatura que se aplican al HLA. El primero, y el más antiguo, se basa en el reconocimiento serológico (basado en anticuerpos). En este sistema, a los antígenos se les asignaron letras y números (p. ej., HLA-B27 o, abreviado, B27). Se desarrolló un sistema paralelo que permitió una definición más refinada de los alelos. En este sistema, se utiliza un "HLA" junto con una letra, *, y un número de cuatro o más dígitos (p. ej., HLA-B*08:01, A*68:01, A*24:02:01N N=Null) para designar un alelo específico en un locus HLA determinado . Los loci HLA se pueden clasificar además en MHC clase I y MHC clase II (o, en raras ocasiones, locus D). Cada dos años, se presenta una nomenclatura para ayudar a los investigadores a interpretar los serotipos de los alelos. [25]
Serotipificación
Para crear un reactivo de tipificación, se extraía sangre de animales o humanos, se dejaba que las células sanguíneas se separaran del suero y el suero se diluía hasta alcanzar su sensibilidad óptima y se utilizaba para tipificar células de otros individuos o animales. De este modo, la serotipificación se convirtió en una forma de identificar de forma rudimentaria los receptores HLA y las isoformas de los receptores. Con el paso de los años, los anticuerpos de serotipificación se fueron perfeccionando a medida que mejoraban las técnicas para aumentar la sensibilidad y seguían apareciendo nuevos anticuerpos de serotipificación. Uno de los objetivos del análisis de serotipos es llenar los vacíos en el análisis. Es posible hacer predicciones basadas en el método de "raíz cuadrada", "máxima verosimilitud" o análisis de haplotipos familiares para dar cuenta de los alelos tipificados adecuadamente. Estos estudios que utilizaban técnicas de serotipificación revelaban con frecuencia, en particular para poblaciones no europeas o del noreste de Asia, muchos serotipos nulos o en blanco. Esto fue particularmente problemático para el locus Cw hasta hace poco, y casi la mitad de los serotipos Cw no se tipificaron en la encuesta de 1991 de la población humana.
Existen varios tipos de serotipos. Un serotipo de antígeno amplio es una medida cruda de la identidad de las células. Por ejemplo, el serotipo HLA A9 reconoce células de individuos portadores de A23 y A24. También puede reconocer células que A23 y A24 no detectan debido a pequeñas variaciones. A23 y A24 son antígenos divididos, pero los anticuerpos específicos para cualquiera de ellos se utilizan normalmente con más frecuencia que los anticuerpos para antígenos amplios.
Escritura celular
Un ensayo celular representativo es el cultivo de linfocitos mixtos (MLC) y se utiliza para determinar los tipos de HLA de clase II. [34] El ensayo celular es más sensible para detectar diferencias de HLA que la serotipificación. Esto se debe a que las diferencias menores no reconocidas por los aloantisueros pueden estimular las células T. Esta tipificación se designa como tipos Dw. El DR1 serotipificado se define celularmente como Dw1 o Dw20 y así sucesivamente para otros DR serotipificados. La Tabla [35] muestra las especificidades celulares asociadas para los alelos DR. Sin embargo, la tipificación celular tiene inconsistencia en la reacción entre individuos de tipo celular, a veces resultando diferente a lo previsto. Junto con la dificultad del ensayo celular para generar y mantener reactivos de tipificación celular, el ensayo celular está siendo reemplazado por el método de tipificación basado en ADN. [34]
Secuenciación genética
Se pueden observar reacciones menores a subregiones que muestran similitud con otros tipos en los productos génicos de alelos de un grupo de serotipos. La secuencia de los antígenos determina las reactividades de los anticuerpos, por lo que tener una buena capacidad de secuenciación (o tipificación basada en secuencias) evita la necesidad de reacciones serológicas. Por lo tanto, las reacciones de diferentes serotipos pueden indicar la necesidad de secuenciar el HLA de una persona para determinar una nueva secuencia génica.
Los tipos amplios de antígenos siguen siendo útiles, como la tipificación de poblaciones muy diversas con muchos alelos HLA no identificados (África, Arabia, [36] el sudeste de Irán [37] y Pakistán, India [38] ). África, el sur de Irán y Arabia muestran la dificultad de tipificar áreas que fueron colonizadas anteriormente. La diversidad alélica hace necesario el uso de una tipificación amplia de antígenos seguida de la secuenciación genética porque existe un mayor riesgo de identificación errónea mediante técnicas de serotipificación.
Al final, un taller, basado en la secuencia, decide qué alelo nuevo va a qué serogrupo, ya sea por secuencia o por reactividad. Una vez que se verifica la secuencia, se le asigna un número. Por ejemplo, un alelo nuevo de B44 puede obtener un serotipo (es decir, B44) y una identificación de alelo, es decir, B*44:65, ya que es el alelo B44 número 65 descubierto. Marsh et al. (2005) [25] puede considerarse un libro de códigos para los serotipos y genotipos de HLA, y un nuevo libro bianual con actualizaciones mensuales en Tissue Antigens .
Fenotipificación
La tipificación genética es diferente de la secuenciación genética y la serotipificación. Con esta estrategia, se utilizan iniciadores de PCR específicos para una región variante del ADN (llamados iniciadores específicos de secuencia). Si se encuentra un producto del tamaño correcto, se supone que se ha identificado el alelo HLA. Las nuevas secuencias genéticas a menudo dan lugar a una apariencia cada vez más ambigua. Debido a que la tipificación genética se basa en la SSP-PCR, es posible que se pasen por alto nuevas variantes, en particular en los loci de clase I y DRB1.
Por ejemplo, la PCR-SSP en situaciones clínicas se suele utilizar para identificar fenotipos HLA. Un ejemplo de fenotipo extendido para una persona podría ser:
A *01:01 / *03:01 , C *07:01 / *07:02 , B *07:02 / *08:01 , DRB1 *03:01 / *15:01 , DQA1 *05:01 / *01:02 , DQB1 *02:01 / *06:02
En general, es idéntico al serotipo extendido: A1, A3, B7, B8, DR3, DR15(2), DQ2, DQ6(1)
En muchas poblaciones, como la japonesa o la europea, se han tipificado tantos pacientes que los alelos nuevos son relativamente raros, y por lo tanto la SSP-PCR es más que adecuada para la resolución de alelos. Los haplotipos se pueden obtener tipificando a los miembros de la familia en áreas del mundo donde la SSP-PCR no puede reconocer alelos y la tipificación requiere la secuenciación de alelos nuevos. Las áreas del mundo donde la SSP-PCR o la serotipificación pueden ser inadecuadas incluyen África central, África oriental, partes del sur de África, Arabia, el sur de Irán, Pakistán e India.
Haplotipos
Un haplotipo HLA es una serie de "genes" HLA (loci-alelos) por cromosoma, uno transmitido por la madre y otro por el padre.
El fenotipo ejemplificado arriba es uno de los más comunes en Irlanda y es el resultado de dos haplotipos genéticos comunes :
A *01:01 ; C *07:01 ; B *08:01 ; DRB1 *03:01 ; DQA1 *05:01 ; DQB1 *02:01 (Por serotipificación A1-Cw7-B8-DR3-DQ2 )
que se llama 'super B8' o 'haplotipo ancestral' y
A *03:01 ; C *07:02 ; B *07:02 ; DRB1 *15:01 ; DQA1 *01:02 ; DQB1 *06:02 (Mediante la serotipificación A3-Cw7-B7-DR15-DQ6 o la versión anterior "A3-B7-DR2-DQ1")
Estos haplotipos se pueden utilizar para rastrear migraciones en la población humana porque a menudo son como una huella dactilar de un evento que ha ocurrido en la evolución. El haplotipo Super-B8 se enriquece en Irlanda occidental, disminuye a lo largo de gradientes que se alejan de esa región y se encuentra solo en áreas del mundo a las que han migrado los europeos occidentales. El haplotipo "A3-B7-DR2-DQ1" está más ampliamente extendido, desde Asia oriental hasta Iberia. El haplotipo Super-B8 está asociado con una serie de enfermedades autoinmunes asociadas con la dieta. Hay cientos de miles de haplotipos extendidos, pero solo unos pocos muestran un carácter visible y nodal en la población humana.
Papel de la variación alélica
Los estudios en humanos y animales sugieren que existe un mecanismo de selección heterocigótico que opera en estos loci como explicación de esta variabilidad. [39] Un mecanismo propuesto es la selección sexual en la que las hembras pueden detectar a los machos con HLA diferentes en relación con su propio tipo. [40] Si bien los loci que codifican DQ y DP tienen menos alelos, las combinaciones de A1:B1 pueden producir un potencial teórico de 7755 heterodímeros DQ y 5270 DP αβ, respectivamente. Si bien no existe una cantidad cercana a esta de isoformas en la población humana, cada individuo puede portar 4 isoformas variables de DQ y DP, lo que aumenta la cantidad potencial de antígenos que estos receptores pueden presentar al sistema inmunológico.
Los estudios de las posiciones variables de DP, DR y DQ revelan que los residuos de contacto de antígenos peptídicos en las moléculas de clase II son con mayor frecuencia el sitio de variación en la estructura primaria de la proteína. Por lo tanto, a través de una combinación de variación alélica intensa y/o apareamiento de subunidades, los receptores de péptidos de clase II son capaces de unirse a una variación casi infinita de péptidos de 9 aminoácidos o más de longitud, protegiendo a las subpoblaciones que se cruzan entre sí de enfermedades nacientes o epidémicas. Los individuos de una población con frecuencia tienen diferentes haplotipos, y esto da como resultado muchas combinaciones, incluso en grupos pequeños. Esta diversidad mejora la supervivencia de dichos grupos e impide la evolución de epítopos en patógenos, que de otro modo podrían ser protegidos del sistema inmunológico.
Anticuerpos
Los anticuerpos HLA normalmente no aparecen de forma natural y, con pocas excepciones, se forman como resultado de un desafío inmunológico a un material extraño que contiene HLA no propios a través de una transfusión de sangre, un embarazo (antígenos heredados del padre) o un trasplante de órgano o tejido.
Se han propuesto anticuerpos contra haplotipos HLA asociados a enfermedades como tratamiento para enfermedades autoinmunes graves. [41]
Se ha descubierto que los anticuerpos HLA específicos del donante están asociados con la falla del injerto en trasplantes renales, cardíacos, pulmonares y hepáticos. Estos anticuerpos HLA específicos del donante pueden existir antes del trasplante como consecuencia de la sensibilización a trasplantes previos o a través de embarazos, pero también pueden aparecer de novo después del trasplante. Existe un vínculo claro entre el riesgo de sensibilización a anticuerpos HLA y el desajuste HLA (molecular) entre donante y receptor. [42]
Compatibilidad de HLA para hermanos enfermos
En algunas enfermedades que requieren trasplante de células madre hematopoyéticas , se puede utilizar el diagnóstico genético preimplantacional para dar lugar a un hermano con HLA compatible, aunque existen consideraciones éticas. [43]
Véase también
Referencias
- ^ abc Choo SY (febrero de 2007). "El sistema HLA: genética, inmunología, pruebas clínicas e implicaciones clínicas". Yonsei Medical Journal . 48 (1): 11–23. doi :10.3349/ymj.2007.48.1.11. PMC 2628004 . PMID 17326240.
- ^ "Antígeno leucocitario humano (HLA)". MS Trust . Diciembre de 2020 . Consultado el 7 de junio de 2021 .
- ^ Nakamura T, Shirouzu T, Nakata K, Yoshimura N, Ushigome H (septiembre de 2019). "El papel del complejo mayor de histocompatibilidad en el trasplante de órganos: el análisis de anticuerpos anticomplejo mayor de histocompatibilidad específicos del donante pasa a la siguiente etapa". Revista internacional de ciencias moleculares . 20 (18): 4544. doi : 10.3390/ijms20184544 . PMC 6769817 . PMID 31540289.
- ^ Matsumura M, Fremont DH, Peterson PA, Wilson IA (agosto de 1992). "Principios emergentes para el reconocimiento de antígenos peptídicos por moléculas de MHC de clase I". Science . 257 (5072): 927–34. Bibcode :1992Sci...257..927M. doi :10.1126/science.1323878. PMID 1323878.
- ^ Burrows SR, Rossjohn J, McCluskey J (enero de 2006). "¿Hemos acortado demasiado el tiempo que nos tomaba el mapeo de los epítopos de CTL?". Trends in Immunology . 27 (1): 11–6. doi :10.1016/j.it.2005.11.001. PMID 16297661.
- ^ Bouzid R, de Beijer MT, Luijten RJ, Bezstarosti K, Kessler AL, Bruno MJ, Peppelenbosch MP, Demmers JA, Buschow SI (mayo de 2021). "Evaluación empírica del uso de la unión computacional de HLA como un filtro temprano para el flujo de trabajo de descubrimiento de epítopos basado en espectrometría de masas". Cánceres . 13 (10): 2307. doi : 10.3390/cancers13102307 . PMC 8150281 . PMID 34065814.
- ^ Galbraith W, Wagner MC, Chao J, Abaza M, Ernst LA, Nederlof MA, et al. (1991). "Citometría de imágenes mediante fluorescencia multiparamétrica". Cytometry . 12 (7): 579–96. doi :10.1002/cyto.990120702. PMID 1782829.
- ^ Brennan PA, Kendrick KM (diciembre de 2006). "Olores sociales de los mamíferos: atracción y reconocimiento individual". Philosophical Transactions of the Royal Society of London. Serie B, Ciencias Biológicas . 361 (1476): 2061–78. doi :10.1098/rstb.2006.1931. PMC 1764843 . PMID 17118924.
- ^ Singal DP, Mickey MR, Mittal KK, Terasaki PI (noviembre de 1968). "Serotipificación para homotrasplante. XVII. Estudios preliminares de subunidades y alelos de HL-A". Trasplante . 6 (8): 904–912. doi : 10.1097/00007890-196811000-00005 . PMID 5696819. S2CID 32428268.
- ^ ab Taylor CJ, Bolton EM, Bradley JA (agosto de 2011). "Consideraciones inmunológicas para el almacenamiento de células madre pluripotentes inducidas y embrionarias". Philosophical Transactions of the Royal Society of London. Serie B, Biological Sciences . 366 (1575): 2312–22. doi :10.1098/rstb.2011.0030. PMC 3130422 . PMID 21727137.
- ^ Agarwal RK, Kumari A, Sedai A, Parmar L, Dhanya R, Faulkner L (septiembre de 2017). "El caso de la tipificación HLA de 6 loci extendida de alta resolución para identificar donantes relacionados en el subcontinente indio". Biología del trasplante de sangre y médula ósea . 23 (9): 1592–1596. doi : 10.1016/j.bbmt.2017.05.030 . PMID 28603069.
- ^ abcdefghij Tabla 5-7 en: Mitchell RS, Kumar V, Abbas AK, Fausto N (2007). Robbins Basic Pathology . Filadelfia: Saunders. ISBN 978-1-4160-2973-1.8va edición.
- ^ ab Los valores se dan para caucásicos, según la página 61 (columna derecha) en: Salmon J, Wallace DJ, Dubois EL, Kirou KA, Hahn B, Lehman TA (2007). Lupus eritematoso de Dubois . Filadelfia: Lippincott Williams & Wilkins. ISBN 978-0-7817-9394-0.
- ^ Margaritte-Jeannin P, Babron MC, Bourgey M, Louka AS, Clot F, Percopo S, et al. (junio de 2004). "Riesgos relativos de HLA-DQ para la enfermedad celíaca en poblaciones europeas: un estudio del Clúster Genético Europeo sobre la Enfermedad Celíaca". Antígenos tisulares . 63 (6): 562–7. doi :10.1111/j.0001-2815.2004.00237.x. PMID 15140032.
- ^ Kurkó J, Besenyei T, Laki J, Glant TT, Mikecz K, Szekanecz Z (octubre de 2013). "Genética de la artritis reumatoide: una revisión exhaustiva". Clinical Reviews in Allergy & Immunology . 45 (2): 170–9. doi :10.1007/s12016-012-8346-7. PMC 3655138 . PMID 23288628.
- ^ Mignot E, Lin L, Rogers W, Honda Y, Qiu X, Lin X, et al. (marzo de 2001). "Las interacciones complejas de HLA-DR y -DQ confieren riesgo de narcolepsia-cataplejía en tres grupos étnicos". American Journal of Human Genetics . 68 (3): 686–99. doi :10.1086/318799. PMC 1274481 . PMID 11179016.
- ^ Jokiniemi A, Magris M, Ritari J, Kuusipalo L, Lundgren T, Partanen J, Kekäläinen J (agosto de 2020). "Emparejamiento genético poscopulatorio: efectos dependientes de HLA del moco cervical en la función del esperma humano". Actas. Ciencias Biológicas . 287 (1933): 20201682. doi :10.1098/rspb.2020.1682. PMC 7482290 . PMID 32811307.
- ^ Jokiniemi A, Kuusipalo L, Ritari J, Koskela S, Partanen J, Kekäläinen J (noviembre de 2020). "Incompatibilidad inmunogenética a nivel de gametos en humanos: ¿hacia una comprensión más profunda de la fertilización y la infertilidad?". Herencia . 125 (5): 281–289. doi :10.1038/s41437-020-0350-8. PMC 7553942 . PMID 32747723. S2CID 220947699.
- ^ "Nomenclatura HLA @ hla.alleles.org". hla.alleles.org . Archivado desde el original el 2 de mayo de 2018 . Consultado el 2 de mayo de 2018 .
- ^ Shennan DH (2006). Evolución y la espiral de la tecnología . Trafford Publishing. ISBN 978-1-55212-518-2.
- ^ Parham P, Ohta T (abril de 1996). "Biología poblacional de la presentación de antígenos por moléculas de MHC de clase I". Science . 272 (5258): 67–74. Bibcode :1996Sci...272...67P. doi :10.1126/science.272.5258.67. PMID 8600539. S2CID 22209086..
- ^ Requena D, Médico A, Chacón RD, Ramírez M, Marín-Sánchez O (2020). "Identificación de nuevos candidatos a epítopos en proteínas del SARS-CoV-2 para América del Sur: una revisión de frecuencias HLA por país". Frontiers in Immunology . 11 : 2008. doi : 10.3389/fimmu.2020.02008 . PMC 7494848 . PMID 33013857.
- ^ Nunes JM, Buhler S, Roessli D, Sanchez-Mazas A (mayo de 2014). "El sistema de análisis de datos HLA-net GENE[RATE] para HLA-net y su aplicación a 145 muestras de población de Europa y áreas vecinas". Antígenos tisulares . 83 (5): 307–23. doi :10.1111/tan.12356. PMID 24738646.
- ^ Sanchez-Mazas A, Buhler S, Nunes JM (2013). "Un nuevo mapa HLA de Europa: variación genética regional y su implicación para la historia del poblamiento, estudios de asociación de enfermedades y trasplante de tejidos". Herencia humana . 76 (3–4): 162–77. doi : 10.1159/000360855 . PMID 24861861.
- ^ abc Marsh SG, Albert ED, Bodmer WF, Bontrop RE, Dupont B, Erlich HA, et al. (abril de 2010). "Nomenclatura de factores del sistema HLA, 2010". Antígenos tisulares . 75 (4): 291–455. doi :10.1111/j.1399-0039.2010.01466.x. PMC 2848993 . PMID 20356336.
- ^ abcd EBI Web Services. «Estadísticas < IMGT/HLA < IPD < EMBL-EBI». www.ebi.ac.uk. Archivado desde el original el 20 de septiembre de 2012. Consultado el 2 de mayo de 2018 .
- ^ Karp DR, Marthandan N, Marsh SG, Ahn C, Arnett FC, Deluca DS, et al. (febrero de 2010). "Análisis de tipo de variante de característica de secuencia novedosa de la asociación genética HLA en la esclerosis sistémica". Human Molecular Genetics . 19 (4): 707–19. doi :10.1093/hmg/ddp521. PMC 2807365 . PMID 19933168.
- ^ "Base de datos IMGT/HLA". Archivado desde el original el 24 de septiembre de 2006.
- ^ "Portal de análisis y base de datos de inmunología (ImmPort)". Archivado desde el original el 26 de julio de 2011.
- ^ abc Middleton D, Gonzalez F, Fernandez-Vina M, Tiercy JM, Marsh SG, Aubrey M, et al. (diciembre de 2009). "Un enfoque bioinformático para determinar la rareza de los alelos HLA". Antígenos tisulares . 74 (6): 480–5. doi :10.1111/j.1399-0039.2009.01361.x. PMID 19793314.
- ^ abcdefghi González-Galarza FF, Mack SJ, Hollenbach J, Fernández-Vina M, Setterholm M, Kempenich J, et al. (febrero de 2013). "16 (th) IHIW: ampliación del número de recursos y análisis bioinformáticos para la investigación de alelos raros de HLA". Revista Internacional de Inmunogenética . 40 (1): 60–5. doi :10.1111/iji.12030. PMID 23198982. S2CID 205192491.
- ^ abcd Cano P, Klitz W, Mack SJ, Maiers M, Marsh SG, Noreen H, et al. (mayo de 2007). "Alelos HLA comunes y bien documentados: informe del comité ad hoc de la sociedad estadounidense de histocompatibilidad e inmunogenética". Inmunología humana . 68 (5): 392–417. doi :10.1016/j.humimm.2007.01.014. PMID 17462507.
- ^ abcdefgh Mack SJ, Cano P, Hollenbach JA, He J, Hurley CK, Middleton D, et al. (abril de 2013). "Alelos HLA comunes y bien documentados: actualización de 2012 del catálogo CWD". Antígenos tisulares . 81 (4): 194–203. doi :10.1111/tan.12093. PMC 3634360 . PMID 23510415.
- ^ ab Hurley CK (1997). "Tipificación basada en ADN de HLA para trasplante". En Leffell MS, Donnenberg AD, Rose NR, eds. (1997) Handbook of Human Immunology. págs. 521–55, Boca Raton: CRC Press , ISBN 0-8493-0134-3 .
- ^ Bodmer JG, Marsh SG, Albert ED, Bodmer WF, Dupont B, Erlich HA, et al. (mayo de 1992). "Nomenclatura de factores del sistema HLA, 1991". Inmunología humana . 34 (1): 4–18. doi :10.1016/0198-8859(92)90079-3. PMID 1399721.
- ^ Valluri V, Valluei V, Mustafa M, Santhosh A, Middleton D, Alvares M, et al. (Agosto de 2005). "Frecuencias de los fenotipos HLA-A, HLA-B, HLA-DR y HLA-DQ en la población de los Emiratos Árabes Unidos". Antígenos tisulares . 66 (2): 107-13. doi :10.1111/j.1399-0039.2005.00441.x. PMID 16029430.
- ^ Farjadian S, Naruse T, Kawata H, Ghaderi A, Bahram S, Inoko H (noviembre de 2004). "Análisis molecular de las frecuencias de alelos y haplotipos de HLA en baluchis de Irán en comparación con poblaciones relacionadas de Pakistán". Antígenos tisulares . 64 (5): 581–7. doi :10.1111/j.1399-0039.2004.00302.x. PMID 15496201.
- ^ Shankarkumar U, Prasanavar D, Ghosh K, Mohanty D (mayo de 2003). "Frecuencias del alelo HLA A*02 y asociaciones del haplotipo B en indios occidentales". Inmunología humana . 64 (5): 562–6. doi :10.1016/S0198-8859(03)00032-6. PMID 12691707.
- ^ Apanius V, Penn D, Slev PR, Ruff LR, Potts WK (1997). "La naturaleza de la selección en el complejo mayor de histocompatibilidad". Critical Reviews in Immunology . 17 (2): 179–224. doi :10.1615/critrevimmunol.v17.i2.40. PMID 9094452..
- ^ Wedekind C, Seebeck T, Bettens F, Paepke AJ (junio de 1995). "Preferencias de pareja dependientes del MHC en humanos". Actas. Ciencias Biológicas . 260 (1359): 245–9. Código Bibliográfico :1995RSPSB.260..245W. doi :10.1098/rspb.1995.0087. PMID 7630893. S2CID 34971350.
- ^ Oshima M, Deitiker P, Ashizawa T, Atassi MZ (mayo de 2002). "La vacunación con un péptido de clase II del MHC atenúa las respuestas celulares y humorales contra el receptor tAChR y suprime la EAMG clínica". Autoinmunidad . 35 (3): 183–90. doi :10.1080/08916930290022270. PMID 12389643. S2CID 5690960.
- ^ Senev A, Coemans M, Lerut E, Van Sandt V, Kerkhofs J, Daniëls L, Driessche MV, Compernolle V, Sprangers B, Van Loon E, Callemeyn J, Claas F, Tambur AR, Verbeke G, Kuypers D, Emonds MP , Naesens M (septiembre de 2020). "Carga de desajuste de Eplet y aparición de novo de anticuerpos anti-HLA específicos del donante, rechazo y fracaso del injerto después del trasplante de riñón: un estudio de cohorte observacional". J. Am Soc Nephrol . 31 (9): 2193–204. doi :10.1681/ASN.2020010019. PMC 7461684 . PMID 32764139.
- ^ Verlinsky Y, Rechitsky S, Schoolcraft W, Strom C, Kuliev A (junio de 2001). "Diagnóstico preimplantacional para anemia de Fanconi combinado con compatibilidad de HLA". JAMA . 285 (24): 3130–3. doi : 10.1001/jama.285.24.3130 . PMID 11427142.
Bibliografía
- Daniel M. Davis, El gen de la compatibilidad , Londres, Penguin Books , 2014 ( ISBN 978-0-241-95675-5 ).
- Zsolt Harsanyi y Richard Hutton, Richard, Profecía genética: más allá de la doble hélice , Londres: Granada, 1982 ( ISBN 0-246-11760-5 ).
Enlaces externos
- Base de datos de secuencias IMGT/HLA en el Instituto Europeo de Bioinformática
- hla.alleles.org
- Grupo de informática HLA en The Anthony Nolan Trust
- Sociedad Británica de Histocompatibilidad e Inmunogenética
- Sociedad Estadounidense de Histocompatibilidad e Inmunogenética
- Herramienta de compatibilidad de HLA HistoCheck para trasplantes de órganos y células madre
- Frecuencias alélicas en loci variables relacionados con el sistema inmunitario
- Antígenos humanos+leucocitarios en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
- dbMHC Home, base de datos del NCBI sobre el complejo mayor de histocompatibilidad
- Proyecto de alelos raros en la base de datos AlleleFrequencies Net (AFND)