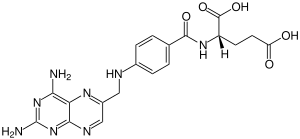
Aminopterina
 | |
 | |
| Nombres | |
|---|---|
| Nombre IUPAC Ácido N- (4-{[(2,4-Diaminopteridin-6-il)metil]amino}benzoil) -L -glutámico | |
| Nombre sistemático de la IUPAC Ácido (2 S )-2-(4-{[(2,4-Diaminopteridin-6-il)metil]amino}benzamido)pentanedioico | |
| Otros nombres Ácido 4-aminofólico Ácido 4-aminopteroilglutámico Aminopterina sódica Ácido aminopteroilglutámico | |
| Identificadores | |
Modelo 3D ( JSmol ) |
|
| Química biológica | |
| Araña química | |
| Tarjeta informativa de la ECHA | 100.000.191 |
| Número CE |
|
Identificador de centro de PubChem |
|
| UNIVERSIDAD | |
Panel de control CompTox ( EPA ) |
|
| |
| |
| Propiedades | |
| C19H20N8O5 | |
| Masa molar | 440,41 g/mol |
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |
La aminopterina (o ácido 4-aminopteroico), el derivado 4-amino del ácido fólico , es un fármaco antineoplásico con propiedades inmunosupresoras que se utiliza a menudo en quimioterapia . La aminopterina es un derivado sintético de la pterina . La aminopterina funciona como un inhibidor enzimático al competir por el sitio de unión del folato de la enzima dihidrofolato reductasa . Su afinidad de unión por la dihidrofolato reductasa bloquea eficazmente la síntesis de tetrahidrofolato . Esto da como resultado el agotamiento de los precursores de nucleótidos y la inhibición de la síntesis de ADN , ARN y proteínas .
Está clasificada como una sustancia extremadamente peligrosa en los Estados Unidos según se define en la Sección 302 de la Ley de Planificación de Emergencias y Derecho a Saber de la Comunidad de los Estados Unidos (42 USC 11002), y está sujeta a estrictos requisitos de notificación por parte de las instalaciones que la producen, almacenan o usan en cantidades significativas. [1]
Usos
Descubierto por Yellapragada Subbarow , el fármaco fue utilizado por primera vez por Sidney Farber en 1947 para inducir remisiones en niños con leucemia . [2] [3] Posteriormente, Lederle Laboratories (Pearl River, Nueva York) comercializó la aminopterina en los Estados Unidos entre 1953 y 1964 para la indicación de leucemia pediátrica. La empresa comercializó simultáneamente durante el mismo período el antifolato metotrexato, estrechamente relacionado . Lederle Laboratories suspendió la aminopterina en favor del metotrexato debido a dificultades de fabricación del primero.
Durante el período en que se comercializó la aminopterina, el agente se utilizó fuera de etiqueta para tratar de manera segura a más de 4000 pacientes con psoriasis en los Estados Unidos, lo que produjo una desaparición espectacular de las lesiones. [4]
El uso de aminopterina en el tratamiento del cáncer fue reemplazado en la década de 1950 por metotrexato debido al mejor índice terapéutico de este último en un modelo de tumor de roedores. [5] Ahora en una preparación más pura y respaldada por evidencia de laboratorio de una captación superior de células tumorales in vitro , la aminopterina se está investigando en ensayos clínicos en leucemia como un antifolato potencialmente superior al metotrexato. [6]
El compuesto se exploró como abortivo en la década de 1960 y antes, pero se asoció con malformaciones congénitas . [7] Se han documentado anomalías congénitas similares con metotrexato, y colectivamente sus efectos teratogénicos se han conocido como el síndrome de aminopterina fetal . Cuando aparece un conjunto similar de anomalías en ausencia de exposición a antifolatos, se lo denomina síndrome similar a la aminopterina sin aminopterina. [8]
La referencia al uso de aminopterina como rodenticida (es decir, veneno para ratas) se remonta a una patente de 1951 emitida a la American Cyanamid Company que se cita comúnmente en una variedad de libros de texto de referencia, incluido el Manual Merck, aunque el uso de aminopterina como rodenticida fue cuestionado posteriormente. [9] La preparación de la molécula es compleja y costosa. También es inestable en el medio ambiente debido a la degradación por la luz y el calor. La asociación aparentemente errónea de la aminopterina con su uso como rodenticida probablemente se remonta a una patente de 1951 emitida a la American Cyanamid Company (entonces la empresa matriz de Lederle Laboratories) que se cita comúnmente en una variedad de libros de texto de referencia. [10] La aminopterina tiene una LD50 de dosis única de 2,5 mg/kg cuando se administra por vía oral a ratas. [11]
La aminopterina se utiliza ampliamente en medios de selección (como el medio HAT ) para el cultivo celular , particularmente en el desarrollo de hibridomas , que secretan anticuerpos monoclonales .
Implicación de la retirada de alimentos de Menu Foods en 2007
El 23 de marzo de 2007, ABC News informó [12] que la aminopterina era la sustancia química relacionada con el incidente de contaminación de alimentos para mascotas de Menu Foods en 2007. El incidente dio lugar a un retiro masivo de los alimentos afectados. [13] El vínculo con la aminopterina fue confirmado por el Comisionado de Agricultura del Estado de Nueva York, Patrick Hooker, y el Dr. Donald Smith, Decano de la Facultad de Medicina Veterinaria de la Universidad de Cornell , en una declaración publicada el mismo día. [14] [15]
El 27 de marzo, el Centro de Control de Envenenamiento Animal de la ASPCA expresó su preocupación por el hecho de que el problema aún no se haya entendido completamente y que otros contaminantes puedan estar involucrados, señalando que "los signos clínicos informados en gatos afectados por los alimentos contaminados no son totalmente consistentes con la ingestión de veneno para ratas que contiene aminopterina". [16] El 30 de marzo se informó ampliamente que la Administración de Alimentos y Medicamentos de los Estados Unidos había encontrado melamina en el gluten de trigo que se utilizó en los alimentos para mascotas en cuestión. Estos mismos informes indicaron que la FDA no había podido encontrar evidencia de aminopterina en el gluten de trigo. Las pruebas en la Universidad de Guelph en Ontario , Canadá, detectaron aminopterina en algunas muestras de alimentos para mascotas , pero solo en concentraciones de partes por billón o partes por billón, cantidades demasiado bajas para causar los síntomas observados. [17]
Exposición y tratamiento
Los síntomas de exposición en humanos incluyen: [18] [19]
- náuseas
- vómitos
- anorexia
- Pérdida de peso
- escalofríos
- fiebre
- Estomatitis : inflamación de la mucosa oral.
- faringitis – inflamación de la faringe
- Erupciones eritematosas : erupciones rojas en la piel.
- Hiperpigmentación : aumento de la pigmentación asociado con la desaparición de las lesiones psoriásicas.
- hemorragia gastrointestinal
- Insuficiencia renal – en dosis altas que implican necesariamente un rescate concomitante con leucovorina
- abortos en mujeres embarazadas
Las dosis supraletales de aminopterina pueden ser rescatadas con el antídoto leucovorina (también conocido como ácido folínico ), una forma reducida de ácido fólico que evita la dihidrofolato reductasa, la enzima inhibida por la aminopterina. La leucovorina se ha utilizado en ratas, perros y humanos para rescatar la toxicidad de la aminopterina. [20] [21] [22] [23] El rescate con leucovorina es una maniobra terapéutica empleada intencionalmente con antifolatos para lograr concentraciones de fármaco tumoricidas que de otra manera serían letales para el paciente. [6]
En humanos, el rescate con leucovorina en sobredosis inferiores a 10 mg de aminopterina en un adulto promedio de 70 kg debe comprender una dosis inicial de leucovorina de al menos 20 mg (10,0 mg/m 2 ), administrada por vía intravenosa (preferiblemente) o por vía oral. [23] Las dosis posteriores de 20 mg (que pueden tomarse por vía oral) deben administrarse a intervalos de 6 horas hasta que mejoren las anomalías hematológicas.
La sobredosis masiva de aminopterina en humanos (es decir, > 40 mg de AMT en un adulto promedio de 70 kg) debe abordarse con una dosis inicial de leucovorina de 100 mg (50 mg/m2 ) , administrada por vía intravenosa y continuada a intervalos de 6 horas hasta que mejoren las anomalías hematológicas (probablemente 8 a 12 ciclos o más). [22] Además, para prevenir la nefrotoxicidad reversible mediada por aminopterina que se manifiesta como aumentos en la creatinina sérica y que retrasa aún más la eliminación del fármaco, se debe realizar la alcalinización urinaria con NaHCO
3y se debe considerar la expansión del volumen en casos de sobredosis masiva de aminopterina, particularmente aquellos que involucran más de 100 mg de AMT en un ser humano adulto promedio de 70 kg.
En consonancia con el conocido ciclo enterohepático del antifolato relacionado, el metotrexato, el carbón activado oral y el catártico salino o el sorbitol pueden promover la excreción si se sospecha una sobredosis de aminopterina. Sin embargo, el rescate con leucovorina debe ser la base del tratamiento.
El ácido fólico es un precursor oxidado de los folatos reducidos que se encuentra aguas arriba del bloqueo de la dihidrofolato reductasa y, en comparación con la leucovorina, se reconoce como un antídoto muy débil contra los efectos tóxicos de los antifolatos, por lo que no es adecuado su uso en casos de intoxicación aguda. Minnich et al. administraron aminopterina y ácido fólico por vía subcutánea a perros mestizos simultáneamente para probar si el ácido fólico puede rescatar a los animales de la letalidad y toxicidad de la aminopterina [24]. A los perros se les administraron 0,020, 0,046, 0,044 aumentados a 0,088 y 0,097 mg/kg de aminopterina cada día durante 7 a 12 días. El ácido fólico se administró en una proporción de peso respecto a la aminopterina de 200:1 a 800:1. Todos los animales sobrevivieron. En cambio, los animales a los que se les administró aminopterina en una cantidad de 0,041 mg/kg/día durante 6 días sin ácido fólico murieron. Por lo tanto, cuando la proporción de ácido fólico a aminopterina era de 200:1 o mayor, todos los sujetos sobrevivieron con regímenes que, de otro modo, habrían sido uniformemente letales para todos los sujetos.
También se han observado efectos similares en especies de roedores, donde el rango de rescate por ácido fólico fue bastante estrecho y altamente dependiente del momento (óptimo de 1 hora antes de la aminopterina) de administración en relación con la aminopterina. [25] [26] La relación temporal entre la administración de ácido fólico y el rescate se ha interpretado como el período de tiempo necesario requerido para que la vitamina se convierta in vivo en formas reducidas.
Referencias
- ^ "40 CFR: Apéndice A de la Parte 355: La lista de sustancias extremadamente peligrosas y sus cantidades límite de planificación" (PDF) (edición del 1 de julio de 2008). Oficina de Imprenta del Gobierno . Archivado desde el original (PDF) el 25 de febrero de 2012. Consultado el 29 de octubre de 2011 .
{{cite journal}}: Requiere citar revista|journal=( ayuda ) - ^ "¿Quién fue el Dr. Sidney Farber?". Instituto Oncológico Dana-Farber . Archivado desde el original el 7 de febrero de 2007. Consultado el 5 de febrero de 2007 .
- ^ Farber S, Diamond LK, Mercer RD, Sylvester RF, Wolff JA (1948). "Remisiones temporales en leucemia aguda en niños producidas por el antagonista del ácido fólico, ácido 4-aminopteroil-glutámico (Aminopterina)". N Engl J Med . 238 (787): 787–93. doi :10.1056/NEJM194806032382301. PMID 18860765.
- ^ Rees RB, Bennett JH, Hamlin EM, Maibach HI (diciembre de 1964). "Aminopterina para la psoriasis. Observación de una década". Arch Dermatol . 90 (6): 544–52. doi :10.1001/archderm.1964.01600060010002. PMID 14206858.[ enlace muerto permanente ]
- ^ Goldin A, Venditti JM, Humphreys SR, Dennis D, Mantel N, Greenhouse SW (junio de 1955). "Una comparación cuantitativa de la eficacia antileucémica de dos antagonistas del ácido fólico en ratones". J. Natl. Cancer Inst . 15 (6): 1657–64. doi :10.1093/jnci/15.6.1657. PMID 14381889.
- ^ ab Cole, PD; Drachtman, RA; Smith, AK; Cate, S; Larson, RA; Hawkins, DS; Holcenberg, J; Kelly, K; Kamen, BA (15 de noviembre de 2005). "Ensayo de fase II de aminopterina oral para adultos y niños con leucemia aguda refractaria". Investigación clínica del cáncer . 11 (22): 8089–96. doi :10.1158/1078-0432.CCR-05-0355. PMC 2906753. PMID 16299240 .
- ^ Emerson D (agosto de 1962). "Malformación congénita debida a intento de aborto con aminopterina". Am J Obstet Gynecol . 84 (3): 356–7. doi :10.1016/0002-9378(62)90132-1. PMID 13890101.
- ^ "Síndromes de anomalías congénitas múltiples/retardo mental (MCA/MR): síndrome de aminopterina fetal". Biblioteca Nacional de Medicina de los Estados Unidos . Consultado el 26 de marzo de 2007 .
- ^ "No se encontró aminopterina en los tejidos de los animales sacrificados por alimentos para mascotas retirados del mercado". PRNewsWire. 30 de marzo de 2007. Archivado desde el original el 9 de mayo de 2007. Consultado el 14 de abril de 2007 .
- ^ US 2575168, Franklin, Alfred L., "Rodenticida que comprende ácido 4-amino-pteroilglutámico", publicado el 13 de noviembre de 1951, asignado a American Cyanamid Company
- ^ "Perfil químico de la EPA: aminopterina". Agencia de Protección Ambiental de los Estados Unidos . 31 de octubre de 1985. Archivado desde el original el 7 de julio de 2007. Consultado el 23 de marzo de 2007 .
- ^ Kerley, David (23 de marzo de 2007). "El veneno para ratas es el culpable de la contaminación de los alimentos para mascotas". ABC News . Consultado el 23 de marzo de 2007 .
- ^ "Menu Foods retira del mercado alimentos húmedos para mascotas específicos en lata y en bolsas de aluminio pequeñas". Departamento de Agricultura de Nueva York. 16 de marzo de 2007. Archivado desde el original el 25 de diciembre de 2016. Consultado el 25 de marzo de 2007 .
- ^ Johnson, Mark (23 de marzo de 2007). "Se encontró veneno para ratas en comida para mascotas contaminada". BusinessWeek . Archivado desde el original el 22 de mayo de 2011. Consultado el 23 de marzo de 2007 .
- ^ "Los laboratorios de Nueva York identifican una toxina en un alimento para mascotas retirado del mercado". Departamento de Agricultura de Nueva York. 23 de marzo de 2007. Archivado desde el original el 11 de febrero de 2017. Consultado el 23 de marzo de 2007 .
- ^ "ASPCA recomienda precaución a medida que aumenta la crisis de retirada de alimentos para mascotas; otros contaminantes pueden estar involucrados en la retirada de alimentos del menú". 27 de marzo de 2007. Archivado desde el original el 13 de mayo de 2007. Consultado el 27 de marzo de 2007 .
- ^ "La FDA encuentra una nueva sustancia química en alimentos para mascotas retirados del mercado y animales enfermos". CNN . 30 de marzo de 2007. Archivado desde el original el 8 de abril de 2007. Consultado el 30 de marzo de 2007 .
- ^ "Ficha técnica química de la aminopterina". CAMEO Chemicals . Administración Nacional Oceánica y Atmosférica de Estados Unidos . Consultado el 25 de marzo de 2007 .
- ^ Berenbaum, MC; Brown, IN (1 de marzo de 1965). "El efecto de la administración retardada de ácido folínico sobre la inhibición inmunológica por metotrexato". Inmunología . 8 (3): 251–9. PMC 1423470 . PMID 14315108.
- ^ Nichol CA, Welch AD (junio de 1950). "Sobre el mecanismo de acción de la aminopterina". Proc. Soc. Exp. Biol. Med . 74 (2): 403–11. doi :10.3181/00379727-74-17922. PMID 15440837. S2CID 44623774.
- ^ Rieselbach RE, Morse EE, Rall DP, Frei E, Freireich EJ (mayo de 1963). "Terapia intratecal con aminopterina de la leucemia meníngea". Arch. Intern. Med . 111 (5): 620–30. doi :10.1001/archinte.1963.03620290086011. PMID 13973810.[ enlace muerto permanente ]
- ^ ab Glode LM, Pitman SW, Ensminger WD, Rosowsky A, Papathanasopoulos N, Frei E (septiembre de 1979). "Un estudio de fase 1 de dosis altas de aminopterina con rescate de leucovorina en pacientes con tumores metastásicos avanzados". Cancer Res . 39 (9): 3707–14. PMID 383286.
- ^ ab Ratliff AF, Wilson J, Hum M, et al. (abril de 1998). "Ensayo de fase I y farmacocinético de aminopterina en pacientes con neoplasias malignas refractarias". J. Clin. Oncol . 16 (4): 1458–64. doi :10.1200/JCO.1998.16.4.1458. PMID 9552052. Archivado desde el original el 15 de abril de 2013.
- ^ Minnich V, Moore CV, Smith DE, Elliott GV (diciembre de 1950). "Estudios sobre los efectos tóxicos agudos del ácido 4-amino-pteroilglutámico en perros, cobayas y conejos. Diferencia en la susceptibilidad de las especies y la acción protectora del ácido fólico". AMA Arch Pathol . 50 (6): 787–99. PMID 14789323.
- ^ Franklin AL, Stokstad EL, et al. (1948). "Observaciones sobre el efecto del ácido 4-amino-pteroilglutámico en ratones". Proc Soc Exp Biol Med . 67 (3): 398–400. doi :10.3181/00379727-67-16320. S2CID 41223103.
- ^ Greenspan EM, Goldin A, Schoenbach EB (septiembre de 1950). "Estudios sobre el mecanismo de acción de los agentes quimioterapéuticos en el cáncer. II. Requisitos para la prevención de la toxicidad de la aminopterina por ácido fólico en ratones". Cáncer . 3 (5): 856–63. doi : 10.1002/1097-0142(1950)3:5<856::AID-CNCR2820030512>3.0.CO;2-A . PMID 14772718.


