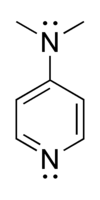
4-Dimetilaminopiridina
| |||
| Nombres | |||
|---|---|---|---|
| Nombres IUPAC N , N -Dimetilpiridin-4-amina Dimetil(piridin-4-il)azano Dimetil(piridin-4-il)amina | |||
| Nombre IUPAC preferido N , N -Dimetilpiridin-4-amina | |||
| Otros nombres 4-(Dimetilamino)piridina N , N -Dimetil-4-aminopiridina DMAP 4-Dimetilaminopiridina 4-(Dimetilamino)azina N , N -dimetil-4-aminoazina 4-(Dimetilamino)azabenceno N , N -Dimetil-4-aminoazabenceno | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.013.049 | ||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades | |||
| C7H10N2 | |||
| Masa molar | 122,17 g/mol | ||
| Apariencia | sólido blanco | ||
| Punto de fusión | 110 a 113 °C (230 a 235 °F; 383 a 386 K) | ||
| Punto de ebullición | 162 °C (324 °F; 435 K) a 50 mmHg | ||
| Acidez (p K a ) | 9,6 en agua, 17,95 (p K a del ácido conjugado en acetonitrilo) [1] | ||
| Peligros | |||
| Etiquetado SGA : | |||
 | |||
| Peligro | |||
| H301 , H310 , H315 , H319 , H335 [2] | |||
| P280 , P305+P351+P338 , P337+P313 [2] | |||
| Dosis o concentración letal (LD, LC): | |||
LD 50 ( dosis media ) | Ratones ciervos: oral, 450 mg/kg [3] Ratones: oral, 350 mg/kg/día [3] | ||
| Ficha de datos de seguridad (FDS) | [2] | ||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
La 4-dimetilaminopiridina ( DMAP ) es un derivado de la piridina con la fórmula química (CH 3 ) 2 NC 5 H 4 N. Este sólido blanco es de interés porque es más básico que la piridina , debido a la estabilización por resonancia del sustituyente NMe 2 .
Debido a su basicidad, el DMAP es un catalizador nucleofílico útil para una variedad de reacciones, como esterificaciones con anhídridos , la reacción de Baylis-Hillman , hidrosililaciones , tritilación, la transposición de Steglich, la síntesis de Staudinger de β-lactamas y muchas más. Los análogos quirales del DMAP se utilizan en experimentos de resolución cinética de alcoholes secundarios principalmente y amidas de tipo auxiliar de Evans. [4] [5] [6]
Preparación
El DMAP se puede preparar mediante un procedimiento de dos pasos a partir de piridina, que primero se oxida al catión 4-piridilpiridinio. Este catión luego reacciona con dimetilamina : [7]
Catalizador de esterificación
En el caso de la esterificación con anhídridos acéticos, el mecanismo aceptado actualmente implica tres pasos. Primero, el DMAP y el anhídrido acético reaccionan en una reacción de preequilibrio para formar un par iónico de acetato y el ion acetilpiridinio. En el segundo paso, el alcohol se agrega al acetilpiridinio y la eliminación de piridina forma un éster . Aquí, el acetato actúa como una base para eliminar el protón del alcohol mientras se agrega nucleofílicamente al acilpiridinio activado. El enlace del grupo acetilo al catalizador se escinde para generar el catalizador y el éster. El proceso descrito de formación y ruptura de enlaces se ejecuta de manera sincrónica y concertada sin la aparición de un intermediario tetraédrico. El ácido acético formado protonará entonces el DMAP. En el último paso del ciclo catalítico, la base auxiliar (generalmente trietilamina o piridina ) desprotona el DMAP protonado, reformando el catalizador. La reacción se lleva a cabo a través de la vía de reacción nucleofílica descrita independientemente del anhídrido utilizado, pero el mecanismo cambia con el valor de pKa del alcohol utilizado. Por ejemplo, la reacción se lleva a cabo a través de una vía de reacción catalizada por una base en el caso de un fenol. En este caso, el DMAP actúa como una base y desprotona el fenol, y el ion fenolato resultante se agrega al anhídrido. [8]
Seguridad
El DMAP tiene una toxicidad relativamente alta y es particularmente peligroso debido a su capacidad de ser absorbido a través de la piel. También es corrosivo. [9]
Compuesto relacionado
Referencias
- ^ Kaljurand, I.; Kütt, A.; Sooväli, L.; Rodima, T.; Mäemets, V.; Leito, I.; Koppel, IA (2005). "Extensión de la escala de basicidad espectrofotométrica autoconsistente en acetonitrilo a un rango completo de 28 unidades de pKa: unificación de diferentes escalas de basicidad". J. Org. Chem . 70 (3): 1019–1028. doi :10.1021/jo048252w. PMID 15675863.
- ^ abc Sigma-Aldrich Co. , 4-(Dimetilamino)piridina. Consultado el 3 de septiembre de 2015.
- ^ abcd Nachtergael, Amandine; Coulembier, Olivier; Dubois, Philippe; Helvenstein, Maxime; Duez, Pierre; Blankert, Bertrand; Mespouille, Laetitia (9 de febrero de 2015). "Paradigma de la organocatálisis revisitado: ¿son los catalizadores libres de metales realmente inofensivos?". Biomacromolecules . 16 (2): 507–514. doi :10.1021/bm5015443. PMID 25490408.
- ^ Donald J Berry; Charles V Digiovanna; Stephanie S Metrick; Ramiah Murugan (2001). "Catálisis por 4-dialquilaminopiridinas". Arkivoc : 201–226. Archivado desde el original el 27 de septiembre de 2007. Consultado el 27 de noviembre de 2006 .
- ^ Höfle, G.; Steglich, W.; Vorbrüggen, H. (1978). "4-Dialquilaminopiridinas como catalizadores de acilación altamente activos". Angew. Chem. Int. Ed. Engl. 17 (8): 569–583. doi :10.1002/anie.197805691.
- ^ Ryan P. Wurz (2007). "Catalizadores de dialquilamina quirales en síntesis asimétrica". Chem. Rev. 107 (12): 5570–5595. doi :10.1021/cr068370e. PMID 18072804.
- ^ Shimizu, Shinkichi; Watanabe, Nanao; Kataoka, Toshiaki; Shoji, Takayuki; Abe, Nobuyuki; Morishita, Sinji; Ichimura, Hisao (2007). "Piridina y derivados de piridina". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a22_399. ISBN 978-3527306732.
- ^ S. Xu; I. Held; B. Kempf; H. Mayr; Wolfgang Steglich ; H. Zipse (2005). "La acetilación de alcoholes catalizada por DMAP: un estudio mecanístico (DMAP = 4-(dimetilamino)-piridina)". Química. Revista Europea de Química. 11 (16): 4751–4757. doi :10.1002/chem.200500398. PMID 15924289.
- ^ Hoja de datos de seguridad del DMAP - Fischer Science
Lectura adicional
- B. Neises; W. Steglich (1990). "Esterificación de ácidos carboxílicos con diciclohexilcarbodiimida/4-dimetilaminopiridina: terc-butil etil fumarato". Síntesis orgánica; Volúmenes recopilados , vol. 7, pág. 93.
- I. Held; P. von den Hoff; DS Stephenson; H. Zipse (2008). "Catálisis dominó en la conversión directa de ácidos carboxílicos en ésteres". Adv. Synth. Catal. 11/12 (11–12): 1891–1900. doi :10.1002/adsc.200800268.