Felandreno
| |||
| Nombres | |||
|---|---|---|---|
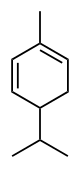
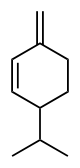
| Nombres IUPAC (α): 2-Metil-5-(propan-2-il)ciclohexa-1,3-dieno (β): 3-Metiliden-6-(propan-2-il)ciclohex-1-eno | |||
| Identificadores | |||
Modelo 3D ( JSmol ) |
| ||
| EBICh |
| ||
| Araña química | |||
| Tarjeta informativa de la ECHA | 100.014.121 | ||
| Número CE |
| ||
| BARRIL |
| ||
Identificador de centro de PubChem |
| ||
| UNIVERSIDAD | |||
Panel de control CompTox ( EPA ) |
| ||
| |||
| |||
| Propiedades [1] | |||
| C10H16 | |||
| Masa molar | 136,24 g/mol | ||
| Apariencia | Aceite incoloro (α y β) | ||
| Densidad | α: 0,846 g/cm 3 β: 0,85 g/cm 3 | ||
| Punto de ebullición | α: 171-172 °C β: 171-172 °C | ||
| Insoluble (α y β) | |||
| Peligros | |||
| Etiquetado SGA : | |||
  | |||
| Peligro | |||
| H226 , H304 | |||
| P210 , P233 , P240 , P241 , P242 , P243 , P280 , P301+P310 , P303+P361+P353 , P331 , P370+P378 , P403+P235 , P405 , P501 | |||
Salvo que se indique lo contrario, los datos se proporcionan para los materiales en su estado estándar (a 25 °C [77 °F], 100 kPa). | |||
Los felandrenos son un par de compuestos orgánicos que tienen una estructura molecular similar y propiedades químicas similares. El α-felandreno y el β-felandreno son monoterpenos cíclicos y son isómeros de doble enlace . En el α-felandreno, ambos enlaces dobles son endocíclicos y en el β-felandreno, uno de ellos es exocíclico. Ambos son insolubles en agua, pero miscibles con éter dietílico .
El α-felandreno debe su nombre al Eucalyptus phellandra , ahora llamado Eucalyptus radiata , del que se puede aislar. [2] También es un componente del aceite esencial de Eucalyptus dives . [3] El β-felandreno se ha aislado del aceite de hinojo acuático y del aceite de bálsamo de Canadá .
Los felandrenos se utilizan en fragancias por sus agradables aromas. El olor del β-felandreno se ha descrito como mentolado y ligeramente cítrico.
El isómero α-felandreno puede formar peróxidos peligrosos y explosivos en contacto con el aire a temperaturas elevadas. [4]
Biosíntesis
La biosíntesis del felandreno comienza con la condensación del pirofosfato de dimetilalilo y el pirofosfato de isopentenilo en una reacción S N 1 para formar pirofosfato de geranilo . El monoterpeno resultante sufre una ciclización para formar una especie catiónica de mentilo. Luego, un desplazamiento de hidruro forma un carbocatión alílico . Finalmente, se produce una reacción de eliminación en una de dos posiciones, lo que produce α-felandreno o β-felandreno. [5]
Referencias
- ^ Índice Merck , 12.ª edición, 7340 , 7341
- ^ Jacobs, SWL, Pickard, J., Plantas de Nueva Gales del Sur , 1981, ISBN 0-7240-1978-2 .
- ^ Boland, DJ, Brophy, JJ y APN House, Aceites de hojas de eucalipto , 1991, ISBN 0-909605-69-6 .
- ^ Urben, Peter (2007). Bretherick's Handobook of Reactive Chemical Hazards . Vol. 1 (7.ª ed.). Butterworth-Heinemann. pág. 1154.
- ^ Dewick, Paul M. (9 de marzo de 2009). Productos naturales medicinales: un enfoque biosintético (3.ª ed.). Chichester, West Sussex, Reino Unido. ISBN 9780470741689.OCLC 259265604 .
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )