Reacción de Pinner
| Reacción de Pinner | |
|---|---|
| Llamado en honor a | Adolfo Pinner |
| Identificadores | |
| Portal de química orgánica | reacción de pinner |
| Identificación de ontología RSC | Número de receta: 0000361 |
La reacción de Pinner se refiere a la reacción catalizada por ácido de un nitrilo con un alcohol para formar una sal de iminoéster ( sal de imidato de alquilo ); a esto a veces se lo denomina sal de Pinner . [1] La reacción recibe su nombre de Adolf Pinner , quien la describió por primera vez en 1877. [2] [3] [4] Las sales de Pinner son reactivas en sí mismas y experimentan adiciones nucleofílicas adicionales para dar varios productos útiles: [5] [6]
- Con un exceso de alcohol para formar un ortoéster
- Con amoniaco o una amina para formar una amidina (los dinitrilos pueden formar imidinas , por ejemplo succinimidina a partir de succinonitrilo ) [7]
- Con agua para formar un éster
- Con sulfuro de hidrógeno para formar un tionoéster
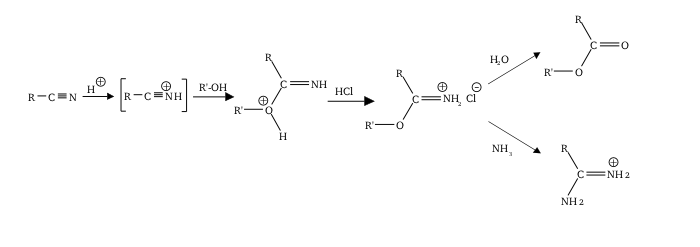
Por lo general, la sal de Pinner no se aísla, sino que se continúa con la reacción para obtener el grupo funcional deseado (ortoéster, etc.) de una sola vez. Las sales de cloruro de imidio son termodinámicamente inestables y las bajas temperaturas ayudan a prevenir la eliminación a amida y cloruro de alquilo . [8]
Se debe tener en cuenta que la reacción de Pinner se refiere específicamente a un proceso catalizado por ácido, pero que a menudo se pueden lograr resultados similares utilizando catálisis básica. Los dos enfoques pueden ser complementarios, y los nitrilos que no reaccionan en condiciones ácidas suelen dar mejores resultados en presencia de una base, y viceversa. [9] El factor determinante suele ser la riqueza o pobreza de electrones del nitrilo. Por ejemplo: un nitrilo pobre en electrones es un buen electrófilo (fácilmente susceptible al ataque de alcóxidos , etc.), pero un nucleófilo pobre normalmente sería más fácil de protonar que de participar en la reacción y, por lo tanto, se esperaría que reaccionara más fácilmente en condiciones básicas que ácidas.
Véase también
- Reacción de Hoesch
- Reordenamiento de Overman
- Isocianuro
- Cloruro de imidoilo
- Síntesis de aldehído de Stephen : esencialmente la misma reacción pero incluyendo una reducción y con agua como nucleófilo; genera el aldehído.
Referencias
- ^ "Reacción de Pinner". Reacciones y reactivos de nombres orgánicos completos (504): 2237–2240. 2010. doi :10.1002/9780470638859.conrr504. ISBN 9780470638859.
- ^ A. Pinner, F. Klein; Klein (1877). "Umwandlung der Nitrile in Imide". Berichte der deutschen chemischen Gesellschaft . 10 (2): 1889–1897. doi :10.1002/cber.187701002154.
- ^ A. Pinner, p. Klein; Klein (1878). "Umwandlung der Nitrile in Imide". Berichte der deutschen chemischen Gesellschaft . 11 (2): 1475-1487. doi :10.1002/cber.18780110258.
- ^ A. Pinner (1883). "Ueber die Umwandlung der Nitrile in Imide". Berichte der deutschen chemischen Gesellschaft . 16 (2): 1643–1655. doi :10.1002/cber.18830160235.
- ^ Roger, R.; Neilson, DG (1961). "La química de los imidatos". Chem. Rev. 61 (2): 179–211. doi :10.1021/cr60210a003.
- ^ Adams, Roger; Thal, AF (1922). "Etil fenilacetato". Síntesis orgánicas . 2 : 27. doi :10.15227/orgsyn.002.0027.
- ^ Elvidge, JA; Linstead, RP (1954). "Aminas e iminas heterocíclicas. Parte III. Succinimidina". Journal of the Chemical Society (Resumen) : 442. doi :10.1039/JR9540000442.
- ^ DeWolfe, Robert H. (1970). Derivados de ácidos ortocarboxílicos . Química orgánica. Vol. 14. Nueva York, NY: Academic Press. p. 5. LCCN 70-84226.
- ^ Schaefer, FC; Peters, GA (1961). "Reacción catalizada por bases de nitrilos con alcoholes. Una ruta conveniente para obtener imidatos y sales de amidina". Journal of Organic Chemistry . 26 (2): 412. doi :10.1021/jo01061a034.