Fosfatidiletanolamina
La fosfatidiletanolamina ( PE ) es una clase de fosfolípidos que se encuentran en las membranas biológicas . [1] Se sintetizan mediante la adición de difosfato de citidina - etanolamina a los diglicéridos , liberando monofosfato de citidina . La S -adenosil metionina puede posteriormente metilar la amina de las fosfatidiletanolaminas para producir fosfatidilcolinas .
Función

En las células
Las fosfatidiletanolaminas se encuentran en todas las células vivas y constituyen el 25% de todos los fosfolípidos. En la fisiología humana, se encuentran particularmente en el tejido nervioso, como la sustancia blanca del cerebro , los nervios, el tejido neural y la médula espinal , donde constituyen el 45% de todos los fosfolípidos. [2]
Las fosfatidiletanolaminas desempeñan un papel en la fusión de membranas y en el desmontaje del anillo contráctil durante la citocinesis en la división celular . [3] Además, se cree que la fosfatidiletanolamina regula la curvatura de la membrana . La fosfatidiletanolamina es un precursor, sustrato o donante importante en varias vías biológicas. [2]
Como grupo de cabeza polar, la fosfatidiletanolamina crea una membrana lipídica más viscosa en comparación con la fosfatidilcolina . Por ejemplo, la temperatura de fusión de la dioleilfosfatidiletanolamina es de -16 °C, mientras que la temperatura de fusión de la dioleilfosfatidilcolina es de -20 °C. Si los lípidos tuvieran dos cadenas de palmitoilo, la fosfatidiletanolamina se fundiría a 63 °C, mientras que la fosfatidilcolina se fundiría ya a 41 °C. [4] Las temperaturas de fusión más bajas corresponden, en una visión simplista, a membranas más fluidas.
En los humanos
En los seres humanos, se cree que el metabolismo de la fosfatidiletanolamina es importante en el corazón. Cuando se restringe el flujo sanguíneo al corazón, se altera la distribución asimétrica de la fosfatidiletanolamina entre las láminas de la membrana y, como resultado, se altera la membrana. Además, la fosfatidiletanolamina desempeña un papel en la secreción de lipoproteínas en el hígado. Esto se debe a que las vesículas para la secreción de lipoproteínas de muy baja densidad que salen del aparato de Golgi tienen una concentración de fosfatidiletanolamina significativamente mayor en comparación con otras vesículas que contienen lipoproteínas de muy baja densidad. [5] La fosfatidiletanolamina también ha demostrado ser capaz de propagar priones infecciosos sin la ayuda de ninguna proteína o ácido nucleico , lo que es una característica única de la misma. [6] También se cree que la fosfatidiletanolamina desempeña un papel en la coagulación sanguínea, ya que trabaja con la fosfatidilserina para aumentar la tasa de formación de trombina al promover la unión al factor V y al factor X , dos proteínas que catalizan la formación de trombina a partir de protrombina . [7] La síntesis del endocannabinoide anandamida se realiza a partir de la fosfatidiletanolamina mediante la acción sucesiva de dos enzimas, la N - acetiltransferasa y la fosfolipasa -D. [8]
En bacterias
Mientras que la fosfatidilcolina es el principal fosfolípido en los animales, la fosfatidiletanolamina es el principal en las bacterias . Una de las funciones principales de la fosfatidiletanolamina en las membranas bacterianas es distribuir la carga negativa causada por los fosfolípidos aniónicos de la membrana . En la bacteria E. coli , la fosfatidiletanolamina desempeña un papel en el apoyo al transporte activo de lactosa por las permeasas de lactosa hacia la célula, y también puede desempeñar un papel en otros sistemas de transporte. La fosfatidiletanolamina desempeña un papel en el ensamblaje de la permeasa de lactosa y otras proteínas de membrana. Actúa como una "chaperona" para ayudar a las proteínas de membrana a plegar correctamente sus estructuras terciarias para que puedan funcionar correctamente. Cuando la fosfatidiletanolamina no está presente, las proteínas de transporte tienen estructuras terciarias incorrectas y no funcionan correctamente. [9]
La fosfatidiletanolamina también permite que los transportadores de múltiples fármacos bacterianos funcionen correctamente y permite la formación de intermediarios que son necesarios para que los transportadores se abran y cierren correctamente. [10]
Estructura

Como lecitina , la fosfatidiletanolamina consiste en una combinación de glicerol esterificado con dos ácidos grasos y ácido fosfórico . Mientras que el grupo fosfato se combina con colina en la fosfatidilcolina, se combina con etanolamina en la fosfatidiletanolamina. Los dos ácidos grasos pueden ser idénticos o diferentes y, por lo general, se encuentran en las posiciones 1 y 2 (con menos frecuencia, en las posiciones 1 y 3).
Síntesis
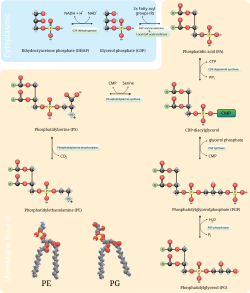
La vía de descarboxilación de la fosfatidilserina y la vía de la citidina difosfato-etanolamina se utilizan para sintetizar fosfatidiletanolamina. La fosfatidilserina descarboxilasa es la enzima que se utiliza para descarboxilar la fosfatidilserina en la primera vía. La vía de descarboxilación de la fosfatidilserina es la principal fuente de síntesis de fosfatidiletanolamina en las membranas de las mitocondrias . La fosfatidiletanolamina producida en la membrana mitocondrial también se transporta por toda la célula a otras membranas para su uso. En un proceso que refleja la síntesis de la fosfatidilcolina , la fosfatidiletanolamina también se produce a través de la vía de la citidina difosfato-etanolamina, utilizando etanolamina como sustrato. A través de varios pasos que tienen lugar tanto en el citosol como en el retículo endoplasmático , la vía de síntesis produce el producto final de la fosfatidiletanolamina. [11] La fosfatidiletanolamina también se encuentra abundantemente en la lecitina de soja o de huevo y se produce comercialmente mediante separación cromatográfica.
Regulación
La síntesis de fosfatidiletanolamina a través de la vía de descarboxilación de la fosfatidilserina ocurre rápidamente en la membrana mitocondrial interna . Sin embargo, la fosfatidilserina se produce en el retículo endoplasmático . Debido a esto, el transporte de fosfatidilserina desde el retículo endoplasmático a la membrana mitocondrial y luego a la membrana mitocondrial interna limita la velocidad de síntesis a través de esta vía. El mecanismo para este transporte es actualmente desconocido pero puede desempeñar un papel en la regulación de la velocidad de síntesis en esta vía. [12]
Presencia en los alimentos, problemas de salud
Las fosfatidiletanolaminas en los alimentos se descomponen para formar productos Amadori unidos a fosfatidiletanolamina como parte de la reacción de Maillard . [13] Estos productos aceleran la peroxidación lipídica de la membrana , provocando estrés oxidativo en las células que entran en contacto con ellos. [14] Se sabe que el estrés oxidativo causa el deterioro de los alimentos y varias enfermedades. Se han encontrado niveles significativos de productos Amadori-fosfatidiletanolamina en una amplia variedad de alimentos como chocolate , leche de soja , fórmula infantil y otros alimentos procesados . Los niveles de productos Amadori-fosfatidiletanolamina son más altos en alimentos con altas concentraciones de lípidos y azúcar que tienen altas temperaturas en el procesamiento. [13] Estudios adicionales han encontrado que la Amadori-fosfatidiletanolamina puede desempeñar un papel en la enfermedad vascular , [15] actuar como el mecanismo por el cual la diabetes puede aumentar la incidencia del cáncer , [16] y potencialmente desempeñar un papel en otras enfermedades también. La amadori-fosfatidiletanolamina tiene una concentración plasmática más alta en pacientes con diabetes que en personas sanas, lo que indica que puede desempeñar un papel en el desarrollo de la enfermedad o ser un producto de la enfermedad. [17]
Véase también
Referencias
- ^ Wellner, Niels; Diep, Thi Ai; Janfelt, cristiano; Hansen, Harald Severin (2012). "N-acilación de fosfatidiletanolamina y sus funciones biológicas en mamíferos". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de lípidos . 1831 (3): 652–62. doi : 10.1016/j.bbalip.2012.08.019. PMID 23000428.
- ^ ab Vance, Jean E.; Tasseva, Guergana (2012). "Formación y función de la fosfatidilserina y la fosfatidiletanolamina en células de mamíferos". Biochimica et Biophysica Acta (BBA) - Biología molecular y celular de los lípidos . 1831 (3): 543–54. doi :10.1016/j.bbalip.2012.08.016. PMID 22960354.
- ^ Emoto, K.; Kobayashi, T; Yamaji, A; Aizawa, H; Yahara, I; Inoue, K; Umeda, M (1996). "Redistribución de fosfatidiletanolamina en el surco de división de células en división durante la citocinesis". Actas de la Academia Nacional de Ciencias . 93 (23): 12867–72. Bibcode :1996PNAS...9312867E. doi : 10.1073/pnas.93.23.12867 . JSTOR 40713. PMC 24012 . PMID 8917511.
- ^ Ver referencias en Wan et al. Biochemistry 47 2008 [ se requiere verificación ]
- ^ Vance, JE (2008). "Serie de revisiones temáticas: glicerolípidos. Fosfatidilserina y fosfatidiletanolamina en células de mamíferos: dos aminofosfolípidos metabólicamente relacionados". The Journal of Lipid Research . 49 (7): 1377–87. doi : 10.1194/jlr.R700020-JLR200 . PMID 18204094.
- ^ Deleault, NR; Piro, JR; Walsh, DJ; Wang, F.; Ma, J.; Geoghegan, JC; Supattapone, S. (2012). "Aislamiento de fosfatidiletanolamina como cofactor solitario para la formación de priones en ausencia de ácidos nucleicos". Actas de la Academia Nacional de Ciencias . 109 (22): 8546–51. Bibcode :2012PNAS..109.8546D. doi : 10.1073/pnas.1204498109 . PMC 3365173 . PMID 22586108.
- ^ Majumder, R.; Liang, X.; Quinn-Allen, MA; Kane, WH; Lentz, BR (2011). "Modulación del ensamblaje y la actividad de la protrombinasa por fosfatidiletanolamina". Journal of Biological Chemistry . 286 (41): 35535–42. doi : 10.1074/jbc.M111.260141 . PMC 3195639 . PMID 21859710.
- ^ Isidro, F. (2014). "Cannabinoides para el tratamiento de la enfermedad de Alzheimer: avanzando hacia la clínica". Frontiers in Pharmacology . 5 : 37. doi : 10.3389/fphar.2014.00037 . PMC 3942876 . PMID 24634659.
- ^ Christie, WW (16 de abril de 2012). "Fosfatidiletanolamina y lípidos relacionados". Biblioteca de lípidos de la AOCS. Archivado desde el original el 21 de agosto de 2012. Consultado el 3 de septiembre de 2012 .
- ^ Gbaguidi, B.; Hakizimana, P.; Vandenbussche, G.; Ruysschaert, J.-M. (2007). "Los cambios conformacionales en un transportador multifármaco bacteriano dependen de la fosfatidiletanolamina" (PDF) . Ciencias de la vida celular y molecular . 64 (12): 1571–82. doi :10.1007/s00018-007-7031-0. PMID 17530171. S2CID 2078590.
- ^ Kelly, Karen (28 de julio de 2011). "Biosíntesis de fosfolípidos". Biblioteca de lípidos de la AOCS . Consultado el 3 de septiembre de 2012 .
- ^ Kuge, Osamu; Nishijima, Masahiro (1 de abril de 2003). «Regulación biosintética y transporte intracelular de fosfatidilserina en células de mamíferos». The Journal of Biochemistry . 133 (4): 397–403. doi :10.1093/jb/mvg052. PMID 12761285. Archivado desde el original el 30 de enero de 2021 . Consultado el 30 de enero de 2021 .
- ^ ab Oak, Jeong-Ho; Nakagawa, Kiyotaka; Miyazawa, Teruo (2002). "Análisis UV de fosfatidiletanolamina glicosilada de Amadori en alimentos y muestras biológicas". The Journal of Lipid Research . 43 (3): 523–9. doi : 10.1016/S0022-2275(20)30158-9 . PMID 11893788.
- ^ Oak, Jeong-Ho; Nakagawa, Kiyotaka; Miyazawa, Teruo (2000). "La fosfatidiletanolamina Amadori-glicada preparada sintéticamente puede desencadenar la peroxidación lipídica a través de reacciones de radicales libres". FEBS Letters . 481 (1): 26–30. Bibcode :2000FEBSL.481...26O. doi : 10.1016/S0014-5793(00)01966-9 . PMID 10984609. S2CID 23265125.
- ^ Oak, Jeong-Ho; Nakagawa, Kiyotaka; Oikawa, Shinichi; Miyazawa, Teruo (2003). "La fosfatidiletanolamina amadori-glicada induce diferenciaciones angiogénicas en células endoteliales de vena umbilical humana cultivadas". FEBS Letters . 555 (2): 419–23. Bibcode :2003FEBSL.555..419O. doi :10.1016/S0014-5793(03)01237-7. PMID 14644453. S2CID 33974755.
- ^ Eitsuka, Takahiro; Nakagawa, Kiyotaka; Ono, Yuichi; Tatewaki, Naoto; Nishida, Hiroshi; Kurata, Tadao; Shoji, Naoki; Miyazawa, Teruo (2012). "La fosfatidiletanolamina glicada amadori regula positivamente la actividad de la telomerasa en células de carcinoma de páncreas humano PANC-1". Cartas FEBS . 586 (16): 2542–7. Código Bib : 2012FEBSL.586.2542E. doi : 10.1016/j.febslet.2012.06.027 . PMID 22750441. S2CID 5452160.
- ^ Ariizumi, Ken; Koike, T; Ohara, S; Inomata, Y; Abe, Y; Iijima, K; Imatani, A; Bueno, T; Shimosegawa, T (2008). "Incidencia de esofagitis por reflujo e infección por H pylori en pacientes diabéticos". Revista Mundial de Gastroenterología . 14 (20): 3212–7. doi : 10.3748/wjg.14.3212 . PMC 2712855 . PMID 18506928.
Enlaces externos
- Fosfatidiletanolaminas en los encabezados de materias médicas (MeSH) de la Biblioteca Nacional de Medicina de EE. UU.
- Fosfatidiletanolamina en la biblioteca de lípidos de la AOCS.