Halohidrina


En química orgánica, una halohidrina (también haloalcohol o β-haloalcohol ) es un grupo funcional en el que un halógeno y un hidroxilo están unidos a átomos de carbono adyacentes, que de otro modo solo tienen grupos hidrógeno o hidrocarbilo (por ejemplo, 2-cloroetanol , 3-cloropropano-1,2-diol ). [1] El término solo se aplica a motivos saturados, ya que compuestos como el 2-clorofenol normalmente no se considerarían halohidrinas. Anualmente se producen megatones de algunas clorhidrinas, por ejemplo, la clorhidrina de propileno , como precursores de polímeros.
Las halohidrinas pueden clasificarse como clorhidrinas, bromohidrinas, fluorohidrinas o yodohidrinas dependiendo del halógeno presente.
Síntesis
De alquenos
Las halohidrinas se preparan generalmente mediante el tratamiento de un alqueno con un halógeno, en presencia de agua. La reacción es una forma de adición electrofílica , en la que el halógeno actúa como electrófilo. [2] En ese sentido, se asemeja a la reacción de adición de halógeno y procede con una adición anti , dejando los grupos X y OH recién añadidos en una configuración trans . La ecuación química para la conversión de etileno en clorhidrina de etileno es:
- H2C =CH2 + Cl2 + H2O → H2 ( OH)C- CH2Cl + HCl
Cuando se desea la bromación, la N -bromosuccinimida (NBS) puede ser preferible al bromo porque se producen menos productos secundarios.

A partir de epóxidos
Las halohidrinas también pueden prepararse a partir de la reacción de un epóxido con un ácido hidrohálico , [3] o un haluro metálico. [4]
Esta reacción se produce a escala industrial para la producción de precursores de clorhidrina para dos epóxidos importantes, epiclorhidrina y óxido de propileno [ cita requerida ] . En un momento dado, el 2-cloroetanol se producía a gran escala como precursor del óxido de etileno , pero este último se prepara ahora mediante la oxidación directa del etileno. [5]
A partir de ácidos 2-cloro
Los ácidos 2-clorocarboxílicos se pueden reducir con hidruro de litio y aluminio para formar 2-cloroalcoholes. Los ácidos 2-clorocarboxílicos requeridos se obtienen de diversas maneras, incluida la halogenación de Hell-Volhard-Zelinsky . El ácido 2-cloropropiónico se produce por cloración del cloruro de propionilo seguida de hidrólisis del cloruro de 2-cloropropionilo. El ácido ( S )-2-cloropropiónico enantioméricamente puro y varios compuestos relacionados se pueden preparar a partir de aminoácidos mediante diazotación . [6]
Reacciones
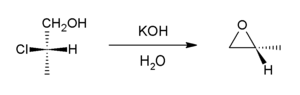
En presencia de una base, las halohidrinas experimentan una reacción interna S N 2 para formar epóxidos . En la industria, la base es el hidróxido de calcio , mientras que en el laboratorio se suele utilizar hidróxido de potasio.
Esta reacción es la inversa de la reacción de formación de un epóxido y puede considerarse una variante de la síntesis del éter de Williamson . La mayor parte del suministro mundial de óxido de propileno surge a través de esta ruta. [7]
Estas reacciones pueden formar la base de procesos más complicados, por ejemplo, la formación de epóxido es uno de los pasos clave en la reacción de Darzens .
Halohidrina halogenada

Compuestos como el 2,2,2-tricloroetanol , que contienen múltiples halógenos geminales adyacentes a un grupo hidroxilo, pueden considerarse halohidrinas (aunque, estrictamente hablando, no cumplen la definición de la IUPAC ) ya que poseen una química similar. En particular, también experimentan ciclización intramolecular para formar grupos dihaloepoxi. Estas especies son altamente reactivas y sintéticamente útiles, y forman la base de la reacción de Jocic-Reeve , la reacción de Bargellini y la reacción de Corey-Link . [8]
Seguridad
Al igual que con cualquier grupo funcional, los peligros de las halohidrinas son difíciles de generalizar, ya que pueden formar parte de una serie casi ilimitada de compuestos, y cada estructura tiene una farmacología diferente. En general, los compuestos de bajo peso molecular más simples suelen ser tóxicos y cancerígenos (por ejemplo, 2-cloroetanol , 3-MCPD ) en virtud de ser agentes alquilantes . Esta reactividad se puede aprovechar, por ejemplo, en el fármaco contra el cáncer mitobronitol . Existe una serie de corticosteroides sintéticos que llevan un motivo de fluorohidrina ( triamcinolona , dexametasona ).
Nombres erróneos
A pesar de sus nombres bastante sugerentes, la epiclorhidrina y la clorhidrina sulfúrica no son halohidrinas, aunque la primera se produce más comúnmente utilizando un intermedio de clorhidrina.
Véase también
Referencias
- ^ IUPAC , Compendio de terminología química , 2.ª ed. (el "Libro de oro") (1997). Versión corregida en línea: (2006–) "halohidrinas". doi :10.1351/goldbook.H02727
- ^ William Reusch. "Reacciones de adición de alquenos". Libro de texto virtual de química orgánica . Archivado desde el original el 14 de diciembre de 2012.
- ^ Travis W.Shaw, Julia A.Kalow, Abigail G.Doyle (2012). "Resolución cinética de epóxidos terminales mediante apertura de anillo de fluoruro: preparación de (S)-2-fluoro-1-feniletanol". Organic Syntheses . 89 : 9. doi : 10.15227/orgsyn.089.0009 .
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ) - ^ Bonini, Carlo; Righi, Giuliana (1994). "Síntesis regio- y quimioselectiva de halohidrinas por escisión de oxiranos con haluros metálicos". Síntesis . 1994 (3): 225–238. doi :10.1055/s-1994-25445.
- ^ Liu, Gordon YT; Richey, W. Frank; Betso, Joanne E.; Hughes, Brian; Klapacz, Joanna; Lindner, Joerg (2014). "Clorhidrinas". Enciclopedia de química industrial de Ullmann . Weinheim: Wiley-VCH. doi :10.1002/14356007.a06_565.pub2. ISBN 978-3527306732.
- ^ Koppenhoefer, Bernhardt; Schurig, Volker (1988). "Ácidos (S)-2-cloroalcanoicos de alta pureza enantiomérica a partir de (S)-2-aminoácidos: ácido (S)-2-cloropropanoico". Organic Syntheses . 66 : 151. doi :10.15227/orgsyn.066.0151.
- ^ Dietmar Kahlich, Uwe Wiechern, Jörg Lindner "Óxido de propileno" en la Enciclopedia de química industrial de Ullmann, 2002 por Wiley-VCH, Weinheim. doi :10.1002/14356007.a22_239 Fecha de publicación del artículo en línea: 15 de junio de 2000
- ^ Snowden, TS (28 de febrero de 2012). "Aplicaciones recientes de intermediarios de gem-dicloroepóxido en síntesis". Arkivoc . 2012 (2): 24–40. doi : 10.3998/ark.5550190.0013.204 . hdl : 2027/spo.5550190.0013.204 .