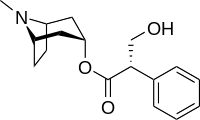
Hiosciamina
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Anaspaz, Levbid, Levsin |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a684010 |
| Vías de administración | Por vía oral , inyección |
| Código ATC |
|
| Estatus legal | |
| Estatus legal | |
| Datos farmacocinéticos | |
| Biodisponibilidad | 50% de unión a proteínas |
| Metabolismo | Hígado |
| Vida media de eliminación | 3–5 horas. |
| Excreción | Riñón |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL |
|
| EBICh | |
| Química biológica | |
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.002.667 |
| Datos químicos y físicos | |
| Fórmula | C17H23NO3 |
| Masa molar | 289,375 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
 norte norte Y (¿que es esto?) (verificar) Y (¿que es esto?) (verificar) | |
La hiosciamina (también conocida como daturina o duboisina ) es un alcaloide tropánico y toxina vegetal de origen natural. Es un metabolito secundario que se encuentra en ciertas plantas de la familia Solanaceae , entre las que se incluyen el beleño , la mandrágora , la trompeta de ángel , el estramonio , el árbol de los hechiceros y la Atropa belladona (belladona mortal). Es el isómero levógiro de la atropina (el tercero de los tres alcaloides principales de las solanáceas) y, por lo tanto, a veces se la conoce como levoatropina. [1]
En 2021, fue el medicamento número 272 más recetado en los Estados Unidos, con más de 900.000 recetas. [2] [3]
Usos médicos
La hiosciamina se utiliza para proporcionar alivio sintomático de los espasmos causados por varios trastornos abdominales inferiores y de la vejiga, incluyendo úlceras pépticas , síndrome del intestino irritable , diverticulitis , pancreatitis , cólicos y cistitis intersticial . [4] [5] [6] También se ha utilizado para aliviar algunos problemas cardíacos, controlar algunos de los síntomas de la enfermedad de Parkinson , así como para el control de síntomas respiratorios anormales y "secreciones hipermucosas" en pacientes con enfermedad pulmonar. [7]

También es útil en el control del dolor neuropático, el dolor crónico y los cuidados paliativos («cuidados paliativos») para quienes padecen dolor intratable debido a enfermedades resistentes al tratamiento, intratables e incurables. Cuando se combina con opioides, aumenta el nivel de analgesia (alivio del dolor) obtenido. [8] Se cree que varios mecanismos contribuyen a este efecto. Los fármacos estrechamente relacionados atropina e hioscina y otros miembros del grupo de fármacos anticolinérgicos como ciclobenzaprina , trihexifenidilo y orfenadrina también se utilizan para este propósito. [9] Cuando se utiliza hiosciamina junto con opioides u otros agentes antiperistálticos, las medidas para prevenir el estreñimiento son especialmente importantes dado el riesgo de íleo paralítico . [10]
Efectos adversos
Los efectos secundarios incluyen boca y garganta secas, aumento del apetito que conduce a un aumento de peso, dolor ocular, visión borrosa, inquietud, mareos, arritmia , enrojecimiento y desmayos. [5] Una sobredosis causará dolor de cabeza, náuseas, vómitos y síntomas del sistema nervioso central que incluyen desorientación, alucinaciones, euforia, excitación sexual, pérdida de memoria a corto plazo y posible coma en casos extremos. Los efectos eufóricos y sexuales son más fuertes que los de la atropina, pero más débiles que los de la hioscina , así como la dicicloverina , la orfenadrina , la ciclobenzaprina , el trihexifenidilo y los antihistamínicos de etanolamina como la feniltoloxamina . [11] [12]
Farmacología
Farmacodinamia
La hiosciamina es un antimuscarínico , es decir, un antagonista de los receptores muscarínicos de acetilcolina . Bloquea la acción de la acetilcolina en las glándulas sudoríparas (simpático) y en los sitios parasimpáticos de las glándulas salivales, las secreciones del estómago, el músculo cardíaco, el nódulo sinoatrial , el músculo liso del tracto gastrointestinal y el sistema nervioso central . Aumenta el gasto cardíaco y la frecuencia cardíaca, reduce la presión arterial y seca las secreciones. [13] Puede antagonizar la serotonina . [14] En dosis comparables, la hiosciamina tiene el 98 por ciento del poder anticolinérgico de la atropina. El otro fármaco principal derivado de Atropa belladonna, la hioscina (conocida en los Estados Unidos como escopolamina), tiene el 92 por ciento de la potencia antimuscarínica de la atropina. [14]
La hiosciamina se ha descrito como un antagonista selectivo del receptor muscarínico de acetilcolina M 2 sin efectos significativos en los otros receptores muscarínicos de acetilcolina. [15] [16] Esto contrasta con los antimuscarínicos relacionados como la atropina y la escopolamina , que son antagonistas no selectivos de los cinco receptores muscarínicos de acetilcolina. [15] [16] El antagonismo tanto del receptor muscarínico de acetilcolina M 1 como del receptor M 2 se ha implicado en efectos negativos sobre la memoria y la cognición . [16] Se ha descrito que la hiosciamina tiene efectos delirantes de manera similar a la escopolamina, la atropina y otros antimuscarínicos. [15] Sin embargo, otras fuentes han informado que la hiosciamina antagoniza potentemente los cinco subtipos de receptores muscarínicos de acetilcolina. [17]
Biosíntesis en plantas

La hiosciamina se puede extraer de plantas de la familia Solanaceae , en particular de Datura stramonium . Como la hiosciamina es un precursor directo en la biosíntesis de la hioscina en la planta , se produce a través de la misma vía metabólica . [18]
La biosíntesis de la hioscina comienza con la descarboxilación de la L - ornitina a putrescina por la acción de la ornitina descarboxilasa (EC 4.1.1.17). La putrescina es metilada a N -metilputrescina por la N -metiltransferasa de la putrescina (EC 2.1.1.53). [18]
Una putrescina oxidasa (EC 1.4.3.10) que reconoce específicamente la putrescina metilada cataliza la desaminación de este compuesto a 4-metilaminobutanal que luego experimenta una formación espontánea de anillo para formar el catión N -metilpirrolio. En el siguiente paso, el catión pirrolio se condensa con ácido acetoacético produciendo higrina . No se pudo demostrar ninguna actividad enzimática que catalice esta reacción. La higrina se reorganiza aún más para formar tropinona . [18]
Posteriormente, la tropinona reductasa I (EC 1.1.1.206) convierte la tropinona en tropina , que se condensa con fenillactato derivado de la fenilalanina para formar litorina. Un citocromo P450 clasificado como Cyp80F1 [19] oxida y reorganiza la litorina para formar aldehído de hiosciamina .

Fundamentos de la medicina natural
Los pueblos aborígenes de los estados orientales de Australia desarrollaron una medicina a base de arbustos a partir del árbol de corcho blando , o Duboisia myoporoides , que fue utilizada por los aliados en la Segunda Guerra Mundial para evitar que los soldados se marearan cuando navegaban por el Canal de la Mancha durante la invasión de Normandía . Más tarde, se descubrió que la misma sustancia podía usarse en la producción de escopolamina e hiosciamina, que se utilizan en cirugía ocular , y se construyó una industria multimillonaria en Queensland basada en esta sustancia. [20]
Sociedad y cultura
Nombres de marca
Los nombres comerciales de hiosciamina incluyen Symax, HyoMax, Anaspaz, Egazil, Buwecon, Cystospaz, Levsin, Levbid, Levsinex, Donnamar, NuLev, Spacol T/S y Neoquess. [21]
Referencias
- ^ Ushimaru R, Ruszczycky MW, Liu HW (enero de 2019). "Cambios en la regioselectividad de la abstracción de átomos de H durante las reacciones de hidroxilación y ciclización catalizadas por la hiosciamina 6β-hidroxilasa". Journal of the American Chemical Society . 141 (2): 1062–1066. doi :10.1021/jacs.8b11585. PMC 6488026 . PMID 30545219.
- ^ "Los 300 mejores de 2021". ClinCalc . Archivado desde el original el 15 de enero de 2024 . Consultado el 14 de enero de 2024 .
- ^ "Hiosciamina - Estadísticas de uso de medicamentos". ClinCalc . Consultado el 14 de enero de 2024 .
- ^ National Clinical Guideline Centre (Reino Unido) (2012). Tratamiento para mejorar el almacenamiento vesical. NBK132836 (8.ª ed.). Reino Unido: Royal College of Physicians . p. 83 – vía National Library of Medicine .
- ^ ab "Usos, efectos secundarios y advertencias de la hiosciamina". Drugs.com . Archivado desde el original el 20 de agosto de 2022. Consultado el 20 de agosto de 2022 .
- ^ "Medicamentos para el control de la vejiga | NIDDK". Instituto Nacional de Diabetes y Enfermedades Digestivas y Renales . Archivado desde el original el 20 de agosto de 2022. Consultado el 20 de agosto de 2022 .
- ^ "Hiosciamina: información sobre medicamentos de MedlinePlus". medlineplus.gov . Archivado desde el original el 20 de agosto de 2022 . Consultado el 20 de agosto de 2022 .
- ^ Harden RN (marzo de 2005). "Dolor neuropático crónico. Mecanismos, diagnóstico y tratamiento". The Neurologist . 11 (2): 111–122. doi :10.1097/01.nrl.0000155180.60057.8e. PMID 15733333. S2CID 12602416.
- ^ Ali-Melkkilä T, Kanto J, Iisalo E (octubre de 1993). "Farmacocinética y farmacodinamia relacionada de fármacos anticolinérgicos". Acta Anestesiológica Scandinavica . 37 (7): 633–642. doi :10.1111/j.1399-6576.1993.tb03780.x. PMID 8249551. S2CID 22808654.
- ^ Kamimura A, Howard S, Weaver S, Panahi S, Ashby J (diciembre de 2020). "El uso de estrategias de medicina complementaria y alternativa, opioides y fármacos antiinflamatorios no esteroideos (AINE) entre pacientes que asisten a una clínica gratuita". Revista de experiencia del paciente . 7 (6): 1701–1707. doi :10.1177/2374373520937514. PMC 7786764 . PMID 33457633.
- ^ Kang M, Galuska MA, Ghassemzadeh S (2022). "Toxicidad de las benzodiazepinas". StatPearls . Treasure Island (FL): StatPearls Publishing. PMID 29489152. Archivado desde el original el 20 de agosto de 2022.
- ^ "Comprimidos sublinguales de sulfato de hiosciamina, 0,125 mg, solo con receta médica". www.dailymed.nlm.nih.gov . Archivado desde el original el 20 de agosto de 2022 . Consultado el 20 de agosto de 2022 .
- ^ Edwards Pharmaceuticals, Inc., Belcher Pharmaceuticals, Inc. (mayo de 2010). «DailyMed». Biblioteca Nacional de Medicina de EE. UU . . Consultado el 13 de enero de 2013 .
- ^ ab Kapoor AK, Raju SM (2013). Farmacología médica ilustrada. JP Medical Ltd. pág. 131. ISBN 9789350906552. Recuperado el 11 de enero de 2014 .
- ^ abc Lakstygal AM, Kolesnikova TO, Khatsko SL, Zabegalov KN, Volgin AD, Demin KA, et al. (mayo de 2019). "Clásicos oscuros en neurociencia química: atropina, escopolamina y otros alucinógenos delirantes anticolinérgicos". ACS Chem Neurosci . 10 (5): 2144–2159. doi :10.1021/acschemneuro.8b00615. PMID 30566832.
- ^ abc Shim KH, Kang MJ, Sharma N, An SS (septiembre de 2022). "La bella de la bestia: alcaloides tropánicos anticolinérgicos en la terapéutica". Nat Prod Bioprospect . 12 (1): 33. doi :10.1007/s13659-022-00357-w. PMC 9478010 . PMID 36109439.
El antagonismo en los receptores M1 y M2 tiene un impacto negativo en la memoria y la cognición [60]. [...] La atropina y la escopolamina son antagonistas competitivos no selectivos de los receptores muscarínicos. La atropina tiene la mayor afinidad por el subtipo M1, seguido de M2 y M3 y una afinidad débil por M4 y M5 [71]. Por otro lado, la escopolamina tiene una fuerte afinidad por M1-M4 en comparación con M5 [72] mientras que la hiosciamina se une solo a M2 [73].
- ^ Lavrador M, Cabral AC, Veríssimo MT, Fernandez-Llimos F, Figueiredo IV, Castel-Branco MM (enero de 2023). "Una lista universal de fármacos con actividad anticolinérgica". Farmacéutica . 15 (1): 230. doi : 10.3390/farmacéutica15010230 . PMC 9863833 . PMID 36678858.
- ^ abc Ziegler J, Facchini PJ (2008). "Biosíntesis de alcaloides: metabolismo y tráfico". Revisión anual de biología vegetal . 59 (1): 735–769. doi :10.1146/annurev.arplant.59.032607.092730. PMID 18251710.
- ^ Li R, Reed DW, Liu E, Nowak J, Pelcher LE, Page JE, et al. (mayo de 2006). "El análisis genómico funcional de la biosíntesis de alcaloides en Hyoscyamus niger revela un citocromo P450 involucrado en la reorganización de la litorina". Química y biología . 13 (5): 513–520. doi : 10.1016/j.chembiol.2006.03.005 . PMID 16720272.
- ^ "Los visitantes de la exposición Art of Healing contaron cómo se les dio medicina natural a los indígenas australianos a todos los soldados aliados que desembarcaron en Normandía el Día D". King's College London . 7 de junio de 2019 . Consultado el 2 de junio de 2020 .
- ^ "Hyoscyamine - lista de marcas comerciales de Drugs.com". Drugs.com . Archivado desde el original el 20 de agosto de 2022 . Consultado el 20 de agosto de 2022 .
