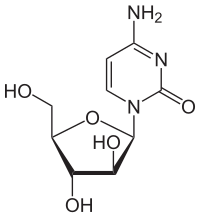
Citarabina
 | |
 | |
| Datos clínicos | |
|---|---|
| Nombres comerciales | Cytosar-U, Depocyt, otros |
| AHFS / Drogas.com | Monografía |
| MedlinePlus | a682222 |
Categoría de embarazo |
|
| Vías de administración | inyectable (inyección o infusión intravenosa, intratecal o subcutánea) |
| Código ATC |
|
| Estatus legal | |
| Estatus legal |
|
| Datos farmacocinéticos | |
| Biodisponibilidad | 20% por vía oral |
| Unión de proteínas | 13% |
| Metabolismo | Hígado |
| Vida media de eliminación | bifásico: 10 min, 1–3 h |
| Excreción | Riñón |
| Identificadores | |
| |
| Número CAS | |
| Identificador de centro de PubChem |
|
| Unión Internacional para la Investigación y el Desarrollo (IUPHAR)/BPS |
|
| Banco de medicamentos | |
| Araña química | |
| UNIVERSIDAD |
|
| BARRIL | |
| EBICh | |
| Química biológica | |
| Ligando PDB |
|
| Panel de control CompTox ( EPA ) |
|
| Tarjeta informativa de la ECHA | 100.005.188 |
| Datos químicos y físicos | |
| Fórmula | C9H13N3O5 |
| Masa molar | 243,219 g·mol −1 |
| Modelo 3D ( JSmol ) |
|
| |
| (verificar) | |
La citarabina , también conocida como arabinósido de citosina ( ara-C ), es un medicamento de quimioterapia que se usa para tratar la leucemia mieloide aguda (LMA), la leucemia linfocítica aguda (LLA), la leucemia mielógena crónica (LMC) y el linfoma no Hodgkin . [2] Se administra mediante inyección en una vena , debajo de la piel o en el líquido cefalorraquídeo . [2] Existe una formulación liposomal para la que hay evidencia tentativa de mejores resultados en el linfoma que afecta las meninges . [2]
Los efectos secundarios comunes incluyen supresión de la médula ósea , vómitos, diarrea, problemas hepáticos , sarpullido, formación de úlceras en la boca y sangrado. [2] Otros efectos secundarios graves incluyen pérdida de conciencia , enfermedad pulmonar y reacciones alérgicas . [2] El uso durante el embarazo puede dañar al bebé. [2] La citarabina pertenece a las familias de medicamentos antimetabolitos y análogos de nucleósidos . [3] Actúa bloqueando la función de la ADN polimerasa . [2]
La citarabina fue patentada en 1960 y aprobada para uso médico en 1969. [4] Está en la Lista de Medicamentos Esenciales de la Organización Mundial de la Salud . [5]
Usos médicos
La citarabina se utiliza principalmente en el tratamiento de la leucemia mieloide aguda , la leucemia linfocítica aguda (LLA) y en los linfomas , [6] donde es la columna vertebral de la quimioterapia de inducción .
La citarabina también posee actividad antiviral y se ha utilizado para el tratamiento de la infección generalizada por herpesvirus . Sin embargo, la citarabina no es muy selectiva en este contexto y causa supresión de la médula ósea y otros efectos secundarios graves. Por lo tanto, ara-C no es un agente antiviral útil en humanos debido a su perfil tóxico. [7]
La citarabina también se utiliza en el estudio del sistema nervioso para controlar la proliferación de células gliales en cultivos, teniendo la cantidad de células gliales un impacto importante en las neuronas . [ cita requerida ]
Efectos secundarios
Una de las toxicidades únicas de la citarabina es la toxicidad cerebelosa cuando se administra en dosis altas, que puede provocar ataxia . La citarabina puede causar granulocitopenia y otras defensas corporales deterioradas, lo que puede provocar infecciones, y trombocitopenia , que puede provocar hemorragias . [ cita requerida ]
Toxicidad: pancreatitis , leucopenia , trombocitopenia, anemia , trastornos gastrointestinales, estomatitis , conjuntivitis , neumonitis , fiebre y dermatitis , eritrodisestesia palmoplantar . En raras ocasiones se ha informado de mielopatía tras la administración intratecal frecuente o en dosis altas de Ara-C. [8]
Cuando se utiliza en protocolos designados como de dosis alta, la citarabina puede causar disfunción cerebral y cerebelosa, toxicidad ocular, toxicidad pulmonar, ulceración gastrointestinal grave y neuropatía periférica (poco frecuente). [ cita requerida ]
Para prevenir los efectos secundarios y mejorar la eficacia terapéutica, se han evaluado diversos derivados de estos fármacos (incluyendo aminoácidos, péptidos, ácidos grasos y fosfatos), así como diferentes sistemas de administración. [9]
Mecanismo de acción
El arabinósido de citosina combina una base de citosina con un azúcar arabinosa . Es un agente antimetabólico con el nombre químico de 1β-arabinofuranosilcitosina . Ciertas esponjas , donde originalmente se encontraron compuestos similares, usan azúcares arabinósidos para la defensa química. [10] El arabinósido de citosina es lo suficientemente similar a la desoxicitosina humana como para incorporarse al ADN humano, pero lo suficientemente diferente como para matar la célula. El arabinósido de citosina interfiere con la síntesis de ADN. Su modo de acción se debe a su rápida conversión en trifosfato de arabinósido de citosina , que daña el ADN cuando el ciclo celular se mantiene en la fase S (síntesis de ADN). Por lo tanto, las células que se dividen rápidamente, que requieren la replicación del ADN para la mitosis , son las más afectadas. El arabinósido de citosina también inhibe tanto las polimerasas de ADN [11] como las de ARN y las enzimas nucleótido reductasas necesarias para la síntesis de ADN. La citarabina es el primero de una serie de fármacos contra el cáncer que modifican el componente de azúcar de los nucleósidos . Otros fármacos contra el cáncer modifican la base. [12]
La citarabina se administra a menudo mediante infusión intravenosa continua, que sigue una eliminación bifásica: una tasa de depuración inicial rápida seguida de una tasa más lenta del análogo. [13] La citarabina es transportada a la célula principalmente por hENT-1. [14] Luego es monofosforilada por la desoxicitidina quinasa y, finalmente, por la citarabina-5'-trifosfato, que es el metabolito activo que se incorpora al ADN durante la síntesis de ADN. [ cita requerida ]
Se han descrito varios mecanismos de resistencia. [15] La citarabina es desaminada rápidamente por la citidina desaminasa en el suero en el derivado inactivo de uracilo. La citarabina-5'-monofosfato es desaminada por la desoxicitidilato desaminasa, lo que conduce al análogo inactivo de uridina-5'-monofosfato. [16] La citarabina-5'-trifosfato es un sustrato para SAMHD1 . [17] Además, se ha demostrado que SAMHD1 limita la eficacia de la citarabina en pacientes. [18]
Cuando se utiliza como antiviral , la citarabina-5'-trifosfato actúa inhibiendo la síntesis de ADN viral. [19] La citarabina es capaz de inhibir la replicación del virus del herpes y del virus vaccinia en células durante el cultivo de tejidos. Sin embargo, el tratamiento con citarabina sólo fue eficaz para la infección por el virus del herpes en un modelo murino. [ cita requerida ]
En ratones, Ara-CTP (citarabina-5'-trifosfato) bloquea la consolidación de la memoria, pero no la memoria a corto plazo, de un evento condicionado por el miedo al contexto. [20] Se propuso que el bloqueo de la consolidación de la memoria se debía a la inhibición por Ara-CTP de la vía de unión de extremos no homólogos del ADN . [20] Por lo tanto, la rotura transitoria del ADN seguida de la unión de extremos no homólogos parecen ser pasos necesarios en la formación de una memoria a largo plazo de un evento. [ cita requerida ]
Historia
El aislamiento de nucleótidos que contienen arabinosa de la esponja caribeña Cryptotheca crypta (ahora Tectitethya crypta ) junto con la comprensión de que estos compuestos podrían actuar como terminadores de la cadena de síntesis de ADN condujeron a la exploración de estos nuevos nucleótidos como posibles terapias contra el cáncer. [21] La citarabina fue sintetizada por primera vez en 1959 por Richard Walwick, Walden Roberts y Charles Dekker en la Universidad de California, Berkeley . [22]
Fue aprobado por la Administración de Alimentos y Medicamentos de los Estados Unidos en junio de 1969, y fue comercializado inicialmente en los EE. UU. por Upjohn bajo la marca Cytosar-U. [ cita requerida ]
Nombres
También se conoce como ara-C (arabinofuranosil citidina). [23]
- Citosar-U
- Tarabina PFS (Pfizer)
- Depocyt (fórmula liposomal de mayor duración )
- AraC
Referencias
- ^ "Lista de todos los medicamentos con advertencias de recuadro negro obtenida por la FDA (use los enlaces Descargar resultados completos y Ver consulta)". nctr-crs.fda.gov . FDA . Consultado el 22 de octubre de 2023 .
- ^ abcdefg «Citarabina». Sociedad Estadounidense de Farmacéuticos de Sistemas de Salud. Archivado desde el original el 11 de junio de 2016. Consultado el 8 de diciembre de 2016 .
- ^ Formulario nacional británico: BNF 69 (69.ª ed.). Asociación Médica Británica. 2015. pág. 589. ISBN 9780857111562.
- ^ Fischer J, Ganellin CR (2006). Descubrimiento de fármacos basado en análogos. John Wiley & Sons. pág. 511. ISBN 9783527607495. Archivado desde el original el 20 de diciembre de 2016.
- ^ Organización Mundial de la Salud (2019). Lista modelo de medicamentos esenciales de la Organización Mundial de la Salud: 21.ª lista , 2019. Ginebra: Organización Mundial de la Salud. hdl : 10665/325771 . OMS/MVP/EMP/IAU/2019.06. Licencia: CC BY-NC-SA 3.0 IGO.
- ^ Pigneux A, Perreau V, Jourdan E, Vey N, Dastugue N, Huguet F, et al. (octubre de 2007). "Adición de lomustina a idarrubicina y citarabina para la quimioterapia de inducción en pacientes mayores con leucemia mieloide aguda: resultados del ensayo BGMT 95". Hematológica . 92 (10): 1327-1334. doi : 10.3324/haematol.11068 . PMID 18024370.
- ^ Lauter CB, Bailey EJ, Lerner AM (noviembre de 1974). "Evaluación del arabinósido de citosina como agente antiviral en humanos". Agentes antimicrobianos y quimioterapia . 6 (5): 598–602. doi :10.1128/aac.6.5.598. PMC 444699. PMID 15825312 .
- ^ Watterson J, Toogood I, Nieder M, Morse M, Frierdich S, Lee Y, et al. (diciembre de 1994). "Toxicidad excesiva de la médula espinal por terapias intensivas dirigidas al sistema nervioso central". Cancer . 74 (11): 3034–3041. doi : 10.1002/1097-0142(19941201)74:11<3034::AID-CNCR2820741122>3.0.CO;2-O . PMID 7954266.
- ^ Chhikara BS, Parang K (diciembre de 2010). "Desarrollo de profármacos de citarabina y sistemas de administración para el tratamiento de la leucemia". Opinión de expertos sobre administración de fármacos . 7 (12): 1399–1414. doi :10.1517/17425247.2010.527330. PMID 20964588. S2CID 2988492.
- ^ Hall D (noviembre de 2019). «Esponjas marinas: farmacias del mar». Smithsonian Ocean . Consultado el 25 de abril de 2023 .
- ^ Perry MJ (2008). El libro de consulta sobre quimioterapia . Filadelfia: Wolters Kluwer Health/Lippincott Williams & Wilkins. pág. 80. ISBN 978-0-7817-7328-7.
- ^ Feist P (abril de 2005). "Un cuento desde el mar hasta Ara C". Archivado desde el original el 6 de marzo de 2007.
- ^ Liliemark JO, Gahrton G, Paul CY, Peterson CO (junio de 1987). "ara-C en plasma y ara-CTP en células leucémicas después de la inyección subcutánea y la infusión intravenosa continua de ara-C en pacientes con leucemia aguda no linfoblástica". Seminars in Oncology . 14 (2 Suppl 1): 167–171. PMID 3589691.
- ^ Clarke ML, Mackey JR, Baldwin SA, Young JD, Cass CE (2002). "El papel de los transportadores de membrana en la resistencia celular a los fármacos nucleósidos contra el cáncer". Resistencia clínicamente relevante en la quimioterapia contra el cáncer . Tratamiento e investigación del cáncer. Vol. 112. págs. 27–47. doi :10.1007/978-1-4615-1173-1_2. ISBN 978-1-4613-5428-4. Número PMID 12481710.
- ^ Shelton J, Lu X, Hollenbaugh JA, Cho JH, Amblard F, Schinazi RF (diciembre de 2016). "Metabolismo, acciones bioquímicas y síntesis química de nucleótidos, nucleótidos y análogos de bases anticancerígenos". Chemical Reviews . 116 (23): 14379–14455. doi :10.1021/acs.chemrev.6b00209. PMC 7717319 . PMID 27960273.
- ^ Drake JC, Hande KR, Fuller RW, Chabner BA (marzo de 1980). "Inhibición de la citidina y la desoxicitidilato desaminasa por análogos de la uridina". Farmacología bioquímica . 29 (5): 807–811. doi :10.1016/0006-2952(80)90561-4. PMID 20227960.
- ^ Hollenbaugh JA, Shelton J, Tao S, Amiralaei S, Liu P, Lu X, et al. (enero de 2017). "Sustratos e inhibidores de SAMHD1". PLOS ONE . 12 (1): e0169052. Código Bibliográfico :2017PLoSO..1269052H. doi : 10.1371/journal.pone.0169052 . PMC 5207538 . PMID 28046007.
- ^ Schneider C, Oellerich T, Baldauf HM, Schwarz SM, Thomas D, Flick R, et al. (febrero de 2017). "SAMHD1 es un biomarcador de la respuesta a la citarabina y un objetivo terapéutico en la leucemia mieloide aguda" (PDF) . Nature Medicine . 23 (2): 250–255. doi :10.1038/nm.4255. PMID 27991919. S2CID 205398095.
- ^ Lemke TL, Williams DH, Foye WO (2002). Principios de química medicinal de Foye . Hagerstwon, MD: Lippincott Williams & Wilkins. pág. 963. ISBN 0-683-30737-1.
- ^ ab Colón-Cesario M, Wang J, Ramos X, García HG, Dávila JJ, Laguna J, et al. (Mayo 2006). "Un inhibidor de la recombinación del ADN bloquea la consolidación de la memoria, pero no la reconsolidación, en el contexto del condicionamiento del miedo". The Journal of Neuroscience . 26 (20): 5524–33. doi :10.1523/JNEUROSCI.3050-05.2006. PMC 6675301 . PMID 16707804.
- ^ Schwartsmann G, Brondani da Rocha A, Berlinck RG, Jimeno J (abril de 2001). "Organismos marinos como fuente de nuevos agentes anticancerígenos". The Lancet. Oncología . 2 (4): 221–225. doi :10.1016/s1470-2045(00)00292-8. PMID 11905767.
- ^ Sneader W (2005). Descubrimiento de fármacos: una historia . Nueva York: Wiley. p. 258. ISBN 0-471-89979-8.
- ^ Ogbomo H, Michaelis M, Klassert D, Doerr HW, Cinatl J (diciembre de 2008). "La resistencia a la citarabina induce la regulación positiva de los ligandos NKG2D y mejora la lisis de las células asesinas naturales de las células leucémicas". Neoplasia . 10 (12): 1402–1410. doi :10.1593/neo.08972. PMC 2586691 . PMID 19048119.

