Aparato de huso

En biología celular , el huso mitótico es la estructura del citoesqueleto de las células eucariotas que se forma durante la división celular para separar las cromátidas hermanas entre las células hijas . Se lo denomina huso mitótico durante la mitosis , un proceso que produce células hijas genéticamente idénticas, o huso meiótico durante la meiosis , un proceso que produce gametos con la mitad del número de cromosomas de la célula madre.
Además de los cromosomas, el aparato del huso está compuesto por cientos de proteínas . [1] [2] Los microtúbulos constituyen los componentes más abundantes de la maquinaria.
Estructura del husillo
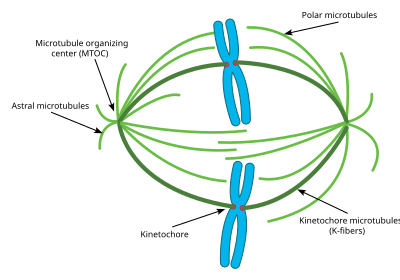
La unión de los microtúbulos a los cromosomas está mediada por los cinetocoros , que controlan activamente la formación del huso y previenen el inicio prematuro de la anafase . La polimerización y despolimerización de los microtúbulos impulsa dinámicamente la constitución de los cromosomas. La despolimerización de los microtúbulos genera tensión en los cinetocoros; [3] la unión bipolar de los cinetocoros hermanos a los microtúbulos que emanan de polos celulares opuestos acopla fuerzas de tensión opuestas, alineando los cromosomas en el ecuador celular y preparándolos para la segregación a las células hijas. Una vez que cada cromosoma está biorientado, comienza la anafase y la cohesina , que acopla las cromátidas hermanas , se corta, lo que permite el tránsito de las cromátidas hermanas a polos opuestos.
El aparato del huso celular incluye los microtúbulos del huso , proteínas asociadas, que incluyen motores moleculares de kinesina y dineína , cromosomas condensados y cualquier centrosoma o áster que pueda estar presente en los polos del huso dependiendo del tipo de célula. [4] El aparato del huso es vagamente elipsoide en sección transversal y se estrecha en los extremos. En la porción media ancha, conocida como la zona media del huso, los microtúbulos antiparalelos están agrupados por kinesinas . En los extremos puntiagudos, conocidos como polos del huso, los microtúbulos están nucleados por los centrosomas en la mayoría de las células animales. Los husos acentrosomales o anastrales carecen de centrosomas o ásteres en los polos del huso, respectivamente, y ocurren, por ejemplo, durante la meiosis femenina en la mayoría de los animales. [5] En este caso, un gradiente de Ran GTP es el principal regulador de la organización y ensamblaje de los microtúbulos del huso. En los hongos , los husos se forman entre los cuerpos de los polos del huso incrustados en la envoltura nuclear , que no se descompone durante la mitosis.
Proteínas asociadas a microtúbulos y dinámica del huso
El alargamiento y acortamiento dinámico de los microtúbulos del huso, a través de un proceso conocido como inestabilidad dinámica, determina en gran medida la forma del huso mitótico y promueve la alineación adecuada de los cromosomas en la zona media del huso. Las proteínas asociadas a los microtúbulos (MAP) se asocian con los microtúbulos en la zona media y los polos del huso para regular su dinámica. La γ-tubulina es una variante especializada de la tubulina que se ensambla en un complejo de anillo llamado γ-TuRC que nuclea la polimerización de los heterodímeros de tubulina α/β en microtúbulos. El reclutamiento de γ-TuRC a la región pericentrosomal estabiliza los extremos negativos de los microtúbulos y los ancla cerca del centro organizador de microtúbulos . La proteína asociada a los microtúbulos Augmin actúa junto con γ-TURC para nuclear nuevos microtúbulos a partir de los microtúbulos existentes. [6]
Los extremos en crecimiento de los microtúbulos están protegidos contra catástrofes por la acción de las proteínas de seguimiento de microtúbulos de extremo positivo (+TIPs) para promover su asociación con cinetocoros en la zona media. Se ha demostrado que CLIP170 se localiza cerca de los extremos positivos de los microtúbulos en células HeLa [7] y se acumula en los cinetocoros durante la prometafase . [8] Aunque no está claro cómo reconoce CLIP170 los extremos positivos, se ha demostrado que sus homólogos protegen contra catástrofes y promueven el rescate, [9] [10] lo que sugiere un papel para CLIP170 en la estabilización de los extremos positivos y posiblemente mediando su unión directa a los cinetocoros. [11] También se ha demostrado que las proteínas asociadas a CLIP como CLASP1 en humanos se localizan en los extremos positivos y el cinetocoro externo, así como también modulan la dinámica de los microtúbulos del cinetocoro (Maiato 2003). Los homólogos de CLASP en Drosophila , Xenopus y levaduras son necesarios para el ensamblaje adecuado del huso; en los mamíferos, CLASP1 y CLASP2 contribuyen al ensamblaje adecuado del huso y a la dinámica de los microtúbulos en la anafase. [12] La polimerización del extremo positivo puede ser moderada aún más por la proteína EB1, que se une directamente a los extremos en crecimiento de los microtúbulos y coordina la unión de otros +TIP. [13] [14]
En oposición a la acción de estas proteínas estabilizadoras de microtúbulos se encuentran varios factores despolimerizadores de microtúbulos que permiten la remodelación dinámica del huso mitótico para promover la constitución cromosómica y la consecución de la bipolaridad . La superfamilia de MAP de la kinesina -13 contiene una clase de proteínas motoras dirigidas al extremo positivo con actividad de despolimerización de microtúbulos asociada, incluidas las bien estudiadas MCAK de mamíferos y Xenopus XKCM1. La MCAK se localiza en las puntas en crecimiento de los microtúbulos en los cinetocoros, donde puede desencadenar una catástrofe en competencia directa con la actividad estabilizadora +TIP. [15] Estas proteínas aprovechan la energía de la hidrólisis de ATP para inducir cambios conformacionales desestabilizadores en la estructura del protofilamento que causan la liberación de kinesina y la despolimerización de microtúbulos. [16] La pérdida de su actividad da como resultado numerosos defectos mitóticos. [15] Otras proteínas desestabilizadoras de microtúbulos incluyen Op18/ estatmina y katanina , que tienen funciones en la remodelación del huso mitótico y promueven la segregación cromosómica durante la anafase. [17]
Las actividades de estos MAP están cuidadosamente reguladas para mantener una dinámica adecuada de los microtúbulos durante el ensamblaje del huso, y muchas de estas proteínas sirven como sustratos de las quinasas Aurora y Polo . [17] [18]
Organización del aparato husillo
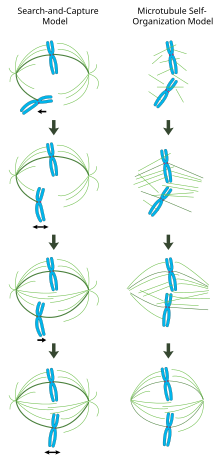
En un huso mitótico correctamente formado, los cromosomas biorientados están alineados a lo largo del ecuador de la célula con microtúbulos del huso orientados aproximadamente perpendicularmente a los cromosomas, sus extremos positivos incrustados en cinetocoros y sus extremos negativos anclados en los polos celulares. La orientación precisa de este complejo es necesaria para asegurar una segregación cromosómica precisa y especificar el plano de división celular. Sin embargo, sigue sin estar claro cómo se organiza el huso. Dos modelos predominan en el campo, que son sinérgicos y no mutuamente excluyentes. En el modelo de búsqueda y captura , el huso está organizado predominantemente por la separación hacia los polos de los centros organizadores de microtúbulos centrosómicos (MTOC). Los microtúbulos del huso emanan de los centrosomas y "buscan" cinetocoros; cuando se unen a un cinetocoro, se estabilizan y ejercen tensión sobre los cromosomas. En un modelo de autoensamblaje alternativo , los microtúbulos experimentan una nucleación acentrosomal entre los cromosomas condensados. Limitados por las dimensiones celulares, las asociaciones laterales con microtúbulos antiparalelos a través de proteínas motoras y las uniones en los extremos a los cinetocoros, los microtúbulos adoptan naturalmente una estructura similar a un huso con cromosomas alineados a lo largo del ecuador celular.
Modelo de "búsqueda y captura" mediado por centrosoma
En este modelo, los microtúbulos se nuclean en los centros organizadores de microtúbulos y experimentan un rápido crecimiento y catástrofe para "buscar" cinetocoros en el citoplasma. Una vez que se unen a un cinetocoro, se estabilizan y su dinámica se reduce. El nuevo cromosoma monoorientado oscila en el espacio cerca del polo al que está unido hasta que un microtúbulo del polo opuesto se une al cinetocoro hermano. Esta segunda unión estabiliza aún más la unión del cinetocoro al huso mitótico. Gradualmente, el cromosoma biorientado es atraído hacia el centro de la célula hasta que la tensión de los microtúbulos se equilibra en ambos lados del centrómero ; el cromosoma congresional oscila entonces en la placa de metafase hasta que el inicio de la anafase libera la cohesión de las cromátidas hermanas.
En este modelo, los centros organizadores de microtúbulos están localizados en los polos celulares, su separación es impulsada por la polimerización de los microtúbulos y el "deslizamiento" de los microtúbulos antiparalelos del huso entre sí en la zona media del huso mediado por kinesinas bipolares dirigidas al extremo positivo. [19] [20] Estas fuerzas de deslizamiento pueden explicar no solo la separación de los polos del huso al comienzo de la mitosis, sino también el alargamiento del huso durante la anafase tardía.
Autoorganización del huso mitótico mediada por cromatina
En contraste con el mecanismo de búsqueda y captura en el que los centrosomas dictan en gran medida la organización del huso mitótico, este modelo propone que los microtúbulos se nuclean acentrosomalmente cerca de los cromosomas y se ensamblan espontáneamente en haces antiparalelos y adoptan una estructura similar a un huso. [21] Los experimentos clásicos de Heald y Karsenti muestran que los husos y núcleos mitóticos funcionales se forman alrededor de perlas recubiertas de ADN incubadas en extractos de huevos de Xenopus y que se forman conjuntos bipolares de microtúbulos en ausencia de centrosomas y cinetocoros. [22] De hecho, también se ha demostrado que la ablación láser de los centrosomas en células de vertebrados no inhibe ni el ensamblaje del huso ni la segregación cromosómica. [23] Según este esquema, la forma y el tamaño del huso mitótico son una función de las propiedades biofísicas de las proteínas motoras de reticulación. [24]
Nucleación de microtúbulos mediada por cromatina mediante el gradiente Ran GTP
El factor de intercambio de nucleótidos de guanina para la pequeña GTPasa Ran (Regulador de la condensación cromosómica 1 o RCC1 ) se une a los nucleosomas a través de las histonas centrales H2A y H2B. [25] Por lo tanto, se genera un gradiente de Ran unido a GTP alrededor de la proximidad de la cromatina mitótica. Las perlas de vidrio recubiertas con RCC1 inducen la nucleación de microtúbulos y la formación del huso bipolar en extractos de huevos de Xenopus , revelando que el gradiente de Ran GTP por sí solo es suficiente para el ensamblaje del huso. [26] El gradiente desencadena la liberación de factores de ensamblaje del huso (SAF) a partir de interacciones inhibidoras a través de las proteínas de transporte importina β/α. Los SAF no unidos promueven entonces la nucleación y estabilización de los microtúbulos alrededor de la cromatina mitótica, y la bipolaridad del huso es organizada por proteínas motoras de los microtúbulos. [27]
Regulación del conjunto del husillo
El ensamblaje del huso está regulado en gran medida por eventos de fosforilación catalizados por quinasas mitóticas. Los complejos de quinasas dependientes de ciclina (CDK) son activados por ciclinas mitóticas, cuya traducción aumenta durante la mitosis. CDK1 (también llamada CDC2) se considera la principal quinasa mitótica en células de mamíferos y es activada por la ciclina B1. Las quinasas Aurora son necesarias para el ensamblaje y la separación adecuados del huso. [28] Aurora A se asocia con los centrosomas y se cree que regula la entrada mitótica. Aurora B es un miembro del complejo pasajero cromosómico y media la unión de los cromosomas a los microtúbulos y la cohesión de las cromátidas hermanas. La quinasa tipo Polo, también conocida como PLK, especialmente PLK1, tiene funciones importantes en el mantenimiento del huso al regular la dinámica de los microtúbulos. [29]
Estructura del cromosoma mitótico
Al final de la replicación del ADN , las cromátidas hermanas están unidas entre sí en una masa amorfa de ADN y proteínas enredadas. La entrada mitótica desencadena una reorganización drástica del genoma duplicado, lo que da como resultado cromátidas hermanas que se desenredan y se separan unas de otras. Los cromosomas también se acortan en longitud, hasta 10.000 veces en las células animales, [30] en un proceso llamado condensación. La condensación comienza en la profase y los cromosomas se compactan al máximo en estructuras con forma de varilla cuando se alinean en el medio del huso en la metafase. Esto da a los cromosomas mitóticos la clásica forma de "X" que se ve en los cariotipos , con cada cromátida hermana condensada unida a lo largo de sus longitudes por proteínas de cohesión y unidas, a menudo cerca del centro, en el centrómero . [30] [31] [32]
Si bien estos reordenamientos dinámicos son de vital importancia para garantizar una segregación precisa y de alta fidelidad del genoma, nuestra comprensión de la estructura de los cromosomas mitóticos sigue siendo en gran medida incompleta. Sin embargo, se han identificado algunos actores moleculares específicos: la topoisomerasa II utiliza la hidrólisis de ATP para catalizar la descatenación de los enredos de ADN, lo que promueve la resolución de las cromátidas hermanas. [33] Las condensinas son complejos de 5 subunidades que también utilizan la hidrólisis de ATP para promover la condensación de los cromosomas. [34] Los experimentos en extractos de huevos de Xenopus también han implicado al ligador Histona H1 como un importante regulador de la compactación de los cromosomas mitóticos. [35]
Punto de control del ensamblaje del huso mitótico
La finalización de la formación del huso es un punto de transición crucial en el ciclo celular, llamado punto de control del ensamblaje del huso . Si los cromosomas no están correctamente unidos al huso mitótico en el momento de este punto de control, el inicio de la anafase se retrasará. [36] La falla de este punto de control del ensamblaje del huso puede resultar en aneuploidía y puede estar involucrada en el envejecimiento y la formación de cáncer. [37]
Orientación del aparato del huso

La orientación de la división celular es de gran importancia para la arquitectura del tejido, el destino celular y la morfogénesis. Las células tienden a dividirse a lo largo de su eje largo de acuerdo con la llamada regla de Hertwig . El eje de la división celular está determinado por la orientación del aparato del huso. Las células se dividen a lo largo de la línea que conecta dos centrosomas del aparato del huso. Después de la formación, el aparato del huso experimenta una rotación dentro de la célula. Los microtúbulos astrales que se originan en los centrosomas alcanzan la membrana celular donde son atraídos hacia pistas corticales específicas. In vitro , la distribución de pistas corticales está establecida por el patrón adhesivo. [38] Las señales de polaridad in vivo están determinadas por la localización de las uniones tricelulares localizadas en los vértices celulares. [39] La distribución espacial de las pistas corticales conduce al campo de fuerza que determina la orientación final del aparato del huso y la orientación posterior de la división celular.
Véase también
Referencias
- ^ CE Walczak; R. Heald (2008). "Mecanismos de ensamblaje y función del huso mitótico". Revista Internacional de Citología . 265 : 111–158. doi :10.1016/s0074-7696(07)65003-7. ISBN 9780123743329. Número de identificación personal 18275887.
- ^ Helmke KJ, Heald R, Wilbur JD (2013). "Interacción entre la arquitectura y la función del huso" (PDF) . Revista internacional de biología celular y molecular. 306 : 83–125. doi :10.1016/B978-0-12-407694-5.00003-1. ISBN . 9780124076945. Número de identificación personal 24016524. Número de identificación personal 8145444.
- ^ E. Nogales; VH Ramey (1 de noviembre de 2009). "Información sobre la estructura y la función del complejo cinetocórico Dam1 de la levadura". J Cell Sci . 122 (21): 3831–3836. doi :10.1242/jcs.004689. PMC 2773187 . PMID 19889968.
- ^ Campbell, Neil A.; Jane B. Reece (2005). Biología, 7.ª edición . San Francisco: Benjamin Cummings. págs. 221–224. ISBN. 0-8053-7171-0.
- ^ Manandhar Gf; Schatten H; Sutovsky P (2005). "Reducción del centrosoma durante la gametogénesis y su importancia". Biol. Reprod . 72 (1): 2–13. doi : 10.1095/biolreprod.104.031245 . PMID: 15385423. S2CID : 37305534.
- ^ Petry S, et al. (2013). "Nucleación de microtúbulos ramificados en extractos de huevos de Xenopus mediada por augmina y TPX2". Cell . 152 (4): 768–777. doi :10.1016/j.cell.2012.12.044. PMC 3680348 . PMID 23415226.
- ^ JE Rickard; TE Kreis (1990). "Identificación de una nueva proteína de unión a microtúbulos sensible a nucleótidos en células HeLa". J Cell Biol . 110 (5): 1623–1633. doi :10.1083/jcb.110.5.1623. PMC 2200191 . PMID 1970824.
- ^ D. Dujardin; UI Wacker; A. Moreau; TA Schroer; JE Rickard; JR DeMey (1998). "Evidencia de un rol de CLIP-170 en el establecimiento de la alineación de cromosomas en metafase". J Cell Biol . 141 (4): 849–862. doi :10.1083/jcb.141.4.849. PMC 2132766 . PMID 9585405.
- ^ D. Brunner; P. Nurse (2000). "CLIP-170-like tip1p organiza espacialmente la dinámica microtubular en la levadura de fisión". Cell . 102 (5): 695–704. doi : 10.1016/S0092-8674(00)00091-X . PMID 11007487. S2CID 11948950.
- ^ YA Komarova; AS Kojima; et al. (2002). "Las proteínas de enlace citoplasmáticas promueven el rescate de microtúbulos in vivo". J Cell Biol . 159 (4): 589–599. doi :10.1083/jcb.200208058. PMC 2173097 . PMID 12446741.
- ^ S. Goldstone; C. Reyes; G. Gay; T. Courthéoux; M. Dubarry; et al. (2010). "La proteína Tip1/CLIP-170 es necesaria para el movimiento correcto de los cromosomas hacia los polos en la levadura de fisión". PLOS ONE . 5 (5): e10634. Bibcode :2010PLoSO...510634G. doi : 10.1371/journal.pone.0010634 . PMC 2869355 . PMID 20498706.
- ^ AL Pereira; AJ Pereira; ARR Maia; et al. (1 de octubre de 2006). "CLASP1 y CLASP2 de mamíferos cooperan para asegurar la fidelidad mitótica regulando la función del huso y del cinetocoro". Mol Biol Cell . 17 (10): 4526–4542. doi :10.1091/mbc.E06-07-0579. PMC 1635371 . PMID 16914514.
- ^ A. Akhmanova; MO Steinmetz (abril de 2008). "Seguimiento de los extremos: una red de proteínas dinámica controla el destino de las puntas de los microtúbulos". Nat Rev Mol Cell Biol . 9 (4): 309–322. doi :10.1038/nrm2369. PMID 18322465. S2CID 24977579.
- ^ JS Tirnauer; S. Grego; ED Salmon; TJ Mitchison (1 de octubre de 2002). "Interacciones EB1-microtúbulos en extractos de huevos de Xenopus: papel de EB1 en la estabilización de los microtúbulos y mecanismos de orientación hacia los microtúbulos". Mol Biol Cell . 13 (10): 3614–3626. doi :10.1091/mbc.02-04-0210. PMC 129970 . PMID 12388761.
- ^ ab ME Tanenbaum; RH Medema; A. Akhmanova (2011). "Regulación de la localización y actividad de la despolimerasa de microtúbulos MCAK". Bioarquitectura . 1 (2): 80–87. doi :10.4161/bioa.1.2.15807. PMC 3158623 . PMID 21866268.
- ^ H. Niederstrasser; H. Salehi-Had; EC Gan; C. Walczak; E. Nogales (2002). "XKCM1 actúa sobre un único protofilamento y requiere el extremo C de la tubulina". J Mol Biol . 316 (3): 817–828. doi :10.1006/jmbi.2001.5360. PMID 11866534.
- ^ ab H. Maiato; P Sampaio; CE Sunkel (2004). "Proteínas asociadas a los microtúbulos y sus funciones esenciales durante la mitosis". Int Rev Cytol . Revista internacional de citología. 241 : 53–153. doi :10.1016/S0074-7696(04)41002-X. hdl : 10216/53621 . ISBN 9780123646453. Número de identificación personal 15548419.
- ^ R. Tournebize; A. Popov; K. Kinoshita; AJ Ashford; et al. (2000). "Control de la dinámica de los microtúbulos mediante las actividades antagónicas de XMAP215 y XKCM1 en extractos de huevos de Xenopus". Nat Cell Biol . 2 (1): 13–19. doi :10.1038/71330. PMID 10620801. S2CID 10732643.
- ^ J. McIntosh; SC Landis (1971). "La distribución de los microtúbulos del huso durante la mitosis en células humanas cultivadas". J Cell Biol . 49 (2): 468–497. doi :10.1083/jcb.49.2.468. PMC 2108320 . PMID 19866774.
- ^ DJ Sharp; KL McDonald; HM Brown; et al. (1999). "La kinesina bipolar, KLP61F, crea enlaces cruzados entre microtúbulos dentro de los haces de microtúbulos interpolares de los husos mitóticos embrionarios de Drosophila". J Cell Biol . 144 (1): 125–138. doi :10.1083/jcb.144.1.125. PMC 2148119 . PMID 9885249.
- ^ MA Hallen; SA Endow (2009). "Conjunto del huso anastral: un modelo matemático". Biophys J . 97 (8): 2191–2201. Bibcode :2009BpJ....97.2191H. doi :10.1016/j.bpj.2009.08.008. PMC 2764103 . PMID 19843451.
- ^ R. Heald; R. Tournebize; et al. (1996). "Autoorganización de microtúbulos en husos bipolares alrededor de cromosomas artificiales en extractos de huevos de Xenopus". Nature . 382 (6590): 420–425. Bibcode :1996Natur.382..420H. doi :10.1038/382420a0. PMID 8684481. S2CID 4238425.
- ^ A. Khodjakov; RW Cole; BR Oakley; CL Rieder (2000). "Formación del huso mitótico independiente del centrosoma en vertebrados". Curr Biol . 10 (2): 59–67. doi : 10.1016/S0960-9822(99)00276-6 . PMID 10662665. S2CID 9976687.
- ^ KS Burbank; TJ Mitchison; DS Fisher (2007). "Modelos de deslizamiento y agrupamiento para el ensamblaje del huso". Curr Biol . 17 (16): 1373–1383. doi : 10.1016/j.cub.2007.07.058 . PMID 17702580.
- ^ Makde R, England J, Yennawar H, Tan S (2010). "Estructura del factor de cromatina RCC1 unido a la partícula central del nucleosoma". Nature . 467 (7315): 562–566. Bibcode :2010Natur.467..562M. doi :10.1038/nature09321. PMC 3168546 . PMID 20739938.
- ^ Halpin D, Kalab P, Wang J, Weis K, Heald R (2011). "Ensamblaje del huso mitótico alrededor de perlas recubiertas de RCC1 en extractos de huevos de Xenopus". PLOS Biol . 9 (12): e1001225. doi : 10.1371/journal.pbio.1001225 . PMC 3246454 . PMID 22215983.
- ^ Fu J, Jiang Q, Zhang C (2010). "Coordinación de eventos del ciclo celular por la GTPasa Ran". Nature Education . 3 (9): 32.
- ^ AR Barr; F. Gergely (2007). "Aurora A: La creadora y destructora de los polos del huso". J Cell Sci . 120 (17): 2987–2996. doi : 10.1242/jcs.013136 . PMID 17715155.
- ^ Peters, U., J. Cherian; et al. (2006). "Investigación del espacio fenotípico de la división celular y de la función de la quinasa tipo Polo utilizando moléculas pequeñas". Nat Chem Biol . 2 (11): 618–26. doi :10.1038/nchembio826. PMID 17028580. S2CID 22213611.
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace ) - ^ ab Morgan DO: El ciclo celular: principios de control (Primers in Biology) Londres: New Science Press Ltd; 2007:297. ISBN 978-0-9539181-2-6
- ^ Belmont AS (2010). "Organización de la cromatina a gran escala: lo bueno, lo sorprendente y lo aún desconcertante". Curr Opin Cell Biol . 26 : 69–78. doi :10.1016/j.ceb.2013.10.002. PMC 3927141 . PMID 24529248.
- ^ Marko, JF. El cromosoma mitótico: estructura y mecánica. 2012. Organización y función del genoma en el núcleo celular. Wiley-VCH, cap. 18, 449-485. doi :10.1002/9783527639991.ch18
- ^ Champoux JJ (2001). "TOPOISOMERASAS DE ADN: Estructura, función y mecanismo". Annu Rev Biochem . 70 (1): 369–413. doi :10.1146/annurev.biochem.70.1.369. PMID 11395412.
- ^ Hirano T (2012). "Condensinas: organizadores universales de cromosomas con diversas funciones". Genes Dev . 26 (15): 1659–1678. doi :10.1101/gad.194746.112. PMC 3418584 . PMID 22855829.
- ^ Maresca TJ, Freedman BS, Heald R (2005). "La histona H1 es esencial para la arquitectura y segregación de los cromosomas mitóticos en extractos de huevos de Xenopus laevis". J. Cell Biol . 169 (6): 859–69. doi :10.1083/jcb.200503031. PMC 2171634. PMID 15967810 .
- ^ Raven, Peter H.; Ray F. Evert; Susan E. Eichhorn (2005). Biología de las plantas, 7.ª edición . Nueva York: WH Freeman and Company Publishers. pág. 59. ISBN 0-7167-1007-2.
- ^ Baker DJ, Chen J, van Deursen JM (2005). "El punto de control mitótico en el cáncer y el envejecimiento: ¿qué nos han enseñado los ratones?". Curr. Opin. Cell Biol . 17 (6): 583–9. doi :10.1016/j.ceb.2005.09.011. PMID 16226453.
- ^ Thery M, Jimenez-Dalmaroni A, Racine V, Bornens M, Julicher F (2007). "Estudio experimental y teórico de la orientación del huso mitótico". Nature . 447 (7143): 493–6. Bibcode :2007Natur.447..493T. doi :10.1038/nature05786. PMID 17495931. S2CID 4391685.
- ^ Bosveld F, Markova O, Guirao B, Martin C, Wang Z, Pierre A, Balakireva M, Gaugue I, Ainslie A, Christophorou N, Lubensky DK, Minc N, Bellaïche Y (2016). "Las uniones tricelulares epiteliales actúan como sensores de forma de células en interfase para orientar la mitosis". Naturaleza . 530 (7591): 496–8. Código Bib :2016Natur.530..495B. doi : 10.1038/naturaleza16970. PMC 5450930 . PMID 26886796.
