Elemento mononucleídico
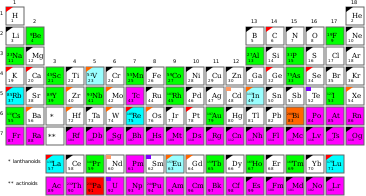
Un elemento mononucleídico o elemento monotópico [1] es uno de los 21 elementos químicos que se encuentran de forma natural en la Tierra esencialmente como un único nucleido (que puede ser, o no, un nucleido estable ). Este único nucleido tendrá una masa atómica característica. Por lo tanto, la abundancia isotópica natural del elemento está dominada por un isótopo que es estable o de vida muy larga. Hay 19 elementos en la primera categoría (que son tanto monoisotópicos como mononucleídicos), y 2 ( bismuto [a] y protactinio ) en la segunda categoría (mononucleídicos pero no monoisotópicos, ya que tienen cero, no un, nucleido estable). Al final de este artículo se ofrece una lista de los 21 elementos mononucleídicos.
De los 26 elementos monoisotópicos que, por definición, tienen un solo isótopo estable, siete no se consideran mononucleídicos, debido a la presencia de una fracción significativa de un radioisótopo de vida muy larga ( primordial ). Estos elementos son el vanadio , el rubidio , el indio , el lantano , el europio , el lutecio y el renio .
Uso en metrología
Muchas unidades de medida se definieron históricamente, o aún se definen, con referencia a las propiedades de sustancias específicas que, en muchos casos, se encontraban en la naturaleza como mezclas de múltiples isótopos, por ejemplo:
| Unidad | Dimensión | Sustancia de referencia | Propiedad relevante | Número de isótopos comunes | Estado actual (2022) |
|---|---|---|---|---|---|
| Segundo | Tiempo | Cesio | Frecuencia de transición hiperfina | 1 | Todavía en uso y una de las 7 unidades básicas del SI [2] |
| Metro | Longitud | Criptón | Longitud de onda de transición | 6 | Redefinido en 1983 [3] |
| Múltiple | Temperatura | Agua | Punto de fusión , punto de ebullición y punto triple. | 2 de hidrógeno y 3 de oxígeno | Redefinido en 2019 [4] o extinto |
| Caloría y unidad térmica británica | Energía | Agua | Capacidad calorífica específica | 2 de hidrógeno y 3 de oxígeno | Caloría redefinida en términos de julios , BTU todavía en uso. [5] Ninguna de las unidades forma parte del SI ni se recomienda su uso en él. |
| Lunar | Cantidad de sustancia | Carbón | Masa atómica | 3 | Redefinido en 2019 [6] |
| Dalton | Masa | Carbón | Masa atómica | 3 | Todavía en uso y aceptado para su uso en el SI (pero no como parte de él) [7] |
| Candela | Intensidad luminosa | Platino | Luminancia en el punto de fusión | 6 | Redefinido en 1979 [8] |
| Milímetro de mercurio | Presión | Mercurio | Densidad | 7 | Redefinido en términos del pascal , no forma parte del SI ni se recomienda su uso en él. |
Dado que las muestras tomadas de diferentes fuentes naturales pueden tener proporciones isotópicas sutilmente diferentes, las propiedades relevantes pueden diferir entre muestras. Si la definición simplemente se refiere a una sustancia sin abordar la composición isotópica, esto puede conducir a cierto nivel de ambigüedad en la definición y variación en las realizaciones prácticas de la unidad por diferentes laboratorios, como se observó con el kelvin antes de 2007. [9] Si la definición se refiere solo a un isótopo (como lo hace la del dalton) o a una proporción isotópica específica, por ejemplo, el agua oceánica media estándar de Viena , esto elimina una fuente de ambigüedad y variación, pero agrega capas de dificultad técnica (preparar muestras de una proporción isotópica deseada) e incertidumbre (con respecto a cuánto difiere una muestra de referencia real de la proporción nominal). El uso de elementos mononucleídicos como material de referencia elude estos problemas y, en particular, la única sustancia a la que se hace referencia en la iteración más reciente del SI es el cesio, un elemento mononucleídico.
Los elementos mononucleídicos también son de importancia científica porque sus pesos atómicos se pueden medir con gran precisión, ya que existe una incertidumbre mínima asociada con las abundancias isotópicas presentes en una muestra determinada. Otra forma de decirlo es que, para estos elementos, el peso atómico estándar y la masa atómica son los mismos. [10]
En la práctica, sólo 11 de los elementos mononucleídicos se utilizan en la metrología de peso atómico estándar. Estos son aluminio , bismuto , cesio , cobalto , oro , manganeso , fósforo, escandio , sodio, terbio y torio . [11]
En la espectroscopia de resonancia magnética nuclear (RMN), los tres núcleos estables más sensibles son el hidrógeno-1 ( 1H ), el flúor-19 ( 19F ) y el fósforo-31 ( 31P ). El flúor y el fósforo son monoisotópicos, al igual que el hidrógeno. La RMN de 1H , la RMN de 19F y la RMN de 31P permiten la identificación y el estudio de compuestos que contienen estos elementos.
Contaminación por isótopos traza inestables
En muestras naturales se encuentran trazas de isótopos inestables de algunos elementos mononucleídicos. Por ejemplo, el berilio-10 ( 10 Be), con una vida media de 1,4 millones de años, es producido por rayos cósmicos en la atmósfera superior de la Tierra ; el yodo-129 ( 129 I), con una vida media de 15,7 millones de años, es producido por diversos mecanismos cosmogénicos y nucleares; el cesio-137 ( 137 Cs), con una vida media de 30 años, es generado por fisión nuclear . Dichos isótopos se utilizan en una variedad de aplicaciones analíticas y forenses.
Lista de los 21 elementos mononucleídicos
Datos de masa isotópica de Pesos atómicos y composiciones isotópicas ed. JS Coursey, DJ Schwab y RA Dragoset, Instituto Nacional de Estándares y Tecnología (2005).
| Elemento | El nucleido más estable | Z ( p ) | N ( n ) | Masa isotópica ( Da ) | Vida media | Segundo nucleido más estable | N ( n ) | Vida media |
|---|---|---|---|---|---|---|---|---|
| berilio | 9 Ser | 4 | 5 | 9.012 182(3) | Estable | 10 Sé | 6 | 1.387(12) × 10 6 años |
| flúor | 19 F | 9 | 10 | 18.998 403 2(5) | Estable | 18 F | 9 | 109.739(9) minutos |
| sodio | 23 de noviembre | 11 | 12 | 22.989 770(2) | Estable | 22 de noviembre | 11 | 2.6018(22) años |
| aluminio | 27 Al | 13 | 14 | 26.981 538(2) | Estable | 26 Al | 13 | 7,17(24) × 10 5 años |
| fósforo | 31 P | 15 | 16 | 30.973 761(2) | Estable | 33 P | 18 | 25.35(11) d |
| escandio | 45 sc | 21 | 24 | 44.955 910(8) | Estable | 46 Sc | 25 | 83.79(4)d |
| manganeso | 55 Mn | 25 | 30 | 54.938 049(9) | Estable | 53 Mn | 28 | 3,7(4) × 10 6 años |
| cobalto | 59 Compañía | 27 | 32 | 58.933 200(9) | Estable | 60 Compañía | 33 | 5.2713(8) y |
| arsénico | 75 como | 33 | 42 | 74.921 60(2) | Estable | 73 Como | 40 | 80.30(6)d |
| itrio | 89 años | 39 | 50 | 88.905 85(2) | Estable | 88 años | 49 | 106.616(13) d |
| niobio | 93 Nb | 41 | 52 | 92.906 38(2) | Estable | 92 Nb | 51 | 3,47(24) × 10 7 años |
| rodio | 103 Rh | 45 | 58 | 102.905 50(2) | Estable | 102 m de latitud norte | 57 | 3.742(10) años |
| yodo | 127 yo | 53 | 74 | 126.904 47(3) | Estable | 129 yo | 76 | 1,57(4) × 10 7 años |
| cesio | 133 C | 55 | 78 | 132.905 45(2) | Estable | 135 C | 80 | 2,3 × 10 6 años |
| praseodimio | 141 Pr | 59 | 82 | 140.907 65(2) | Estable | 143 Pr | 84 | 13.57(2)d |
| terbio | 159 terabytes | 65 | 94 | 158.925 34(2) | Estable | 158 terabytes | 93 | 180(11) años |
| holmio | 165 años | 67 | 98 | 164.930 32(2) | Observacionalmente estable | 163 años | 97 | 4570(25) años |
| tulio | 169 Tm | 69 | 100 | 168.934 21(2) | Observacionalmente estable | 171 Tm | 102 | 1,92(1) años |
| oro | 197 Au | 79 | 118 | 196.966 55(2) | Observacionalmente estable | 195 Au | 116 | 186.098(47) d |
| bismuto | 209 Bi | 83 | 126 | 208.980 38(2) | 2.01(8) × 10 19 años | Bici de 210 m | 127 | 3.04(6) × 10 6 años |
| protactinio | 231 Pa | 91 | 140 | 231.035 88(2) | 3.276(11) × 10 4 años | 233 Pa | 142 | 26.975(13) d |
Véase también
- Elemento primordial
- Tabla de nucleidos ordenados por vida media
- Tabla de nucleidos
- Geoquímica de isótopos
- Radionúclido
- Lista de elementos según la estabilidad de sus isótopos
Notas
- ^ Hasta 2003, se pensaba que el 209 Bi pertenecía a la primera categoría. Luego se descubrió que tenía una vida media de 10 19 años, aproximadamente mil millones de veces la edad del universo. Véase Bismuto
Referencias
- ^ Housecroft, CE; Sharpe, AG (2012). Química inorgánica (4.ª ed.). Prentice Hall. pág. 2. ISBN 978-0273742753.
- ^ "Segundo - BIPM".
- ^ "Metro - BIPM".
- ^ "Kelvin-BIPM".
- ^ "Unidades térmicas británicas (Btu) - Administración de Información Energética de Estados Unidos (EIA)".
- ^ "Topo - BIPM".
- ^ https://www.bipm.org/documents/20126/41483022/SI-Brochure-9-EN.pdf/2d2b50bf-f2b4-9661-f402-5f9d66e4b507 [ URL desnuda PDF ]
- ^ "Candela-BIPM".
- ^ "Resolución 10 - BIPM".
- ^ NE Holden, "Valores de peso atómico estándar para los elementos mononucleídicos - 2001", BNL-NCS-68362, Brookhaven National Laboratory (2001)
- ^ Lista IUPAC de mononucleidos para fines de metrología