Detergente

Un detergente es un surfactante o una mezcla de surfactantes con propiedades limpiadoras cuando se encuentran en soluciones diluidas . [1] Existe una gran variedad de detergentes, una familia común son los alquilbencenosulfonatos , que son compuestos similares al jabón que son más solubles en agua dura , porque el sulfonato polar (de los detergentes) tiene menos probabilidades que el carboxilato polar (del jabón) de unirse al calcio y otros iones que se encuentran en el agua dura.
Definiciones
La palabra detergente se deriva del adjetivo latino detergens , del verbo detergere , que significa limpiar o pulir. El detergente puede definirse como un tensioactivo o una mezcla de tensioactivos con propiedades limpiadoras cuando se encuentran en soluciones diluidas . [1] Sin embargo, convencionalmente, detergente se usa para referirse a compuestos de limpieza sintéticos en lugar de jabón (una sal del ácido graso natural ), aunque el jabón también es un detergente en el verdadero sentido. [2] En contextos domésticos, el término detergente se refiere a productos de limpieza del hogar como el detergente para ropa o el detergente para platos , que son de hecho mezclas complejas de diferentes compuestos, no todos los cuales son en sí mismos detergentes.
La detergencia es la capacidad de eliminar sustancias no deseadas denominadas "suciedad" de un sustrato (por ejemplo, ropa). [3]
Estructura y propiedades
Los detergentes son un grupo de compuestos con una estructura anfifílica, donde cada molécula tiene una cabeza hidrófila (polar) y una cola hidrófoba larga (apolar). La porción hidrófoba de estas moléculas puede ser hidrocarburos de cadena lineal o ramificada , o puede tener una estructura esteroide . La porción hidrófila es más variada, pueden ser iónicas o no iónicas, y pueden variar desde una estructura simple hasta una relativamente elaborada. [4] Los detergentes son surfactantes ya que pueden disminuir la tensión superficial del agua. Su naturaleza dual facilita la mezcla de compuestos hidrófobos (como aceite y grasa) con agua. Debido a que el aire no es hidrófilo, los detergentes también son agentes espumantes en diversos grados.
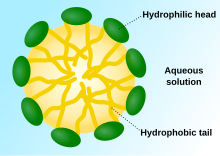
Las moléculas de detergente se agregan para formar micelas , lo que las hace solubles en agua. El grupo hidrofóbico del detergente es la principal fuerza impulsora de la formación de micelas; su agregación forma el núcleo hidrofóbico de las micelas. La micela puede eliminar grasa, proteínas o partículas de suciedad. La concentración a la que comienzan a formarse las micelas es la concentración micelar crítica (CMC), y la temperatura a la que las micelas se agregan aún más para separar la solución en dos fases es el punto de enturbiamiento cuando la solución se vuelve turbia y la detergencia es óptima. [4]
Los detergentes funcionan mejor en un pH alcalino. Las propiedades de los detergentes dependen de la estructura molecular del monómero . La capacidad de formar espuma puede estar determinada por el grupo principal; por ejemplo, los surfactantes aniónicos son muy espumantes, mientras que los surfactantes no iónicos pueden ser poco o nada espumantes. [5]
Clasificaciones químicas de los detergentes
Los detergentes se clasifican en cuatro grandes grupos, dependiendo de la carga eléctrica de los surfactantes. [6]
Detergentes aniónicos
Los detergentes aniónicos típicos son los sulfonatos de alquilbenceno . La porción de alquilbenceno de estos aniones es lipofílica y el sulfonato es hidrófilo. Se han popularizado dos variedades, las que tienen grupos alquilo ramificados y las que tienen grupos alquilo lineales. Las primeras fueron eliminadas en gran medida en las sociedades económicamente avanzadas porque son poco biodegradables. [7]
Los detergentes aniónicos son la forma más común de detergentes y se estima que anualmente se producen 6 mil millones de kilogramos de detergentes aniónicos para los mercados domésticos.
Los ácidos biliares , como el ácido desoxicólico (DOC), son detergentes aniónicos producidos por el hígado para ayudar en la digestión y absorción de grasas y aceites.

Detergentes catiónicos
Los detergentes catiónicos son similares a los aniónicos, pero el amonio cuaternario reemplaza al grupo sulfonato aniónico hidrofílico. El centro de sulfato de amonio tiene carga positiva. [7] Los surfactantes catiónicos generalmente tienen una detergencia deficiente.
Detergentes no iónicos
Los detergentes no iónicos se caracterizan por sus grupos de cabeza hidrófilos sin carga. Los detergentes no iónicos típicos se basan en polioxietileno o un glicósido . Los ejemplos comunes de los primeros incluyen Tween , Triton y la serie Brij. Estos materiales también se conocen como etoxilatos o PEGilatos y sus metabolitos, nonilfenol . Los glicósidos tienen un azúcar como su grupo de cabeza hidrófilo sin carga. Los ejemplos incluyen octiltioglucósido y maltósidos . Los detergentes de las series HEGA y MEGA son similares, poseen un alcohol de azúcar como grupo de cabeza.
Detergentes anfóteros
Los detergentes anfóteros o zwitteriónicos tienen iones zwitteriónicos dentro de un rango de pH particular y poseen una carga neta cero que surge de la presencia de cantidades iguales de grupos químicos con carga +1 y -1. Algunos ejemplos incluyen CHAPS .
Historia
Se sabe que el jabón se ha utilizado como surfactante para lavar la ropa desde la época sumeria en el año 2500 a. C. [8] En el antiguo Egipto , la soda se utilizaba como aditivo para el lavado. En el siglo XIX, comenzaron a crearse surfactantes sintéticos, por ejemplo a partir del aceite de oliva. [9] El silicato de sodio (vidrio de agua) se utilizó en la fabricación de jabón en los Estados Unidos en la década de 1860, [10] y en 1876, Henkel vendió un producto a base de silicato de sodio que se puede utilizar con jabón y se comercializó como un "detergente universal" ( Universalwaschmittel ) en Alemania. Luego, la soda se mezcló con silicato de sodio para producir el primer detergente de marca de Alemania, Bleichsoda. [11] En 1907, Henkel también agregó un agente blanqueador , perborato de sodio, para lanzar el primer detergente para ropa "autoactuante" Persil para eliminar el laborioso frotado de la ropa a mano. [12]
Durante la Primera Guerra Mundial , hubo escasez de aceites y grasas necesarios para hacer jabón. Para encontrar alternativas al jabón, los químicos alemanes fabricaron detergentes sintéticos utilizando materia prima derivada del alquitrán de hulla. [13] [14] [9] Sin embargo, estos primeros productos no proporcionaban suficiente detergencia. En 1928, se fabricó un detergente eficaz mediante la sulfatación de alcohol graso , pero la producción a gran escala no fue factible hasta que los alcoholes grasos de bajo costo estuvieron disponibles a principios de la década de 1930. [15] El detergente sintético creado fue más eficaz y tenía menos probabilidades de formar espuma que el jabón en agua dura, y también puede eliminar las reacciones ácidas y alcalinas y descomponer la suciedad. Los productos detergentes comerciales con sulfatos de alcohol graso comenzaron a venderse, inicialmente en 1932 en Alemania por Henkel . [15] En los Estados Unidos, los detergentes fueron vendidos en 1933 por Procter & Gamble ( Dreft ) principalmente en áreas con agua dura. [14] Sin embargo, las ventas en los EE. UU. crecieron lentamente hasta la introducción de detergentes "construidos" con la adición de un eficaz constructor de fosfato desarrollado a principios de la década de 1940. [14] El constructor mejora el rendimiento de los surfactantes al suavizar el agua a través de la quelación de iones de calcio y magnesio, lo que ayuda a mantener un pH alcalino, además de dispersar y mantener las partículas sucias en solución. [16] El desarrollo de la industria petroquímica después de la Segunda Guerra Mundial también produjo material para la producción de una gama de surfactantes sintéticos, y los sulfonatos de alquilbenceno se convirtieron en los surfactantes detergentes más importantes utilizados. [17] En la década de 1950, los detergentes para ropa se habían generalizado y reemplazaron en gran medida al jabón para limpiar la ropa en los países desarrollados. [15]
A lo largo de los años, se han desarrollado muchos tipos de detergentes para una variedad de propósitos, por ejemplo, detergentes de baja espuma para usar en lavadoras de carga frontal, detergentes de alta resistencia eficaces para eliminar la grasa y la suciedad, detergentes multiusos y detergentes especiales. [14] [18] Se incorporan en varios productos fuera del uso de lavandería, por ejemplo en detergentes para lavavajillas , champú, pasta de dientes, limpiadores industriales y en lubricantes y combustibles para reducir o prevenir la formación de lodos o depósitos. [19] La formulación de productos detergentes puede incluir blanqueador , fragancias, colorantes y otros aditivos. Sin embargo, el uso de fosfatos en detergentes generó preocupaciones sobre la contaminación por nutrientes y la demanda de cambios en la formulación de los detergentes. [20] También se plantearon preocupaciones sobre el uso de surfactantes como el sulfonato de alquilbenceno ramificado (sulfonato de tetrapropilenbenceno) que permanece en el medio ambiente, lo que llevó a su reemplazo por surfactantes que son más biodegradables, como el sulfonato de alquilbenceno lineal. [15] [17] Los desarrollos a lo largo de los años han incluido el uso de enzimas , sustitutos de fosfatos como la zeolita A y NTA , TAED como activador de blanqueador , surfactantes a base de azúcar que son biodegradables y más suaves para la piel, y otros productos ecológicos , así como cambios en la forma de administración, como tabletas, geles y cápsulas . [21] [22]
Principales aplicaciones de los detergentes

Limpieza del hogar
Una de las aplicaciones más importantes de los detergentes es la limpieza de hogares y comercios, incluido el lavado de vajilla y de ropa . Estos detergentes suelen estar disponibles en forma de polvos o soluciones concentradas, y sus formulaciones suelen ser mezclas complejas de una variedad de productos químicos además de los surfactantes, lo que refleja las diversas demandas de la aplicación y el mercado de consumo altamente competitivo. Estos detergentes pueden contener los siguientes componentes: [21]
- surfactantes
- reguladores de espuma
- constructores
- lejía
- activadores de lejía
- enzimas
- tintes
- Fragancias
- Otros aditivos
Aditivos para combustible
Tanto los carburadores como los componentes de los inyectores de combustible de los motores de combustión interna se benefician de los detergentes en los combustibles para evitar la formación de incrustaciones . Las concentraciones son de aproximadamente 300 ppm . Los detergentes típicos son las aminas y amidas de cadena larga, como la poliisobutenoamina y la poliisobutenoamida/ succinimida . [23]
Reactivo biológico
Los detergentes de grado reactivo se emplean para el aislamiento y la purificación de proteínas integrales de membrana que se encuentran en células biológicas . [24] La solubilización de las bicapas de la membrana celular requiere un detergente que pueda entrar en la monocapa de la membrana interna . [25] Los avances en la pureza y sofisticación de los detergentes han facilitado la caracterización estructural y biofísica de proteínas de membrana importantes, como los canales iónicos , que también alteran la membrana uniéndose a lipopolisacáridos , [26] transportadores , receptores de señalización y fotosistema II . [27]
Véase también
- Detergente escindible
- Líquido lavavajillas
- Dispersante
- Limpieza ecológica
- Limpiador de superficies duras
- Detergente para ropa
- Lista de productos de limpieza
- Tritón X-100
Referencias
- ^ ab IUPAC , Compendio de terminología química , 2.ª ed. (el "Libro de oro") (1997). Versión corregida en línea: (2006–) "detergente". doi :10.1351/goldbook.D01643
- ^ NIIR Board of Consultants Engineers (2013). El libro completo de tecnología sobre detergentes (2.ª edición revisada). Servicios de consultoría de proyectos de Niir. pág. 1. ISBN 9789381039199– a través de Google Books.
- ^ Arno Cahn, ed. (2003). 5.ª Conferencia Mundial sobre Detergentes. Sociedad Estadounidense de Químicos del Petróleo. pág. 154. ISBN 9781893997400– a través de Google Books.
- ^ ab Neugebauer, Judith M. (1990). "[18] Detergentes: una descripción general". Detergentes: una descripción general . Métodos en enzimología. Vol. 182. págs. 239–253. doi :10.1016/0076-6879(90)82020-3. ISBN 9780121820831. Número de identificación personal 2314239.
- ^ Niir Board (1999). Manual sobre jabones, detergentes y lechadas ácidas (3.ª edición revisada). Asia Pacific Business Press. pág. 270. ISBN 9788178330938– a través de Google Books.
- ^ Mehreteab, Ammanuel (1999). Guy Broze (ed.). Manual de detergentes, parte A. Taylor & Francis. págs. 133-134. ISBN 9781439833322– a través de Google Books.
- ^ ab Eduard Smulders, Wolfgang Rybinski, Eric Sung, Wilfried Rähse, Josef Steber, Frederike Wiebel, Anette Nordskog, "Detergentes para ropa" en la Enciclopedia de química industrial de Ullmann 2002, Wiley-VCH, Weinheim. doi :10.1002/14356007.a08_315.pub2
- ^ Jürgen Falbe, ed. (2012). Tensioactivos en productos de consumo. Springer-Verlag. págs. 1–2. ISBN 9783642715457– a través de Google Books.
- ^ de Paul Sosis, Uri Zoller, ed. (2008). Manual de detergentes, parte F. CRC Press. pág. 5. ISBN 9781420014655.
- ^ Aftalion, Fred (2001). Una historia de la industria química internacional. Chemical Heritage Press. pág. 82. ISBN 9780941901291.
- ^ Ward, James; Löhr (2020). La perfección del clip. Atria Books. pág. 190. ISBN 9781476799872.
- ^ Jakobi, Günter; Löhr, Albrecht (2012). Detergentes y Lavado de Textiles. Springer-Verlag. págs. 3–4. ISBN 9780895736864.
- ^ "Jabones y detergentes: Historia (desde 1900 hasta la actualidad)". Instituto Americano de Limpieza.Recuperado el 6 de enero de 2015
- ^ abcd David O. Whitten; Bessie Emrick Whitten (1 de enero de 1997). Manual de historia empresarial estadounidense: industrias extractivas, manufactura y servicios. Greenwood Publishing Group. págs. 221–222. ISBN 978-0-313-25199-3– a través de Google Books.
- ^ abcd Jürgen Falbe, ed. (2012). Surfactantes en productos de consumo. Springer-Verlag. págs. 3-5. ISBN 9783642715457– a través de Google Books.
- ^ Urban, David G. (2003). Cómo formular y combinar detergentes industriales. David G. Urban. págs. 4-5. ISBN 9781588988683.
- ^ de Paul Sosis, Uri Zoller, ed. (2008). Manual de detergentes, parte F. CRC Press. pág. 6. ISBN 9781420014655.
- ^ Paul Sosis, Uri Zoller, ed. (2008). Manual de detergentes, parte F. pág. 497. ISBN 9781420014655.
- ^ Uri Zoller, ed. (2008). Manual de detergentes, Parte E: Aplicaciones. Taylor y Francisco. pag. 331.ISBN 9781574447576.
- ^ David O. Whitten; Bessie Emrick Whitten (1999). Manual de detergentes, parte A. Taylor & Francis. pág. 3. ISBN 9781439833322– a través de Google Books.
- ^ ab Middelhauve, Birgit (2003). Arno Cahn (ed.). 5.ª Conferencia Mundial sobre Detergentes. Sociedad Estadounidense de Químicos del Petróleo. pp. 64–67. ISBN 9781893997400.
- ^ Long, Heather. "Historia del detergente para ropa". Me encantaría saberlo .
- ^ Werner Dabelstein, Arno Reglitzky, Andrea Schütze, Klaus Reders "Combustibles para automóviles" en la Enciclopedia de química industrial de Ullmann 2002, Wiley-VCH, Weinheim doi :10.1002/14356007.a16_719.pub2
- ^ Koley D, Bard AJ (2010). "Efectos de la concentración de Triton X-100 en la permeabilidad de la membrana de una sola célula HeLa mediante microscopía electroquímica de barrido (SECM)". Actas de la Academia Nacional de Ciencias de los Estados Unidos de América . 107 (39): 16783–7. Bibcode :2010PNAS..10716783K. doi : 10.1073/pnas.1011614107 . PMC 2947864 . PMID 20837548.
- ^ Lichtenberg D, Ahyayauch H, Goñi FM (2013). "El mecanismo de solubilización de bicapas lipídicas por detergentes". Revista Biofísica . 105 (2): 289–299. Bibcode :2013BpJ...105..289L. doi :10.1016/j.bpj.2013.06.007. PMC 3714928 . PMID 23870250.
- ^ Doyle, DA; Morais Cabral, J; Pfuetzner, RA; Kuo, A; Gulbis, JM; Cohen, SL; Chait, BT; MacKinnon, R (1998). "La estructura del canal de potasio: base molecular de la conducción y selectividad de K+". Science . 280 (5360): 69–77. Bibcode :1998Sci...280...69D. doi :10.1126/science.280.5360.69. PMID 9525859.
- ^ Umena, Yasufumi; Kawakami, Keisuke; Shen, Jian-Ren; Kamiya, Nobuo (2011). "Estructura cristalina del fotosistema II que desprende oxígeno a una resolución de 1,9 A" (PDF) . Nature . 473 (7345): 55–60. Bibcode :2011Natur.473...55U. doi :10.1038/nature09913. PMID 21499260. S2CID 205224374.
Enlaces externos
- About.com: ¿Cómo limpian los detergentes? Archivado el 6 de enero de 2011 en Wayback Machine
- Consejos de Campbell sobre química de detergentes, surfactantes e historia relacionada con el lavado de ropa, métodos de desmanchado y suciedad.
- Formulación de detergente

