Tocoferol
Los tocoferoles ( / t oʊ ˈ k ɒ f ə ˌ r ɒ l / ; [1] TCP ) son una clase de compuestos orgánicos que comprenden varios fenoles metilados , muchos de los cuales tienen actividad de vitamina E. Debido a que la actividad de la vitamina se identificó por primera vez en 1936 a partir de un factor de fertilidad dietético en ratas, se le denominó tocoferol , del griego τόκος tókos 'nacimiento' y φέρειν phérein 'dar a luz o llevar', es decir 'llevar un embarazo', con la terminación -ol que significa su estado como un alcohol químico .
El α-tocoferol es la principal fuente que se encuentra en los suplementos y en la dieta europea, donde las principales fuentes dietéticas son los aceites de oliva y girasol, [2] mientras que el γ-tocoferol es la forma más común en la dieta estadounidense debido a una mayor ingesta de aceite de soja y maíz. [2] [3]
Los tocotrienoles , que son compuestos relacionados, también tienen actividad de vitamina E. Todos estos diversos derivados con actividad vitamínica pueden denominarse correctamente " vitamina E ". Los tocoferoles y los tocotrienoles son antioxidantes liposolubles , pero también parecen tener muchas otras funciones en el organismo.
Formularios
La vitamina E existe en ocho formas diferentes, cuatro tocoferoles y cuatro tocotrienoles . Todas tienen un anillo de cromanol , con un grupo hidroxilo que puede donar un átomo de hidrógeno para reducir los radicales libres y una cadena lateral hidrófoba que permite la penetración en las membranas biológicas . Tanto los tocoferoles como los tocotrienoles se presentan en formas α (alfa), β (beta), γ (gamma) y δ (delta), determinadas por el número y la posición de los grupos metilo en el anillo de cromanol.
| Forma | Estructura |
|---|---|
| α-tocoferol |  |
| β-tocoferol |  |
| γ-tocoferol | 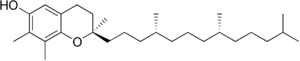 |
| δ-Tocoferol |  |
Los tocotrienoles tienen la misma estructura de metilo en el anillo y la misma notación de la letra griega metilo, pero se diferencian de los tocoferoles análogos por la presencia de tres enlaces dobles en la cadena lateral hidrofóbica. La insaturación de las colas da a los tocotrienoles solo un carbono estereoisomérico único (y, por lo tanto, dos isómeros posibles por fórmula estructural, uno de los cuales se produce de forma natural), mientras que los tocoferoles tienen tres centros (y ocho estereoisómeros posibles por fórmula estructural, nuevamente, solo uno de los cuales se produce de forma natural).
Cada forma tiene una actividad biológica diferente . [4] [5] En general, los l-isómeros no naturales de los tocotrienoles carecen de casi toda la actividad vitamínica, y la mitad de los 8 isómeros posibles de los tocoferoles (aquellos con quiralidad 2S en la unión de la cola del anillo) también carecen de actividad vitamínica. De los estereoisómeros que conservan la actividad, el aumento de la metilación, especialmente la metilación completa a la forma alfa, aumenta la actividad vitamínica. En los tocoferoles, esto se debe a la mayor energía de unión de la forma α-tocoferol de la vitamina a la proteína de unión al tocoferol.
Como aditivo alimentario , el tocoferol se etiqueta con estos números E : E306 (tocoferol), E307 (α-tocoferol), E308 (γ-tocoferol) y E309 (δ-tocoferol). Todos ellos están aprobados en los EE. UU. [6] , la UE [7] y Australia y Nueva Zelanda [8] para su uso como antioxidantes.
α-tocoferol
El α-tocoferol es la forma de vitamina E que se absorbe y acumula preferentemente en los seres humanos. [9] La medición de la actividad de la "vitamina E" en unidades internacionales (UI) se basó en la mejora de la fertilidad mediante la prevención de abortos espontáneos en ratas preñadas en relación con el α-tocoferol.
Aunque la forma monometilada ddd-γ-tocoferol es la forma más frecuente de vitamina E en los aceites, hay evidencia de que las ratas pueden metilar esta forma al α-tocoferol preferido, ya que varias generaciones de ratas conservaron niveles de α-tocoferol en los tejidos, incluso cuando esas generaciones fueron alimentadas solo con γ-tocoferol durante sus vidas.
Hay tres estereocentros en el α-tocoferol, por lo que se trata de una molécula quiral . [10] Los ocho estereoisómeros del α-tocoferol difieren en la disposición de los grupos alrededor de estos estereocentros. En la imagen de RRR -α-tocoferol que aparece a continuación, los tres estereocentros están en la forma R. Sin embargo, si se cambiara el centro de los tres estereocentros (de modo que el hidrógeno apuntara ahora hacia abajo y el grupo metilo hacia arriba), esta se convertiría en la estructura del RSR -α-tocoferol. Estos estereoisómeros también pueden nombrarse en una nomenclatura alternativa más antigua, donde los estereocentros están en la forma d o l . [11]

1 UI de tocoferol se define como ⅔ miligramos de RRR -α-tocoferol (anteriormente llamado d-α-tocoferol o, a veces, ddd-α-tocoferol). 1 UI también se define como 1 miligramo de una mezcla igual de los ocho estereoisómeros, que es una mezcla racémica llamada acetato de all-rac -α-tocoferilo . Esta mezcla de estereoisómeros a menudo se llama acetato de dl-α-tocoferilo, aunque es más precisamente acetato de dl,dl,dl-α-tocoferilo). Sin embargo, 1 UI de esta mezcla racémica ahora no se considera equivalente a 1 UI de α-tocoferol natural (RRR), y el Instituto de Medicina y el USDA ahora convierten las UI de la mezcla racémica a miligramos de RRR equivalente utilizando 1 UI de mezcla racémica = 0,45 "miligramos de α-tocoferol". [12] : 20–21
Tocotrienoles
Los tocotrienoles , aunque menos conocidos, también pertenecen a la familia de la vitamina E. Los tocotrienoles tienen cuatro isómeros 2' d naturales (tienen un carbono estereoisomérico solo en la posición de la cola del anillo 2'). Los cuatro tocotrienoles (en orden de metilación decreciente: d-α-, d-β-, d-γ- y d-δ-tocotrienol) tienen estructuras que corresponden a los cuatro tocoferoles, excepto con un enlace insaturado en cada una de las tres unidades de isopreno que forman la cola de hidrocarburo, mientras que los tocoferoles tienen una cola de fitilo saturada (la cola de fitilo de los tocoferoles da la posibilidad de 2 sitios estereoisoméricos más en estas moléculas que los tocotrienoles no tienen). El tocotrienol ha sido objeto de menos estudios clínicos y ha sido objeto de menos investigación en comparación con el tocoferol. Sin embargo, existe un creciente interés en los efectos de estos compuestos sobre la salud. [13]
Funciones y recomendaciones dietéticas

Mecanismo de acción
Los tocoferoles son captadores de radicales, que liberan un átomo de H para extinguir los radicales libres. A 323 kJ/mol, el enlace OH en los tocoferoles es aproximadamente un 10% más débil que en la mayoría de los otros fenoles . [14] Este enlace débil permite que la vitamina done un átomo de hidrógeno al radical peroxilo y a otros radicales libres , minimizando su efecto dañino. El radical tocoferilo así generado es relativamente poco reactivo, pero se revierte a tocoferol mediante una reacción redox con un donador de hidrógeno como la vitamina C. [ 15] Como son liposolubles, los tocoferoles se incorporan a las membranas celulares, que así quedan protegidas del daño oxidativo.
Consideraciones dietéticas
La ingesta diaria recomendada (IDR) para adultos en los Estados Unidos es de 15 mg/día. [16] La IDR se basa en la forma de α-tocoferol porque es la forma más activa, como se probó originalmente. Los suplementos de vitamina E se absorben mejor cuando se toman con las comidas. [17] El Instituto de Medicina de los Estados Unidos ha establecido un nivel máximo de ingesta tolerable (UL) para la vitamina E en 1000 mg (1500 UI) por día. [18] La Autoridad Europea de Seguridad Alimentaria establece el UL en 300 mg equivalentes de α-tocoferol/día. [19]
Equivalentes de α-tocoferol
Para fines dietéticos, la actividad de los isómeros de vitamina E se expresa como equivalentes de α-tocoferol (a-TE). Un a-TE se define por la actividad biológica de 1 mg (natural) de d-α-tocoferol en la prueba de resorción-gestación. Según las listas de la FAO y otros, el β-tocoferol debe multiplicarse por 0,5, el γ-tocoferol por 0,1 y el α-tocotrienol por 0,3. [4] La UI se convierte en aTE multiplicándola por 0,67. [20] Estos factores no se correlacionan con la actividad antioxidante de los isómeros de vitamina E, donde los tocotrienoles muestran una actividad incluso mucho mayor in vivo. [21]
Fuentes
El Departamento de Agricultura de los Estados Unidos (USDA), Servicios de Investigación Agrícola, mantiene una base de datos de composición de alimentos. La última revisión importante fue la del lanzamiento 28, en septiembre de 2015. [12] En general, las fuentes de alimentos con las concentraciones más altas de vitamina E son los aceites vegetales , seguidos de los frutos secos y las semillas . Sin embargo, si se ajustan los tamaños de las porciones típicas, para muchas personas en los Estados Unidos las fuentes más importantes de vitamina E incluyen los cereales de desayuno fortificados . [12]
Deficiencia
La deficiencia de vitamina E es poco frecuente y, en casi todos los casos, se debe a una enfermedad subyacente y no a una dieta pobre en vitamina E. [18] La deficiencia de vitamina E causa problemas neurológicos debido a una mala conducción nerviosa. Estos incluyen problemas neuromusculares como la ataxia espinocerebelosa y las miopatías . [11] La deficiencia también puede causar anemia , debido al daño oxidativo a los glóbulos rojos.
Suplementos
Los suplementos comerciales de vitamina E pueden clasificarse en varias categorías distintas:
- Vitamina E totalmente sintética, "dl-α-tocoferol", la forma de suplemento más barata y más vendida, generalmente como éster de acetato.
- Ésteres de vitamina E semisintéticos de "fuente natural", las formas de "fuente natural" utilizadas en comprimidos y multivitamínicos; son d-α-tocoferol altamente fraccionado o sus ésteres, a menudo elaborados mediante metilación sintética de vitámeros de tocoferol gamma y beta d,d,d extraídos de aceites vegetales.
- Suplementos con "tocoferoles mixtos naturales" menos fraccionados y con una fracción alta de d-γ-tocoferol
Sintético totalmente racémico
La vitamina E sintética derivada de productos derivados del petróleo se fabrica como acetato de α-tocoferol totalmente racémico con una mezcla de ocho estereoisómeros. En esta mezcla, una molécula de α-tocoferol de cada ocho moléculas se encuentra en forma de RRR -α-tocoferol (12,5% del total). [22]
El isómero 8 de la vitamina E all-rac siempre aparece en las etiquetas simplemente como dl-tocoferol o acetato de dl-tocoferol , aunque (si está escrito con todas las letras) sea dl,dl,dl-tocoferol. Los mayores fabricantes actuales de este tipo son DSM y BASF .
El α-tocoferol natural es la forma RRR-α (o ddd-α). La forma sintética dl,dl,dl-α ("dl-α") no es tan activa como la forma natural ddd-α ("d-α") del tocoferol. Esto se debe principalmente a la actividad reducida de las vitaminas de los cuatro estereoisómeros posibles que están representados por el enantiómero l o S en el primer estereocentro (una configuración S o l entre el anillo de cromanol y la cola, es decir, los estereoisómeros SRR, SRS, SSR y SSS). [10] Los tres estereoisómeros "2R" no naturales con configuración R natural en este estereocentro 2', pero S en uno de los otros centros en la cola (es decir, RSR, RRS, RSS), parecen retener una actividad sustancial de la vitamina RRR, porque son reconocidos por la proteína de transferencia de alfa-tocoferol y, por lo tanto, se mantienen en el plasma, mientras que los otros cuatro estereoisómeros (SRR, SRS, SSR y SSS) no lo son. Por lo tanto, el all-rac-α-tocoferol sintético, en teoría, tendría aproximadamente la mitad de la actividad vitamínica del RRR-α-tocoferol en humanos. Experimentalmente, la relación de actividades de la mezcla racémica de 8 estereoisómeros con la vitamina natural es de 1 a 1,36 en el modelo de embarazo de ratas (lo que sugiere una relación de actividad medida de 1/1,36 = 74% de la natural, para la mezcla racémica de 8 isómeros). [23]
Si bien está claro que las mezclas de estereoisómeros no son tan activas como la forma natural RRR -α-tocoferol, en las proporciones analizadas anteriormente, no se encuentra fácilmente disponible información específica sobre los efectos secundarios de los siete estereoisómeros sintéticos de la vitamina E.
Ésteres

Los fabricantes también suelen convertir la forma fenólica de las vitaminas (con un grupo hidroxilo libre ) en ésteres , utilizando ácido acético o succínico. Estos ésteres de tocoferol son más estables y son fáciles de usar en suplementos vitamínicos. Los ésteres de α-tocoferol se desesterifican en el intestino y luego se absorben como tocoferol libre. [24] [25] Los ésteres de nicotinato de tocoferol, linolato de tocoferol y palmitato de tocoferol también se utilizan en cosméticos y algunos productos farmacéuticos.
Tocoferoles mixtos
Los "tocoferoles mixtos" en los EE. UU. contienen al menos un 20 % p/p de otros tocoferoles naturales R, R, R-, es decir, un contenido de R, R, R-α-tocoferol más al menos un 25 % de R, R, R-β-, R, R, R-γ-, R, R, R-δ-tocoferoles. [ cita requerida ]
Algunas marcas pueden contener 20,0 % p/p o más de otros tocoferoles y tocotrienoles medibles. Algunos tocoferoles mixtos con un contenido más alto de γ-tocoferol se comercializan como "alto contenido de gamma-tocoferol". La etiqueta debe indicar cada componente en miligramos, excepto el R, R, R-α-tocoferol, que aún puede indicarse en UI. Los tocoferoles mixtos también pueden encontrarse en otros suplementos nutricionales. [ cita requerida ]
Usos
Los estudios observacionales que miden la ingesta dietética y/o la concentración sérica, y los estudios experimentales que idealmente son ensayos clínicos aleatorizados (ECA), son dos medios para examinar los efectos o la falta de ellos de una intervención propuesta sobre la salud humana. [26] Se puede esperar que los resultados de la atención médica concuerden entre las revisiones de estudios observacionales y experimentales. Si no hay acuerdo, entonces se deben considerar otros factores además del diseño. [27] En los estudios observacionales sobre la vitamina E, una correlación inversa entre la ingesta dietética y el riesgo de una enfermedad, o la concentración sérica y el riesgo de una enfermedad, puede considerarse sugestiva, pero cualquier conclusión también debe basarse en ensayos clínicos aleatorizados de tamaño y duración suficientes para medir resultados clínicamente significativos. Una preocupación con las correlaciones es que otros nutrientes y compuestos no nutrientes (como los polifenoles) pueden ser más altos en las mismas dietas que son más altas en vitamina E. Otra preocupación para la relevancia de los RCT descritos a continuación es que mientras que los estudios observacionales están comparando el riesgo de enfermedad entre la ingesta dietética baja y alta de vitamina E natural de los alimentos (cuando a nivel mundial, la ingesta dietética media de los adultos es de 6,2 mg/d para d-α-tocoferol; 10,2 mg/día cuando se incluyen todos los isómeros de tocoferol y tocotrienol), [28] los RCT prospectivos a menudo utilizaron 400 UI/día de dl-α-tocoferol sintético como producto de prueba, equivalente a 268 mg de equivalentes de α-tocoferol. [18]
Popularidad de los suplementos a lo largo del tiempo
En los EE. UU., la popularidad de la vitamina E como suplemento dietético puede haber alcanzado su punto máximo alrededor del año 2000. El Estudio de Salud de Enfermeras (NHS, por sus siglas en inglés) y el Estudio de Seguimiento de Profesionales de la Salud (HPFS, por sus siglas en inglés) rastrearon el uso de suplementos dietéticos por parte de personas mayores de 40 años durante los años 1986-2006. Para las mujeres, la prevalencia de uso fue del 16,1% en 1986, 46,2% en 1998, 44,3% en 2002, pero había disminuido al 19,8% en 2006. De manera similar, para los hombres, la prevalencia para los mismos años fue del 18,9%, 52,0%, 49,4% y 24,5%. Los autores teorizaron que la disminución del uso en estas poblaciones conscientes de las ciencias de la salud puede deberse a las publicaciones de estudios que no mostraron beneficios o consecuencias negativas de los suplementos de vitamina E. [29] Existen otras evidencias de que el uso de vitamina E está en declive. En el servicio militar de los Estados Unidos, se hizo un seguimiento de las prescripciones de vitaminas para militares en activo, en reserva y retirados, y sus dependientes, durante los años 2007-2011. Las prescripciones de vitamina E disminuyeron un 53%, mientras que las de vitamina C se mantuvieron constantes y las de vitamina D aumentaron un 454%. [30] Un informe sobre el volumen de ventas de vitamina E en los Estados Unidos documentó una disminución del 50% entre 2000 y 2006, [31] con una causa importante atribuida a un metaanálisis muy publicitado que había concluido que la vitamina E en dosis altas aumentaba la mortalidad por todas las causas. [32]
Degeneración macular relacionada con la edad
Una revisión Cochrane publicada en 2017 (actualizada en 2023) sobre suplementos de vitaminas y minerales antioxidantes para retardar la progresión de la degeneración macular relacionada con la edad (DMRE) identificó solo un ensayo clínico de vitamina E. [33] Ese ensayo comparó 500 UI/día de α-tocoferol con placebo durante cuatro años y no informó ningún efecto sobre la progresión de la DMRE en personas ya diagnosticadas con la enfermedad. [33] Otra revisión Cochrane, del mismo año, de los mismos autores, revisó la literatura sobre el α-tocoferol que previene el desarrollo de la DMRE. Esta revisión identificó cuatro ensayos, con una duración de 4 a 10 años, y no informó ningún cambio en el riesgo de desarrollar DMRE. [34] Un gran ensayo clínico conocido como AREDS comparó β-caroteno (15 mg), vitamina C (500 mg) y α-tocoferol (400 UI) con placebo durante hasta diez años, con la conclusión de que la combinación de antioxidantes ralentizó significativamente la progresión. Sin embargo, como en el ensayo no había ningún grupo que recibiera sólo vitamina E, no se pudieron sacar conclusiones sobre la contribución de la vitamina al efecto. [35]
Medicina complementaria y alternativa
Los defensores de la terapia con megavitaminas y de la medicina ortomolecular abogan por los tocoferoles naturales. [3] Mientras tanto, los ensayos clínicos se han concentrado en gran medida en el uso de acetato de d-α-tocoferol sintético totalmente racémico o acetato de dl-α-tocoferol sintético. [ cita requerida ]
Teoría de los antioxidantes
Se ha descrito que el tocoferol funciona como antioxidante. Se realizó un ensayo de determinación de dosis en personas con estrés oxidativo crónico atribuido a un nivel elevado de colesterol sérico. Se seleccionó la concentración plasmática de F2-isoprostano como biomarcador de la peroxidación lipídica mediada por radicales libres. Solo las dos dosis más altas (1600 y 3200 UI/día) redujeron significativamente el F2-isoprostano. [36]
Enfermedad de Alzheimer
La enfermedad de Alzheimer (EA) y la demencia vascular son causas comunes de deterioro de las funciones cerebrales que ocurren con la edad. La EA es una enfermedad neurodegenerativa crónica que empeora con el tiempo. [37] El proceso de la enfermedad está asociado con placas y ovillos en el cerebro. [38] La demencia vascular puede ser causada por infartos isquémicos o hemorrágicos que afectan múltiples áreas del cerebro, incluido el territorio de la arteria cerebral anterior , los lóbulos parietales o el giro cingulado . [39] Ambos tipos de demencia pueden estar presentes. Se conjetura que el estado de vitamina E (y el de otros nutrientes antioxidantes) tiene un posible impacto en el riesgo de enfermedad de Alzheimer y demencia vascular. Una revisión de estudios de ingesta dietética informó que un mayor consumo de vitamina E de los alimentos redujo el riesgo de desarrollar EA en un 24%. [40] Una segunda revisión examinó los niveles séricos de vitamina E y informó vitamina E sérica más baja en pacientes con EA en comparación con personas sanas de la misma edad. [41] En 2017, una declaración de consenso de la Asociación Británica de Psicofarmacología incluyó que hasta que haya más información disponible, no se puede recomendar la vitamina E para el tratamiento o la prevención de la enfermedad de Alzheimer. [42]
Cáncer
A partir de revisiones de estudios observacionales, las dietas con mayor contenido de vitamina E se asociaron con un menor riesgo relativo de cáncer de riñón , [43] cáncer de vejiga , [44] y cáncer de pulmón . [45] Cuando se hicieron comparaciones entre los grupos más bajos y más altos para el consumo dietético de vitamina E de los alimentos, las reducciones promedio en el riesgo relativo estuvieron en el rango de 16-19%. Para todas estas revisiones, los autores señalaron que los hallazgos debían confirmarse mediante estudios prospectivos. [43] [44] [45] De los ensayos clínicos aleatorizados (ECA) en los que se administró α-tocoferol como suplemento dietético, los resultados difirieron de las revisiones de la ingesta dietética. Un ECA de 400 UI/día de α-tocoferol no redujo el riesgo de cáncer de vejiga. [46] En fumadores de tabaco masculinos, 50 mg/día no tuvieron impacto en el desarrollo de cáncer de pulmón. [47] Una revisión de ECA para cáncer colorrectal informó la falta de una reducción estadísticamente significativa en el riesgo. [48] En fumadores masculinos, 50 mg/día redujeron el riesgo de cáncer de próstata en un 32%, [49] pero en un ensayo diferente, en el que la mayoría de los no fumadores eran fumadores, 400 UI/día aumentaron el riesgo en un 17%. [50] En mujeres que consumieron placebo o 600 UI de vitamina E de fuente natural en días alternos durante un promedio de 10,1 años, no hubo diferencias significativas para el cáncer de mama , el cáncer de pulmón o el cáncer de colon. [51]
En 1993, la Administración de Alimentos y Medicamentos de los Estados Unidos inició un proceso de revisión y aprobación de las declaraciones de propiedades saludables de los alimentos y los suplementos dietéticos. En 2012, se emitió una Declaración de propiedades saludables calificada que permite afirmar en la etiqueta del producto que la vitamina E puede reducir el riesgo de cáncer de riñón, vejiga y colorrectal, con la condición de que la etiqueta incluya una frase calificativa obligatoria: “La FDA ha concluido que hay muy poca evidencia científica para esta declaración”. [52] La Autoridad Europea de Seguridad Alimentaria (AESA) revisa las declaraciones de propiedades saludables propuestas para los países de la Unión Europea . A marzo de 2018, la AESA no ha evaluado ninguna declaración de propiedades saludables de la vitamina E y la prevención del cáncer.
Cataratas
Un metanálisis de 2015 informó que en los estudios que informaron sobre el tocoferol sérico, una mayor concentración sérica se asoció con una reducción del 23 % en el riesgo relativo de cataratas relacionadas con la edad (ARC), y el efecto se debió a diferencias en la catarata nuclear en lugar de la catarata cortical o subcapsular posterior, las tres clasificaciones principales de cataratas relacionadas con la edad. [53] Sin embargo, este artículo y un segundo metanálisis que informó sobre ensayos clínicos de suplementación con α-tocoferol no informaron cambios estadísticamente significativos en el riesgo de ARC en comparación con placebo. [53] [54]
Enfermedades cardiovasculares
Las investigaciones sobre los efectos de la vitamina E en las enfermedades cardiovasculares han producido resultados contradictorios. Se ha observado una relación inversa entre la enfermedad coronaria y el consumo de alimentos ricos en vitamina E, así como una mayor concentración sérica de α-tocoferol. [55] En uno de los estudios observacionales más grandes, se hizo un seguimiento de casi 90.000 enfermeras sanas durante ocho años. En comparación con las que se encontraban en el quinto más bajo en cuanto a consumo informado de vitamina E (de alimentos y suplementos dietéticos), las que se encontraban en el quinto más alto tenían un riesgo 34% menor de enfermedad coronaria grave. [56] Una dieta con un contenido más alto de vitamina E también puede ser más alta en otros componentes no identificados que promueven la salud cardíaca, o las personas que eligen dichas dietas pueden estar haciendo otras elecciones de estilo de vida saludables. [55] [56] Hay algunas pruebas de apoyo de ensayos clínicos aleatorizados (ECA). Un metaanálisis sobre los efectos de la suplementación con α-tocoferol en ECA sobre aspectos de la salud cardiovascular informó que cuando se consumía sin ningún otro nutriente antioxidante, el riesgo relativo de ataque cardíaco se reducía en un 18%. [57] Los resultados no fueron consistentes para todos los ensayos individuales incorporados al metanálisis. Por ejemplo, el Physicians' Health Study II no mostró ningún beneficio después de 400 UI cada dos días durante ocho años, para el ataque cardíaco, el accidente cerebrovascular, la mortalidad coronaria o la mortalidad por todas las causas. [58] Los efectos de la suplementación con vitamina E en la incidencia de accidente cerebrovascular se resumieron en 2011. No hubo beneficios significativos para la vitamina E frente al placebo para el riesgo de accidente cerebrovascular, o para el análisis de subconjuntos para accidente cerebrovascular isquémico , accidente cerebrovascular hemorrágico , accidente cerebrovascular fatal o accidente cerebrovascular no fatal. [59]
En 2001, la Administración de Alimentos y Medicamentos de los Estados Unidos rechazó las afirmaciones propuestas sobre los beneficios para la salud de la vitamina E y la salud cardiovascular. [60] Los Institutos Nacionales de Salud de los Estados Unidos también revisaron la literatura y concluyeron que no había evidencia suficiente para apoyar la idea de que el uso rutinario de suplementos de vitamina E previene la enfermedad cardiovascular o reduce su morbilidad y mortalidad. [18] En 2010, la Autoridad Europea de Seguridad Alimentaria revisó y rechazó las afirmaciones de que se había establecido una relación de causa y efecto entre la ingesta dietética de vitamina E y el mantenimiento de la función cardíaca normal o de la circulación sanguínea normal. [61]
Embarazo
Se ha propuesto que las vitaminas antioxidantes como suplementos dietéticos tienen beneficios si se consumen durante el embarazo. Para la combinación de vitamina E con vitamina C suplementada a mujeres embarazadas, una revisión Cochrane de 21 ensayos clínicos concluyó que los datos no respaldan la suplementación con vitamina E (la mayoría de los ensayos α-tocoferol a 400 UI/día más vitamina C a 1000 mg/día) como eficaz para reducir el riesgo de muerte fetal , muerte neonatal , parto prematuro , preeclampsia o cualquier otro resultado materno o infantil, ya sea en mujeres sanas o en aquellas consideradas en riesgo de complicaciones del embarazo. [62] La revisión identificó solo tres ensayos pequeños en los que se complementó con vitamina E sin co-suplementación con vitamina C. Ninguno de estos ensayos informó ninguna información clínicamente significativa. [62]
Actual
Aunque el uso de la vitamina E como medicamento tópico está muy extendido y se afirma que mejora la cicatrización de heridas y reduce el tejido cicatricial , las revisiones han concluido repetidamente que no hay pruebas suficientes para respaldar estas afirmaciones. [63] [64]
Efectos secundarios
La Junta de Alimentos y Nutrición de los Estados Unidos estableció un nivel máximo de ingesta tolerable (UL) en 1000 mg (1500 UI) por día derivado de modelos animales que demostraron sangrado a dosis altas. [16] La Autoridad Europea de Seguridad Alimentaria revisó la misma cuestión de seguridad y estableció un UL en 300 mg/día. [19] Un metaanálisis de ensayos clínicos a largo plazo informó un aumento no significativo del 2% en la mortalidad por todas las causas cuando el α-tocoferol fue el único suplemento utilizado. [65] Otro metaanálisis informó un aumento no significativo del 1% en la mortalidad por todas las causas cuando el α-tocoferol fue el único suplemento. El análisis de subconjuntos no informó ninguna diferencia entre el α-tocoferol natural (extraído de la planta) o sintético, o si la cantidad utilizada fue menor o mayor que 400 UI/día. [66] Existen informes de dermatitis alérgica de contacto inducida por vitamina E a causa del uso de derivados de la vitamina E, como linoleato de tocoferol y acetato de tocoferol en productos para el cuidado de la piel. La incidencia es baja a pesar de su uso generalizado. [67]
Interacciones farmacológicas
Las cantidades de α-tocoferol, otros tocoferoles y tocotrienoles que son componentes de la vitamina E dietética, cuando se consumen a partir de alimentos, no parecen causar ninguna interacción con medicamentos. El consumo de α-tocoferol como suplemento dietético en cantidades superiores a 300 mg/día puede provocar interacciones con aspirina , warfarina , tamoxifeno y ciclosporina A de formas que alteran la función. En el caso de la aspirina y la warfarina, las altas cantidades de vitamina E pueden potenciar la acción anticoagulante. [18] [68] Un pequeño ensayo demostró que la vitamina E a 400 mg/día redujo la concentración sanguínea del fármaco contra el cáncer de mama tamoxifeno. En varios ensayos clínicos, la vitamina E redujo la concentración sanguínea del fármaco inmunosupresor, ciclosporina A. [68] La Oficina de Suplementos Dietéticos de los Institutos Nacionales de Salud de los Estados Unidos plantea la preocupación de que la administración conjunta de vitamina E podría contrarrestar los mecanismos de la radioterapia contra el cáncer y algunos tipos de quimioterapia, por lo que desaconseja su uso en estas poblaciones de pacientes. Las referencias citadas informaron de casos de efectos adversos reducidos del tratamiento, pero también de una menor supervivencia del cáncer, lo que plantea la posibilidad de protección del tumor frente al daño oxidativo previsto por los tratamientos. [18]
Síntesis
El d-α-tocoferol de origen natural se puede extraer y purificar a partir de aceites de semillas, o el γ-tocoferol se puede extraer, purificar y metilar para crear d-alfa-tocoferol. A diferencia del α-tocoferol extraído de plantas, que también se denomina d-α-tocoferol, la síntesis industrial crea dl-α-tocoferol. "Se sintetiza a partir de una mezcla de tolueno y 2,3,5-trimetil-hidroquinona que reacciona con isofitol para formar todo-rac-α-tocoferol, utilizando hierro en presencia de gas cloruro de hidrógeno como catalizador. La mezcla de reacción obtenida se filtra y se extrae con sosa cáustica acuosa. El tolueno se elimina por evaporación y el residuo (todo el rac-α-tocoferol) se purifica por destilación al vacío". La especificación del ingrediente es >97% puro. [69] Este dl-α-tocoferol sintético tiene aproximadamente el 50% de la potencia del d-α-tocoferol. Los fabricantes de suplementos dietéticos y alimentos fortificados para humanos o animales domésticos convierten la forma fenólica de la vitamina en un éster utilizando ácido acético o ácido succínico porque los ésteres son químicamente más estables, lo que proporciona una vida útil más larga. Las formas de éster se desesterifican en el intestino y se absorben como α-tocoferol libre.
Historia
En 1922, durante experimentos de alimentación con ratas, Herbert McLean Evans concluyó que, además de las vitaminas B y C, existía una vitamina desconocida. [70] Aunque las ratas tenían todos los demás nutrientes, no eran fértiles. Esta condición se podía cambiar con una alimentación adicional con germen de trigo. Pasaron varios años hasta 1936, cuando se aisló la sustancia del germen de trigo y se determinó la fórmula C 29 H 50 O 2 . Evans también descubrió que el compuesto reaccionaba como un alcohol y concluyó que uno de los átomos de oxígeno era parte de un grupo OH (hidroxilo). Como se señaló en la introducción, Evans le dio su nombre a la vitamina a partir de palabras griegas que significan "tener crías" con la adición del -ol como alcohol. [71] La estructura se determinó poco después, en 1938. [72]
Véase también
Referencias
- ^ "Tocoferol". Dictionary.com Unabridged (en línea). sf . Consultado el 28 de febrero de 2018 .
- ^ ab Wagner KH, Kamal-Eldin A, Elmadfa I (2004). "Gamma-tocoferol: ¿una vitamina subestimada?". Anales de nutrición y metabolismo . 48 (3): 169–88. doi :10.1159/000079555. PMID 15256801. S2CID 24827255.
En América del Norte, se ha estimado que la ingesta de γ-tocoferol supera a la de α-tocoferol en un factor de 2 a 4 ... debido al hecho de que el aceite de soja es el aceite vegetal predominante en la dieta estadounidense (76,4 %), seguido del aceite de maíz y el aceite de canola (ambos 7 %) ... El suministro de grasas dietéticas ... es mucho más diverso en Europa ... Los aceites que se consumen principalmente en Europa, es decir, el aceite de girasol, oliva y canola, proporcionan menos γ-tocoferol pero más α-tocoferol ... [L]a relación de α-:γ-tocoferol es al menos 1:2. Por lo tanto, la ingesta promedio de γ-tocoferol puede estimarse en 4-6 mg/día, que es aproximadamente el 25-35 % de la ingesta de EE. UU. De acuerdo con la ingesta europea estimada más baja de γ-tocoferol, los niveles séricos de γ-tocoferol en las poblaciones europeas son entre 4 y 20 veces inferiores a los de α-tocoferol.
- ^ ab Jiang Q, Christen S, Shigenaga MK, Ames BN (diciembre de 2001). "El gamma-tocoferol, la principal forma de vitamina E en la dieta estadounidense, merece más atención". The American Journal of Clinical Nutrition . 74 (6): 714–22. doi : 10.1093/ajcn/74.6.714 . PMID 11722951.
- ^ ab Organización de las Naciones Unidas para la Agricultura y la Alimentación , Organización Mundial de la Salud (2001). "9. Vitamina E". Consulta conjunta de expertos FAO/OMS sobre necesidades humanas de vitaminas y minerales (informe). Bangkok (Tailandia): FAO Roma.
- ^ Burton GW, Ingold KU (1981). "Autooxidación de moléculas biológicas. 1. Actividad antioxidante de la vitamina E y antioxidantes fenólicos rompedores de cadena relacionados in vitro". Journal of the American Chemical Society . 103 (21): 6472–6477. doi :10.1021/ja00411a035.
- ^ Administración de Alimentos y Medicamentos de Estados Unidos: "Listado de estatus de aditivos alimentarios Parte II". Administración de Alimentos y Medicamentos . Archivado desde el original el 8 de noviembre de 2011. Consultado el 27 de octubre de 2011 .
- ^ Agencia de Normas Alimentarias del Reino Unido: «Aditivos aprobados actualmente por la UE y sus números E». Archivado desde el original el 7 de octubre de 2010. Consultado el 27 de octubre de 2011 .
- ^ Código de normas alimentarias de Australia y Nueva Zelanda "Norma 1.2.4 - Etiquetado de ingredientes". 8 de septiembre de 2011.
- ^ Rigotti A (2007). "Absorción, transporte y administración tisular de vitamina E". Aspectos moleculares de la medicina . 28 (5–6): 423–36. doi :10.1016/j.mam.2007.01.002. PMID 17320165.
- ^ ab Jensen S, Lauridsen C (2007). Estereoisómeros de α-tocoferol . vol. 76, págs. 281–308. doi :10.1016/S0083-6729(07)76010-7. ISBN 9780123735928. Número de identificación personal 17628178.
{{cite book}}:|journal=ignorado ( ayuda ) - ^ ab Brigelius-Flohé R, Traber MG (julio de 1999). "Vitamina E: función y metabolismo". FASEB Journal . 13 (10): 1145–55. doi : 10.1096/fasebj.13.10.1145 . PMID 10385606. S2CID 7031925.
- ^ abc Nutrient Data Laboratory (septiembre de 2015). Composición de alimentos crudos, procesados y preparados: Base de datos nacional de nutrientes del USDA para referencia estándar, versión 28 (PDF) (informe) (edición ligeramente revisada). Beltsville, MA: Beltsville Human Nutrition Research Center, Agricultural Research Service , Departamento de Agricultura de los Estados Unidos . págs. 20–21. SR28.
- ^ Sen CK, Khanna S, Roy S (marzo de 2006). "Tocotrienoles: la vitamina E más allá de los tocoferoles". Ciencias de la vida . 78 (18): 2088–98. doi :10.1016/j.lfs.2005.12.001. PMC 1790869 . PMID 16458936.
- ^ Lide DR, ed. (2006). Manual de química y física del CRC (87.ª edición). Boca Raton, FL: CRC Press . ISBN 0-8493-0487-3.
- ^ Traber MG, Stevens JF (septiembre de 2011). "Vitaminas C y E: efectos beneficiosos desde una perspectiva mecanicista". Free Radical Biology & Medicine . 51 (5): 1000–13. doi :10.1016/j.freeradbiomed.2011.05.017. PMC 3156342 . PMID 21664268.
- ^ Instituto de Medicina (2000). "Vitamina E". Ingesta dietética de referencia para vitamina C, vitamina E, selenio y carotenoides . Washington, DC: The National Academies Press. págs. 186-283. doi :10.17226/9810. ISBN. 978-0-309-06935-9. PMID 25077263. Archivado desde el original el 26 de febrero de 2018.
- ^ Iuliano L, Micheletta F, Maranghi M, Frati G, Diczfalusy U, Violi F (octubre de 2001). "Biodisponibilidad de la vitamina E en función de la ingesta de alimentos en sujetos sanos: efectos sobre la actividad de eliminación de peróxido plasmático y los productos de oxidación del colesterol". Arteriosclerosis, trombosis y biología vascular . 21 (10): E34-7. doi : 10.1161/hq1001.098465 . PMID 11597949.
- ^ abcdef Institutos Nacionales de Salud (26 de marzo de 2021). «Vitamina E: Hoja informativa para profesionales de la salud». Hojas informativas sobre suplementos dietéticos . Oficina de Suplementos Dietéticos . Consultado el 19 de mayo de 2021 .
- ^ ab Niveles máximos tolerables de ingesta de vitaminas y minerales (PDF) , Autoridad Europea de Seguridad Alimentaria, 2006, archivado (PDF) desde el original el 16 de marzo de 2016
- ^ "Vitaminas". Archivado desde el original el 20 de marzo de 2013. Consultado el 26 de marzo de 2013 .Centro de coordinación de nutrición y vitaminas de la Universidad de Minnesota
- ^ Packer L, Weber SU, Rimbach G (febrero de 2001). "Aspectos moleculares de la acción antioxidante del alfa-tocotrienol y la señalización celular". The Journal of Nutrition . 131 (2): 369S–73S. doi : 10.1093/jn/131.2.369S . PMID 11160563.
- ^ Weiser H, Riss G, Kormann AW (octubre de 1996). "La biodiscriminación de los ocho estereoisómeros de α-tocoferol da como resultado una acumulación preferencial de las cuatro formas 2R en los tejidos y el plasma de ratas". The Journal of Nutrition . 126 (10): 2539–49. doi : 10.1093/jn/126.10.2539 . PMID 8857515.
- ^ "En conjunto, estos datos indican que de los ocho estereoisómeros (RRR, RSR, RRS, RSS, SRR, SSR, SRS, SSS) del all-rac-α-tocoferol, sólo las cuatro formas 2R (RRR, RSR, RSS, RRS) son reconocidas por el α-TTP y se mantienen en el plasma. De hecho, el Food and Nutrition Board (Food and Nutrition Board and Institute of Medicine, 2000) ha definido que sólo el α-tocoferol, específicamente las formas 2R del α-tocoferol, pueden satisfacer el requerimiento humano de vitamina E. Por lo tanto, el all-rac-α-tocoferol tiene sólo la mitad de la actividad del RRR-α-tocoferol". Tomado de la discusión en Lauridsen C, Engel H, Craig AM, Traber MG (marzo de 2002). "Bioactividad relativa de los acetatos de RRR y all-rac-α-tocoferol en la dieta de cerdos evaluada con vitamina E marcada con deuterio" (PDF) . Journal of Animal Science . 80 (3): 702–7. doi :10.2527/2002.803702x. PMID 11890405. Archivado desde el original (PDF) el 2008-12-17 . Consultado el 2008-03-12 .
- ^ Mathias PM, Harries JT, Peters TJ, Muller DP (julio de 1981). "Estudios sobre la absorción in vivo de soluciones micelares de tocoferol y acetato de tocoferol en la rata: demostración y caracterización parcial de una esterasa mucosa localizada en el retículo endoplasmático del enterocito". Journal of Lipid Research . 22 (5): 829–37. doi : 10.1016/S0022-2275(20)37355-7 . PMID 7288289.
- ^ Ajandouz EH, Castan S, Jakob S, Puigserver A (2006). "Un método de HPLC rápido y sensible para la determinación de la actividad de esterasa en acetato de α-tocoferol". Journal of Chromatographic Science . 44 (10): 631–3. doi : 10.1093/chromsci/44.10.631 . PMID 17254374.
- ^ Munnangi S, Boktor SW (18 de diciembre de 2018). "Epidemiología del diseño de estudios". EstadísticasPerlas . Estadísticas de perlas. PMID 29262004.
- ^ Toews I, Anglemyer A, Nyirenda JL, Alsaid D, Balduzzi S, Grummich K, et al. (4 de enero de 2024). "Resultados de la atención sanitaria evaluados con diseños de estudios observacionales en comparación con los evaluados en ensayos aleatorizados: un estudio metaepidemiológico". Base de datos Cochrane de revisiones sistemáticas . 1 (1): MR000034. doi :10.1002/14651858.MR000034.pub3. ISSN 1469-493X. PMC 10765475. PMID 38174786.
- ^ Péter S, Friedel A, Roos FF, Wyss A, Eggersdorfer M, Hoffmann K, et al. (diciembre de 2015). "Una revisión sistemática del estado global de alfa-tocoferol evaluado por los niveles de ingesta nutricional y las concentraciones séricas en sangre". Revista internacional de investigación sobre vitaminas y nutrición . 85 (5–6): 261–281. doi : 10.1024/0300-9831/a000281 . PMID 27414419.
- ^ Kim HJ, Giovannucci E, Rosner B, Willett WC, Cho E (marzo de 2014). "Tendencias longitudinales y seculares en el uso de suplementos dietéticos: Estudio de salud de enfermeras y estudio de seguimiento de profesionales de la salud, 1986-2006". Revista de la Academia de Nutrición y Dietética . 114 (3): 436–43. doi :10.1016/j.jand.2013.07.039. PMC 3944223 . PMID 24119503.
- ^ Morioka TY, Bolin JT, Attipoe S, Jones DR, Stephens MB, Deuster PA (julio de 2015). "Tendencias en las prescripciones de suplementos de vitamina A, C, D, E y K en centros de tratamiento militares: 2007 a 2011". Medicina militar . 180 (7): 748–53. doi : 10.7205/MILMED-D-14-00511 . PMID 26126244.
- ^ Tilburt JC, Emanuel EJ, Miller FG (septiembre de 2008). "¿La evidencia marca una diferencia en el comportamiento del consumidor? Ventas de suplementos antes y después de la publicación de resultados de investigación negativos". Journal of General Internal Medicine . 23 (9): 1495–8. doi :10.1007/s11606-008-0704-z. PMC 2518024 . PMID 18618194.
- ^ Miller ER, Pastor-Barriuso R, Dalal D, Riemersma RA, Appel LJ, Guallar E (enero de 2005). "Metaanálisis: la suplementación con vitamina E en dosis altas puede aumentar la mortalidad por todas las causas". Annals of Internal Medicine . 142 (1): 37–46. doi :10.7326/0003-4819-142-1-200501040-00110. PMID 15537682. S2CID 35030072.
- ^ ab Evans JR, Lawrenson JG (13 de septiembre de 2023). "Suplementos de vitaminas y minerales antioxidantes para retardar la progresión de la degeneración macular relacionada con la edad". Base de datos Cochrane de revisiones sistemáticas . 2023 (9): CD000254. doi :10.1002/14651858.CD000254.pub5. ISSN 1469-493X. PMC 10498493. PMID 37702300 .
- ^ Evans JR, Lawrenson JG (julio de 2017). "Suplementos de vitaminas y minerales antioxidantes para prevenir la degeneración macular relacionada con la edad". Base de datos Cochrane de revisiones sistemáticas . 2017 (7): CD000253. doi : 10.1002/14651858.CD000253.pub4. PMC 6483250. PMID 28756617.
- ^ Chew EY, Clemons TE, Agrón E, Sperduto RD, Sangiovanni JP, Kurinij N, et al. (Agosto de 2013). "Efectos a largo plazo de las vitaminas C y E, el β-caroteno y el zinc sobre la degeneración macular relacionada con la edad: informe AREDS nº 35". Oftalmología . 120 (8): 1604–11.e4. doi :10.1016/j.ophtha.2013.01.021. PMC 3728272 . PMID 23582353.
- ^ Roberts LJ, Oates JA, Linton MF, Fazio S, Meador BP, Gross MD, et al. (noviembre de 2007). "La relación entre la dosis de vitamina E y la supresión del estrés oxidativo en humanos". Free Radical Biology & Medicine . 43 (10): 1388–93. doi :10.1016/j.freeradbiomed.2007.06.019. PMC 2072864 . PMID 17936185.
- ^ Burns A, Iliffe S (febrero de 2009). "Enfermedad de Alzheimer". BMJ . 338 : b158. doi :10.1136/bmj.b158. PMID 19196745. S2CID 8570146.
- ^ Ballard C, Gauthier S, Corbett A, Brayne C, Aarsland D, Jones E (marzo de 2011). "Enfermedad de Alzheimer". Lanceta . 377 (9770): 1019–31. doi :10.1016/S0140-6736(10)61349-9. PMID 21371747. S2CID 20893019.
- ^ Love S (diciembre de 2005). "Investigación neuropatológica de la demencia: una guía para neurólogos". Journal of Neurology, Neurosurgery, and Psychiatry . 76 Suppl 5 (suplemento 5): v8-14. doi :10.1136/jnnp.2005.080754. PMC 1765714 . PMID 16291923.
- ^ Li FJ, Shen L, Ji HF (2012). "Ingesta dietética de vitamina E, vitamina C y β-caroteno y riesgo de enfermedad de Alzheimer: un metaanálisis". Journal of Alzheimer's Disease . 31 (2): 253–8. doi :10.3233/JAD-2012-120349. PMID 22543848.
- ^ Dong Y, Chen X, Liu Y, Shu Y, Chen T, Xu L, et al. (febrero de 2018). "¿Los niveles bajos de vitamina E en suero aumentan el riesgo de enfermedad de Alzheimer en personas mayores? Evidencia de un metaanálisis de estudios de casos y controles". Revista Internacional de Psiquiatría Geriátrica . 33 (2): e257–e263. doi :10.1002/gps.4780. PMID 28833475. S2CID 44859128.
- ^ O'Brien JT, Holmes C, Jones M, Jones R, Livingston G, McKeith I, et al. (febrero de 2017). "Práctica clínica con fármacos contra la demencia: una declaración de consenso revisada (tercera) de la Asociación Británica de Psicofarmacología" (PDF) . Revista de Psicofarmacología . 31 (2): 147–168. doi :10.1177/0269881116680924. PMID 28103749. S2CID 52848530.
- ^ ab Shen C, Huang Y, Yi S, Fang Z, Li L (noviembre de 2015). "Asociación de la ingesta de vitamina E con un riesgo reducido de cáncer de riñón: un metaanálisis de estudios observacionales". Medical Science Monitor . 21 : 3420–6. doi :10.12659/MSM.896018. PMC 4644018 . PMID 26547129.
- ^ ab Wang YY, Wang XL, Yu ZJ (2014). "Ingesta de vitamina C y E y riesgo de cáncer de vejiga: un metaanálisis de estudios observacionales". Revista internacional de medicina clínica y experimental . 7 (11): 4154–64. PMC 4276184 . PMID 25550926.
- ^ ab Zhu YJ, Bo YC, Liu XX, Qiu CG (marzo de 2017). "Asociación de la ingesta dietética de vitamina E con el riesgo de cáncer de pulmón: un metanálisis de dosis-respuesta". Revista de nutrición clínica de Asia Pacífico . 26 (2): 271–277. doi :10.6133/apjcn.032016.04. PMID 28244705.
- ^ Lotan Y, Goodman PJ, Youssef RF, Svatek RS, Shariat SF, Tangen CM, et al. (junio de 2012). "Evaluación de la suplementación con vitamina E y selenio para la prevención del cáncer de vejiga en el estudio SELECT coordinado por SWOG". The Journal of Urology . 187 (6): 2005–10. doi :10.1016/j.juro.2012.01.117. PMC 4294531 . PMID 22498220.
- ^ Alpha-Tocopherol BC (abril de 1994). "El efecto de la vitamina E y el betacaroteno en la incidencia del cáncer de pulmón y otros tipos de cáncer en fumadores masculinos". The New England Journal of Medicine . 330 (15): 1029–35. doi : 10.1056/NEJM199404143301501 . PMID 8127329.
- ^ Arain MA, Abdul Qadeer A (abril de 2010). "Revisión sistemática sobre la vitamina E y la prevención del cáncer colorrectal"". Revista pakistaní de ciencias farmacéuticas . 23 (2): 125–30. PMID 20363687.
- ^ Heinonen OP, Albanes D, Virtamo J, Taylor PR, Huttunen JK, Hartman AM, et al. (marzo de 1998). "Cáncer de próstata y suplementación con α-tocoferol y betacaroteno: incidencia y mortalidad en un ensayo controlado". Journal of the National Cancer Institute . 90 (6): 440–6. doi : 10.1093/jnci/90.6.440 . PMID 9521168.
- ^ Klein EA, Thompson IM, Tangen CM, Crowley JJ, Lucia MS, Goodman PJ, et al. (octubre de 2011). "Vitamina E y riesgo de cáncer de próstata: ensayo de prevención del cáncer con selenio y vitamina E (SELECT)". JAMA . 306 (14): 1549–56. doi :10.1001/jama.2011.1437. PMC 4169010 . PMID 21990298.
- ^ Lee IM, Cook NR, Gaziano JM, Gordon D, Ridker PM, Manson JE, et al. (julio de 2005). "Vitamina E en la prevención primaria de enfermedades cardiovasculares y cáncer: el Estudio de Salud de la Mujer: un ensayo controlado aleatorizado". JAMA . 294 (1): 56–65. doi : 10.1001/jama.294.1.56 . PMID 15998891.
- ^ Alliance for Natural Health v. Sebelius, caso n.º 09-1546 (DDC), Administración de Alimentos y Medicamentos de los Estados Unidos, 17 de mayo de 2012
- ^ ab Zhang Y, Jiang W, Xie Z, Wu W, Zhang D (octubre de 2015). "Vitamina E y riesgo de cataratas relacionadas con la edad: un metaanálisis". Public Health Nutrition . 18 (15): 2804–14. doi : 10.1017/S1368980014003115 . PMC 10271701 . PMID 25591715.
- ^ Mathew MC, Ervin AM, Tao J, Davis RM (junio de 2012). "Suplementación con vitaminas antioxidantes para prevenir y retardar la progresión de las cataratas relacionadas con la edad". Base de datos Cochrane de revisiones sistemáticas . 2012 (6): CD004567. doi :10.1002/14651858.CD004567.pub2. PMC 4410744. PMID 22696344 .
- ^ ab Kirmizis D, Chatzidimitriou D (2009). "Efectos antiaterogénicos de la vitamina E: la búsqueda del Santo Grial". Salud vascular y gestión de riesgos . 5 : 767–74. doi : 10.2147/vhrm.s5532 . PMC 2747395. PMID 19774218 .
- ^ ab Stampfer MJ, Hennekens CH, Manson JE, Colditz GA, Rosner B, Willett WC (mayo de 1993). "Consumo de vitamina E y riesgo de enfermedad coronaria en mujeres". The New England Journal of Medicine . 328 (20): 1444–9. doi : 10.1056/NEJM199305203282003 . PMID 8479463.
- ^ Loffredo L, Perri L, Di Castelnuovo A, Iacoviello L, De Gaetano G, Violi F (abril de 2015). "La suplementación con vitamina E sola se asocia con una reducción del infarto de miocardio: un metaanálisis". Nutrición, metabolismo y enfermedades cardiovasculares . 25 (4): 354–63. doi :10.1016/j.numecd.2015.01.008. PMID 25779938.
- ^ Sesso HD, Buring JE, Christen WG, Kurth T, Belanger C, MacFadyen J, et al. (noviembre de 2008). "Vitaminas E y C en la prevención de enfermedades cardiovasculares en hombres: ensayo controlado aleatorizado Physicians' Health Study II". JAMA . 300 (18): 2123–33. doi :10.1001/jama.2008.600. PMC 2586922 . PMID 18997197.
- ^ Bin Q, Hu X, Cao Y, Gao F (abril de 2011). "El papel de la suplementación con vitamina E (tocoferol) en la prevención del accidente cerebrovascular. Un metaanálisis de 13 ensayos controlados aleatorizados". Trombosis y hemostasia . 105 (4): 579–85. doi :10.1160/TH10-11-0729. PMID 21264448. S2CID 23237227.
- ^ Carta sobre la afirmación de que el suplemento dietético contiene vitamina E y tiene efectos beneficiosos sobre las enfermedades cardíacas (expediente n.º 99P-4375) Administración de Alimentos y Medicamentos de Estados Unidos.
- ^ Dictamen científico sobre la fundamentación de las declaraciones de propiedades saludables relacionadas con la vitamina E y la protección del ADN, las proteínas y los lípidos frente al daño oxidativo (ID 160, 162, 1947),... mantenimiento de la función cardíaca normal (ID 166),... mantenimiento de la circulación sanguínea normal (ID 216)... de conformidad con el artículo 13(1) del Reglamento (CE) n.º 1924/2006 Autoridad Europea de Seguridad Alimentaria EFSA Journal 2010;8(10):1816.
- ^ ab Rumbold A, Ota E, Hori H, Miyazaki C, Crowther CA (septiembre de 2015). "Suplementación con vitamina E durante el embarazo". Base de datos Cochrane de revisiones sistemáticas . 2016 (9): CD004069. doi : 10.1002 /14651858.CD004069.pub3. PMC 8406700. PMID 26343254.
- ^ Sidgwick GP, McGeorge D, Bayat A (agosto de 2015). "Una revisión exhaustiva basada en evidencia sobre el papel de los productos tópicos y los apósitos en el tratamiento de las cicatrices de la piel". Archivos de investigación dermatológica . 307 (6): 461–77. doi :10.1007/s00403-015-1572-0. PMC 4506744 . PMID 26044054.
- ^ Tanaydin V, Conings J, Malyar M, van der Hulst R, van der Lei B (septiembre de 2016). "El papel de la vitamina E tópica en el tratamiento de las cicatrices: una revisión sistemática". Revista de cirugía estética . 36 (8): 959–65. doi : 10.1093/asj/sjw046 . PMID 26977069.
- ^ Bjelakovic G, Nikolova D, Gluud C (2013). "Análisis de metarregresión, metanálisis y análisis secuenciales de ensayos de los efectos de la suplementación con betacaroteno, vitamina A y vitamina E de forma individual o en diferentes combinaciones sobre la mortalidad por todas las causas: ¿tenemos evidencia de la falta de daño?". PLOS ONE . 8 (9): e74558. Bibcode :2013PLoSO...874558B. doi : 10.1371/journal.pone.0074558 . PMC 3765487 . PMID 24040282.
- ^ Curtis AJ, Bullen M, Piccenna L, McNeil JJ (diciembre de 2014). "Suplementación con vitamina E y mortalidad en personas sanas: un metaanálisis de ensayos controlados aleatorizados". Medicamentos y terapia cardiovascular . 28 (6): 563–73. doi :10.1007/s10557-014-6560-7. PMID 25398301. S2CID 23820017.
- ^ Kosari P, Alikhan A, Sockolov M, Feldman SR (2010). "Vitamina E y dermatitis alérgica de contacto". Dermatitis . 21 (3): 148–53. doi :10.2310/6620.2010.09083. PMID 20487657. S2CID 38212099.
- ^ ab Podszun M, Frank J (diciembre de 2014). "Interacciones entre la vitamina E y otros fármacos: base molecular y relevancia clínica". Nutrition Research Reviews . 27 (2): 215–31. doi : 10.1017/S0954422414000146 . PMID 25225959.
- ^ Opinión científica sobre la seguridad y eficacia del α-tocoferol sintético para todas las especies animales (2012) Autoridad Europea de Seguridad Alimentaria EFSA Journal 2012;10(7):2784
- ^ Evans HM, Bishop KS (diciembre de 1922). "Sobre la existencia de un factor dietético esencial para la reproducción hasta ahora no reconocido". Science . 56 (1458): 650–1. Bibcode :1922Sci....56..650E. doi :10.1126/science.56.1458.650. PMID 17838496.
- ^ Evans HM, Emerson OH, Emerson GA (1 de febrero de 1936). «El aislamiento del aceite de germen de trigo de un alcohol, a-tocoferol, que tiene las propiedades de la vitamina E». Journal of Biological Chemistry . 113 (1): 319–332. doi : 10.1016/S0021-9258(18)74918-1 . Archivado desde el original el 29 de septiembre de 2007.
- ^ FernholzE (1938). "Sobre la constitución del α-tocoferol". Revista de la Sociedad Química Estadounidense . 60 (3): 700–705. doi :10.1021/ja01270a057.
Enlaces externos
- Artículo de la Oficina de Suplementos Dietéticos de Estados Unidos sobre la vitamina E
- Evaluación de riesgos de la vitamina E Archivado el 2 de enero de 2006 en Wayback Machine , Grupo de expertos sobre vitaminas y minerales, Agencia de Normas Alimentarias del Reino Unido , 2003