Metabolismo xenobiótico

El metabolismo xenobiótico (del griego xenos "extraño" y biótico "relativo a los seres vivos") es el conjunto de vías metabólicas que modifican la estructura química de los xenobióticos , que son compuestos ajenos a la bioquímica normal de un organismo, como fármacos y venenos. Estas vías son una forma de biotransformación presente en todos los grupos principales de organismos, y se considera que tienen un origen antiguo. Estas reacciones a menudo actúan para desintoxicar compuestos venenosos; sin embargo, en casos como en el metabolismo del alcohol , los intermediarios en el metabolismo xenobiótico pueden ser ellos mismos la causa de los efectos tóxicos.
El metabolismo de los xenobióticos se divide en tres fases. En la fase I, enzimas como las oxidasas del citocromo P450 introducen grupos reactivos o polares en los xenobióticos. Estos compuestos modificados se conjugan a continuación con compuestos polares en reacciones de la fase II. Estas reacciones son catalizadas por enzimas transferasas como las glutatión S-transferasas . Por último, en la fase III, los xenobióticos conjugados pueden seguir procesándose, antes de ser reconocidos por los transportadores de eflujo y bombeados fuera de las células.
Las reacciones en estas vías son de particular interés en medicina como parte del metabolismo de fármacos y como un factor que contribuye a la resistencia a múltiples fármacos en enfermedades infecciosas y quimioterapia contra el cáncer . Las acciones de algunos fármacos como sustratos o inhibidores de enzimas involucradas en el metabolismo xenobiótico son una razón común para interacciones farmacológicas peligrosas . Estas vías también son importantes en la ciencia ambiental , donde el metabolismo xenobiótico de microorganismos determina si un contaminante se descompondrá durante la biorremediación o persistirá en el medio ambiente. Las enzimas del metabolismo xenobiótico, particularmente las glutatión S-transferasas, también son importantes en la agricultura, ya que pueden producir resistencia a pesticidas y herbicidas .
Barreras de permeabilidad y desintoxicación
Una característica importante del estrés tóxico xenobiótico es que los compuestos exactos a los que se expone un organismo son en gran medida impredecibles y pueden variar ampliamente con el tiempo. [1] El principal desafío que enfrentan los sistemas de desintoxicación xenobiótica es que deben poder eliminar la cantidad casi ilimitada de compuestos xenobióticos de la compleja mezcla de sustancias químicas involucradas en el metabolismo normal. La solución que ha evolucionado para abordar este problema es una elegante combinación de barreras físicas y sistemas enzimáticos de baja especificidad .
Todos los organismos utilizan las membranas celulares como barreras de permeabilidad hidrofóbica para controlar el acceso a su entorno interno. Los compuestos polares no pueden difundirse a través de estas membranas celulares , y la captación de moléculas útiles está mediada por proteínas de transporte que seleccionan específicamente sustratos de la mezcla extracelular. Esta captación selectiva significa que la mayoría de las moléculas hidrófilas no pueden entrar en las células, ya que no son reconocidas por ningún transportador específico. [2] Por el contrario, la difusión de compuestos hidrófobos a través de estas barreras no se puede controlar y, por lo tanto, los organismos no pueden excluir a los xenobióticos solubles en lípidos utilizando barreras de membrana.
Sin embargo, la existencia de una barrera de permeabilidad significa que los organismos pudieron desarrollar sistemas de desintoxicación que explotan la hidrofobicidad común a los xenobióticos permeables a la membrana. Por lo tanto, estos sistemas resuelven el problema de la especificidad al poseer especificidades de sustrato tan amplias que metabolizan casi cualquier compuesto no polar. [1] Los metabolitos útiles quedan excluidos ya que son polares y, en general, contienen uno o más grupos cargados.
La desintoxicación de los subproductos reactivos del metabolismo normal no se puede lograr mediante los sistemas descritos anteriormente, porque estas especies se derivan de constituyentes celulares normales y generalmente comparten sus características polares. Sin embargo, dado que estos compuestos son pocos en número, enzimas específicas pueden reconocerlos y eliminarlos. Ejemplos de estos sistemas de desintoxicación específicos son el sistema de glioxalasa , que elimina el aldehído reactivo metilglioxal, [3] y los diversos sistemas antioxidantes que eliminan las especies reactivas de oxígeno. [4]
Fases de la desintoxicación
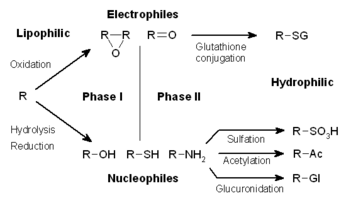
El metabolismo de los xenobióticos suele dividirse en tres fases: modificación, conjugación y excreción. Estas reacciones actúan en conjunto para desintoxicar los xenobióticos y eliminarlos de las células.
Fase I - modificación
En la fase I, una variedad de enzimas actúan para introducir grupos reactivos y polares en sus sustratos. Una de las modificaciones más comunes es la hidroxilación catalizada por el sistema de oxidasas de función mixta dependiente del citocromo P-450 . Estos complejos enzimáticos actúan para incorporar un átomo de oxígeno en hidrocarburos no activados, lo que puede dar como resultado la introducción de grupos hidroxilo o la N-, O- y S-desalquilación de sustratos. [5] El mecanismo de reacción de las oxidasas P-450 se produce a través de la reducción del oxígeno unido al citocromo y la generación de una especie de oxiferrilo altamente reactiva, de acuerdo con el siguiente esquema: [6]
Fase II - conjugación
En reacciones de fase II posteriores, estos metabolitos xenobióticos activados se conjugan con especies cargadas como el glutatión (GSH), el sulfato , la glicina o el ácido glucurónico . Estas reacciones son catalizadas por un gran grupo de transferasas de amplia especificidad, que en combinación pueden metabolizar casi cualquier compuesto hidrofóbico que contenga grupos nucleofílicos o electrófilos. [1] Uno de los más importantes de estos grupos son las glutatión S-transferasas (GST). La adición de grandes grupos aniónicos (como el GSH) desintoxica los electrófilos reactivos y produce metabolitos más polares que no pueden difundirse a través de las membranas y, por lo tanto, pueden transportarse activamente.
Fase III: modificación adicional y excreción
Después de las reacciones de fase II, los conjugados xenobióticos pueden metabolizarse aún más. Un ejemplo común es el procesamiento de conjugados de glutatión a conjugados de acetilcisteína ( ácido mercaptúrico ). [7] Aquí, los residuos de γ-glutamato y glicina en la molécula de glutatión son eliminados por la gamma-glutamil transpeptidasa y las dipeptidasas . En el paso final, el residuo de cistina en el conjugado se acetila .
Los conjugados y sus metabolitos pueden excretarse de las células en la fase III de su metabolismo, y los grupos aniónicos actúan como etiquetas de afinidad para una variedad de transportadores de membrana de la familia de proteínas de resistencia a múltiples fármacos (MRP). [8] Estas proteínas son miembros de la familia de transportadores de casete de unión a ATP y pueden catalizar el transporte dependiente de ATP de una gran variedad de aniones hidrófobos, [9] y, por lo tanto, actúan para eliminar los productos de la fase II al medio extracelular, donde pueden metabolizarse o excretarse aún más. [10]
Toxinas endógenas
La desintoxicación de metabolitos reactivos endógenos, como peróxidos y aldehídos reactivos , a menudo no se puede lograr mediante el sistema descrito anteriormente. Esto se debe a que estas especies se derivan de constituyentes celulares normales y, por lo general, comparten sus características polares. Sin embargo, dado que estos compuestos son pocos en número, es posible que los sistemas enzimáticos utilicen un reconocimiento molecular específico para reconocerlos y eliminarlos. Por lo tanto, la similitud de estas moléculas con metabolitos útiles significa que, por lo general, se requieren diferentes enzimas de desintoxicación para el metabolismo de cada grupo de toxinas endógenas. Algunos ejemplos de estos sistemas de desintoxicación específicos son el sistema de glioxalasa , que actúa para eliminar el aldehído reactivo metilglioxal , y los diversos sistemas antioxidantes que eliminan las especies reactivas de oxígeno .
Historia
Los estudios sobre cómo las personas transforman las sustancias que ingieren comenzaron a mediados del siglo XIX, cuando los químicos descubrieron que los productos químicos orgánicos como el benzaldehído podían oxidarse y conjugarse con aminoácidos en el cuerpo humano. [11] Durante el resto del siglo XIX, se descubrieron varias otras reacciones básicas de desintoxicación, como la metilación , la acetilación y la sulfonación .
A principios del siglo XX, se pasó a investigar las enzimas y las vías responsables de la producción de estos metabolitos. Este campo se definió como un área de estudio independiente con la publicación por Richard Williams del libro Detoxication mechanisms en 1947. [12] Esta investigación bioquímica moderna dio como resultado la identificación de las glutatión S -transferasas en 1961, [13] seguida por el descubrimiento de los citocromos P450 en 1962, [14] y la comprensión de su papel central en el metabolismo xenobiótico en 1963. [15] [16]
Véase también
- Diseño de fármacos
- Metabolismo de fármacos
- Biodegradación microbiana
- Biodegradación
- Biorremediación
- Antioxidante
- SPORCalc, un proceso de ejemplo para explorar bases de datos de metabolismo de fármacos y xenobióticos [17]
Referencias
- ^ abc Jakoby WB, Ziegler DM (5 de diciembre de 1990). "Las enzimas de la desintoxicación". J. Biol. Chem . 265 (34): 20715–8. doi : 10.1016/S0021-9258(17)45272-0 . PMID 2249981.
- ^ Mizuno N, Niwa T, Yotsumoto Y, Sugiyama Y (2003). "Impacto de los estudios de transportadores de fármacos en el descubrimiento y desarrollo de fármacos". Pharmacol. Rev. 55 ( 3): 425–61. doi :10.1124/pr.55.3.1. PMID 12869659.
- ^ Thornalley PJ (1 de enero de 1990). "El sistema de la glioxalasa: nuevos avances hacia la caracterización funcional de una vía metabólica fundamental para la vida biológica". Biochem. J . 269 (1): 1–11. doi :10.1042/bj2690001. PMC 1131522 . PMID 2198020.
- ^ Sies H (1997). "Estrés oxidativo: oxidantes y antioxidantes" (PDF) . Exp Physiol . 82 (2): 291–5. doi :10.1113/expphysiol.1997.sp004024. PMID 9129943.
- ^ Guengerich FP (2001). "Reacciones comunes y poco comunes del citocromo P450 relacionadas con el metabolismo y la toxicidad química". Chem. Res. Toxicol . 14 (6): 611–50. doi :10.1021/tx0002583. PMID 11409933.
- ^ Schlichting I, Berendzen J, Chu K, et al. (2000). "La vía catalítica del citocromo p450cam a resolución atómica". Science . 287 (5458): 1615–22. Bibcode :2000Sci...287.1615S. doi :10.1126/science.287.5458.1615. PMID 10698731.
- ^ Boyland E, Chasseaud LF (1969). "El papel del glutatión y las glutatión S-transferasas en la biosíntesis del ácido mercaptúrico". Avances en enzimología y áreas relacionadas de la biología molecular . Avances en enzimología y áreas relacionadas de la biología molecular. Vol. 32. págs. 173–219. doi :10.1002/9780470122778.ch5. ISBN 978-0-470-64961-9. Número PMID 4892500.
{{cite book}}:|journal=ignorado ( ayuda ) - ^ Homolya L, Váradi A, Sarkadi B (2003). "Proteínas asociadas a la resistencia a múltiples fármacos: bombas de exportación para conjugados con glutatión, glucuronato o sulfato". Biofactors . 17 (1–4): 103–14. doi :10.1002/biof.5520170111. PMID 12897433.
- ^ König J, Nies AT, Cui Y, Leier I, Keppler D (1999). "Bombas de exportación conjugadas de la familia de proteínas de resistencia a múltiples fármacos (MRP): localización, especificidad de sustrato y resistencia a fármacos mediada por MRP2". Biochim. Biophys. Acta . 1461 (2): 377–94. doi : 10.1016/S0005-2736(99)00169-8 . PMID 10581368.
- ^ Commandeur JN, Stijntjes GJ, Vermeulen NP (1995). "Enzimas y sistemas de transporte implicados en la formación y disposición de los S-conjugados de glutatión. Función en los mecanismos de bioactivación y desintoxicación de xenobióticos". Pharmacol . Rev. 47 (2): 271–330. PMID 7568330.
- ^ Murphy PJ (1 de junio de 2001). "Metabolismo xenobiótico: una mirada desde el pasado hacia el futuro". Drug Metab. Dispos . 29 (6): 779–80. PMID 11353742.
- ^ Neuberger, A.; Smith, RL (1982). "Richard Tecwyn Williams. 20 de febrero de 1909-29 de diciembre de 1979". Memorias biográficas de miembros de la Royal Society . 28 : 685–717. doi :10.1098/rsbm.1982.0026. JSTOR 769915.
- ^ Booth J, Boyland E, Sims P (1 de junio de 1961). "Una enzima del hígado de rata que cataliza conjugaciones con glutatión". Biochem. J . 79 (3): 516–24. doi :10.1042/bj0790516. PMC 1205680 . PMID 16748905.
- ^ Omura T, Sato R (1 de abril de 1962). "Un nuevo citocromo en los microsomas hepáticos". J. Biol. Chem . 237 (4): 1375–6. doi : 10.1016/S0021-9258(18)60338-2 . PMID 14482007.
- ^ Estabrook RW (2003). "Una pasión por los P450 (recuerdos de la historia temprana de la investigación sobre el citocromo P450)". Drug Metab. Dispos . 31 (12): 1461–73. doi :10.1124/dmd.31.12.1461. PMID 14625342.
- ^ Estabrook RW, Cooper DY, Rosenthal O (1963). "La inhibición reversible ligera del sistema de la hidroxilasa esteroide C-21 en la corteza suprarrenal por monóxido de carbono". Biochem. Z. 338 : 741–55. PMID 14087340.
- ^ Smith J, Stein V (2009). "SPORCalc: Un desarrollo de un análisis de base de datos que proporciona reacciones enzimáticas metabólicas putativas para el diseño de fármacos basado en ligandos". Computational Biology and Chemistry . 33 (2): 149–159. doi :10.1016/j.compbiolchem.2008.11.002. PMID 19157988.
Lectura adicional
- H. Parvez y C. Reiss (2001). Respuestas moleculares a los xenobióticos . Elsevier. ISBN 0-345-42277-5.
- C. Ioannides (2001). Sistemas enzimáticos que metabolizan fármacos y otros xenobióticos . John Wiley and Sons. ISBN 0-471-89466-4.
- M. Richardson (1996). Xenobióticos ambientales . Taylor & Francis Ltd. ISBN 0-7484-0399-X.
- C. Ioannides (1996). Citocromos P450: aspectos metabólicos y toxicológicos . CRC Press Inc. ISBN 0-8493-9224-1.
- YC Awasthi (2006). Toxicología de las S-transferasas de glutatión . CRC Press Inc. ISBN 0-8493-2983-3.
Enlaces externos
Bases de datos
- Base de datos sobre el metabolismo de fármacos
- Directorio de sistemas que contienen P450
- Base de datos de biocatálisis y biodegradación de la Universidad de Minnesota
Metabolismo de fármacos
- Metabolismo de fármacos de moléculas pequeñas
- Portal del metabolismo de fármacos
Biodegradación microbiana
- Biodegradación, biorremediación y biotransformación microbiana
Historia
- Historia del metabolismo xenobiótico
